Известные и потенциальные возможности урсотерапии
Урсотерапия – применение с лечебной целью препаратов урсодезоксихолевой кислоты (УДХК) – находит все большее распространение в клинической практике. УДХК была обнаружена в желчи гималайского (китайского) медведя в 1902 г. В 1954 г. T. Kanasawa описал процесс синтеза УДХК.
В литературе, посвященной УДХК, обращаясь к исторической справке, традиционно ссылаются на широкое применение медвежьей желчи в древнекитайской медицине. Однако желчь некоторых животных, в том числе и медвежья, находила использование в лечебной практике у разных народов. Следует сразу оговорить, что не все эти сведения прошли научную проверку, поэтому имеют лишь исторический интерес [1]. Вот несколько таких примеров. «Желчь козла хороша от звона в ушах, зубной боли, от темноты в глазах; сгоняет пятна с лица». «Желчь зайца, смешанная с сахаром, если закапывать в глаз, сгоняет пятна, а если в уши – возвращает слух». «Желчь петуха сгоняет пятна с лица и помогает при воспалительных заболеваниях глаз». «Желчь камбалы – от глухоты». «Желчь щуки сгоняет бельмо, помогает от лихорадки». «Бычья желчь при приеме внутрь разбивает мокроты и отворяет засоренные протоки. Примененная снаружи способствует рассасыванию припухлостей». В одном из старинных лечебников есть рецепт от простуды: «овечьего молока ложку, да желчи медвежьей с зерно горошку, да стерши испити на тще сердце». Подобные рецепты с использованием желчи приводит и Авиценна. А вот как пишет о ней автор «Солернского кодекса здоровья»:
Желчь, хоть она и горька,
презирать отнюдь не годится.
Но в небреженье она,
ибо свойства ее неизвестны,
И незаслуженно,
ибо нередко она помогает.
Сегодня состав желчи и ее свойства подробно изучены. Основным компонентом желчи являются желчные кислоты (ЖК) – производные не встречающейся в природе холановой кислоты. Желчь разных видов млекопитающих имеет свои особенности по составу, количеству и структуре ЖК, которые отличаются друг от друга числом и пространственным расположением гидроксильных групп. Наиболее ценной по своим свойствам в настоящее время признана УДХК, основная составляющая желчи медведя.
Продукция желчи является одной из основных функций печени. Желчь вырабатывается печенью постоянно. В организме человека ежедневно секретируется около 0,5-1,0 л желчи. Вне процесса пищеварения желчь накапливается и концентрируется в желчном пузыре. Гепатоциты в значительной степени определяют состав желчи, основными компонентами которой являются вода (82%), ЖК (12%), лецитин и другие фосфолипиды (4%), холестерин (0,7%), остальное приходится на прямой билирубин, белки (IgA, продукты распада гормонов, которые метаболизируются в печени, и т.д.), электролиты, слизь, часто также лекарства и их метаболиты.
Первичные ЖК (холевая и хенодезоксихолевая) образуются в гепатоцитах из холестерина, конъюгируются с глицином и таурином и попадают в составе желчи в кишечник, где без изменений всасываются частично путем диффузии и главным образом за счет активного транспорта в дистальном отделе подвздошной кишки, возвращаясь в печень. Вторичные ЖК (дезоксихолевая и литохолевая) образуются под воздействием бактерий. 10-20% холевой и хенодезоксихолевой кислот доходят до толстого кишечника. Другие вторичные ЖК (УДХК) образуются в очень малом количестве. Они также всасываются в кишечнике и поступают в печень. Всасываясь, ЖК попадают в портальный кровоток, быстро захватываются гепатоцитами, где снова подвергаются конъюгации и секретируются в составе желчи. Такой механизм энтерогепатической циркуляции обеспечивает сохранение ЖК в организме.
Естественное процентное соотношение ЖК в желчи человека следующее: хенодезоксихолевая 38-54%, холевая 26-39%, дезоксихолевая 16-33%, УДХК и литохолевая кислота – 0,1-5%.
В зависимости от количества и состава продуктов, употребляемых человеком, в процессе переваривания пищи весь резерв ЖК (2-4 г) проходит через кишечник минимум 1 раз. Обычно пул ЖК рециркулирует в течение суток 5-10 раз. В кишечнике всасывается около 95% ЖК, потеря с калом составляет всего 0,3-0,6 г/сут. Это компенсируется их синтезом гепатоцитами, за счет чего общий пул поддерживается на постоянном уровне.
ЖК, которые возвращаются в печень, тормозят синтез первичных ЖК из холестерина путем ингибирования холестерин-7α-гидроксилазы. Максимальная скорость синтеза ЖК в печени составляет около 5 г/сут, поэтому при тяжелых нарушениях всасывания в кишечнике возможно истощение их резерва.
ЖК составляют около 60% органических соединений желчи и являются, по сути, ее единственным функциональным компонентом. Они способствуют перевариванию жиров, всасыванию жирорастворимых витаминов, оказывают бактериостатический эффект на кишечную микрофлору, стимулируют экзокринную функцию поджелудочной железы и моторную функцию кишечника. ЖК во многом определяют физико-химические свойства желчи и способствуют удержанию холестерина в растворе.
ЖК – это амфипатические соединения, имеющие оба домена: как гидрофильный (поскольку существует полярная пептидная связь, карбоксильные и гидроксильные группы), так и гидрофобный. Поэтому ЖК склонны образовывать мицеллы с гидрофильной поверхностью наружу и гидрофобной поверхностью внутрь. По определенной концентрации, которую называют критической концентрацией мицелл, все ЖК, поступающие в раствор, образуют мицеллы. Липиды накапливаются в мицеллах с холестерином в гидрофобном центре, а амфипатические фосфолипиды и ЖК протягивают гидрофильные головки наружу, а гидрофобные хвосты – к центру. Мицеллы играют важную роль в удержании липидов в растворе, транспортировке их к щеточной кайме интестинальных эпителиальных клеток, где они абсорбируются. Таким образом, мицеллы позволяют транспортировать холестерин из печени в кишечник, не давая ему выпадать в виде кристаллов, причем абсолютные значения трех веществ (ЖК, холестерин, фосфолипиды) в пределах их физиологических концентраций значения не имеют, важно только их соотношение.
Предполагается, что формирование холестериновых желчных камней может происходить при увеличении доли дезоксихолевой кислоты в пуле ЖК. Дезоксихолевая кислота является продуктом бактериального 7-α-дегидроксилирования ЖК в кишечнике. Установлено, что пациенты с желчными камнями имеют более высокий уровень 7-α-дегидроксилирующих фекальных бактерий, принадлежащих к роду Clostridium. Поэтому в последнее время особое внимание уделяется активности нормальной микрофлоры, связанной с ее участием в метаболизме ЖК. Все больше сторонников насчитывает гипотеза о важном значении микробиоты и ее связи с различными вариантами спонтанных воспалительных заболеваний желчевыводящих путей (ЖВП). Выявление этой связи и механизмов ее реализации могло бы значительно продвинуть вперед проблему лечения как воспалительных заболеваний кишечника (язвенный колит и болезнь Крона), так и первичных и вторичных холангитов.
В поисках решения этой проблемы проведено экспериментальное исследование на мышах [2]. Сравнивались линии мышей с экспериментально вызванным воспалением ЖВП и без такового. Изучались микробные профили содержимого и слизистой оболочки слепой кишки мышей обеих линий методом извлечения ДНК и секвенирования 16S р РНК последовательностей. Результаты работы четко продемонстрировали, что микробные профили мышей с воспалением ЖВП существенно отличаются от здоровых. Улучшение кишечной микробиоты с помощью медикаментозного воздействия приводило к значительному уменьшению показателей поражения ЖВП: снижению количества инфарктов и меньшей степени расширения вне- и внутрипеченочных желчных протоков. Таким образом, результаты исследования демонстрируют тесную связь кишечной микробиоты и воспалительных заболеваний ЖВП в виде значительного влияния, оказываемого на их возникновение и течение составом кишечной микрофлоры. Приведенная работа важна в свете имеющихся данных о благоприятном влиянии препаратов УДХК на поддержание и нормализацию микробиоты кишечника.
ЖК отличаются между собой количеством и позицией гидроксильных групп и карбоксильной группой на боковой цепи. По возрастанию гидрофобных свойств ЖК располагаются в таком порядке: холевая (3α, 7α, 12α)> УДХК (3α, 7β)> хенодезоксихолевая (3α, 7α)> дезоксихолевая (3α, 12α)> литохолевая (3α).
Гидрофобные (липофильные) ЖК оказывают важные эффекты, связанные с пищеварением (эмульгация жиров, стимуляция панкреатической липазы, образование мицелл с жирными кислотами и др.), стимулируют выход в желчь холестерина и фосфолипидов, снижают синтез α-интерферона гепатоцитами. Липофильные свойства обусловливают токсичность ЖК при нарушении динамики желчи. Они проникают в липидные слои плазматических мембран клеток и мембран их митохондрий, что вызывает изменение функционирования органелл и даже гибель клеток. Гидрофильные ЖК также принимают участие в процессах пищеварения, кроме того они могут снижать кишечную абсорбцию холестерина, его синтез в гепатоцитах и поступление в желчь, стимулируют синтез α-интерферона. Оптимальное соотношение гидрофильных и гидрофобных ЖК обеспечивает нормальное течение процессов пищеварения, а также здоровое состояние гепатобилиарной системы.
УДХК является стереоизомером хенодезоксихолевой кислоты, отличаясь от нее только в отношении экваториального ориентирования 7β-гидроксильной группы. Однако именно это определяет более выраженную гидрофильность и отсутствие токсичных свойств УДХК по сравнению с другими ЖК.
Согласно современным представлениям, распределение УДХК ограничивается плазмой крови и органами печеночной системы. После приема внутрь максимальная концентрация УДХК в плазме крови достигается в пределах 30-60 мин за счет того, что препарат хорошо всасывается частично путем пассивной диффузии, частично с помощью систем активного транспорта в подвздошной кишке. Несмотря на хорошее всасывание УДХК в кишечнике, ее уровень в плазме крови остается сравнительно низким из-за быстрого печеночного клиренса. Около 50-75% дозы препарата, поступающего в организм, подвергается «эффекту первого прохождения» через печень, поэтому концентрация УДХК в плазме крови не является показателем ее биодоступности.
Терапевтическая эффективность препарата при заболеваниях печени и желчного пузыря обусловлена его концентрацией в этих органах. Установлено, что концентрация УДХК в желчи возрастает в зависимости от дозы и достигает плато при применении в дозе 10-14 мг/кг массы тела в сутки. Последующее увеличение суточной дозы не приводит к повышению концентрации УДХК в желчи из-за снижения всасывания в кишечнике. В связи с аутоингибированием всасывания УДХК необходимо учитывать, что максимальная однократная доза на прием должна составлять не более 750 мг [3]. Кроме того, при повышении дозы УДХК увеличивается риск побочных реакций, в частности диареи. Поэтому увеличивать рекомендованную дозу, рассчитывая на повышение клинической эффективности, не стоит. Если доза УДХК не превышает 750 мг, то препарат принимают однократно вечером, при большей суточной дозировке оставшуюся часть дозы принимают после обеда. Акцент на прием УДХК во второй половине дня, преимущественно в вечернее время, делают исходя из того, что физиологический пик синтеза холестерина наблюдается ночью.
При регулярном приеме УДХК становится основной желчной кислотой, составляя до 40-50% общего содержания ЖК в желчи. Более низкое накопление УДХК в желчи наблюдается при заболеваниях печени. Это обусловлено снижением ее всасывания вследствие уменьшения образования эндогенных мицелл из ЖК в дуоденальной желчи или с уменьшением ее секреции.
УДХК выводится преимущественно с калом. Анализ, который проводился в течение 3 суток после перорального приема здоровыми людьми 500 мг УДХК, показал, что с калом выделяется 37% принятой дозы. Несмотря на то что ЖК попадают также в почки, они почти не выводятся с мочой через их реабсорбцию в канальцах. Биологический период полураспада после применения УДХК составляет от 3,5 до 5,8 дня.
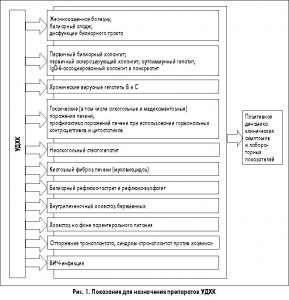
Первоначально УДХК была рекомендована для растворения желчных камней. Сегодня накоплен значительный опыт ее применения для проведения как перорального литолиза, так и для профилактики образования желчных камней при разных состояниях [4]. В 1980-1990-е гг. спектр показаний к ее назначению существенно расширился и продолжает обновляться за счет включения заболеваний печени, желудка, пищевода и других органов (рис. 1) [5].
В настоящее время УДХК признана золотым стандартом терапии первичных холестатических заболеваний печени. К этой группе относят первичный билиарный холангит (ПБХ), по старой номенклатуре первичный билиарный цирроз, и первичный склерозирующий холангит (ПСХ). Относительно недавно был открыт частичный агонизм УДХК к кортикостероидным рецепторам, что может объяснять ее адъювантный эффект при лечении аутоиммунных заболеваний [6].
При ПБХ рекомендуется прием УДХК в суточной дозе из расчета 13-15 мг/кг массы тела, разделенной на три приема. Через 3 мес можно перейти на однократный прием препарата на ночь. Установлено, что чем раньше начата терапия, тем больше вероятность достижения успеха. В случае ранней диагностики, раннего назначения УДХК и ответа на терапию выживаемость больных с ПБХ сопоставима с таковой у здоровых лиц [7]. Лечение должно быть постоянным, без перерывов, многолетним, то есть пока оно оказывает эффект у данного пациента.
Чтобы понять, какой пациент будет более подвержен терапии УДХК, у кого будет лучше прогноз на фоне лечения, G.M. Hirschfield, M.E. Gershwin [8] предложили 5 клинических фенотипов пациентов с ПБХ.
- По-видимому, самая многочисленная группа – это женщины среднего возраста со скудной или вообще отсутствующей симптоматикой, когда диагноз ставится только на основе лабораторных данных. У них ответ на УДХК хороший, соответственно, они имеют относительно благоприятный прогноз.
- Пациенты любого возраста, характеризующиеся слабым ответом на УДХК, с медленным, но неуклонным прогрессированием до формирования цирроза, который тем не менее длительное время может оставаться компенсированным.
- Дебют в среднем возрасте. Клинико-биохимическая симптоматика неяркая, декомпенсация наступает только на седьмом-восьмом десятилетии жизни.
- Пациенты старческого возраста. Прогрессирование до цирроза идет неуклонно, в то же время цирроз, как и во второй группе, длительный период может оставаться в компенсированной стадии.
- Наиболее тяжелая для клиницистов группа – это молодые женщины с быстро прогрессирующим исчезновением желчных протоков и абсолютной резистентностью к терапии УДХК.
В качестве целевых показателей, снижение которых является хорошим прогностическим фактором ответа на лечение УДХК, приняты, в первую очередь, щелочная фосфатаза, а также аспартатаминотрансфераза, уровень общего билирубина (не должен превышать нормы). Оценка их динамики уже в процессе терапии УДХК позволяет выделить группы с хорошим и плохим прогнозом, то есть группы, в которых целесообразно продолжать монотерапию УДХК или добавлять другие препараты.
При ПСХ результаты клинических исследований, полученные на основе доказательной медицины, дают основания утверждать, что УДХК в дозе 15-20 мг/кг/сут улучшает прогноз заболевания и результаты серологических печеночных показателей, но не оказывает достоверного положительного влияния на выживаемость [9]. Также известно, что УДХК улучшает качество жизни пациентов с ПСХ за счет уменьшения кожного зуда.
В лечении взрослых больных ПСХ не используются кортикостероиды и другие иммуносупрессивные препараты, за исключением пациентов с наличием перекрестного синдрома.
Интересные разработки, касающиеся ПСХ, были представлены в 2009 г. G.J. Webster и соавт. [10]. В частности, было высказано предположение, что IgG4-ассоциированный холангит может являться ранней стадией ПСХ и ответ на стероидную терапию может определяться длительностью течения болезни. Согласно теории G.J. Webster и соавт. (2009), на ранней стадии патологических процессов в билиарном тракте преобладает иммунное воспаление, которое отвечает на терапию преднизолоном в сочетании с УДХК. На поздней стадии преобладает фиброгенез, резистентный к лечению. Аутоиммунный панкреатит нередко сочетается с IgG4-ассоциированным холангитом. Поскольку это сопутствующее заболевание, как и все панкреатиты, имеет яркую клинику, оно позволяет диагностировать IgG4-холангита на ранних стадиях, поэтому такие пациенты раньше становятся объектом внимания врача и мишенью для применения адекватной терапии. ПСХ плохо поддается терапии из-за поздней диагностики, но на более ранних стадиях в ряде случаев ПСХ может представлять собой IgG4-ассоциированный холангит.
Причины возникновения и патогенез холестатических заболеваний до сих пор остаются неизвестными. Между тем заболеваемость ими в мире растет и представляет серьезную угрозу. В настоящее время обсуждается так называемая теория «восходящей патофизиологии» холестатических заболеваний печени [11], которая охватывает ПБХ и ПСХ. Рассматривается идея о том, что патология не проявляется сразу как внутрипеченочный холестаз. Изменения возникают сначала в нижележащих ЖВП, а потом восходят «вверх по течению». Первые и ранние поражения, происходящие в нижних отделах, ведут к застойным явлениям и повышению давления в вышестоящих желчных капиллярах и канальцах, где создается высокая концентрация токсичных ЖК, которые приводят к их поражению. Авторы отмечают, что печень обладает огромным потенциалом адаптации к холестазу, в связи с чем создается и чем объясняется большой временной интервал субклинического течения этих заболеваний. Отсутствие или бедность клинических проявлений приводят, как правило, к позднему распознаванию этих состояний.
Подобный подход к холестатическим заболеваниям печени ставит перед медицинским сообществом ряд неотложных задач. Прежде всего это раннее выявление ПБХ и ПСХ на начальных стадиях, для чего необходимо, с одной стороны, создать надежные биомаркеры этих заболеваний, а с другой – привлечь внимание врачей к активному поиску и распознаванию этих заболеваний. Новый взгляд на природу холестатических заболеваний печени и предполагаемая непосредственная причинная связь с патологическим воздействием токсичных ЖК ставят на повестку дня раннее превентивное применение УДХК, препараты которой способны нейтрализовать это воздействие.
Наиболее свежие данные о результатах применения УДХК в лечении нехолестатических заболеваний печени представлены в систематическом обзоре, включившем только те исследования, которые отвечают современным канонам доказательной медицины [12]. В нем рассмотрена клиническая эффективность УДХК при таких заболеваниях, как неалкогольная и алкогольная жировая болезнь печени (НАЖБП и АЖБП), стеатогепатит, аутоиммунный гепатит (АИГ), посттрансплантационное поражение печени (отторжение трансплантата), ишемическое реперфузионное поражение печени, хронические и острые гепатиты В и С, гепатиты другой этиологии.
На фоне применения УДХК отмечена позитивная динамика биохимических печеночных проб: достоверно при НАЖБП, АИГ, острых и хронических вирусных гепатитах В и С. При АЖБП и отторжении трансплантата убедительных данных не получено. Особо подчеркнута безопасность УДХК. Урсотерапия практически не имеет побочных эффектов за исключением диареи, которая легко купируется коррекцией дозы.
Авторы обзора отмечают, что целесообразность применения УДХК при большинстве нехолестатических заболеваний печени можно считать доказанной, отмечая при этом, что из-за длительности курсов лечения УДХК (до 12 мес) информации о долгосрочных влияниях недостаточно, что требует дальнейших исследований.
Накапливаются экспериментальные и клинические данные о протекторном действии УДХК при колоректальном раке, в том числе при ПСХ. Экспериментально установлено, что дезоксихолевая кислота участвует в патогенезе рака толстой кишки посредством влияния на процессы пролиферации, дифференцировки и апоптоза колоноцитов. УДХК, в отличие от дезоксихолевой кислоты, подавляет вызванную ею активацию транскрипционного фактора NF-kappa B и активирующего протеина АР-1 [13]. Поэтому при ПСХ УДХК следует назначать в первую очередь пациентам из группы высокого риска, особенно больным с отягощенным наследственным анамнезом в отношении колоректального рака, колоректальной неоплазии или длительно протекающего экстенсивного колита. Имеются также указания на снижение частоты развития колоректального рака на фоне применения УДХК у больных с воспалительными заболеваниями кишечника [14].
Получены сведения о противоопухолевом эффекте УДХК и эффективности при раке иной локализации. Так, в рандомизированном контролируемом исследовании, включавшем 102 пациента с компенсированным циррозом печени в исходе хронического гепатита С, продемонстрировано статистически значимое снижение частоты формирования гепатоцеллюлярной карциномы в течение 5 лет по сравнению с контрольной группой, причем независимо от уровня аланинаминотрансферазы (17,9 против 39,1%; р=0,025) [15].
В последние годы появляются все новые работы, в которых УДХК рассматривается в качестве претендента на препарат, способный модифицировать состояние нервных клеток человека, в частности дофаминергических, уменьшая нейротоксичность, в связи с признанным антиапоптотическим и противовоспалительным действием. Исследование на крысиной модели болезни Паркинсона продемонстрировало, что УДХК заметно улучшает продукцию и приостанавливает снижение дофамина в полосатом теле, благоприятно влияя на функции митохондрий [16]. На это указывает повышение АТФ, падение уровня фактора некроза опухолей, снижение активности каспазы 8, 9 и 3. Показанная способность УДХК повышать синтез дофамина и регулировать митохондриальные функции может оказаться благоприятной для лечения болезни Паркинсона.
Таким образом, несмотря на то что с момента внедрения УДХК в практику прошло более 35 лет, взгляды на ее значение для жизнедеятельности организма еще окончательно не сложились. И возможно, нас ждут открытия, выходящие за рамки привычных показаний к ее применению.
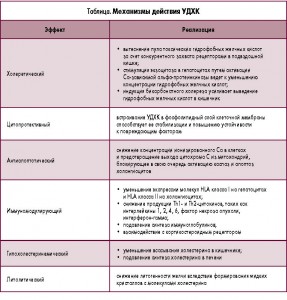
Разнообразие нозологических форм, при которых наблюдаются положительные результаты терапии, определяют сложные механизмы действия УДХК (табл.) [17].
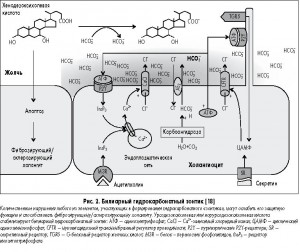
Механизмы реализации эффектов УДХК продолжают интенсивно изучаться. Особого внимания заслуживает одна из последних теоретических разработок по УДХК – теория гидрокарбонатного зонтика [18]. Установлено, что билиарная секреция гидрокарбонат-ионов создает протективный слой на апикальной мембране холангиоцитов. У человека почти половина желчи секретируется холангиоцитами. Секреция гидрокарбонат-ионов защищает холангиоциты от неконтролируемого трансмембранного тока гликохенодезоксихолевой кислоты, которая обладает цитотоксическим эффектом, поскольку протонированные соли данной кислоты индуцируют апоптоз холангиоцитов.
При ПБХ доказано нарушение экспрессии транспортера гидрокарбонат-иона AE2 и, соответственно, секреции этого гидрокарбонат-иона, а при ПСХ определен вариант так называемого гена риска, который кодирует рецептор желчных солей и модулятор секреции гидрокарбонат-иона TGR5. Таким образом, в норме мы имеем зонтик, защищающий холангиоциты от неблагоприятных воздействий, при холестатических заболеваниях этот зонтик становится дырявым и пропускает токсичные для холангиоцитов ЖК (рис. 2).
С патофизиологической точки зрения более высокий потенциал стимуляции гидрокарбонатного холереза может способствовать предотвращению апоптоза холангиоцитов – основного патогенетического механизма развития иммуноопосредованных холестатических заболеваний печени. Поэтому считается, что эта теория может послужить новым толчком к разработке средств лечения ПБХ и ПСХ.
Количественные нарушения любого из элементов, участвующих в формировании гидрокарбонатного зонтика, могут ослабить его защитную функцию и способствовать фиброзирующему/склерозирующему холангиту. УДХК или норУДХК стабилизируют билиарный гидрокарбонатный зонтик.
Таким образом, механизмы действия УДХК при гепатобилиарной патологии и других заболеваниях, не связанных с пищеварительной системой, должны стать предметом серьезных исследований. Новые знания, которые будут получены при этом, возможно, обеспечат выявление ранее неизвестных показаний к урсотерапии и позволят достичь благоприятных результатов лечения и профилактики определенных нозологических форм.
На фармацевтическом рынке препараты УДХК представлены достаточно широко. В медицинской практике при выборе лекарственных средств вызывает интерес качество как субстанции, так и вспомогательных веществ. В Украине гастроэнтерологи имеют возможность выбора различных качественных препаратов УДХК: Урсосан чешской фармацевтической компании PRO.MED.CS Praha a.s., Урсолив таиландской фармацевтической компании «Мега Лайфсайенсиз», Урсохол отечественной фармацевтической фирмы «Дарница» и другие.
Литература
- Корпачев В.В. Целебная фауна. – М.: Наука, 1989. – 189 с.
- Schrumpf E., Kummen M., Valestrand L. еt al. // J. Hepatol. – 2016. – Okt 5 Pll; SO 168-8278(16)30559-1.
- Walker S., Rudolph G., Raedsch R., Stiehl A. Intestinal absorption of ursodeoxycholic acid in patients with extrahepatic biliary obstruction and bile drainage // Gastroenterology. – 1992. – Vol. 102, № 3. – P. 810-815.
- Щербинина М.Б. Желчнокаменная болезнь: терапевтические аспекты. – Киев: Медкнига, 2012. – 228 с.
- Knas M., Dutkiewicz E., Szajda S.D. et al. Ursodeoxycholic acid – panacea for liver diseases? // E&C Hepatology. – 2006. – Vol. 2. – Р. 12-19.
- Solа S., Amaral J.D., Castro R.E. et al. Nuclear translocation of UDCA by the glucocorticoid receptor is required to reduce TGF-beta1-induced apoptosis in rat hepatocytes // Hepatology. – 2005. – Vol. 42, № 4. – P. 925-934.
- Kuiper E.M., Hansen B.E., de Vries R.A. еt al. // Improved prognosis of patients with primary biliary cirrhosis that have a biochemical response to ursodeoxycholic acid // Gastroenterology. – 2009. – Apr; 136 (4). – Р.1281-7. doi: 10.1053/j.gastro.2009.01.003. Epub 2009 Jan 14.
- Hirschfield G.M., Gershwin M.E. The immunobiology and pathophysiology of primary biliary cirrhosis // Ann. Rev. Pathol. – 2013. – Vol. 8. – Р.303-330.
- EASL Clinical Practice Guidelines: Management of cholestatic liver diseases // J. of Hepatology. – 2009. – Vol. 51. – Р. 237-267.
- Webster G.J., Pereira S.P., Chapman R.W.J. Autoimmune pancreatitis/IgG4-associated cholangitis and primary sclerosing cholangitis – overlapping or separate diseases? // Hepatol. – 2009. – Aug; 51 (2). – Р. 398-402. doi: 10.1016/j.jhep.2009.04.010. Epub 2009 May 12.
- Jansen P.L., Ghallab A., Varta K.N. et al. The ascending pathophysiology of cholestatic liver disease // Hepatology. – 2016. – Dec. 16 Doi:10.1002/hep.28965
- Reardon J., Hussaini T., Alsahafi M. et al. Ursodeoxycholic acid in treatment of Non-cholestatic liver Diseases: a systematic review // J. Clin. Transl. Hepatol. – 2016. – Sep 28; 4 (3). – Р. 192-205.
- Shah S.A., Looby E., Volkov Y. et al. Ursodeoxycholic acid inhibits translocation of protein kinase C in human colonic cancer cell lines // Eur. J. Cancer. – 2005. – Vol. 41, № 14. – P. 2160-2169.
- Wang R., Leong R.W. Primary sclerosing cholangitis as an independent risk factor for colorectal cancer in the context of inflammatory bowel disease: a review of the literature // World J. Gastroenterol. – 2014. – Vol. 20, № 27. – P. 8783-8789.
- Tarao K., Fujiyama S., Ohkawa S. et al. Ursodiol use is possibly associated with lower incidence of hepatocellular carcinoma in hepatitis C virus-associated liver cirrhosis // Cancer Epidemiol. Biomarkers. Prev. – 2005. – Vol. 14, № 1. – P. 164-169.
- Abdelkader N.F., Safar M.M., Salem H.A. Ursodeoxycholic Acid Ameliorates Apoptotic Cascade in the Rotenone Model of Parkinson’s Disease: Modulation of Mitochondrial Perturbations. // Mol Neurobiol. – 2016. – Mar; 53 (2). – Р.810-817. doi: 10.1007/s12035-014-9043-8. Epub 2014 Dec 15.
- Roma M.G., Toledo F.D., Boaglio A.C. et al. Ursodeoxycholic acid in cholestasis: linking action mechanisms to therapeutic applications // Clin. Sci. (Lond.). – 2011. – Vol. 121, № 12. – P. 523-544.
- Beuers U., Hohenester S., de Buy Wenniger L. J. et al. The biliary HCO3-umbrella: a unifying hypothesis on pathogenetic and therapeutic aspects of fibrosing cholangiopathies // Hepatol. – 2010. – Vol. 52 (4). – P. 1489-1496. doi: 10.1002/hep.23810.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...