Рання терапія аторвастатином покращує імунозапальні маркери і функціональний результат після гострого ішемічного інсульту
Разом з гіполіпідемічними ефектами статини також можуть позитивно впливати на церебральний кровообіг і паренхіму головного мозку при ішемічному інсульті і реперфузії.
В експериментальному дослідженні Asahi і співавт. (2005) статини підвищували рівні ендотеліальної синтази оксиду азоту (eNOS) і мРНК тканевого активатора плазміногену-1 (tPA), не пливаючи на рівні мРНК інгібітора активатора плазміногену-1 (РАІ-1), а аторвастатин зменшував об’єм ішемічної тканини і покращував неврологічні наслідки артеріальної тромбоемболії. Aslanyan і співавт. (2005) встановили, що використання статинів асоціюється зі зниженою смертністю протягом 1 міс після інсульту.
У відомому дослідженні SPARCL (2006) у пацієнтів з нещодавнім ішемічним інсультом або транзиторною ішемічною атакою аторвастатин 80 мг/добу знижував загальну частоту інсультів і кардіоваскулярних подій.
Нещодавно Pignatelli і співавт. (2012) отримали перші докази того, що аторвастатин швидко й одночасно зменшує окислювальний стрес і агрегацію тромбоцитів шляхом прямого інгібування тромбоцитарної Nox2, ізопростанів і тромбоксану А2, продемонструвавши доцільність використання цього препарату для профілактики і модулювання тромбозу.
Запалення відіграє основну роль у розвитку всіх стадій атеросклеротичного процесу. Так само тромбоз і фібриноліз можуть спричиняти прогресування вогнищ атеросклерозу. Цікаво, що обидва ці механізми можуть брати участь у патогенезі атеросклерозу великих внутрішньочерепних артерій і ішемічного інсульту, особливо його атеросклеротичного підтипу.
У пацієнтів із кардіоемболічним й атеротромботичним підтипами інсульту значно підвищуються плазмові рівні фактора некрозу пухлини (TNF), інтерлейкіну (IL) 6 і IL‑1β, тоді як у хворих із лакунарним інсультом ці показники суттєво знижуються. У багатьох дослідженнях також було встановлено, що плазмові рівні імунозапальних маркерів достовірно корелюють з об’ємом вогнища ішемії.
Метою цього дослідження було оцінити вплив аторвастатину 80 мг/добу на імунозапальні маркери і функціональні результати в пацієнтів з нещодавнім гострим ішемічним інсультом, класифікованим як атеротромботичний інсульт, які не отримували тромболітичної терапії.
Матеріали і методи
У дослідженні могли взяти участь пацієнти з ішемічним інсультом (великим атеросклеротичним інсультом – LAAS за класифікацією TOAS) з чітким часом початку, дефіцитом, виміряним за шкалою NIHSS, і вихідною комп’ютерною томографією головного мозку, яка показала відсутність внутрішньочерепного крововиливу. Критерії виключення: тромболізис; запальні або інфекційні захворювання; рак; хвороби крові; важка печінкова або ниркова недостатність; лікування протизапальними препаратами. Інсульт діагностували за вогнищевими неврологічними ознаками і симптомами вірогідно судинного походження, які зберігалися протягом ≥24 год, з подальшим підтвердженням комп’ютерною томографією або магнітно-резонансною томографією головного мозку.
Пацієнтів рандомізували на дві групи: група А отримувала аторвастатин (Ліпримар®, Pfizer) 80 мг 1 р/добу починаючи з дня госпіталізації із продовженням лікування після виписки, як це відбувалось у дослідженні SPARCL; група В до виписки аторвастатин не отримувала, а після виписки препарат призначався так само, як у дослідженні SPARCL.
Пацієнтам з порушеннями свідомості або ковтання аторвастатин призначали за допомогою назогастрального зонда після розчинення таблетки.
Як маркери імунозапальної активації оцінювали плазмові рівні IL‑1β, TNF, IL‑6, IL‑10, Е-селектину, Р-селектину, розчинної молекули міжклітинної адгезії (sICAM‑1) і розчинної молекули адгезії ендотелію судин (sVACM‑1). Крім того, визначали плазмові рівні фактора фон Віллебранда (VWF; маркер ендотеліальної дисфункції), tРА-атигену і РАІ‑1 (маркери тромбозу і фібринолізу відповідно). Лабораторні дослідження здійснювали через 72 год і 7 днів після появи симптомів.
Первинною кінцевою точкою була різниця в середніх рівнях імунозапальних маркерів між групами А і Б через 72 год і 7 днів після інсульту. Вторинними кінцевими точками були різниця в середній оцінці за шкалою тяжкості інсульту NIHSS через 72 год і 7 днів після інсульту між групами А і Б, а також різниця в середній оцінці за модифікованою шкалою Rankin (mRS) через 7 днів після інсульту між групами А і Б.
Результати
У дослідженні взяли участь 42 пацієнти з гострим ішемічним інсультом, класифікованим як LAAS; із них 22 пацієнти були рандомізовані в групу А (лікування аторвастатином) і 20 – у групу Б. За вихідними клініко-демографічними характеристиками, у тому числі факторами кардіоваскулярного ризику (артеріальна гіпертензія, діабет, дисліпідемія, інсульт в анамнезі), лабораторними показниками (лейкоцити, тромбоцити, ліпідний профіль та ін.) і кардіоваскулярною терапією перед інсультом (антитромбоцитарні, антигіпертензивні препарати, статини), групи були подібними.
Жоден пацієнт не припинив лікування досліджуваним препаратом через м’язову, печінкову токсичність або інші небажані ефекти. Призначення аторвастатину 80 мг не супроводжувалося будь-якими змінами сироваткових рівнів аланінамінтрансферази, аспартатамінорансферази, γ-глутамілтрансферази або лужної фосфатази.
 Середній час появи симптомів інсульту до початку лікування аторвастатину становив 12±4,8 год.
Середній час появи симптомів інсульту до початку лікування аторвастатину становив 12±4,8 год.
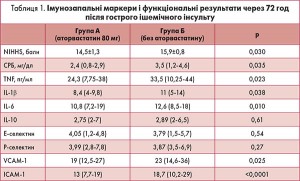
Через 72 год і 7 днів після інсульту у групі А порівняно із групою Б спостерігалися значно нижчі плазмові рівні С-реактивного білка, TNF, прозапальних інтерлейкінів і молекул адгезії (табл. 1, 2). За рівнями IL‑10 (протизапальний інтерлейкін), Е- і Р-селектину групи в обидва періоди суттєво не відрізнялись.
У пацієнтів, які отримували аторвастатин 80 мг, через 72 год і 7 днів після інсульту спостерігались значно кращі оцінки за шкалою NIHSS порівняно із хворими, які цей препарат не приймали (табл. 2).
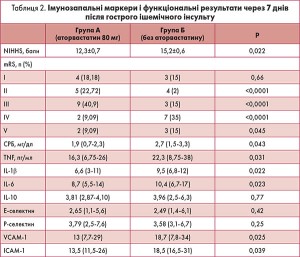
Щодо шкали mRS, через 7 днів у групі А (лікування аторвастатином) було значно більше пацієнтів із кращими функціональними результатами порівняно з групою Б (табл. 2).
Цікаво, що в пацієнтів з найбільшим зниженням імунозапальних маркерів через 7 днів спостерігалися також найкращі функціональні результати. Так, у пацієнтів з TNF >20 пг/мл, IL‑1β >7 пг/мл і IL‑6 >9 пг/мл середня оцінка NIHSS становила 17,5±1,8, 17,8±1,8 і 18,0±1,4 відповідно, тоді як у пацієнтів з TNF <20 пг/мл, IL‑1β <7 пг/мл і IL‑6 <9 пг/мл – 12,8±1,7, 10,1±1,5 і 11,3±1,6 відповідно. Аналогічна картина спостерігалась і для оцінки за шкалою mRS: при TNF >20 пг/мл, IL‑1β >7 пг/мл і IL‑6 >9 пг/мл – 3,9±0,9, 4,0±0,5 і 3,9±0,4; при TNF <20 пг/мл, IL‑1β <7 пг/мл і IL‑6 <9 пг/мл – 2,0±0,8, 2,9±0,3 і 2,8±0,3 відповідно.
Обговорення
Результати дослідження надали перші докази того, що аторвастатин, призначений у високій дозі в ранньому періоді після атеросклеротичного ішемічного інсульту, значно знижує маркери імунозапальної активації в гострому періоді інсульту й асоціюється з кращими функціональними результатами щодо гострого неврологічного дефіциту і ступеня дисфункціональних порушень. Після 7 днів від розвитку інсульту суттєвих змін ліпідного профілю не спостерігалося, тобто вищенаведені нейропротекторні ефекти аторвастатину досягались незалежно від його гіполіпідемічної дії.
Отже, значний вплив аторвастатину на маркери імунозапальної активації в гострій фазі інсульту і функціональні результати вірогідно пояснюються плейотропними ефектами препарату, у тому числі протизапальною, імуномодулюючою, ендотелійпротекторною, антитромботичною і антиоксидантною дією.
Завдяки нейропротекторним і регенеративним ефектам у головному мозку аторвастатин розглядається як перспективний препарат у профілактиці і лікуванні хвороби Альцгеймера та інших нейродегенеративних хвороб. Так, у дослідженні Piermartiri і співавт. (2010) було доведено, що лікування аторвастатином ефективно захищає клітини мозку від дегенерації, обумовленою β-амілоїдом.
Раніше в пілотному рандомізованому дослідженні Montaner і співавт. (2008) оцінювали вплив симвастатину в гострій фазі ішемічного інсульту на імунозапальні маркери (IL‑6, IL‑8, IL‑10, ICAM‑1, VCAM‑1, СРБ, TNF та ін.) і неврологічні результати через 1, 3, 5, 7 і 90 днів. Симвастатин застосовували в початковій дозі 40 мг/добу протягом 7 днів з подальшим переходом на дозу 20 мг/добу. У результаті жодних відмінностей у біомаркерах між групами терапії виявлено не було. Це може пояснюватися тим, що нейропротекторні ефекти аторвастатину не властиві всьому класу статинів, а є унікальними саме для цього препарату.
Висновки
Отримані дані свідчать про ефективність раннього призначення високодозової терапії аторвастатином у пацієнтів з гострим ішемічним інсультом з метою нейропротекції. Доцільним вбачається подальше вивчення потенційної нейропротекторної ролі аторвастатину при інших гострих неврологічних розладах, таких як травматичний інсульт головного мозку і церебральний крововилив.
Стаття друкується в скороченні.
Список літератури знаходиться в редакції.
Tuttolomondo A., Di Raimondo D., Pecoraro R. et al. Early High-dosage Atorvastatin Treatment Improved Serum Immune-inflammatory Markers and Functional Outcome in Acute Ischemic Strokes Classified as Large Artery Atherosclerotic Stroke: A Randomized Trial. Medicine (Baltimore). 2016; 95 (13): e3186.
Переклав з англ. Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 2 (399), січень 2017 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Кору та листя верби тисячоліттями використовували як знеболювальний та жарознижувальний засіб. У ХІХ ст. із цих рослинних продуктів кристалізовано активну речовину – саліцин, згодом синтезували саліцилову кислоту, а в 1899 році її ацетильовану форму – ацетилсаліцилову кислоту (АСК) запатентовано як удосконалений лікарський засіб під назвою «аспірин» [1]. Лише в другій половині ХХ ст. детально вивчено молекулярні мішені АСК; зокрема, отримав належну оцінку та пояснення її антитромботичний ефект....
Артеріальна гіпертензія (АГ) є провідною причиною смерті та інвалідизації у всьому світі. Відповідно до серії досліджень Global Burden of Disease, ≈13% смертей так чи інакше пов’язані з АГ (Forouzanfar M.H. et al., 2017; Lewington S. et al., 2002; World Health Organization, 2009)....
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9). Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи. ...




