Современные возможности терапии второй линии при немелкоклеточном раке легкого
Одним из наиболее важных механизмов борьбы со злокачественными клетками является образование специфических Т-лимфоцитов. Комплексы антиген-представляющих клеток активируют Т-лимфоциты, и активированные CD4 и CD8 клетки разрушают опухоль. Понимание того, что опухолевые клетки для ухода от надзора иммунной системы используют механизмы, которые в норме служат с целью контроля выраженности и длительности иммунного ответа, стало предпосылкой для создания нового класса иммунотерапевтических препаратов. Настоящим прорывом в терапии злокачественных новообразований, в том числе при немелкоклеточном раке легкого (НМРЛ), стала разработка препаратов моноклональных антител, действие которых направлено не на разрушение опухолевых клеток, а на устранение вызванной опухолью иммуносупрессии.
Внедрение в клиническую практику современных иммунотерапевтических препаратов позволило изменить прогноз для многих больных злокачественными новообразованиями. Ингибиторы иммунных контрольных точек предотвращают ускользание опухолевых клеток от иммунного надзора. Иммунные контрольные точки – это сигнальные молекулы, которые регулируют защитные реакции организма и могут как подавлять, так и активировать иммунную систему. В настоящее время наиболее изучены два ингибирующих сигнальных пути, при помощи которых опухолевые клетки уклоняются от иммунного надзора – CTLA‑4 и PD‑1/PD-L1.
CTLA‑4 фокусируется на регулировании активации Т-лимфоцитов, в то время как PD‑1 подавляет активность Т-лимфоцитов в периферических тканях, с тем чтобы избежать аутоиммунных реакций. Рецептор PD‑1 на поверхности Т-лимфоцитов, отвечающий за отрицательную регуляцию сигнала, имеет два лиганда – PD-L1 и PD-L2.
В ответ на иммунную атаку раковые клетки избыточно экспрессируют PD-L1 и тем самым подавляют активность Т-лимфоцитов в микроокружении опухоли, обеспечивая себе выживание и пролиферацию. Сигнальный путь PD‑1/PD-L1 регулирует подавление иммунитета посредством индукции апоптоза активированных Т-лимфоцитов или снижения их выживаемости [1].
При НМРЛ избыточная экспрессия PD‑1 на CD8+ Т-лимфоцитах предполагает уменьшение их пролиферации и продукции различных цитокинов. Аномальная экспрессия PD-L1 при НМРЛ наблюдается в 19-100% случаев и связана с плохим прогнозом. Было выявлено, что экспрессия PD-L1 на опухолевых клетках при НМРЛ значительно выше по сравнению с прилегающей паренхимой легкого.
Разработаны препараты – ингибиторы иммунных контрольных точек, воздействующие соответственно на PD‑1 и PD-L1 и предотвращающие ускользание опухоли от иммунного надзора. Блокирование PD‑1 и PD‑L1 дает сходные результаты, но блокирование PD-L1 связано с меньшим риском аутоиммунных реакций, поскольку остается активным PD‑1/PD-L2 путь регуляции иммунной системы. Следовательно, блокирование PD-L1 приводит к восстановлению противоопухолевого иммунитета и позволяет опухоль-специфическим Т-лимфоцитам раскрыть полный арсенал возможностей в отношении раковых клеток и минимально воздействовать на здоровые клетки [2].
Основной целью системной терапии при распространенном НМРЛ является уменьшение клинических проявлений заболевания, увеличение качества и продолжительности жизни при минимальной токсичности. За последние десятилетия с одобрением новых препаратов подход к терапии второй линии значительно изменился.
В 2015-2016 гг. в США для клинического применения при НМРЛ во второй линии терапии были одобрены препараты с анти-PD‑1 (ниволумаб и пембролизумаб) и анти-PD-L1 активностью (атезолизумаб). Прогноз пациентов с распространенным НМРЛ с прогрессированием заболевания после платиносодержащей терапии значительно улучшился с появлением этих препаратов.
Применение второй линии терапии в НМРЛ стало возможным в 2000 г. после публикации результатов двух рандомизированных исследований: доцетаксел во второй линии терапии показал увеличение выживаемости, качества жизни, контроль симптомов по сравнению с лучшей поддерживающей терапией и химиотерапией с винорелбином или ифосфамидом.
К 2009 г. в руководстве по системной терапии рака IV стадии Американского общества клинических онкологов (ASCO) были указаны четыре препарата для терапии второй линии: доцетаксел, пеметрексед, эрлотиниб и гефитиниб.
Пеметрексед ассоциируется с лучшей выживаемостью при неплоскоклеточной карциноме, а доцетаксел – при плоскоклеточном раке. Метаанализ шести рандомизированных исследований показал, что дуплетная химиотерапия не улучшает показателей выживаемости по сравнению с монотерапией, но ассоциирована с большей токсичностью. Несмотря на опции, доступные во второй линии терапии, клинические исходы долгое время оставались неблагоприятными. Частота ответа в среднем составляла <10%, а средняя продолжительность жизни – 7-9 мес от начала терапии второй линии [3].
Активное изучение возможностей таргетной терапии привело к созданию нового класса препаратов – ингибиторов тирозинкиназы. Активация EGFR запускает внутриклеточные сигнальные каскады, которые приводят к увеличению пролиферации раковых клеток, стимуляции процессов инвазии ангиогенеза и метастазирования. Препараты блокируют каскад сигнальных реакций, в результате чего угнетается пролиферация клеток и запускается внутренний путь клеточной гибели (Yarden et al., 2001, Jorissen et al., 2003).
Исследование III фазы BR.21 продемонстрировало увеличение выживаемости на фоне приема эрлотиниба во второй линии терапии по сравнению с плацебо (6,7 мес против 4,7). Таким образом, у пациентов с неопределенным типом EGFR, которые не являются кандидатами для дальнейшей ХТ, эрлотиниб может быть показан в качестве второй или третьей линии терапии. Хотя гефитиниб не превосходит плацебо в отношении выживаемости и качества жизни, он продемонстрировал сходные с доцетакселом результаты во второй линии терапии при НМРЛ [4].
Настоящим прорывом во второй линии терапии при НМРЛ стала разработка препаратов моноклональных антител, действие которых направлено не на разрушение опухолевых клеток, а на устранение иммуносупрессии, вызванной опухолью. Так, на фоне приема ниволумаба удалось достичь медианы выживаемости без прогрессирования (ВБП) 2,3 мес, а медианы общей выживаемости (ОВ) – 9,9 мес. При сравнении пембролизумаба с доцетакселом медиана ОВ составила 10,4 мес в группе терапии пембролизумабом в дозе 2 мг/кг, 12,7 мес в группе терапии пембролизумабом 10 мг/кг и 8,5 мес в группе доцетаксела. Точно так же атезолизумаб демонстрирует впечатляющие результаты: по сравнению с доцетакселом, медиана выживаемости составила 12,6 мес против 8,9.
Выбор режима системной терапии второй линии при НМРЛ у пациентов с прогрессированием заболевания во время или после терапии первой линии основывается на данных о специфической генетической мутации, гистологическом подтипе и клиническом течении заболевания, а также на общем состоянии пациента (функциональном статусе – ФС).
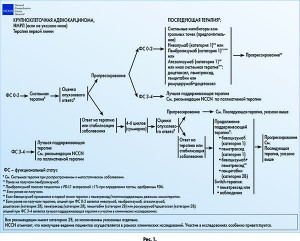
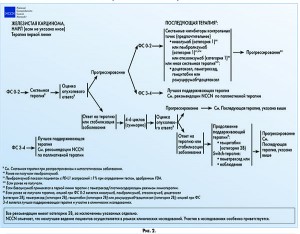
Вторая линия терапии применяется при прогрессировании заболевания после 4-6 циклов химиотерапии. Согласно рекомендациям NCCN (рекомендации по ведению пациентов с НМРЛ, 4.2017), ингибиторы контрольных точек (ниволумаб, пембролизумаб, атезолизумаб) предпочтительны во второй и последующей линиях терапии у пациентов с метастатическим НМРЛ при ФС 0-2, пембролизумаб показан пациентам с PD-L1 экспрессией ≥1% при определении тестом, одобренным Управлением по контролю качества пищевых продуктов и лекарственных препаратов США (FDA) (рис. 1 и 2). Применение ингибиторов контрольных точек ассоциировано с лучшей выживаемостью, более длительным ответом на терапию и меньшим количеством побочных явлений по сравнению с цитостатической химиотерапией. Возможными вариантами системной терапии являются доцетаксел (категория 2B), пеметрексед (категория 2B), гемцитабин (категория 2B) или рамуцирумаб+доцетаксел (категория 2B); при ФС 3-4 показана лучшая поддерживающая терапия и участие в клинических исследованиях.
Если опухоль отвечает на терапию первой линии или наблюдается стабилизация заболевания, то возможно проведение дальнейшей поддерживающей терапии в том же режиме. При крупноклеточной аденокарциноме это бевацизумаб, пеметрексед, бевацизумаб+пеметрексед, гемцитабин. При железистой карциноме – гемцитабин, в режиме Switch-терапии может использоваться пеметрексед [6].
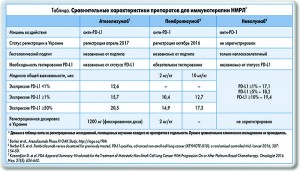
Рекомендация ниволумаба (категория 1) в качестве последующей терапии при железистом и нежелезистом НМРЛ основана на данных рандомизированного исследования III фазы (CheckMate‑057). Пембролизумаб показан согласно данным рандомизированных исследований II/III фазы (KEYNOTE‑10) и исследования KEYNOTE‑001. Атезолизумаб рекомендован при метастатическом железистом и нежелезистом НМРЛ по данным рандомизированного исследования III фазы OAK, а также исследования II фазы POPLAR. Все три препарата одобрены FDA и могут использоваться при НМРЛ. Выбор препарата для конкретного пациента производится с учетом особенностей действия этих препаратов, показаний, преимуществ и недостатков (табл.).
Предполагается, что использование PD-L1 в качестве терапевтической мишени будет сопровождаться меньшей токсичностью благодаря модуляции иммунного ответа селективно в микроокружении опухоли. Ингибирование PD-L1 является многообещающим направлением в иммунотерапии различных онкологических заболеваний, в том числе и НМРЛ.
Атезолизумаб представляет собой IgG1 антитело анти-PD-L1, способное препятствовать клеточно-опосредованной цитотоксичности в отношении нормальных активированных Т-клеток с экспрессией PD-L1. Он одобрен FDA для лечения пациентов с метастатическим НМРЛ, которые прогрессировали во время или после платиносодержащей химиотерапии. У пациентов с мутацией EGFR или ALK должны прогрессировать заболевания на соответствующей таргетной терапии перед приемом атезолизумаба.
В первом исследовании III фазы OAK применение ингибитора PD-L1 атезолизумаба у пациентов с НМРЛ, ранее получавших лечение, привело к значимому увеличению ОВ по сравнению со стандартной химиотерапией.
В исследовании OAK приняли участие 1225 пациентов с НМРЛ, которые ранее получили по крайней мере 1-2 линии химиотерапии, одна из которых включала в себя препараты платины. У всех пациентов предварительно определялся статус PD-L1. Проводилась также стратификация в зависимости от уровня экспрессии PD-L1, количества и схем предшествующей химиотерапии, а также данных гистологического исследования. Пациенты были рандомизированы на две группы в соотношении 1:1, одна группа получала атезолизумаб внутривенно в дозе 1200 мг каждые 3 недели, вторая – доцетаксел в дозе 75 мг/м2 каждые 3 недели.
Первичной конечной точкой была оценка ОВ:
– у всех пациентов, принимавших участие в исследовании;
– у пациентов в подгруппах ИК1/2/3 или ОК1/2/3 (с уровнем экспрессии PD-L1 ≥1% в иммунных и опухолевых клетках – ИК и ОК соответственно).
Вторичная конечная точка включала в себя частоту объективного ответа (ЧОО), ВБП, длительность ответа (ДО) и безопасность.
Первичный анализ данных 850 пациентов показал увеличение ОВ на 27% у тех, кто получал атезолизумаб, в сравнении с группой доцетаксела, независимо от уровня экспрессии PD-L1, в том числе с экспрессией PD-L1 <1%.
Медиана общей продолжительности жизни в общей популяции пациентов составила 13,8 мес в группе атезолизумаба и 9,6 мес в группе доцетаксела. После стратификации пациентов в зависимости от уровня экспрессии PD-L1 у пациентов с высоким уровнем экспрессии (55% участников) атезолизумаб показал увеличение ОВ на 59% по сравнению с пациентами, получавшими доцетаксел: медиана выживаемости составила 15,7 и 10,3 мес соответственно.
Значительное преимущество в ОВ наблюдалось у пациентов с максимальной экспрессией PD-L1 (ОК3 и ИК3), а это 16% больных: медиана выживаемости 20,5 мес против 8,9 в группе доцетаксела. Даже у PD-L1-негативных пациентов (ОК0 и ИК0) на фоне приема атезолизумаба ОВ была на 25% выше, чем у тех, кто принимал доцетаксел. Медиана выживаемости составила 12,6 (против 8,9 мес в группе доцетаксела). Преимущество в ОВ не зависело от данных гистологического заключения; улучшение показателей ОВ было сходным у больных с плоскоклеточным и неплоскоклеточным раком. Медиана продолжительности жизни у пациентов с неплоскоклеточным раком легкого составила 15,6 мес в группе атезолизумаба по сравнению с 11,2 мес в группе доцетаксела, аналогично и у пациентов с плоскоклеточным раком легкого – 8,9 и 7,7 мес.
Побочные эффекты 3-4 степени наблюдались у 15% пациентов группы атезолизумаба; на фоне терапии доцетакселом частота побочных эффектов составила 43%.
По результатам исследования, атезолизумаб был предложен в качестве второй линии терапии для пациентов с НМРЛ вне зависимости от статуса экспрессии PD-L1 клетками опухоли.
Таким образом, иммунотерапия при НМРЛ открывает новые возможности. По результатам многих исследований, применение моноклональных антител к PD-1/PD‑L1 значительно увеличивает ОВ. В исследовании OAK применение анти-PD-L1 антитела – атезолизумаба – привело к значимому увеличению ОВ по сравнению со стандартной химиотерапией. По результатам этого исследования атезолизумаб одобрен FDA для лечения пациентов с метастатическим НМРЛ, который прогрессировал во время или после платиносодержащей химиотерапии независимо от уровня PD-L1 экспрессии и гистологического подтипа опухоли.
Литература
1. He J., Hu Y. Development of PD‑1/PD-L1 Pathway in Tumor Immune Microenvironment and Treatment for Non-Small Cell Lung Cancer, 2015.
2. Ji M., Liu Y. PD‑1/PD-L1 pathway in non-small-cell lung cancer and its relation with EGFR mutation, 2015.
3. Historical Evolution of Second-Line Therapy in Non-Small Cell Lung Cancer, Chiara Lazzari, 2017.
4. Chan B.A., Hughes B.G. Targeted therapy for non-small cell lung cancer: current standards and the promise of the future, 2015.
5. Gettinger S. Immunotherapy of non-small cell lung cancer with immune checkpoint inhibition, 2017.
6. NCCN Guidelines Version 4.2017, Non-small cell lung cancer, 2017.
7. Rittmeyer A. et al. Atezolizumab versus docetaxel in patients with previously treated non-small-cell lung cancer (OAK): a phase 3, open-label, multicentre randomised controlled trial, 2016.
Подготовила Екатерина Марушко
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...