Хроническая суставная боль при остеоартрозе/остеоартрите: как помочь больному?
Заболевания костно-мышечной системы по распространенности в мировой популяции занимают 4-е место. При этом ревматологическая патология является одной из ведущих причин первичной инвалидности. На боли в суставах, существенно понижающие качество жизни, чаще всего жалуются пациенты на приеме у семейного врача. Своевременная диагностика и корректное лечение суставного синдрома (СС) позволяют максимально сохранить функцию суставов и социальную адаптацию пациентов.
Согласно данным статистики, у каждого 5-го пациента, обратившегося за медицинской помощью к врачу общей практики, имеет место СС той или иной степени выраженности. Своевременная и правильная интерпретация заболевания, назначение адекватного, в т. ч. патогенетического, лечения во многом определяют дальнейший прогноз и течение болезни, качество жизни пациента и сохранение трудоспособности (Триполка С. А., Благовещенская А. В., 2011).
В дифференциальной диагностике СС важную роль играют:
- пол, возраст, профессия, образ жизни пациента;
- суточная динамика болевого синдрома;
- предшествующие состояния (травма, инфекция, характер питания, прием лекарств, наличие глазных заболеваний).
При осмотре пациента и сборе анамнеза необходимо выяснить:
- характер начала заболевания – острое, подострое, хроническое, приступообразное (подагра), рецидивирующее, прогрессирующее;
- характер болей – воспалительный или механический;
- распространенность (моноартрит/полиартрит), локализацию (крупные/мелкие) и симметричность поражения суставов;
- наличие внесуставных проявлений.
В поисках правильного диагноза
Если причиной обращения пациента к врачу общей практики – семейной медицины является не травма, тогда СС связан, скорее всего, с остеоартрозом (ОА) – наиболее частым заболеванием суставов, клинические симптомы которого наблюдаются более чем у 10-20% населения земного шара. Ввиду высокого риска развития ограничений функции опорно-двигательного аппарата, которые приводят к нарушению трудоспособности и снижению качества жизни больного, важно выявлять ОА на ранних стадиях заболевания (Чичасова Н. В., 2014).
Болевой синдром – наиболее выраженный симптом при ОА. Именно сустав является при этом основным органом-мишенью, поэтому суставная боль в наибольшей степени определяет клинику заболевания.
Типы боли при ОА:
- Механические – возникают под влиянием дневной физической нагрузки и стихают в период ночного отдыха, что связано со снижением амортизационных способностей хряща и костных подхрящевых структур. Это самый частый тип болей при ОА.
- Непрерывные тупые ночные (чаще в первой половине ночи) – связаны с венозным стазом в субхондральной спонгиозной части кости и повышением внутрикостного давления.
- Стартовые – носят кратковременный характер (15-20 мин), возникают после периодов покоя и проходят в процессе двигательной активности. Обусловлены трением суставных поверхностей, на которых оседает детрит. При первых движениях в суставе детрит выталкивается в завороты суставной сумки.
- Блокада сустава – развивается вследствие ущемления «суставной мыши», т. е. костного или хрящевого фрагмента между суставными поверхностями. При этом типе боли невозможны даже минимальные движения в суставе.
- Постоянные – обусловлены рефлекторным спазмом близлежащих мышц, а также развитием реактивного синовита.
Если пациент испытывает хроническую суставную боль, которая позволяет заподозрить ОА, следует обратить внимание на другие признаки ОА:
- физикально определяемые крепитация, локальная болезненность, деформация суставов за счет разрастаний (узелки Гебердена и Бушара), припухлость, атрофия окружающих мышц;
- повышенные значения скорости оседания эритроцитов (СОЭ) при нормальных значениях общего анализа крови;
- лейкоцитоз в синовиальной жидкости в пределах 2000 в 1 мм3 за счет мононуклеаров.
Рентгенологические признаки:
- сужение суставной щели;
- остеосклероз;
- остеофитоз;
- кисты в костной ткани.
Как отличить ОА от других заболеваний, сопровождающихся СС?
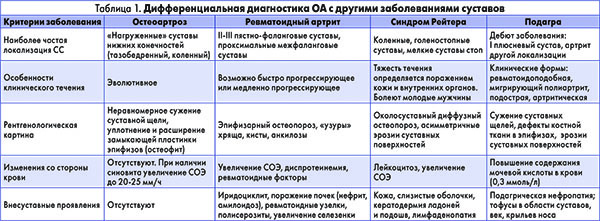
Чаще всего врачу приходится проводить дифференциальную диагностику между ОА, ревматоидным и реактивным артритом, подагрой (табл. 1.).
Правильно установить окончательный диагноз ОА позволяют диагностические критерии, приведенные в таблице 2.
Как диагностику, так и лечение ОА осуществляет врач-терапевт или семейный врач. Для лечения ОА применяют немедикаментозные методы и лекарственные препараты.
Немедикаментозные методы лечения ОА
В 2013 г. Европейская противоревматическая лига (European League Against Rheumatism – EULAR) опубликовала обширные рекомендации по нефармакологическому лечению ОА тазобедренных и коленных суставов. Документ рекомендует составлять для каждого пациента индивидуальный план терапии (уровень доказательств 1b), который должен включать следующее:
- информационные и обучающие материалы относительно контроля течения болезни;
- индивидуальную программу физических упражнений;
- сведения о поддержании физической активности и темпе выполнения нагрузок;
- мероприятия по снижению массы тела при избыточном весе и ожирении;
- рекомендации, направленные на минимизацию влияния негативных механических факторов (к примеру, ношение соответствующей обуви);
- советы по использованию вспомогательных устройств и соответствующих технологий для облегчения процесса ходьбы.
Ожирение существенно увеличивает нагрузку на суставы нижних конечностей, по значимости этот фактор даже превосходит наследственность. Снижение веса на 5 кг уменьшает риск возникновения симптомов ОА почти на 50%.
Групповые и индивидуальные занятия лечебной физкультурой (ЛФК) должны стать обязательной частью лечения больных ОА. Основные задачи ЛФК при ОА – предупреждение и коррекция функциональных нарушений; снижение болевого синдрома путем приспособления суставов к дозированной нагрузке; борьба с гипотрофией и атрофией мышц; повышение общего тонуса и трудоспособности. Лечебная гимнастика должна включать статические и динамические упражнения. Многие авторы считают, что следует рекомендовать пациентам смешанные программы. Для пациентов с ОА большое значение имеет ношение удобной обуви. Этот пункт в 2013 г. был единогласно одобрен рабочей группой EULAR (уровень доказательств Ib) (Вакуленко О. Ю. и соавт., 2016).
Терапия симптоматическая или модифицирующая?
Что касается медикаментозного лечения ОА, то препараты, использующиеся с этой целью, подразделяют на симптоматические средства быстрого действия (нестероидные противовоспалительные препараты – НПВП; опиоидные аналгетики, кортикостероиды и др.) и модифицирующие средства замедленного действия (глюкозамин, диацериин, хондроитин, гиалуроновая кислота, неомыляемые соединения авокадо и сои). Эффект последних проявляется более медленно, однако при этом он сохраняется по окончании их применения. Данные фармакологические агенты обладают хондромодифицирующим действием, предупреждая деградацию суставного хряща. Традиционно используемые НПВП оказывают симптоматическое действие: уменьшают болевой синдром и проявления воспаления в суставах. Основным недостатком препаратов этого класса является наличие выраженных побочных реакций, особенно в отношении желудочно-кишечного тракта (ЖКТ) и сердечно-сосудистой системы. Кроме того, некоторые НПВП отрицательно влияют на метаболизм суставного хряща. В большинстве случаев пациенты с ОА – лица пожилого возраста с множественной коморбидностью, поэтому применение НПВП у них допускается короткими (максимально безопасными) курсами для купирования острой боли.
Симптом-модицифицирующие препараты замедленного действия (symptomatic slow acting drugs for osteoarthritis – SYSADOA) потенциально способны положительно влиять на обменные процессы в хряще и замедлять прогрессирование болезни. Их действие на болевой синдром и функцию суставов сопоставимо с таковым НПВП (хотя и развивается значительно медленнее), но при этом безопасность при длительном применении несравнимо выше. Глюкозамин (ГА), образующийся в организме в виде глюкозамина 6-фосфата, является фундаментальным строительным блоком, необходимым для биосинтеза гликолипидов, гликопротеинов, гликозоаминогликанов, гиалуроната и протеогликанов. Хондроитинсульфат (ХС) – класс гликозаминогликанов, необходимый для формирования протеогликанов суставного хряща. ГА стимулирует биосинтез компонентов структурной матрицы сустава. ХС, абсорбируется ли он неповрежденным или в виде компонентов, обеспечивает дополнительный субстрат для формирования здоровой суставной матрицы, так как является компонентом протеогликанов. Как ГА, так и ХС способны повышать синтез протеогликанов и коллагена, уменьшать активность лейкоцитарной эластазы, коллагеназы и аггрекеназы, подавлять стимулированный интерлейкином‑1 синтез простагландинов фибробластами. В то же время имеются принципиальные различия между ГА и ХС в действии на субхондральную кость и синовиальную оболочку. Поэтому сочетанное применение ХС и ГА в комбинированных препаратах позволяет реализовать весь спектр механизмов их действия (Чичасова Н. В., 2014).
В 2014 г. были опубликованы рекомендации Европейского общества по клиническим и экономическим аспектам остеопороза и остеоартрита (Тhe European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis – ESCEO), которые содержат простой пошаговый алгоритм лечения ОА.
1-й шаг
- Препараты первой линии, которые необходимо назначить сразу после установления диагноза ОА, – парацетамол и SYSADOA (ГА и ХС).
- ГА и ХС – единственные препараты в группе SYSADOA, рекомендуемые для длительной терапии ОА.
- Наружные НПВП – могут быть назначены дополнительно для более результативной аналгезии с учетом их кратковременного симптоматического эффекта.
- Немедикаментозное лечение – обучение пациентов, снижение массы тела у пациентов с избыточным весом, создание соответствующей программы упражнений и др.
2-й шаг
- Назначение пероральных НПВП – не назначаются длительными, но могут применяться повторными курсами.
- Возможно введение кристаллических пролонгированных глюкокортикоидов и препаратов гиалуроновой кислоты.
При неэффективности лечения на первых двух шагах пациента следует направить к специалисту узкого профиля.
3-й шаг
Больным с далеко зашедшим ОА и выраженным болевым синдромом показаны слабые пероральные опиоиды или антидепрессанты, которые могут быть эффективны у лиц, не ответивших на предыдущую терапию.
4-й шаг
- Хирургическое лечение (эндопротезирование).
- Использование классических опиоидов как альтернативы для больных, которым противопоказано хирургическое вмешательство.
Для врачей-терапевтов и семейных врачей наиболее важны первые шаги, потому что грамотное лечение на этом этапе способно повлиять на течение ОА, замедлить разрушение хряща и отсрочить хирургическое вмешательство путем оптимальной комбинации методов физиотерапии, ЛФК и медикаментозной терапии с применением SYSADOA. Проведено большое количество исследований, где изучалась эффективность ГА и ХС в лечении ОА различной локализации. Результаты этих испытаний были обобщены в обзорах и метаанализах B. F. Leeb и соавт. (2000), T.E. McAlindon и соавт. (2000), F. Richi и соавт. (2003), T. E. Towheed и соавт. (2005). По данным L. Lippielo и соавт. (1999), совместное применение ХС и ГА в эксперименте увеличивало продукцию глюкозаминогликанов хондроцитами на 96,6% по сравнению с 32% при монотерапии.
Комбинированным препаратом с хондропротекторной активностью является Терафлекс®, представляющий собой комбинацию двух солей – XC (400 мг) и ГА гидрохлорида (500 мг) в одной капсуле. В 2003 г. R. J. Tallarida доказал, что более выраженным, по сравнению с другими комбинациями SYSADOA и НПВП, синергизмом обезболивающих эффектов обладает комбинация ГА сульфата и ибупрофена; то есть дополнительное назначение ГА сульфата позволяет достичь хорошего клинического результата при использовании меньшей дозы ибупрофена. Это послужило основанием для создания препарата Терафлекс Адванс®, в котором объединены ибупрофен, ГА сульфат и ХС. Этот препарат быстро снижает болевой синдром и длительное время поддерживает модифицирующий эффект. Доза ибупрофена в препарате в 2 раза меньше средней и в 4 раза меньше максимальной, которые используются в терапевтической практике. Терафлекс Адванс® содержит: ХС 200 мг, ГА сульфата 250 мг и ибупрофена 100 мг.
Таким образом, ОА остается серьезной медико-социальной проблемой в связи с высоким риском утраты функции пораженных суставов и инвалидизации пациента. Лечение ОА проводят немедикаментозными методами, симптоматическими препаратами быстрого действия и SYSADOA. ГА и ХС способны модифицировать обменные процессы в хряще и замедлять прогрессирование ОА, а их действие на болевой синдром и функцию суставов развивается хотя и более медленно, но сопоставимо с таковым НПВП.
Препарат Терафлекс® оказывает на больных ОА достоверное симптом-модифицирующее действие, проявляющееся в уменьшении боли, скованности и улучшении двигательной активности. Последовательный прием Терафлекса Адванс с переходом на Терафлекс® позволяет добиться более быстрого обезболивающего эффекта и тем самым улучшить комплайенс пациентов. Применение Терафлекса позволяет уменьшить потребность в НПВП, а длительное (2-3 года) проведение повторных курсов лечения этим препаратом позволяет добиться долгосрочного симптом-модифицирующего эффекта. Терафлекс® безопасен, хорошо переносится и может быть рекомендован пациентам с ОА и коморбидными состояниями.
Подготовила Мария Маковецкая
Медична газета «Здоров’я України 21 сторіччя» № 6 (403), березень 2017 р.
СТАТТІ ЗА ТЕМОЮ Ревматологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....
Зв’язок між рівнем сироваткової сечової кислоти (ССК) і ризиком серцево-судинних захворювань (ССЗ) упродовж багатьох років є предметом вивчення дослідників. Установлено, що рівень ССК – незалежний предиктор смерті від усіх причин і серцево-судинної смерті, зокрема від гострого коронарного синдрому, інсульту та серцевої недостатності (СН). Також опубліковано багато робіт про зв’язок між ССК і функцією нирок. Попри значну кількість публікацій, деякі моменти, а саме: яким є оптимальний поріг ССК для визначення ризику ССЗ, чи необхідна корекція значень ССК для функції нирок, чи є ССК ключовим патологічним елементом метаболічної дисрегуляції, потребують прояснення....