Лекарственные поражения печени – «темная сторона» медикаментозной терапии
За последние десятилетия распространенность лекарственных поражений печени (ЛПП) многократно возросла, стойкая тенденция к дальнейшему росту сохраняется и в настоящий момент. Поскольку ЛПП является диагнозом исключения и часто воспринимается лечащим врачом как побочный эффект, то лечение либо отсутствует, либо назначается с большим опозданием.
Отличить симптомы основного заболевания от побочных эффектов терапии порой бывает действительно непросто, и во многих случаях ЛПП диагностируются поздно или вообще рассматриваются вне связи с приемом медикаментов. Однако, согласно имеющимся в литературе сведениям, ЛПП встречаются в общей медицинской практике с частотой как минимум 1 случай на 1 тыс. пролеченных пациентов, составляя 10% всех побочных реакций медикаментозной терапии. В структуре нежелательных явлений, связанных с приемом препаратов, частота лекарственных гепатитов варьирует в пределах от 1 до 28%. Истинная распространенность ЛПП представляется еще более высокой. Примерно у 2% больных, госпитализированных по поводу желтухи, ее причиной оказываются лекарства. В США в 25% случаев фульминантная печеночная недостаточность обусловлена применением медикаментов (Полунина Т. Е., Маев И. В., 2011; Еремина Е. Ю., 2012). При обследовании больных с хроническим гепатитом неясной этиологии в 10% случаев изменение лабораторных показателей можно связать с приемом лекарств. Среди больных старше 50 лет этот показатель достигает 40% (Хомерики С. Г., Хомерики Н. М., 2012).
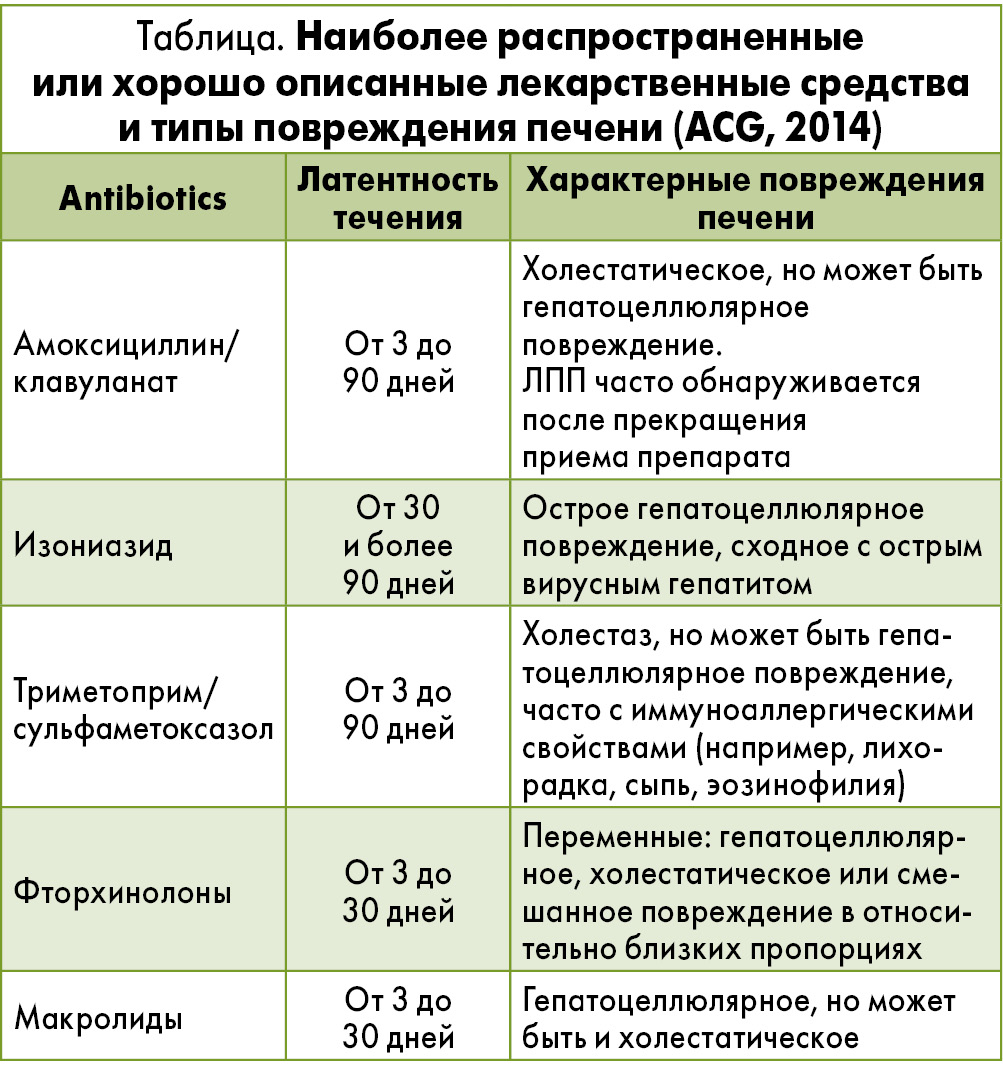 Достаточно высокие показатели распространенности ЛПП во многом связаны со свободным доступом населения к безрецептурным лекарственным средствам. С одной стороны, продвижение многих безрецептурных препаратов подкреплено достаточно агрессивной рекламой, с другой – большинство конечных потребителей (и, к сожалению, некоторые врачи) уверены в безопасности средств, отпускаемых без рецепта (например, фитопрепаратов), и не располагают информацией о возможных побочных эффектах. Между тем, в 2014 году в The American Journal of Gastroenterology были опубликованы клинические рекомендации по ведению пациентов с ЛПП (Chalasani N. P., Hayashi P. H. et al., 2014). В данных рекомендациях подчеркивается, что противомикробные средства, фитопрепараты и биологически активные пищевые добавки (БАД) занимают лидирующие позиции среди причин ЛПП в западных странах. Антибиотики как основной класс лекарственных средств, приводящих к ЛПП, отмечены и другими авторами (Devarbhabi H., 2012). Наибольшее значение в развитии ЛПП вследствие приема антибактериальных препаратов имеют аминопенициллины (табл.).
Достаточно высокие показатели распространенности ЛПП во многом связаны со свободным доступом населения к безрецептурным лекарственным средствам. С одной стороны, продвижение многих безрецептурных препаратов подкреплено достаточно агрессивной рекламой, с другой – большинство конечных потребителей (и, к сожалению, некоторые врачи) уверены в безопасности средств, отпускаемых без рецепта (например, фитопрепаратов), и не располагают информацией о возможных побочных эффектах. Между тем, в 2014 году в The American Journal of Gastroenterology были опубликованы клинические рекомендации по ведению пациентов с ЛПП (Chalasani N. P., Hayashi P. H. et al., 2014). В данных рекомендациях подчеркивается, что противомикробные средства, фитопрепараты и биологически активные пищевые добавки (БАД) занимают лидирующие позиции среди причин ЛПП в западных странах. Антибиотики как основной класс лекарственных средств, приводящих к ЛПП, отмечены и другими авторами (Devarbhabi H., 2012). Наибольшее значение в развитии ЛПП вследствие приема антибактериальных препаратов имеют аминопенициллины (табл.).
Поскольку ЛПП – это диагноз исключения, важно тщательное изучение анамнеза. В этой связи врачу необходимо помнить, что любое лекарственное средство, растительный препарат или БАД могут привести к развитию ЛПП (Еремина Е. Ю., 2012). Помимо антибиотиков, растительных препаратов и БАД, ЛПП наиболее часто обусловливают гормональные контрацептивы, нестероидные противовоспалительные препараты (НПВП), антигистаминные, пероральные сахароснижающие, системные противогрибковые и противотуберкулезные средства. Некоторые препараты не вызывают клиническую картину острого лекарственного гепатита или холестаза, а приводят к прогрессирующему в течение месяцев и лет повреждению печени. К таким препаратам относятся метотрексат, азатиоприн, оральные контрацептивы, тамоксифен (Devarbhabi H., 2012).
Факторы риска ЛПП чрезвычайно многообразны и условно разделены на внешние и внутренние. К внешним относятся употребление алкоголя, одновременный прием нескольких медикаментов, аллергические реакции на лекарственное средство в анамнезе. Отдельное значение имеют доза, длительность и способ введения препарата, особенности его фармакокинетики и иммуногенность. К внутренним факторам риска можно причислить женский пол, генетическую предрасположенность (различия в активности ферментов, метаболизирующих лекарства), возраст старше 40 лет, беременность, ожирение, кахексию, сопутствующие хронические заболевания печени, почек, сердца. Одну из ключевых ролей в возникновении ЛПП играет полипрагмазия. Так, при одновременном приеме 6 препаратов вероятность ЛПП достигает 80%, а нерациональные сочетания лекарственных средств являются причиной 35% ЛПП.
Имеется определенная специфика развития ЛПП у различных категорий пациентов. У детей ЛПП развиваются редко. У женщин в постменопаузе печень особенно чувствительна к НПВП, у молодых пациентов – к парацетамолу и ацетилсалициловой кислоте, у пожилых – к противотуберкулезным препаратам, нитрофуранам и другим антибиотикам. Пациенты, имеющие хронические заболевания печени (неалкогольный стеатоз, вирусный гепатит и т. д.), более подвержены гепатотоксическому воздействию лекарственных средств и их метаболитов. Группу риска также составляют беременные, особенно с различными формами гестозов, жировым гепатозом, внутрипеченочным холестазом, принимавшие ранее пероральные контрацептивы, перенесшие процедуру экстракорпорального оплодотворения. В литературе имеются данные о том, что потенциально фатальное осложнение, наблюдаемое у данного контингента, – острая жировая печень беременных, – в 21% случаев ассоциируется с приемом лекарств (Еремина Е. Ю., 2012).
Холестаз – одно из самых частых проявлений ЛПП. В отличие от лекарственных гепатитов холестатический вариант ЛПП характеризуется меньшей летальностью и является более доброкачественным. Однако именно холестатические варианты ЛПП чаще приобретают затяжное и хроническое течение (Devarbhabi H., 2012). В ряде случаев к нарушению оттока желчи присоединяется поражение желчных протоков по типу острого или хронического холангита. Различают канальцевый, паренхиматозно-канальцевый и внутрипротоковый холестаз. ЛПП по типу канальцевого холестаза часто связано с приемом гормональных препаратов, имеющих в своем составе циклопентанпергидрофенантреновое кольцо (андрогенов и эстрогенов), а также циклоспорина А. Клинически у таких пациентов наблюдаются кожный зуд при незначительном уровне билирубинемии и транзиторное увеличение трансаминаз. Повышение щелочной фосфатазы регистрируется не всегда, часто ее концентрация остается в пределах нормы. Для внутрипротокового холестаза характерно заполнение протоков и канальцев сгустками концентрированной желчи без воспалительной реакции в окружающих тканях. Данный тип ЛПП встречается довольно редко.
Паренхиматозно-канальцевый холестаз – наиболее частый вариант холестатического синдрома у пациентов с ЛПП, которому наряду с нарушением оттока желчи присуще значительное повреждение гепатоцитов, что связывают с иммунным поражением клеток печени. При этом варианте холестатического синдрома клинические проявления холестаза могут сохраняться в течение нескольких месяцев и даже лет, несмотря на отмену причинного препарата. Паренхиматозно-канальцевый холестаз чаще всего вызывают хлорпромазин, сульфаниламиды, полусинтетические и синтетические пенициллины (оксациллин, ампициллин, амоксициллин, карбенициллин, метициллин, флуклоксациллин), макролиды (эритромицин, олеандомицин), блокаторы Н2-гистаминовых рецепторов (циметидин, ранитидин), некоторые пероральные сахароснижающие препараты (гликлазид, глибенкламид) (Хомерики С. Г., Хомерики Н. М., 2012).
Перечисленные выше медикаменты широко используются в клинической практике у пациентов всех возрастов и категорий. Это означает, что врач любой специальности потенциально может столкнуться с ЛПП на фоне стандартной, адекватно назначенной терапии. Пациенты с установленным ЛПП должны проходить клиническое и биохимическое обследование до полного разрешения процесса. К сожалению, примерно у 15-20% пациентов острое ЛПП приобретает хроническое течение, поэтому отмены препарата, вызвавшего данное состояние, недостаточно; требуется профильное лечение.
Как показывают клинические наблюдения, лечение тяжелых ЛПП кортикостероидами (в режиме пульс-терапии или последовательного снижения дозы) и урсодезоксихолевой кислотой (УДХК) является безопасным методом и приводит к более быстрому снижению уровней билирубина и трансаминаз, чем отсутствие соответствующей терапии (Wree A. et al., 2011). УДХК (наряду с аллопуринолом и мелатонином) обладает терапевтическим потенциалом в защите от циклоспорининдуцированного повреждения печени (Akbulut S. et al., 2015). УДХК также зарекомендовала себя как эффективный гепатопротектор при ЛПП, вызванном амоксициллином/клавуланатом (El-Sherbiny G.A. et al., 2009). Эти данные позволяют рекомендовать УДХК в качестве препарата выбора при ЛПП, сопровождающихся холестазом.
Урсохол – современный препарат УДХК отечественного производства, который обладает широким спектром терапевтических эффектов, в том числе холеретическим, литолитическим, гипохолестеринемическим, цитопротекторным, антиапоптотическим, антифибротическим, антиоксидантным, иммуномодулирующим. Молекула УДХК способна встраиваться в фосфолипидный слой клеточной мембраны, делая ее более устойчивой по отношению к повреждающим факторам. Урсохол снижает всасывание холестерина в кишечнике, его синтез в печени и экскрецию в желчь, уменьшает литогенность и улучшает реологические свойства желчи.
Антихолестатические свойства Урсохола реализуются путем снижения концентрации токсичных для печеночной клетки желчных кислот через активацию Са2+-зависимой протеинкиназы и стимуляции экзоцитоза в гепатоцитах. Кроме того, Урсохол как холеретик индуцирует выделение желчи, богатой бикарбонатами, что приводит к увеличению пассажа желчи и более активному выведению токсичных желчных кислот через кишечник. Литолитическую активность Урсохол демонстрирует путем формирования жидких кристаллов с молекулами холестерина, что предупреждает образование и стимулирует растворение холестериновых камней. Снижение всасывания холестерина в кишечнике и уменьшение его синтеза в печени объясняют гипохолестеринемическое действие препарата. Иммуномодулирующий эффект Урсохола обусловлен уменьшением экспрессии антигенов гистосовместимости HLA‑1 на гепатоците и HLA‑2 на холангиоците, нормализацией активности естественных киллеров, снижением продукции сенсибилизированных к печеночной ткани цитотоксичных Т-лимфоцитов и уменьшением повреждения печеночной паренхимы иммуноглобулинами. Антифибротическое влияние выражается в снижении апоптозиндуцированной активации звездчатых клеток печени, ответственных за фиброгенез, уменьшении уровня маркеров фиброгенеза, стабилизации цитохрома Р450 и щелочной фосфатазы, подавлении коллагенообразования. УДХК достоверно замедляет прогрессирование фиброза у пациентов с первичным билиарным циррозом и снижает риск развития варикозного расширения вен пищевода. Благодаря блокаде высвобождения свободных радикалов и торможению процессов перекисного окисления липидов Урсохол оказывает антиоксидантный эффект.
Описанные эффекты позволяют рекомендовать Урсохол к применению в лечении пациентов с медикаментозным повреждением печени и синдромом холестаза, поскольку молекула УДХК эффективно воздействует на все патогенетические звенья ЛПП.
Таким образом, ЛПП – серьезная проблема современной медицины, которая выходит за рамки гепатологии. К ЛПП может приводить прием антибактериальных средств, гормональных контрацептивов, сахароснижающих, антигистаминных медикаментов, а также растительных препаратов и БАД. Синдром холестаза – одно из наиболее частых клинических проявлений ЛПП. Учитывая иммунно-воспалительный патогенез холестаза при ЛПП, можно утверждать, что УДХК является оптимальной молекулой для лечения ЛПП. Урсохол – современный украинский препарат УДХК, обладающий гепатопротекторным, холеретическим, иммуномодулирующим, антиапоптотическим и антифибротическим эффектами, необходимыми для терапии ЛПП.
Подготовила Мария Марчук
Медична газета «Здоров’я України 21 сторіччя» № 4 (425), лютий 2018 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...




