Роль коррекции фолиеводефицитных состояний в профилактике акушерских и перинатальных осложнений
Важность создания максимально благоприятных условий для раннего развития плода доказана в ряде масштабных эпидемиологических исследований. Кроме того, за последнее время получены дополнительные данные о фундаментальной роли метилирования ДНК в функционировании эпигенетического механизма, который формируется в эмбриогенезе и оказывает значительное влияние на здоровье человека в последующем.
Для адекватного метилирования требуется соответствующий метаболизм фолатов, обеспечивающий метаболизм аминокислот, биосинтез пурина и пиримидина – строительных блоков для синтеза ДНК и РНК, а также образование первичного метилирующего агента S-аденозилметионина (SAM), являющегося универсальным донором для ДНК, гистонов, белков и липидов. Обеспечить адекватный фолатный обмен во время беременности может поступление в организм женщины надлежащего количества фолиевой кислоты в преконцепционном периоде и в ранней гестации.
Биологические эффекты фолиевой кислоты
Фолиевая кислота – синтетическая диетическая добавка, которая содержится в искусственно обогащенных пищевых продуктах и фармацевтических витаминах. Термин «фолат» (витамин B9, один из 13 эссенциальных витаминов) обычно используется в качестве общего названия группы химически родственных соединений на основе структуры фолиевой кислоты.
Витамин В9 не может быть синтезирован de novo организмом и должен поступать либо из пищевых продуктов, либо из диетических добавок, при этом ни фолат, ни фолиевая кислота не являются метаболически активными и должны быть метаболизированы в l‑5-метилтетрагидрофолат (1-метилфолат) – преобладающую микронутриентную форму, которая циркулирует в плазме и участвует в биологических процессах.
Профилактика акушерских и перинатальных осложнений с помощью применения фолиевой кислоты
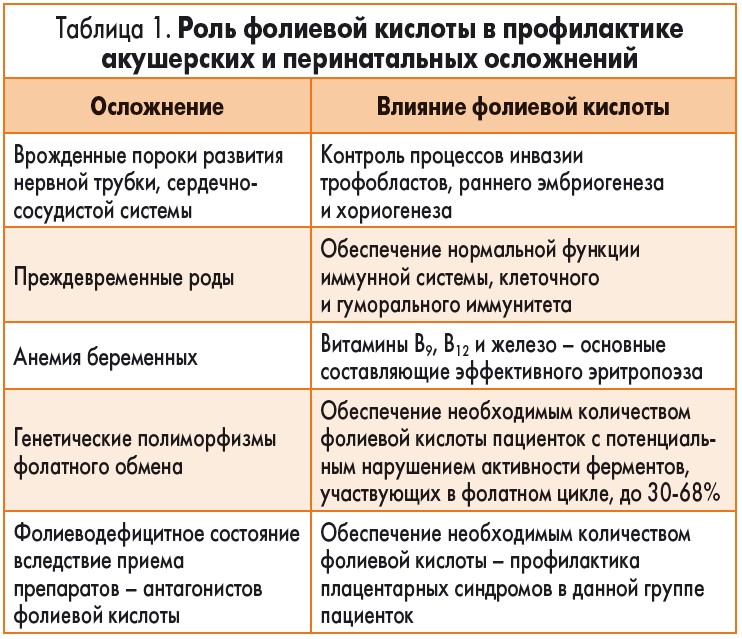
На сегодняшний день доказано, что роль фолиевой кислоты в профилактике акушерских и перинатальных осложнений намного больше, чем только профилактика врожденных пороков развития (табл. 1).
Профилактика врожденных пороков нервной и сердечно-сосудистой систем
Врожденные пороки сердца и центральной нервной системы являются причиной не только около 50% смертей детей (40 и 10% соответственно) от врожденных аномалий во всем мире, но и высокой заболеваемости, дистресса и серьезных физических, психологических и социальных нарушений у детей.
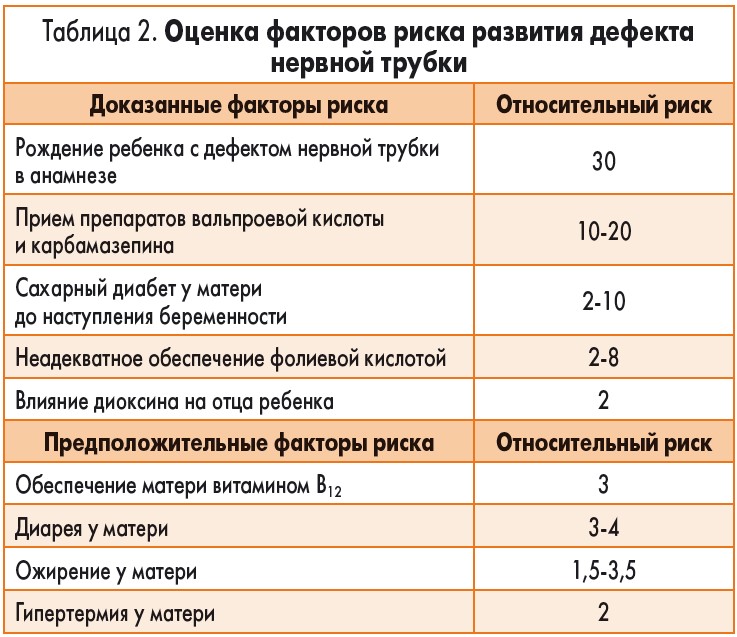
Причины врожденных аномалий остаются неизвестными в 50-60% случаев, эпигенетические и многофакторные причины выявляются в 20-25% случаев, хромосомные или генетические с единственной генной мутацией – почти в 15% случаев, эпигенетические, приобретенные и монофакторные, под влиянием воздействия окружающей среды (тяжелая патология у матери, инфекции, медикаменты, ионизирующее излучение и алкоголь) – примерно в 10% случаев (табл. 2) [6, 7].
Поэтому роль фолиевой кислоты как агента, обеспечивающего адекватность одноуглеродного метаболизма, влияющего на основные ДНК-процессы, бесспорна в отношении эпигенетического влияния, предупреждения последствий генетического полиморфизма, действия приобретенных и монофакторных причин.
Многочисленными исследованиями доказана эффективность добавок фолиевой кислоты в профилактике врожденных пороков развития.
Национальный институт здоровья США и Институт медицины рекомендуют прием 600 мкг фолиевой кислоты ежедневно в І триместре беременности и продолжение приема на протяжении всей беременности с последующим уменьшением дозы до 500 мкг во время лактации [4, 6, 7].
В настоящее время американские рекомендации по профилактическому приему фолиевой кислоты включают:
- для женщин с высоким риском рождения ребенка с дефектом нервной трубки (ДНТ) – родившим ребенка с ДНТ, а также с наличием ДНТ в семейном и личном анамнезе, принимающим препараты – антагонисты фолиевой кислоты – 5 мг фолиевой кислоты ежедневно до зачатия;
- для женщин репродуктивного возраста – от 0,4 до 1 мг фолиевой кислоты ежедневно в течение по меньшей мере 2-3 мес до зачатия, во время беременности и в послеродовом периоде.
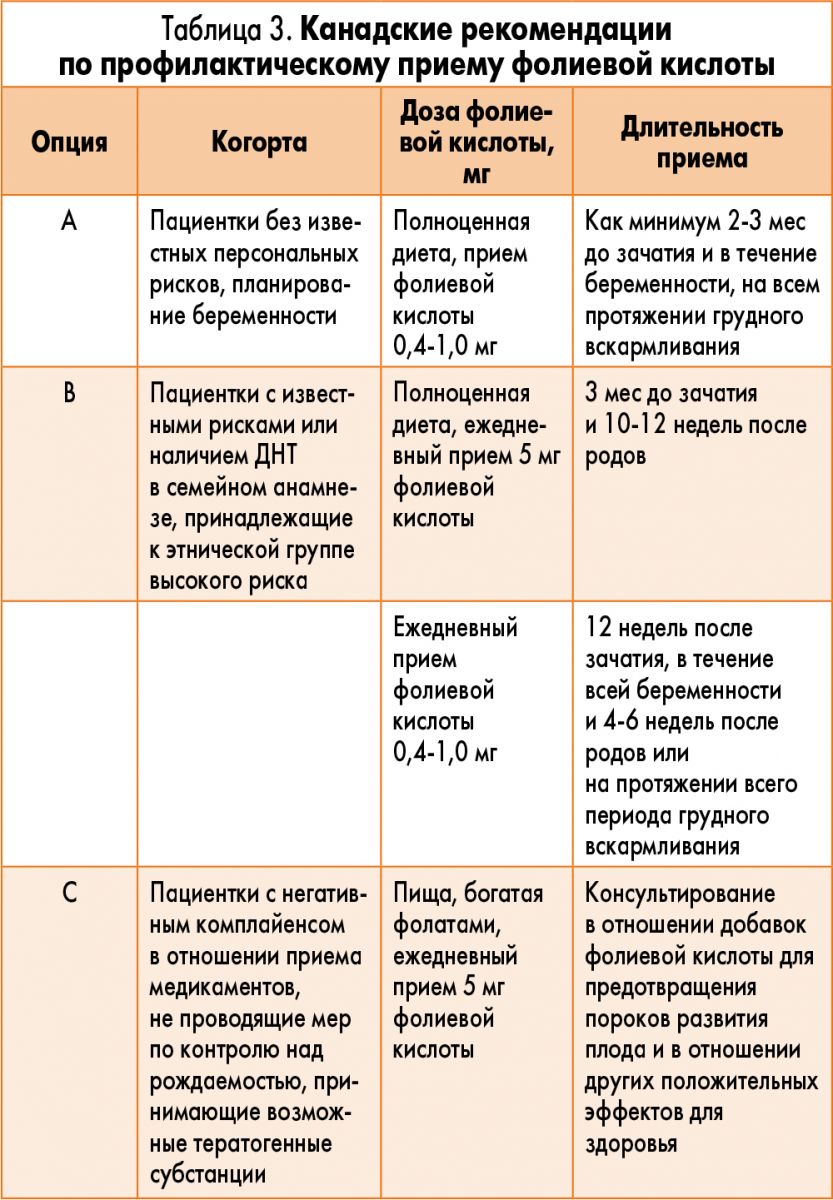
- Канадские рекомендации представлены в таблице 3 [8].
Роль фолиевой кислоты в профилактике преждевременных родов
Проблема профилактики преждевременных родов весьма актуальна, поскольку на сегодняшний день есть только один перспективный метод – применение препаратов прогестерона, но его эффективность доказана лишь в ограниченной когорте женщин с преждевременными родами в анамнезе или с короткой шейкой матки, что составляет, соответственно, 3,3 и 1,7% всех беременных, находящихся в группе риска [1, 3, 5].
Необходимы методы, позволяющие проводить профилактику спонтанных преждевременных родов в больших группах женщин. В ряде исследований доказана связь между более низкими концентрациями фолиевой кислоты и более короткой продолжительностью беременности. Кроме того, исследования на животных моделях показали, что недостаточная продолжительность беременности может быть последствием неблагоприятных условий для зачатия и раннего эмбрио- и хориогенеза.
В США проведено исследование FASTER (1999-2002 гг.), в которое включено 34 480 женщин с одноплодной беременностью. Всех испытуемых опрашивали о дозе и продолжительности приема фолиевой кислоты в І триместре беременности.
Доказано, что в группе женщин, принимавших фолатные добавки в течение ≥1 года, частота спонтанных преждевременных родов была значительно ниже, чем в группе не принимавших (относительный риск – ОР – 0,22 для родов в 20-28 недель, 0,45 – для родов в сроке 28-32 недели, 95% доверительный интервал).
Основным выводом данного исследования было то, что преконцепционный прием фолата уменьшал риск спонтанных преждевременных родов, эта ассоциация была сильной, специфической, дозозависимой. Кроме того, продолжительность приема фолиевой кислоты может быть столь же важна, как и доза [1, 3, 4].
Вероятно, положительное воздействие фолиевой кислоты на профилактику преждевременных родов объясняется тем, что нормальный обмен фолатов является важным для иммунной функции, что, в свою очередь, является необходимым условием для противодействия аномальному воспалительному ответу, одному из ведущих причин патогенеза преждевременных родов.
У людей с фолиеводефицитными состояниями имеет место дисфункция клеточно-опосредованного и гуморального иммунитета, кроме того, снижение фагоцитарных и бактерицидных способностей полиморфно-ядерных лейкоцитов, что приводит к повышенной восприимчивости к инфекциям, в том числе к бессимптомной бактериурии.
Получены доказательства, что профилактический прием фолиевой кислоты не только улучшает функцию иммунной системы, но способствует снижению циркулирующих биомаркеров воспаления, включая α1-ацидный гликопротеин и C-реактивный белок [1, 3, 4].
Кроме того, в последнее время обнаружено несколько генетических вариаций в ключевых генах, участвующих в метаболизме фолиевой кислоты и ответственных за преждевременные роды. Один из таких вариантов включает делецию пары (bp) 19 гена в гене DHFR. Делеционный аллель DHFR19-bp препятствует метаболизму фолата и переносу восстановленного фолата через плаценту.
Другим примером является изменение последовательности аминокислот в гене SHMT1, что приводит к меньшей транскрипционной активности оксиметилтрансферазы‑1 серина и связано с повышенным риском спонтанных преждевременных родов [1, 3, 5, 6].
Роль фолиевой кислоты в профилактике анемии у беременных
Как известно, во время беременности увеличивается объем циркулирующей крови, в основном за счет плазмы, что приводит к гемодилюции. Кроме того, повышается потребность в железе для обеспечения нужд плода и матери, что приводит к изменениям эритропоэза.
Для обеспечения адекватного эритропоэза необходимо наличие достаточных ресурсов трех основных субстанций: фолиевой кислоты, кобаламина (витамина B12) и железа, что позволяет осуществить адекватный перенос метильной группы из l-метилфолата в гомоцистеин через метилкобаламин для восстановления в метионин.
Таким образом, в условиях низкого уровня фолата и/или витамина B12 может возникнуть анемия, что требует приема доз фолиевой кислоты 0,4-0,8 мг и кобаламина на протяжении всей беременности [2, 4-6].
Генетические полиморфизмы и метаболизм фолиевой кислоты: оценка влияния
Генетические вариации в некоторых случаях могут приводить к образованию протеинов с измененной биологической активностью. Среди белков, принимающих участие в метаболизме фолатов, идентифицированы такие гены. Наиболее изучены метаболические процессы, задействующие донацию метильных групп, которые регулируются ферментом MTHFR (метилтетрагидрофолат-редуктаза).
Выявлено, что в США до 60% населения являются гетерозиготными для генетического полиморфизма фермента MTHFR, в то время как около 25% – гомозиготны для этих генетических вариаций. В той или иной степени эти полиморфизмы ухудшают превращение фолата в его активную форму – 1-метилфолат.
Так, у людей, имеющих признаки нарушенного метаболизма фолатов, отмечается гомозиготность по общему варианту генотипа MTHFR677C->Т. При гомозиготном варианте регистрируется нарушение метаболизма фолата и около 30% активности фермента, обнаруженного у пациентов с вариантом дикого типа (CC), а при гетерозиготном типе – 65% активности.
При другом варианте полиморфизма MTHFR1298A->C у гомозиготных индивидуумов может проявляться каталитическая активность фермента, которая снижается до 68% активности дикого типа. В данных группах пациентов необходима тщательная профилактика фолиеводефицитных состояний [3, 5, 7, 8].
Профилактика фолиеводефицитных состояний у пациенток, получающих антагонисты фолиевой кислоты
Антагонисты фолиевой кислоты используются в лечении ряда заболеваний, включая эпилептические приступы, нарушения настроения и инфекции мочевых путей. Антагонисты фолиевой кислоты можно разделить на две группы: ингибиторы фермента DHFR (сульфаметоксазол-триметоприм) и другие антагонисты фолиевой кислоты, состоящие в основном из противосудорожных препаратов (фенобарбитал, фенитоин, примидон и карбамазепин), а также спазмофен (спазмолитический препарат, который содержит низкие дозы фенобарбитала) и холестирамин.
В ряде исследований (группа получавших ингибиторы DHFR составила 12 546 человек, другие антагонисты фолиевой кислоты – 1565 человек) доказано повышение риска развития преэклампсии, тяжелой преэклампсии, преждевременной отслойки нормально расположенной плаценты, задержки роста плода и антенатальной гибели плода (скорректированный ОР, соответственно, 1,52; 1,77; 1,32; 1,22; 1,35).
Это объясняется тем, что дефицит фолата может влиять на повышение частоты аномалий имплантации и плацентации, на ранние стадии формирования плаценты, особенно на регулирование инвазии трофобластов, а впоследствии эти ранние нарушения приводят к развитию плацентарных синдромов [1, 3, 5-7].
Поэтому группе пациенток, получающих препараты с антифолатным действием для лечения основного заболевания, требуется проведение мультидисциплинарного преконцепционного консультирования, возможно, коррекция терапии и обязательная профилактика дефицита фолатов в период прегравидарной подготовки.
Итак, ключевыми основаниями необходимости профилактики дефицита фолиевой кислотой в периконцепционном периоде и во время беременности являются:
- роль периконцепционной профилактики фолиеводефицитных состояний намного шире, чем только профилактика врожденных пороков развития;
- необходим дифференцированный подход к определению дозы и длительности профилактики фолиеводефицитных состояний;
- женщинам без доказанных нарушений фолатного обмена в периконцепционном периоде с профилактической целью назначается доза фолиевой кислоты 0,4-1,0 мг. Национальный институт здоровья США рекомендует дозу во время гестации 0,6 мг с последующим переходом на 0,5 мг во время лактации при условии полноценного питания женщины;
- для профилактики дефицита железа и развития железодефицитной анемии, кроме обеспечения фолиевой кислотой, целесообразен прием витамина В12, железа и других необходимых организму матери нутриентов как в ходе прегравидарной подготовки, так и во время беременности и лактации. Наиболее часто для этого используют доступные на рынке витаминно-минеральные комплексы (ВМК).
Учитывая серьезность описанных клинических ситуаций, решение о рекомендации таких ВМК должно основываться на критериях ответственного выбора [10]:
- регистрация в статусе лекарственного средства, свидетельствующая о наличии полного регистрационного досье с данными клинических исследований эффективности и безопасности препарата;
- производство, обеспечивающее высокий стандарт качества (подтвержденный сертификатом GMP), промежуточный контроль и анализ качества готовой лекарственной формы в соответствии с международными стандартами;
- соответствие состава и суточных доз активных ингредиентов ВМК современным международным рекомендациям по прегравидарной подготовке для профилактики врожденных пороков развития плода и анемии;
- доказательная база эффективности и безопасности применения готовой лекарственной формы по зарегистрированным показаниям.
Этим требованиям в полной мере соответствует Элевит® Пронаталь – лекарственное средство, содержащее 12 витаминов, 7 макро- и микроэлементов в оптимальном для беременных количестве (витамины: А – 3600 ME, В1 – 1,6 мг, В2 – 1,8 мг, В6 – 2,6 мг, В12 – 4 мкг, С – 100 мг, D3 – 500 ME, Е – 15 мг, биотин – 0,2 мг, пантотенат кальция – 10 мг, никотинамид – 19 мг; кальций – 125 мг, магний – 100 мг, фосфор – 125 мг, железо – 60 мг, медь – 1 мг, марганец – 1 мг, цинк – 7,5 мг, фолиевая кислота – 800 мкг).
На сегодняшний день Элевит® Пронаталь – единственный ВМК для беременных и женщин, планирующих беременность, с клинически доказанной эффективностью в отношении предупреждения целого ряда врожденных пороков развития, продемонстрированной в серии клинических исследований с участием 11 262 женщин [9].
Литература
1. Behrman R.E., Butler A.S., editors. Preterm Birth: Causes, Consequences, and Prevention. Institute of Medicine. Washington, DC: The National Academies Press; 2007.
2. Bentley S., Hermes A., Phillips D. et al. Comparative effectiveness of a prenatal medical food to prenatal vitamins on hemoglobin levels and adverse outcomes: a retrospective analysis. Clin Therapeut. 2011; 33: 204-210.
3. Bodnar L.M., Himes K.P., Venkataramanan R. et al. Maternal serum folate species in early pregnancy and risk of preterm birth. Am J Clin Nutr. 2010; 92: 864-871.
4. Bukowski R., Malone F.D., Porter F.T. et al. Preconceptional folate supplementation and the risk of spontaneous preterm birth: a cohort study. PLoS Med. 2009; 6.
5. De Regil L.M., Fernandez-Gaxiola A.C., Dowswell T., Pena-Rosas J.P. Effects and safety of periconceptional folate supplementation for preventing birth defects. Cochrane Database Syst Rev 2010.
6. Safi J., Joyeux L., Chalouhi G. E. Periconceptional Folate Deficiency and Implications in Neural Tube Defects. Journal of Pregnancy.Volume 2012.
7. Talaulikar V.S., Arulkumaran S. Folic acid in obstetric practice: a review, Obstetrical and Gynecological Survey, vol. 66, no. 4, pp. 240-247, 2011.
8. Wilson R.D., Johnson J.A., Wyatt P. et al. Genetics Committee of the Society of Obstetricians and Gynaecologists of Canada and The Motherrisk Program. Pre-conceptional vitamin/folic acid supplementation 2007: the use of folic acid in combination with a multivitamin supplement for the prevention of neural tube defects and other congenital anomalies. J Obstet Gynaecol Can. 2007; 29: 1003-1026.
9. Czeizel A.E. Primary prevention of neural-tube defects and some other major congenital abnormalities: recommendations for the appropriate use of folic acid during pregnancy. Paediatr Drugs. 2000, Nov-Dec; 2(6): 437-49.
10. Ministry of Health NZ. 2006. Food and Nutrition Guidelines for Healthy Pregnant and Breastfeeding Women: A background paper.
Тематичний номер «Гінекологія, Акушерство, Репродуктологія» № 1 (29), березень 2018 р.
СТАТТІ ЗА ТЕМОЮ Акушерство/гінекологія
Чи варто змінювати свої харчові звички під час вагітності? Довкола цієї теми є багато суперечностей і рекомендацій, у яких легко заплутатися. Команда платформи доказової інформації про здоров’я «Бережи себе» спільно з лікарем-дієтологом Тетяною Лакустою з’ясували, чим раціон жінки в цей період особливий та на що слід звернути увагу. ...
Хронічний тазовий біль (ХТБ) є поширеним патологічним станом, який відзначається у жінок будь-якого віку і супроводжується сексуальною дисфункцією, емоційною лабільністю, аномальними матковими кровотечами, порушенням сечовипускання, розладами з боку кишечника тощо. Пацієнтки, які страждають на ХТБ, часто скаржаться на симптоми тривоги та депресії, що негативно позначається на їхній повсякденній активності, включаючи зниження працездатності та погіршення якості життя [1]. Сьогодні проблема ХТБ є економічним тягарем, пов’язаним із прямими або непрямими медичними витратами, які в середньому в різних країнах світу оцінюються у 4,9 млрд доларів на рік [2]. Раціональна фармакотерапія,спрямована на полегшення та контроль симптомів болю, є ключовою стратегією боротьби із ХТБ...
Дефіцит заліза є найпоширенішим патологічним станом у світі та однією з п’яти основних причин інвалідності. У той час як низький показник феритину у сироватці крові є діагностичною ознакою залізодефіциту, підвищений його рівень визначається як гострофазовий маркер, що може реєструватися при запальних станах уже в І триместрі вагітності. Відповідно до сучасних настанов, проведення рутинного скринінгу на залізодефіцит у невагітних та вагітних жінок за відсутності ознак анемії не рекомендоване. З огляду на останні літературні дані ця рекомендація має бути переглянута...
Наказ Міністерства охорони здоров’я України від 25.08.2023 № 1533 ...