Резистентність до антитромбоцитарних препаратів у пацієнтів зі стабільною ішемічною хворобою серця
Антитромбоцитарна терапія є невід’ємною складовою лікування пацієнтів з ішемічною хворобою серця (ІХС). Згідно з настановами Європейського товариства кардіологів (ESC, 2013), усі пацієнти зі стабільною ІХС з метою профілактики кардіоваскулярних подій повинні отримувати ацетилсаліцилову кислоту (АСК) у низькій дозі (75-150 мг), у разі непереносимості АСК альтернативним препаратом є клопідогрель. Аналогічні рекомендації містяться в уніфікованому клінічному протоколі (наказ МОЗ України від 2 березня 2016 р. № 152). Попри доведену ефективність цих антитромбоцитарних препаратів у вторинній профілактиці їх застосування не запобігає всім кардіоваскулярним подіям, і однією з причин цього може бути резистентність до лікування.
Ацетилсаліцилова кислота
Антитромбоцитарний ефект АСК забезпечується шляхом незворотного інгібування циклооксигенази (ЦОГ)-1 у тромбоцитах, яка необхідна їм для продукування тромбоксану А2 (ТХА2) – потужного стимулятора агрегації. Оскільки тромбоцити не мають ядер і не можуть синтезувати ЦОГ, дія АСК триває протягом усього життя тромбоцитів, тобто 7-10 днів. АСК також має низку ЦОГ-незалежних ефектів, як-от модуляція сигнального шляху NO/NF-kB, антиоксидантна дія, інгібування молекул адгезії VCAM‑1 та ICAM‑1, пригнічення ангіогенезу тощо. Рандомізовані клінічні дослідження підтвердили, що при застосуванні у вторинній профілактиці АСК знижує ризик кардіоваскулярних подій (коронарних подій і всіх типів інсульту), а також загальну і кардіоваскулярну смертність однаково ефективно в чоловіків і жінок. Згідно з рекомендаціями Консенсусу з використання антитромбоцитарних препаратів (АТС, 2002), користь від терапії АСК значно перевищує ризик гастроінтестинальних кровотеч, що дає підстави застосовувати АСК для первинної та вторинної профілактики кардіоваскулярних подій.
Під лабораторною (біохімічною) резистентністю до АСК («аспіринорезистентністю») розуміють недостатнє пригнічення реактивності тромбоцитів АСК. Клінічна аспіринорезистентність передбачає розвиток атеротромботичних подій, незважаючи на прийом АСК. Однак слід виділити справжню резистентність – недостатнє інгібування тромбоцитів внаслідок генетичних причин – і псевдорезистентність, обумовлену низьким комплаєнсом, клінічними особливостями пацієнтів (коморбідність, лікарські взаємодії) та іншими зовнішніми факторами (наприклад, неадекватне надходження діючої речовини в системний кровообіг при застосуванні АСК у кишковорозчинній оболонці). На застосування АСК у кишковорозчинній оболонці як важливу причину резистентності вказують багато дослідників. Так, А. О. Maree і співавт. (2005) встановили, що доза 75 мг кишковорозчинної форми АСК є недостатньою для повного пригнічення агрегації тромбоцитів у пацієнтів з кардіоваскулярною патологією. У ході дослідження пацієнти (n=131) приймали 75 мг АСК у кишковорозчинній оболонці. Підвищену активність ЦОГ (тромбоксан B2 >2,2 нг/мл) виявили в 58 (44%) пацієнтів.
D. Cox і співавт. (2006) у дослідженні за участю здорових добровольців тестували 3 варіанти терапії: 75 мг АСК у кишковорозчинній оболонці, 75 мг АСК у звичайній формі і комбінований препарат, що містить 200 мг дипіридамолу та 25 мг АСК (призначався для прийому двічі на добу). В усіх учасників визначали активність ЦОГ початково і через 2 тиж терапії. Після періоду «вимивання» тривалістю 2 тиж призначення між групами змінювалися. Первинним критерієм ефективності був рівень інгібування тромбоксану В2 через 2 тиж терапії. Неефективність лікування, яка визначалася як <95% інгібування тромбоксану В2, спостерігалася в 13% пацієнтів, які отримували АСК у кишковорозчинній формі, і у 8% учасників на тлі комбінованої антиагрегантної терапії. У групі пацієнтів, які приймали звичайну (шлунковорозчинну) форму АСК, не було виявлено жодного випадку неефективності терапії.
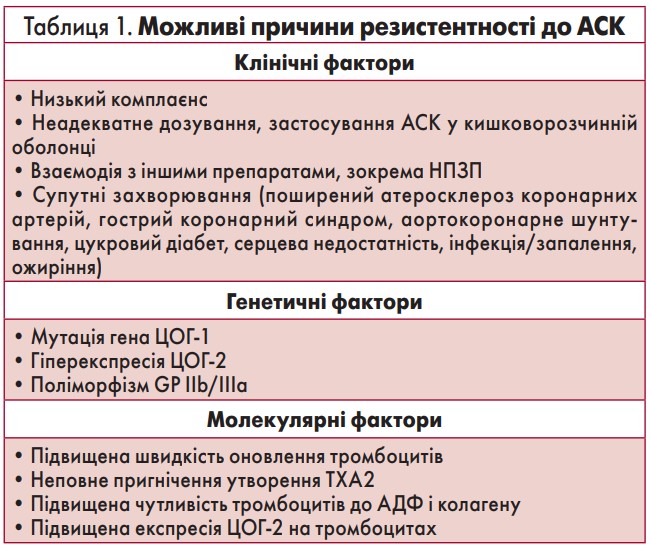 У дослідженні T. Grosser і співавт. (2013) 40 учасників отримували шлунковорозчинну форму АСК, а 360 – АСК у кишковорозчинній оболонці. У 40 пацієнтів, які застосовували АСК у звичайній формі, інгібування ЦОГ через 8 год було достатнім. Натомість у групі прийому АСК у кишковорозчинній оболонці достатнього ефекту щодо інгібування ЦОГ було досягнуто лише у 83% випадків. Можливі причини резистентності до АСК наведені в таблиці 1.
У дослідженні T. Grosser і співавт. (2013) 40 учасників отримували шлунковорозчинну форму АСК, а 360 – АСК у кишковорозчинній оболонці. У 40 пацієнтів, які застосовували АСК у звичайній формі, інгібування ЦОГ через 8 год було достатнім. Натомість у групі прийому АСК у кишковорозчинній оболонці достатнього ефекту щодо інгібування ЦОГ було досягнуто лише у 83% випадків. Можливі причини резистентності до АСК наведені в таблиці 1.
За даними літератури, поширеність аспіринорезистентності варіює в широких межах. У здорових дорослих вона становить близько 8,3%, в осіб з одним і більше факторами ризику – від 0,7 до 23,4%, у пацієнтів зі стабільною ІХС – від 0,4 до 29%, у хворих судинними захворюваннями, яким проводять реваскуляризаційні втручання, – 50-70%. Натомість, за даними комбінації трьох найбільш часто використовуваних лабораторних тестів (VerifyNow, оптичної агрегометрії і PFA‑100), поширеність аспіринорезистентності в пацієнтів із транзиторними ішемічними атаками й інсультом становить близько 2%.
Значна розбіжність у показниках поширеності аспіринорезистентності навіть в однакових категорій пацієнтів насамперед пояснюється використанням різних нестандартизованих тестів для оцінки активації тромбоцитів. В одного і того самого пацієнта аспіринорезистентність може визначатися за даними одних методів і бути відсутньою за результатами інших, а також зникати через 12 тиж при повторному дослідженні. Крім того, існує залишкова активація тромбоцитів (первинна хвиля агрегації), яка не піддається впливу АСК і не залежить від недостатньої прихильності пацієнтів до лікування або неадекватного дозування АСК. У деяких хворих залишкова агрегація може бути досить вираженою. Агрегація тромбоцитів може відбуватися кількома шляхами, при цьому доступні лабораторні методи оцінюють лише один або два з них. Більшість із цих шляхів не є залежними виключно від ТХА2 і, отже, не можуть вважатися АСК-специфічними. Зрештою, майже в усіх дослідженнях, які вивчали аспіринорезистентність, не визначали початкову функцію тромбоцитів. На думку американських дослідників, значна варіабельність поширеності аспіринорезистентності є відображенням гетерогенності відповіді тромбоцитів у різних пацієнтів (Mehta J. L., Mohandas B., 2010).
У деяких ранніх дослідженнях аспіринорезистентність асоціювалась з підвищеним ризиком кардіоваскулярних подій, проте ці дослідження мали суттєві методологічні обмеження, зокрема невеликий розмір вибірки, короткий період спостереження, застосування нестандартизованих тестів тощо.
Датське дослідження Larsen і співавт. (2017) – найбільше на сьогодні проспективне дослідження, у якому вивчалась агрегація тромбоцитів у пацієнтів, що отримували вторинну профілактику АСК. У ньому взяли участь 900 хворих на ІХС з інфарктом міокарда та/або діабетом в анамнезі. Агрегацію тромбоцитів визначали через 1 год після прийому АСК за допомогою тестів VerifyNow і Multiplate Analyzer.
Первинною кінцевою точкою була комбінація нефатального інфаркту міокарда, ішемічного інсульту та кардіоваскулярної смерті, вторинними кінцевими точками – ці події окремо. Після 3 років спостереження висока агрегація тромбоцитів не асоціювалася з підвищеним ризиком жодної кінцевої точки. Також із цим ризиком не корелював рівень тромбоксану В2. Єдиним клінічним фактором ризику первинної та вторинних кінцевих точок виявилася ниркова недостатність.
Клопідогрель
Згідно з американськими, європейськими та українськими настановами, у пацієнтів зі стабільною ІХС клопідогрель слід розглядати як альтернативу АСК у разі її непереносимості (AHA/ACC, 2016; ESC, 2013; УКПМД, 2016). Рекомендація щодо застосування клопідогрелю в пацієнтів зі стабільною ІХС ґрунтувалася лише на одному великому дослідженні – CAPRIE, яке мало низку обмежень (зокрема неоднозначні результати в різних підгрупах та порівняння з АСК у дозі 325 мг, що не є найбільш безпечною). Це пояснює місце клопідогрелю лише як препарату другої лінії.
Клопідогрель інгібує АДФ-індуковану активацію тромбоцитів шляхом незворотного блокування рецепторів P2Y12, локалізованих переважно (але не тільки) на поверхні тромбоцитів. Також клопідогрель певною мірою пригнічує агрегацію тромбоцитів, індуковану колагеном або тромбіном, проте ця дія нівелюється в разі підвищення концентрації вказаних індукторів.
Поширеність резистентності до клопідогрелю, за даними різних досліджень, становить від 5 до 44%. Такий широкий діапазон зумовлений передусім широкою генетичною варіабельністю ферменту CYP3A4, який відповідає за перетворення клопідогрелю на активний метаболіт.
Слід зазначити, що, як і у випадку АСК, стандартизованих методів оцінки відповіді тромбоцитів на клопідогрель не існує.
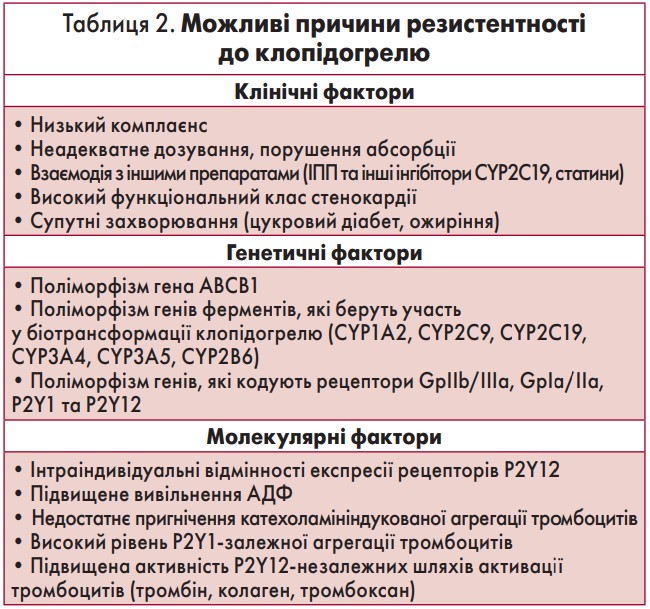 У таблиці 2 наведено потенційні причини резистентності до клопідогрелю. У низці досліджень резистентність асоціювалася з підвищеним ризиком кардіоваскулярних подій, проте більшість цих досліджень були проведені в пацієнтів з гострими формами ІХС або у хворих після стентування. У дослідженні Matetzky і співавт. (2004) у пацієнтів з гострим інфарктом міокарда з елевацією сегмента ST, резистентних до клопідогрелю (а таких було майже 25%), ризик повторної кардіоваскулярної події був найвищим і становив 40%. Схожі результати були отримані в дослідженнях PREPARE POST STENTING та CLEAR PLATELETS.
У таблиці 2 наведено потенційні причини резистентності до клопідогрелю. У низці досліджень резистентність асоціювалася з підвищеним ризиком кардіоваскулярних подій, проте більшість цих досліджень були проведені в пацієнтів з гострими формами ІХС або у хворих після стентування. У дослідженні Matetzky і співавт. (2004) у пацієнтів з гострим інфарктом міокарда з елевацією сегмента ST, резистентних до клопідогрелю (а таких було майже 25%), ризик повторної кардіоваскулярної події був найвищим і становив 40%. Схожі результати були отримані в дослідженнях PREPARE POST STENTING та CLEAR PLATELETS.
Практичні рекомендації
З огляду на відсутність стандартизованих тестів для оцінки антитромбоцитарних ефектів АСК або клопідогрелю, а також відсутність чітких доказів на користь чи проти клінічної значимості резистентності, рутинне визначення резистентності в пацієнтів, які отримують низькодозовану АСК або клопідогрель, не рекомендується, і немає офіційних даних стосовно дій у разі виявлення резистентності.
Розповсюдженість справжньої аспіринорезистентності є низькою, проте можлива індивідуальна варіабельність відповіді на АСК. Отже, доза АСК, необхідна для досягнення оптимального інгібування тромбоцитів, може відрізнятись у різних пацієнтів. Наприклад, у пацієнтів з ІХС, резистентних до лікування АСК у дозі 75 мг/добу, підвищення дози до 150 мг/добу через 4 тиж забезпечило адекватну відповідь у 62,5% випадків (Han Y., 2016). На думку Mehta та Mohandas (2010), призначення більш високої дози АСК (150 або 325 мг/добу) може бути доцільним у пацієнтів з багатьма факторами ризику та наявністю ознак прогресуючого ураження судин, а також у хворих з повторними оклюзіями коронарних судин. Підвищення дози не рекомендоване у випадку, якщо АСК призначається разом з інгібіторами P2Y12 (клопідогрелем, тикагрелором), через відсутність клінічної користі та підвищений ризик кровотечі.
Щодо дозування клопідогрелю, у дослідженнях CURRENT OASIS‑7 та CLEAR PLATELETS були встановлені фармакодинамічні переваги подвоєної дози препарату (з 300 до 600 мг), натомість в інших дослідженнях (GRAVITAS, ISAR-CHOICE) не було продемонстровано доцільності застосування вищих доз.
У пацієнтів з недостатньою відповіддю на клопідогрель (або за наявності факторів ризику резистентності) можуть застосовуватися більш сучасні антагоністі P2Y12, такі як тикагрелор, кангрелор чи прасугрель. Сам клопідогрель не має переваг як альтернатива низькодозованій АСК стосовно як резистентності, так і ефективності та безпеки. Нещодавно Lemesle і співавт. (2016) проаналізували дані 2832 учасників дослідження CORONOR і встановили, що в амбулаторних пацієнтів зі стабільною ІХС клопідогрель не забезпечував зменшення частоти ішемічних подій (5,8 vs 4,2% у групі АСК; р=0,056), при цьому за частотою кровотеч групи також не відрізнялися.
У попередньому дослідженні CAPRIE не виявлено користі від лікування клопідогрелем замість АСК у пацієнтів з інсультом чи інфарктом міокарда в анамнезі.
Висновки
1. На сьогодні відсутні стандартизовані методи оцінки відповіді тромбоцитів на АСК чи клопідогрель.
2. Розповсюдженість справжньої (генетично детермінованої) резистентності до АСК та клопідогрелю є низькою.
3. Розвиток ішемічних подій на тлі застосування антитромбоцитарних препаратів найбільш часто зумовлений недостатньою прихильністю до лікування.
4. Специфічною причиною недостатньої відповіді на АСК може бути застосування низької дози АСК у кишковорозчинній оболонці, натомість антитромбоцитарний ефект клопідогрелю може зменшуватись у разі супутньої терапії інгібіторами протонної помпи чи статинами.
5. Низькодозована АСК залишається препаратом першої лінії для пожиттєвого застосування в пацієнтів зі стабільною ІХС, клопідогрель вважається альтернативним антитромбоцитарним препаратом у разі непереносимості АСК.
Підготував Олексій Терещенко
За підтримки «Такеда Україна».
UA/MAGNH/0518/0033
Медична газета «Здоров’я України 21 сторіччя» № 10 (431), травень 2018 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9). Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи. ...
Застосування статинів середньої інтенсивності в комбінації з езетимібом порівняно зі статинами високої інтенсивності окремо може забезпечити більше зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у пацієнтів із нещодавнім ішемічним інсультом. Пропонуємо до вашої уваги огляд статті Keun-Sik Hong et al. «Moderate-Intensity Rosuvastatin Plus Ezetimibe Versus High-Intensity Rosuvastatin for Target Low-Density Lipoprotein Cholesterol Goal Achievement in Patients With Recent Ischemic Stroke: A Randomized Controlled Trial», опублікованої у виданні Journal of Stroke (2023; 25(2): 242‑250). ...
Артеріальна гіпертензія (АГ) сьогодні є одним із найпоширеніших серцево-судинних захворювань (ССЗ), що асоціюється з високим кардіоваскулярним ризиком, особливо в коморбідних пацієнтів. Навіть помірне підвищення артеріального тиску (АТ) пов’язане зі зменшенням очікуваної тривалості життя. До 40% хворих на АГ не підозрюють у себе недугу, бо це захворювання на початку може мати безсимптомний перебіг. Оптимальний контроль АТ є вагомим чинником профілактики фатальних серцево-судинних подій (ССП) для забезпечення якісного та повноцінного життя таких хворих. ...




