Екзокринна недостатність підшлункової залози: практичний підхід
Мальдигестію та мальабсорбцію поживних речовин можуть спричиняти низка захворювань травного тракту, зокрема целіакія [1], запальні захворювання кишечнику [2], синдром надлишкового бактеріального росту (СНБР) у тонкій кишці [4] та анатомічні аномалії травного тракту [5]. Окрім цього, ще однією основною причиною розвитку синдромів мальдигестії та мальабсорбції є екзокринна недостатність підшлункової залози (ЕНПЗ) – зменшення кількості та/або активності панкреатичних ферментів до рівня, який є недостатнім для підтримання нормального процесу травлення [5, 6]. Етіологічні фактори ЕНПЗ численні і не обмежуються зниженням рівня продукції панкреатичних ферментів. Цей патологічний стан може бути пов’язаний з відносним зниженням кількості функціонуючих ферментів, які досягають хімусу у тонкій кишці під час травлення. ЕНПЗ також можуть зумовлювати інгібування секреції ферментів підшлункової залози, їх інактивація внаслідок вкрай низького (кислого) значення рН та незадовільного змішування з їжею [6, 7].
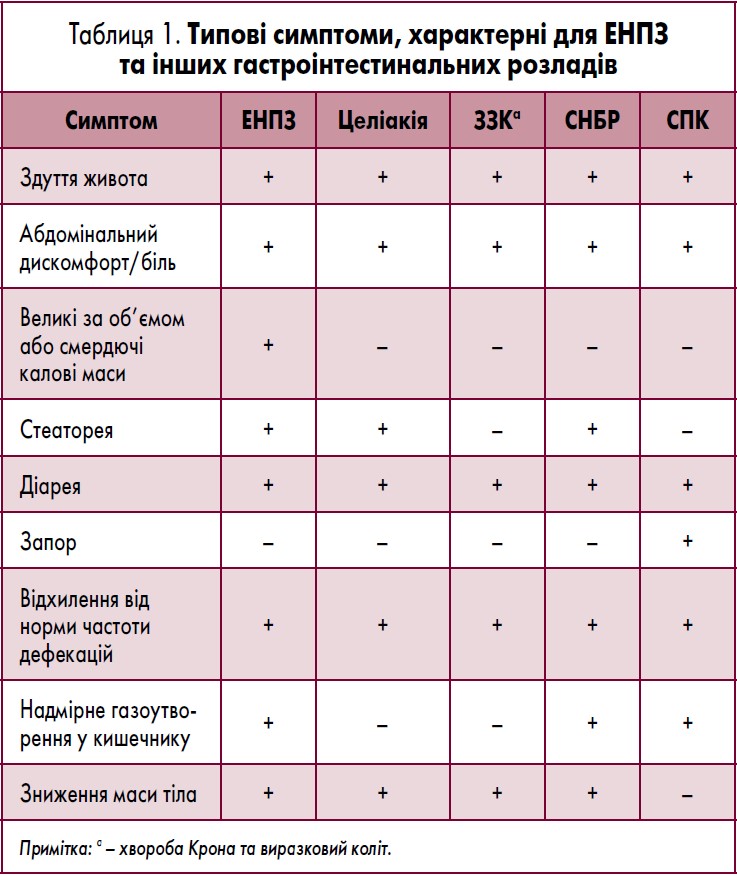
ЕНПЗ спочатку може проявлятися неспецифічними симптомами, такими як здуття живота, абдомінальний дискомфорт, стеаторея, діарея, надмірне газоутворення у кишечнику та зниження маси тіла. Ці симптоми також характерні й для іншої патології шлунково-кишкового тракту (ШКТ), включаючи синдром подразненого кишечнику (СПК), целіакію, запальні захворювання кишечнику (ЗЗК) та СНБР (табл. 1) [3, 6, 8-15].
Ця публікація має на меті підвищити обізнаність лікарів-практиків первинної ланки охорони здоров’я щодо ЕНПЗ та її наслідків, а також висвітлити практичний підхід до диференційної діагностики ЕНПЗ із іншими патологічними станами, які супроводжуються мальабсорбцією.
Поширеність ЕНПЗ
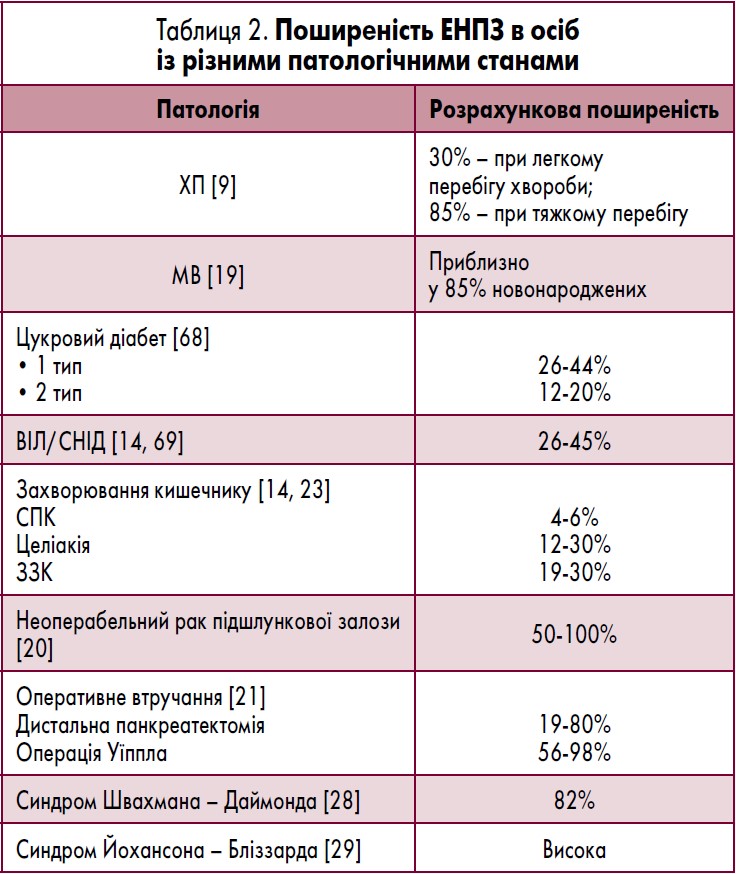
Дані щодо поширеності ЕНПЗ у загальній популяції невідомі. Однак цей показник може бути досить високим у певних підгрупах пацієнтів (табл. 2) – із хронічним панкреатитом (ХП) [9], муковісцидозом (МВ) [19], раком підшлункової залози [20] та хворих, яким було виконано резекцію підшлункової залози [21]. ЕНПЗ також може поєднуватися з такими захворюваннями ШКТ, як ЗЗК, целіакія або СПК (табл. 2), що підвищують ризик її розвитку [22-24].
ЕНПЗ особливо часто (30% випадків) зустрічається у пацієнтів із діареєю, зокрема, при СПК (6%) [22] або целіакії (незважаючи на дотримання ними безглютенової дієти) [25]. Поширеність цього патологічного стану зростає з віком [26, 27]. ЕНПЗ також може спостерігатися в осіб із рідкісними генетичними захворюваннями, такими як синдром Швахмана – Даймонда [28] та синдром Йохансона – Бліззарда [29].
Етіологія та патофізіологія ЕНПЗ
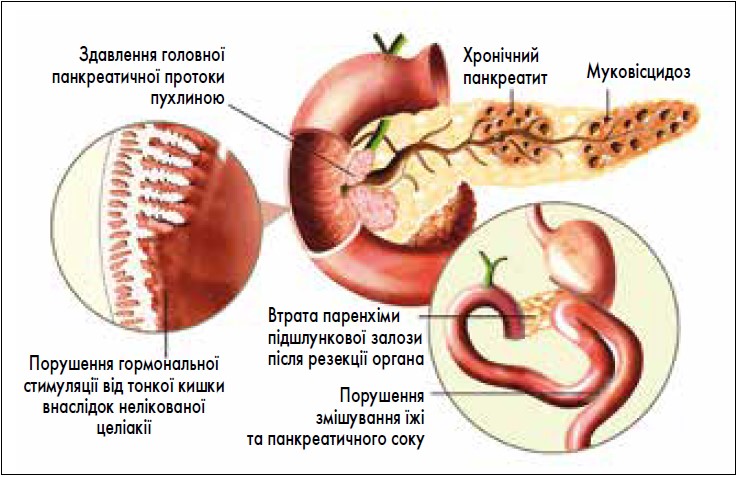
Найчастіше ЕНПЗ виникає внаслідок часткової або повної втрати паренхіми підшлункової залози через ХП, МВ або резекцію органа [6, 7]. Її розвиток також можуть спричиняти низка інших захворювань (рис. 1; за B. Lindkvist // World J Gastroenterol, 2013; 19: 7258-7266).
Рис. 1. Патогенез ЕНПЗ (за B. Lindkvist )
Механічна обструкція панкреатичної протоки, спричинена пухлиною підшлункової залози, також може призводити до розвитку ЕНПЗ [20]. Порушення секреції панкреатичних ферментів може бути наслідком зниженої нейрогормональної стимуляції з тонкої кишки (наприклад, при целіакії) [14, 30, 31]. Панкреатичні ферменти можуть інактивуватися через гіперпродукцію кислоти шлункового соку при синдромі Золлінгера – Еллісона [6] або при неадекватній нейтралізації кислого шлункового хімусу в ситуації, коли підшлункова залоза не здатна належним чином продукувати або вивільняти бікарбонати [7]. Змішування шлункового хімусу з панкреатичними ферментами у дванадцятипалій кишці може виявитися неефективним при анатомічних порушеннях (наприклад, після перенесеної операції з шунтування шлунка) [7] або при дискоординації процесу травлення, що призводить до постпрандіальної дискінезії. Такі менш очевидні стани, як езофагектомія [32], СПК [22], цукровий діабет 1 типу [33, 34] та «панкреатогенний» діабет 3с типу (вторинний відносно ХП або раку підшлункової залози), також асоціюються з розвитком екзокринної дисфункції [35, 36]. Цукровий діабет може у кінцевому підсумку призвести до дисфункції підшлункової залози, оскільки при цьому захворюванні орган уражається внаслідок мікросудинної патології [37, 38].
Важливість діагностики ЕНПЗ
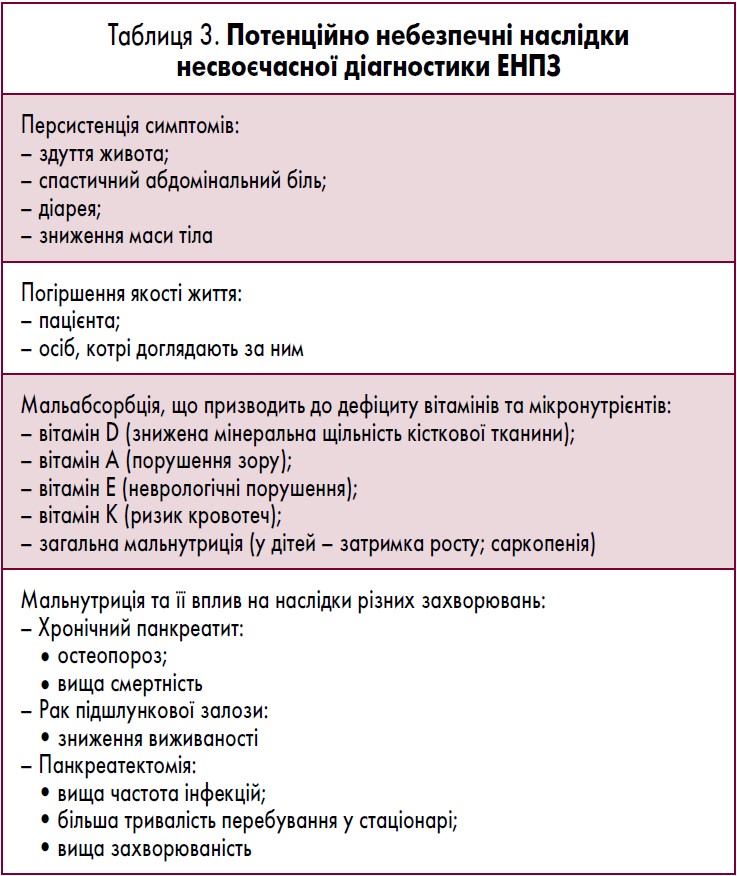
Симптоми та ступінь тяжкості ЕНПЗ істотно варіюють у різних пацієнтів [9]. Типові симптоми ЕНПЗ (наприклад, здуття живота, абдомінальний дискомфорт, стеаторея, діарея, надмірне газоутворення у кишечнику, зниження маси тіла) часто спостерігаються при інших захворюваннях ШКТ (табл. 1). А отже, лікар може випустити ЕНПЗ із переліку диференційної діагностики, за винятком пацієнтів із відомими патологічними станами, які підвищують ризик розвитку ЕНПЗ, такими як ХП [39], МВ [40], резекція підшлункової залози [21] або рак підшлункової залози [20]. На жаль, це може призвести до затримки у встановленні діагнозу ЕНПЗ, що може мати потенційно небезпечні наслідки (табл. 3).
Більш того, фоновий патологічний стан, такий як ХП або злоякісне новоутворення підшлункової залози, може перебігати нерозпізнаним, із потенційно значимими довготривалими наслідками. В осіб із ЕНПЗ клінічно значима мальдигестія може розвинутися раніше, ніж явні симптоми (табл. 3) [9, 41, 42]. Особливо це стосується всмоктування жиророзчинних вітамінів [5], оскільки вони втрачаються з жиром у фекаліях. У пацієнтів з ЕНПЗ низькі рівні вітаміну D можуть призводити до розвитку остепорозу. У пацієнтів із ХП ступінь тяжкості ЕНПЗ була достовірно асоційована з нижчою мінеральною щільністю кісткової тканини, виміряної за допомогою двоенергетичної рентгенівської абсорбціометрії або за даними звичайної рентгенографії. Це явище визначає високий ризик переломів кісток у пацієнтів із ХП [43]. Низькі рівні вітаміну А можуть призводити до порушень зору, особливо у темряві [5]. Знижені концентрації вітаміну Е можуть спричиняти неврологічні порушення, такі як атаксія та периферична нейропатія [5]. Дефіцит вітаміну К підвищує ризик кровотеч, який клінічно може проявлятися у вигляді екхімозів [5]. У дітей із МВ мальабсорбція білків та жирів, спричинена нелікованою ЕНПЗ, асоціюється з затримкою росту [44]. У дорослих із захворюваннями підшлункової залози ЕНПЗ чітко асоціюється з м’язовою атрофією (p<0,001) [45].
Наслідки мальнутриції, пов’язаної з ЕНПЗ, у подальшому можуть погіршитися, якщо пацієнти свідомо уникають споживання певних продуктів харчування, які можуть спричинити симптоми дискомфорту [46]. ЕНПЗ є одним із факторів, що сприяють розвитку мальнутриції, яка часто спостерігається у пацієнтів із раком підшлункової залози (табл. 3) [47]. В одному з досліджень у більшості пацієнтів, котрим виконано часткову резекцію підшлункової залози з приводу раку, розвивалася ЕНПЗ при найбільш ранній оцінці після операції (6 тижнів); при цьому у більшості пацієнтів ЕНПЗ зберігалася на 3-, 6- та 12-му місяці подальшого спостереження [48].
Мальнутриція є предиктором несприятливих результатів перенесеного оперативного втручання з приводу раку підшлункової залози [47]. Аналіз за участю пацієнтів, котрим виконано резекцію підшлункової залози з приводу раку, показав, що у хворих із високим ризиком розвитку мальнутриції в 5 разів частіше спостерігалися місцеві ускладнення у місці втручання, у 4 рази частіше подовжувався термін перебування у стаціонарі, а також був вищий показник загальної захворюваності порівняно з пацієнтами з низьким ризиком розвитку мальнутриції [49]. Тяжкий ступінь зниження маси тіла (>8,4% від маси тіла до операції) після резекції раку підшлункової залози асоціювався з достовірно вищою смертністю порівняно з пацієнтами з легким ступенем зниження маси тіла [50]. За результатами аналізу за участю пацієнтів із прогресуючим раком підшлункової залози більш тяжка ЕНПЗ була достовірно асоційована зі зниженням виживаності [51]. Натомість інший аналіз показав, що нутритивна підтримка була достовірно та незалежно асоційована з більш тривалою виживаністю у пацієнтів з ЕНПЗ (63% із них – із симптомами) [52]. Мальнутриція, спричинена ЕНПЗ, також може розвиватися у пацієнтів із ХП (табл. 3) [53]. Пацієнти з ХП мають підвищений ризик остеопорозу [54] та смертності [55], що може бути пов’язаним із мальнутрицією. Навіть субклінічна ЕНПЗ може призводити до мальнутриції; в невеликому дослідженні за участі пацієнтів із целіакією 4% із них мали ЕНПЗ без симптомів, але з ознаками нутритивного дефіциту за даними аналізу сироватки крові [56].
Диференційна діагностика ЕНПЗ
Підхід до діагностики ЕНПЗ
Загальний алгоритм диференційної діагностики ЕНПЗ наведено на рисунку 2. Аналіз анамнезу та фізикальне обстеження пацієнта надають найбільш цінну інформацію для визначення послідовності подальших досліджень, не всі з яких можуть бути дійсно необхідними.
Клінічне обстеження пацієнта розпочинають з детального аналізу симптомів та збору анамнезу; дані первинних аналізів дають змогу визначити найбільш доцільну послідовність подальших досліджень. Після цього слід виключити низку патологічних станів на підставі даних анамнезу та результатів фізикального обстеження, лабораторних (FE‑1, на наявність жиру в калі), візуалізаційних досліджень та емпіричного призначення різних видів консервативного лікування. Пацієнту можна запропонувати емпіричне призначення замісної терапії панкреатичними ферментами (ЗТПФ), ґрунтуючись на даних анамнезу та аналізу симптоматики або результатах лабораторних досліджень. Нарешті, для підтвердження діагнозу ЕНПЗ можна провести прямі тести з оцінки функції підшлункової залози (за можливості).
Рис. 2. Загальний алгоритм диференційної діагностики ЕНПЗ КТ – комп’ютерна томографія; FE-1 – фекальна еластаза-1; МРТ – магнітно-резонансна томографія; НПЗП – нестероїдні протизапальні препарати; ЗТПФ – замісна терапія панкреатичними ферментами; ІПП – інгібітор протонної помпи; СЗЕ – синдром Золлінгера – Еллісона.
Анамнез
Ретельний збір медичного, хірургічного, сімейного та соціального анамнезу має пріоритетне значення для з’ясування симптомів та планування досліджень із визначення можливих причин ЕНПЗ та відповідних терапевтичних мішеней. Якщо в анамнезі пацієнта наявні такі персистуючі симптоми, як здуття живота, діарея, непереносимість жирної їжі та абдомінальний біль, поряд з іншими можливими діагнозами, з високою ймовірністю слід запідозрити ЕНПЗ. Анамнестичні дані про алкогольну залежність і куріння мають важливе значення, адже ці фактори сприяють поступовому розвитку ХП, асоційованого з ЕНПЗ [57]. Куріння асоціюється з підвищеним ризиком розвитку ХП, раку підшлункової залози та ЕНПЗ. За даними проведеного у Німеччині масштабного дослідження з вивчення асоціативного зв’язку в загальній популяції, з віком (≥60 років) ризик розвитку ХП також зростає [27]. Стійке зниження маси тіла може супроводжуватися мальдигестією та мальабсорбцією [46]. Однак, оскільки ЕНПЗ може розвинутися в будь-який період життя, цей патологічний стан може спостерігатися й у осіб більш молодого віку та навіть у осіб із надлишковою масою тіла або ожирінням. Анамнестичні дані про хронічне зловживання алкоголем та куріння підвищують ймовірність фонової наявності у пацієнта злоякісного новоутворення, зокрема раку підшлункової залози [58].
Лабораторні аналізи
Традиційно деякі клініцисти призначають тестування на наявність жиру в калі [59]. Однак відсутність стеатореї – це звичне явище, оскільки навіть резидуальна продукція ендогенної ліпази є достатньою для того, щоб замаскувати цей симптом, або пацієнт може свідомо уникати споживання жирної їжі, тому що вона провокує появу відповідних симптомів з боку ШКТ [9, 44]. Наявність вираженої стеатореї або позитивний результат якісного аналізу на наявність жиру в калі хоча і є аргументом на користь діагнозу ЕНПЗ, проте не є чутливим або специфічним лабораторним маркером [6, 14, 60]. Кількісне визначення жиру у калі є інформативним, але це дослідження потребує дотримання пацієнтом дієти з високим вмістом жиру протягом 5 діб або довше та збору усіх зразків калу протягом останніх 72 год дотримання вказаного дієтичного режиму [9, 61]. Огляд калу на наявність крапель жиру є набагато простішим із будь-якого погляду, проте він надає лише якісні результати, які можуть бути інтерпретовані по-різному [5, 9, 61]. Жодний із методів визначення жиру в калі не є специфічним стосовно ЕНПЗ, оскільки такі самі результати можна отримати при інших патологічних станах [9].
Прямі тести з визначення функції підшлункової залози ґрунтуються на стимуляції виділення панкреатичного соку за допомогою секретину та холецистокініну; вони мають високу інформативність, але проводяться тільки в умовах спеціалізованих центрів, є інвазивними та складними у виконанні (попри використання ендоскопічних технік), а отже, потребують досвідченого персоналу [9, 61]. Нещодавно з метою оцінки ЕНПЗ почали використовувати тестування на фекальну еластазу-1 (FE‑1) – фермент, який виробляє та вивільняє підшлункова залоза, що залишається інтактним під час інтестинального транзиту [6]. Визначення FE‑1 є високочутливим та специфічним методом моніторингу прогресування ЕНПЗ, але менш надійним при більш легкому перебігу ЕНПЗ, а також у пацієнтів, котрим виконано резекцію підшлункової залози, або у хворих із водянистою діареєю [6, 14, 60]. Пацієнта слід проконсультувати щодо належного збору зразків для того, щоб уникнути хибних результатів (наприклад, через «розведення» зразка калу при діареї), хоча це може й не вплинути на них [62], оскільки тестування в умовах лабораторії дозволяє видалити надлишок води шляхом центрифугування або ліофілізації [9, 63]. Визначення рівня фекального хімотрипсину не слід використовувати як діагностичний тест на наявність ЕНПЗ, оскільки він має більш низьку чутливість порівняно з FE‑1 [9, 60].
Лікування і ведення пацієнтів з ЕНПЗ
Головна мета лікування хворих із ЕНПЗ полягає у полегшенні симптомів з боку ШКТ та коригуванні або поліпшенні нутритивного статусу пацієнта [39]. З огляду на різноманітні причини та різні ступені тяжкості ЕНПЗ лікування є дуже індивідуальним та часто – напівемпіричним. Розроблено численні професійні рекомендації з лікування ЕНПЗ [5, 15, 44, 64, 65], деякі з яких узагальнені у досить зручному форматі [66]. Пацієнтів, які курять або зловживають алкоголем, слід проконсультувати щодо необхідності позбутися шкідливої звички [15]. Замісна терапія панкреатичними ферментами є наріжним каменем у лікуванні хворих з ЕНПЗ; ферментні препарати призначають перорально, їх приймають під час основних прийомів їжі або під час перекусів у дозах, які з терапевтичною метою можуть бути скориговані [66]. Ефективність схеми лікування оцінюють за досягненням задовільних нутритивних результатів та купіруванням симптомів [66].
Контроль наслідків ЕНПЗ
Мультидисциплінарна команда, яка має здійснювати ведення пацієнта з ЕНПЗ, включає лікаря первинної ланки охорони здоров’я, гастроентеролога, нутриціолога, ендокринолога та часто – хірурга, який спеціалізується на оперативних втручаннях на підшлунковій залозі. Наступним етапом має бути оцінка загального нутритивного статусу, визначення рівнів жиророзчинних вітамінів та проведення денситометрії. Необхідно здійснити адекватну компенсацію дефіциту жиророзчинних вітамінів [53]. Слід виконати тестування на наявність цукрового діабету 3с типу та порушеної толерантності до глюкози (і у разі виявлення призначити відповідне лікування), враховуючи підвищений ризик панкреатичної ендокринної дисфункції за наявності захворювань підшлункової залози [67].
Висновки
Таким чином, ЕНПЗ є частою причиною мальабсорбції, яка проявляється як синдром, що характеризується широким спектром симптомів: дискомфортом у животі, здуттям живота, надмірним газоутворенням у кишечнику, діареєю, зниженням маси тіла та стеатореєю (табл. 4).
Ці неспецифічні симптоми ускладнюють диференційну діагностику ЕНПЗ, оскільки вони перехрещуються з симптомами інших захворювань ШКТ. Важливо своєчасно встановити діагноз, оскільки за відсутності лікування цей патологічний стан може спричиняти у дітей затримку росту, призводити до небажаних наслідків мальнутриції та зниження загальної виживаності, а також погіршувати якість життя пацієнта. Встановлення діагнозу ЕНПЗ здійснюють шляхом детального аналізу анамнезу, виключення іншої патології за допомогою специфічних тестів та підтвердження результатів діагностики шляхом емпіричного призначення терапії, яка дозволяє купірувати симптоми та покращити прогностичні наслідки.
Список літератури, що включає 69 джерел, знаходиться в редакції
Othman M.O., Harb D., Barkin J.A. Introduction and practical approach to exocrine pancreatic insufficiency for the practicing clinician.
Int J Clin Pract. 2018; 72: e13066.
Переклала з англ. Олена Терещенко
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 2 (48), травень 2018 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...