Глутатион как универсальный гепатопротектор с плейотропными эффектами
 С 2000 г. распространенность хронических диффузных заболеваний печени (ХДЗП) резко повысилась. Так, в мире ежегодно фиксируется около 170 млн пациентов с одной из форм ХДЗП, причем 25-30% из них уже имеют выраженный фиброз или цирроз печени. Среди гастроэнтерологических заболеваний в Европе и США цирроз является одной из наиболее частых «неопухолевых» причин смерти, а также основной патологией, предрасполагающей к развитию гепатоцеллюлярной карциномы (ГЦК) – злокачественного новообразования, занимающего пятое место по частоте выявления и третье в структуре смертности онкологических пациентов. В течение ближайших 10-15 лет ожидается пик заболеваемости и распространенности ХДЗП, при этом большей части таких пациентов потребуется ортотопическая трансплантация печени. Прогнозируется, что количество пациентов с прогрессирующими заболеваниями печени за это время возрастет на 160%, увеличившись к 2030 г. примерно с 3,3 до 7,9 млн. При этом заболеваемость декомпенсированным циррозом печени увеличится на 168% (до 105 430 случаев), в то время как частота ГЦК – на 137% (до 12 240 случаев). Общий рост смертности от заболеваний печени в 2030 г. составит 178% (примерно 78 300 смертей). До 2030 г. предполагается около 800 000 дополнительных случаев смерти от болезней печени.
С 2000 г. распространенность хронических диффузных заболеваний печени (ХДЗП) резко повысилась. Так, в мире ежегодно фиксируется около 170 млн пациентов с одной из форм ХДЗП, причем 25-30% из них уже имеют выраженный фиброз или цирроз печени. Среди гастроэнтерологических заболеваний в Европе и США цирроз является одной из наиболее частых «неопухолевых» причин смерти, а также основной патологией, предрасполагающей к развитию гепатоцеллюлярной карциномы (ГЦК) – злокачественного новообразования, занимающего пятое место по частоте выявления и третье в структуре смертности онкологических пациентов. В течение ближайших 10-15 лет ожидается пик заболеваемости и распространенности ХДЗП, при этом большей части таких пациентов потребуется ортотопическая трансплантация печени. Прогнозируется, что количество пациентов с прогрессирующими заболеваниями печени за это время возрастет на 160%, увеличившись к 2030 г. примерно с 3,3 до 7,9 млн. При этом заболеваемость декомпенсированным циррозом печени увеличится на 168% (до 105 430 случаев), в то время как частота ГЦК – на 137% (до 12 240 случаев). Общий рост смертности от заболеваний печени в 2030 г. составит 178% (примерно 78 300 смертей). До 2030 г. предполагается около 800 000 дополнительных случаев смерти от болезней печени.
Резкому увеличению количества пациентов с ХДЗП способствуют повышение заболеваемости вирусными и токсическими (алкогольными и медикаментозными) гепатитами, а также существенный рост числа больных с ожирением и сахарным диабетом. Эти заболевания являются основной причиной развития сравнительно новой нозологической формы – неалкогольной жировой болезни печени (НАЖБП), частота которой возросла не менее чем в 2 раза. Так, согласно официальной статистике США, если с 1988 по 1994 г. доля НАЖБП в структуре ХДЗП составляла 46,8%, то в 1994-2004 гг. – 62,84%, а в 2004-2008 гг. – уже 75,1%. Прогнозируется, что распространенность НАЖБП в США до 2030 г. повысится на 21% (с 83,1 до 100,9 млн случаев), а неалкогольного стеатогепатита (НАСГ) – на 63% (с 16,52 до 27,00 млн случаев). Предполагается также, что общая распространенность НАЖБП среди взрослого населения (в возрасте ≥15 лет) до 2030 г. составит 33,5%.
Такой выраженный и стремительный рост частоты ХДЗП обуславливает необходимость поиска новых эффективных и безопасных методов их профилактики и лечения. Современная программа комплексного лечения и профилактики заболеваний печени включает два основных направления: этиотропную и патогенетическую терапию. Этиотропная терапия, как правило, применяется при вирусных гепатитах с парентеральным механизмом передачи и направлена на подавление репликации возбудителя заболевания и его элиминацию. Основу патогенетической терапии составляют гепатопротекторы – препараты, влияющие на структуру и функцию гепатоцитов. К ним относятся представители разных групп лекарственных средств (препараты растительного и животного происхождения, эссенциальные фосфолипиды, аминокислоты или их производные, витамины-антиоксиданты и др.), повышающие устойчивость гепатоцитов к патологическим воздействиям; усиливающие их обезвреживающую функцию и способствующие восстановлению печеночными клетками нарушенных функций. Действие гепатопротекторов направлено на восстановление гомеостаза в печени, повышение ее устойчивости к действию патогенных факторов, нормализацию функциональной активности и стимуляцию в органе процессов регенерации. В широком смысле показаниями к применению гепатопротекторов являются алкогольные и неалкогольные стеатогепатиты и циррозы печени, лекарственные, токсические, холестатические и вирусные поражения печени (в дополнение к этиотропной терапии). Однако на практике назначение того или иного гепатопротектора во многом зависит от наличия и выраженности определенного клинико-биохимического синдрома/синдромов повреждения печени, таких как цитолиз, холестаз, гиперазотемия, снижение белково-синтетической функции печени, портальная гипертензия и др.
Поиски универсального гепатопротектора, способного воздействовать не на один, а сразу на несколько синдромов повреждения печени, продолжаются на протяжении многих лет. Основные требования к оптимальному гепатопротектору впервые были сформулированы R. Preisig еще в 1970 г. Согласно им, такой гепатопротектор должен быть нетоксичным, иметь естественный метаболизм, характеризоваться хорошей переносимостью, достаточно полной абсорбцией, эффектом первого прохождения через печень и экстенсивной энтерогепатической циркуляцией, проявлять противовоспалительную активность и выраженную способность связывать/предотвращать образование высокоактивных повреждающих соединений, подавлять фиброгенез и стимулировать регенерацию печени. Впоследствии были сформулированы дополнительные требования, а именно – воздействие на ключевые моменты патогенеза заболеваний печени, плейотропность гепатопротекторных эффектов и универсальность при любой патологии печени.
К сожалению, ни один из используемых в настоящее время в медицинской практике гепатопротекторов этим требованиям в полной мере не отвечает, хотя есть препараты, максимально приближающиеся к обозначенному стандарту. К ним, в частности, относится глутатион, который в Украине известен под торговой маркой Гепавал®. Этот гепатопротектор подвергается естественному метаболизму в печени, проявляет выраженную детоксикационную активность, характеризуется высоким профилем безопасности и хорошей переносимостью, а также оказывает другие положительные эффекты, обнаруженные в последнее время.
Глутатион – трипептид, состоящий из аминокислот глутамина, цистеина, глицина, обладающих выраженной детоксикационной активностью. Глутатион содержится в каждой клетке организма, а глутатионзависимые ферменты обеспечивают детоксикацию в различных ее органеллах. Глутатион – единственный из антиоксидантов, участвующий в трех из четырех линий антиоксидантной защиты клеток. В настоящее время глутатион рассматривается как главный внутриклеточный антиоксидант с мощным детоксикационным действием. Система глутатиона в организме восстанавливает более 300 окисленных субстанций, в частности, связывает свободные радикалы, восстанавливает перекиси, а также продукты перекисного окисления липидов, фосфолипидов мембран, белков, нуклеиновых кислот и выводит их из организма в виде нетоксичных конъюгатов, восстанавливает другие антиоксиданты (витамины С и Е). Глутатион нейтрализует токсины в желудочно-кишечном тракте до их абсорбции, а также выводит токсины и химические вещества, которые уже абсорбировались и циркулируют в организме. Кроме того, глутатион обладает иммуномодулирующими свойствами, в частности активирует естественные киллеры (NK-клетки) и модулирует функциональную активность Т-лимфоцитов.
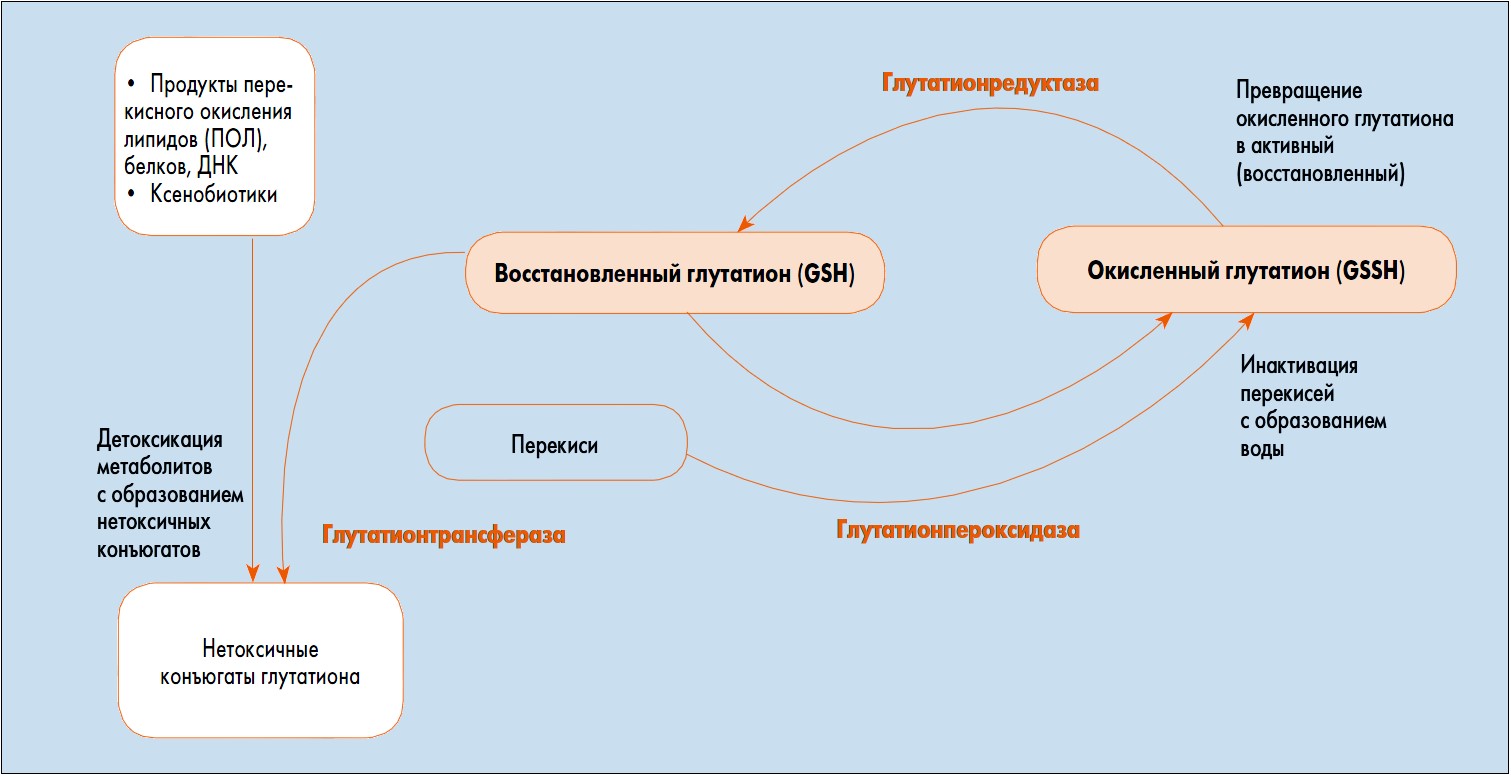
В клетках организма глутатион содержится преимущественно в восстановленной форме (GSH), причем отношение восстановленной (активной) формы к окисленной (неактивной) форме (GSSG) является маркером оксидативного стресса в организме (в норме GSH/GSSG=10/1). Общепризнано, что наличие достаточной концентрации восстановленного глутатиона является критическим фактором выживания клеток в условиях оксидативого стресса (рис.).
Рис. Наличие восстановленного глутатиона – критический фактор выживания клеток
В мировой медицинской практике глутатион применяется уже более 40 лет. Изначально он был синтезирован в Японии в начале 1970-х гг., после чего началось его широкое клиническое применение в Японии, Китае, Италии, Испании, США и других странах. В настоящее время глутатион включен в европейскую, японскую и американскую фармакопеи.
Согласно многочисленным исследованиям, глутатион эффективен практически при любой неопухолевой патологии печени. Наиболее высокая терапевтическая эффективность глутатиона отмечена при токсических гепатитах – медикаментозноиндуцированном и алкогольном поражении печени. Так, по результатам мультицентрового (10 клинических госпиталей в г. Шанхае, Китай) исследования эффективности и безопасности инъекционной формы глутатиона у 245 пациентов с хроническими заболеваниями печени, которые в течение 3 недель получали глутатион в дозе 1200 мг в сутки (при этом в процессе лечения исключалось применение любых противовирусных, иммуномодулирующих препаратов, а также препаратов, которые могли бы снижать уровень печеночных ферментов), у 100% пациентов с медикаментозно-индуцированным гепатитом и у 86% пациентов с алкогольным гепатитом определялся отличный и хороший терапевтический эффект. В частности, у 57% пациентов с медикаментозно-индуцированным гепатитом исчезали субъективные симптомы, уменьшалась выраженность гепатоспленомегалии, нормализовались уровни аланинаминотрансферазы (АлАТ), аспартатаминотрансферазы (АсАТ) и/или билирубина, а у 43% пациентов отмечалось уменьшение или отсутствие прогрессирования субъективных симптомов, отсутствие прогрессирования гепатоспленомегалии и снижение уровней АлАТ, АсАТ и/или билирубина более чем на 50%.
В другом исследовании установлено, что у пациентов с алкогольной болезнью печени глутатион (600 мг внутривенно капельно в течение 1 мес) через 30 дней терапии эффективно снижал показатели цитолитического и холестатического синдромов. Еще одно исследование, проведенное в 2017 г., показало, что повышение дозы глутатиона до 1200 мг позволяет уменьшить продолжительность лечения и достичь хороших и отличных результатов у пациентов с алкогольной болезнью печени уже через 15 дней.
В нескольких исследованиях оценивали возможность и целесообразность применения глутатиона при хроническом вирусном гепатите С. Так, изучение концентрации глутатиона у лиц с хроническим вирусным гепатитом С показало, что у таких пациентов, особенно в случае ассоциации гепатита С с ВИЧ-инфекцией, отмечается системное истощение глутатиона. Было также выявлено, что активность заболевания коррелирует со степенью снижения уровня глутатиона в плазме крови. Был сделан вывод, что это истощение может быть фактором, лежащим в основе устойчивости к терапии интерферонами и антиретровирусными препаратами. Полученные данные представляют собой биологическую основу для заместительной терапии глутатионом у пациентов с хроническим вирусным гепатитом С.
В фундаментальном исследовании была проведена оценка зависимости концентрации восстановленного глутатиона в биоптатах печени 52 пациентов с хроническим вирусным гепатитом С в зависимости от генотипа. Было установлено, что у больных со всеми исследуемыми генотипами отмечалось снижение уровня восстановленного глутатиона по сравнению с таковым в контрольной группе. Особенно оно выражено у пациентов с генотипом 1b, что может обусловливать устойчивость к базисной терапии интерферонами. Кроме того, у пациентов с генотипом 1b было выявлено значительное снижение концентрации глутатиона в ткани печени, лимфоцитах и плазме крови, а также цитотоксической активности мононуклеаров (снижение экспрессии CD4+, CD16+, CD25+-антигенов) периферической крови по сравнению с пациентами с генотипами 2а/2с, 3а и контрольной группы. Был сделан вывод, что увеличение продукции свободных радикалов наряду с выявленными изменениями системы глутатиона при генотипе 1b может лежать в основе резистентности к интерферонотерапии и прогрессирования поражения печени, вызванного цитопатическим действием вируса гепатита С.
В исследованиях последних лет была продемонстрирована эффективность глутатиона и при НАСГ. В частности, в одном из исследований в 2016 г. было установлено, что у больных НАСГ после 3 мес терапии пероральной формой глутатиона уровень АлАТ снизился на 52%, а уровень гамма-глутамилтрансферазы на 35%. В этом же исследовании также определяли уровень маркеров оксидативного стресса, которые у пациентов с НАСГ всегда повышены: продуктов перекисного окисления клеточных структур и наиболее показательного маркера – 8-OHdG (8-гидрокси‑2-дезоксигуанозин), являющегося продуктом окисления ДНК. В результате было выявлено, что пероральное применение глутатиона в суточной дозе 300 мг в течение 3 мес снижает уровень 8-OHdG в крови пациентов с НАСГ на 45%. Еще в одном исследовании у пациентов с НАЖБП изучали как уровни ферментов, так и маркеры фиброза печени: коллагена ІІІ типа (РС III) и гиалуроновой кислоты. Было установлено, что в группе глутатиона общая терапевтическая эффективность лечения по совокупности всех показателей составила 94,7%, а уровни маркеров фиброза снизились более чем в 2 раза. В связи с этим был сделан вывод, что глутатион потенциально может подавлять развитие фиброза печени у пациентов с НАЖБП.
Таким образом, известные и новые исследовательские данные свидетельствуют о том, что глутатион обеспечивает многогранные плейотропные эффекты, которые находят свое широкое клиническое применение. Благодаря плейотропности эффектов глутатион (Гепавал®) эффективен почти при всех ХДЗП, что позволяет рассматривать его как один из универсальных гепатопротекторов-детоксикантов. Имеющиеся на сегодняшний день доказательные данные позволяют рекомендовать глутатион (Гепавал®) к широкому применению практически при любой патологии печени.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 2 (48), травень 2018 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Реімбурсація – це повне або часткове відшкодування аптечним закладам вартості лікарських засобів або медичних виробів, що були відпущені пацієнту на підставі рецепта, за рахунок коштів програми державних гарантій медичного обслуговування населення. Серед громадськості програма реімбурсації відома як програма «Доступні ліки». Вона робить для українців лікування хронічних захворювань доступнішим....
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....