Безопасный ингибитор протонной помпы: смена лидера, стандарта или мировоззрения?
Большинство имеет определенное мировоззрение, которое определено меньшинством.
Станислав Ежи Лец
 Сейчас сложно поверить, что относительно недавно, в начале ХХ столетия, лечение язвенной и гастроэзофагеальной рефлюксной болезни (ГЭРБ) заключалось в назначении щелочных продуктов питания – молока, яиц, пюре. Несколько позже первую скрипку в терапии этих заболеваний стала играть питьевая сода – она облегчала состояние больных, но, к сожалению, не предотвращала развитие осложнений. В середине ХХ столетия появились холиноблокаторы, и на сцену вышел атропин, частично ингибировавший продукцию соляной кислоты посредством блокады мускариновых рецепторов париетальных клеток. Незначительная эффективность, многочисленные побочные эффекты не позволили атропину длительное время удерживать лидирующие позиции в лечении кислотозависимых заболеваний (КЗЗ), и ему на смену пришли блокаторы Н2-рецепторов.
Сейчас сложно поверить, что относительно недавно, в начале ХХ столетия, лечение язвенной и гастроэзофагеальной рефлюксной болезни (ГЭРБ) заключалось в назначении щелочных продуктов питания – молока, яиц, пюре. Несколько позже первую скрипку в терапии этих заболеваний стала играть питьевая сода – она облегчала состояние больных, но, к сожалению, не предотвращала развитие осложнений. В середине ХХ столетия появились холиноблокаторы, и на сцену вышел атропин, частично ингибировавший продукцию соляной кислоты посредством блокады мускариновых рецепторов париетальных клеток. Незначительная эффективность, многочисленные побочные эффекты не позволили атропину длительное время удерживать лидирующие позиции в лечении кислотозависимых заболеваний (КЗЗ), и ему на смену пришли блокаторы Н2-рецепторов.
Настало время ранитидина и фамотидина – они внесли существенные изменения в устоявшиеся принципы лечения КЗЗ: механизм их действия заключался в блокировании гистаминовых рецепторов в париетальных клетках, что сопровождалось достижением непродолжительного контроля над синтезом соляной кислоты.
Несмотря на более высокую эффективность по сравнению с М-холиноблокаторами, применение Н2-блокаторов редко приводило к полному восстановлению и заживлению дефектов слизистой по причине неспособности этих препаратов длительно блокировать секрецию соляной кислоты и долго удерживать целевое рН.
И вот, наконец, на небосклоне появилась новая путеводная звезда – омепразол, представитель ранее неизвестной группы лекарственных средств, а именно: ингибиторов протонной помпы (ИПП). Эффект, произведенный появлением омепразола, часто сравнивают с масштабной терапевтической революцией: высокая афинность к протонной помпе париетальных клеток желудка и более благоприятный по сравнению с предшественниками профиль побочных действий перевернули ранее господствовавшие представления о лечении КЗЗ. .
Годы широкомасштабного клинического применения, множество сравнительных клинических исследований убедительно подтвердили превосходство первого представителя класса ИПП над Н2-блокаторами. Такая убедительная победа омепразола в лечении язвенной болезни и ГЭРБ создали предпосылки для синтеза других ИПП. И вскоре семейство ИПП пополнилось новыми членами – лансопразол, пантопразол, рабепразол, эзомепразол присоединились к своему родоначальнику в борьбе с КЗЗ. Количество назначений ИПП быстро возросло: только в течение 8 лет (с 2000 по 2008 год) частота применения ИПП увеличилась на 200,8%, тогда как число назначений Н2-блокаторов значительно сократилось. Вот так постепенно, с появлением новых препаратов и современных знаний менялись мировоззрение, стандарты и подходы к лечению КЗЗ.
Немного фармакологии
ИПП, попадая в организм в неактивном виде, пролекарства активируются исключительно в суперкислой среде (при рН 1,0-2,0), которая создается исключительно в протоках париетальных клеток желудка. Краткость, необратимость и избирательность действия ИПП позволяют быстро и надежно вывести из строя активированные протонные насосы. Возобновление синтеза соляной кислоты возможно только через определенный промежуток времени, необходимый для синтеза новых белковых молекул, входящих в состав протонной помпы.
ИПП – очень недолго живущие препараты (период полувыведения – 0,5-2 ч) – способны обеспечить чрезвычайно длительный кислотосупрессивный эффект при однократном приеме в течение суток. В настоящее время ИПП продолжают прочно удерживать пальму первенства среди всех существующих классов антисекреторных лекарственных средств: они способны удерживать рН в желудке ≥4,0 на протяжении 18 ч в течение суток. После приема стандартной дозы ИПП синтез соляной кислоты полностью возобновляется только спустя 72-96 ч, а биодоступность препаратов возрастает с приемом каждой последующей дозы.
Короткий период полувыведения ИПП обуславливает низкую токсичность препаратов этой группы, даже у пожилых больных или пациентов с почечной/печеночной недостаточностью. Только в случаях выраженной печеночной недостаточности может понадобиться уменьшение дозы этих препаратов.
В отличие от ИПП, Н2-блокаторы начинают действовать значительно быстрее, однако прием этих препаратов сопровождается развитием тахифилаксии, а выраженность их антисекреторного действия начинает снижаться уже спустя первые 12-24 ч после приема данных лекарственных средств.
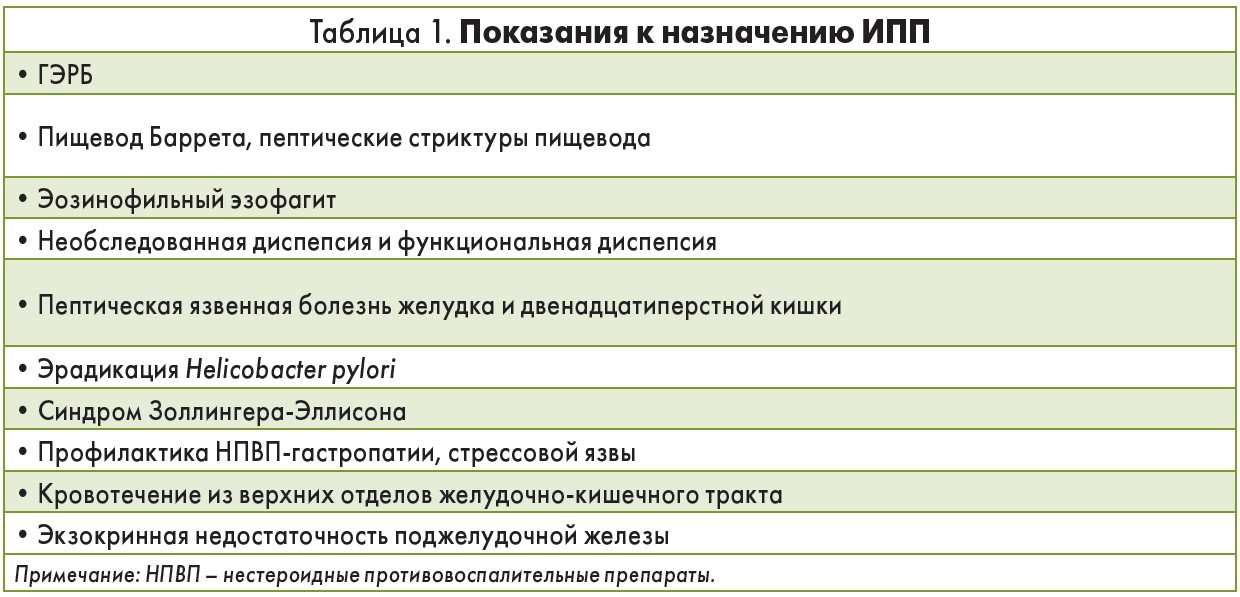
В настоящее время Н2-блокаторы используются достаточно редко и назначаются для лечения крайне ограниченного круга заболеваний (легкая неэрозивная ГЭРБ, легкое течение функциональной диспепсии, гиперчувствительность к ИПП), тогда как спектр применения ИПП гораздо шире (табл. 1).
В руководстве Европейского общества кардиологов (European Society of Cardiology, ESC) по лечению острого коронарного синдрома у пациентов без персистирующего повышения сегмента ST, увидевшего свет в 2016 г., приводится еще одно показание для назначения ИПП (табл. 2).
Упорное соревнование, жаркие споры и неожиданный парадокс
Ситуацию равенства и братства в семействе ИПП нарушило желание учеников превзойти учителя: кто-то казался сильнее, кто-то – быстрее, а кто-то – длительнее. Однако выраженность кислотосупрессивного действия оказалась сопоставимой с таковой остальных ИПП, а длительность поддержания внутрижелудочного рН ≈4 омепразола (11,8 ч), хотя и уступала эзомепразолу (14 ч) и рабепразолу (12 ч), но превосходила лансопразол (11,5 ч) и пантопразол (10,1 ч) (Miner et al., 2003). Доказано, что использование омепразола у больных, принимающих ДАТТ с включением низких доз АСК, предотвращает повреждение слизистой оболочки верхних отделов ЖКТ и уменьшает риск кровотечений (Дорофеев А. Э., 2017).
Изучение механизмов действия омепразола позволило установить, что, помимо значительного снижения секреции соляной кислоты, под влиянием омепразола достоверно увеличивается экспрессия гена Bcl‑2 и синтез протеина Ki‑67 у больных с НПВП-ассоциированными язвами, осложненными кровотечением. Именно благодаря этим свойствам ограничивается активность апоптоза и стимулируется пролиферация эпителия желудочно-кишечного тракта, ускоряется репарация эрозивно-язвенных поражений, вызванных приемом НПВП (Rantanen T. et. al., 2014).
Однако самые жаркие споры о превосходстве одного ИПП над другими разгорелись на почве безопасности их применения в отдельной группе больных – у пациентов, получающих ДАТТ ацетилсалициловой кислотой и ингибитором P2Y12 (клопидогрель). В ходе наблюдательных исследований, изучавших возможные взаимодействия при одновременном приеме ИПП и клопидогреля, были получены неоднозначные результаты: некоторые свидетельствовали об ухудшении сердечно-сосудистых исходов, другие не подтверждали наличие подобной связи. Тщательный анализ вероятных неблагоприятных последствий сочетанного применения ИПП и ингибитора P2Y12 показал, что возможная причина их возникновения кроется в особенностях метаболизма указанных медикаментов.
Оказалось, что метаболизм этих препаратов происходит в печени с участием преимущественно трех изоферементов системы цитохрома Р450: CYP2С19, CYP2С9, CYP3А4. Высказано предположение, что ИПП, вступая во взаимодействие с перечисленными ферментами, тем самым ингибируют превращение клопидогреля в его активный метаболит, снижая эффективность последнего и косвенно усиливая агрегацию тромбоцитов.
На первый взгляд все оказалось достаточно просто: клопидогрель метаболизируется посредством CYP2С19, следовательно, при необходимости одновременного приема клопидогреля и ИПП необходимо использовать такой кислотосупрессивный препарат, который бы не воздействовал на указанный изофермент.
Управление по контролю за качеством продуктов питания и лекарственных средств США (FDA, 2009) поспешило опубликовать предостережение о нежелательности применения клопидогреля и ИПП, особенно омепразола и эзомепразола (наиболее изученных представителей этого класса лекарственных средств в то время), и рекомендовало к применению менее изученный препарат – пантопразол, который, предположительно, не влиял на CYP2С19.
Последовавшее за этой публикацией активное клиническое применение пантопразола, а также тщательное изучение свойств других ИПП заставило экспертов усомниться в правильности сделанных умозаключений. Оказалось, что метаболизм клопидогреля осуществляется не только за счет CYP2С19, но и при помощи CYP2С9, CYP3А4, а разные представители группы ИПП оказывают различное воздействие на метаболизм системы цитохрома Р450. Поэтому влияние ИПП на метаболизм клопидогреля и последующие сердечно-сосудистые исходы могут существенно отличаться.
Три сокрушительных удара по устоявшемуся стереотипу
 Вскоре появились результаты клинических исследований и метаанализов. Первый сокрушительный удар, поколебавший устоявшийся стереотип в отношении способности омепразола увеличивать сердечно-сосудистый риск у больных, получающих ДАТТ, нанесло исследование COGENT (Clopidogrel and the Optimization of Gastrointestinal Events Trial, 2010).
Вскоре появились результаты клинических исследований и метаанализов. Первый сокрушительный удар, поколебавший устоявшийся стереотип в отношении способности омепразола увеличивать сердечно-сосудистый риск у больных, получающих ДАТТ, нанесло исследование COGENT (Clopidogrel and the Optimization of Gastrointestinal Events Trial, 2010).
Это международное рандомизированное двойное слепое контролируемое с помощью двух плацебо параллельное групповое исследование (n=3873) эффективности и безопасности фиксированной комбинации клопидогреля (75 мг) и омепразола (20 мг) по сравнению с монотерапией клопидогрелем предоставило неожиданные результаты (все пациенты в этом исследовании дополнительно принимали ацетилсалициловую кислоту).
На протяжении всего периода наблюдения, длительность которого составляла 180 дней, поражение желудочно-кишечного тракта (явное / скрытое кровотечение, симптоматические гастродуоденальные язвы / эрозии, обструкция, перфорация) зафиксировано у 51 пациента, при этом они достоверно реже возникали у больных, получавших омепразол (1,1%), по сравнению с участниками, принимавшими плацебо (2,9%; отношение рисков для омепразола 0,3; 95% ДИ 0,03-0,56; р=0,001).
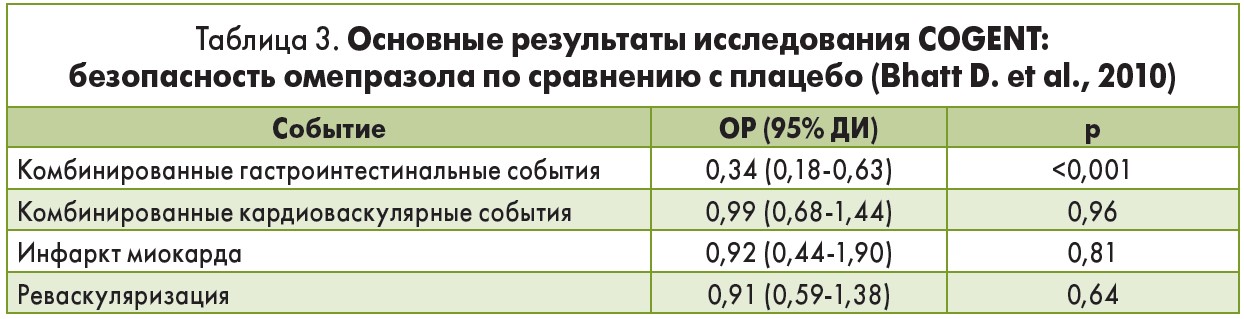
При этом частота возникновения нефатального инфаркта миокарда, инсульта, реваскуляризации, летального исхода по кардиоваскулярным причинам достоверно не отличалась в группах омепразола (4,9%) и плацебо (5,7%; ОР 0,99; 95% ДИ 0,68-1,44; р=0,96). Опубликовав полученные данные (табл. 3, рис. 1), авторы исследования резюмировали, что не зафиксировано значимых кардиоваскулярных взаимодействий между клопидогрелем и омепразолом, но эти результаты не позволяют в полной мере исключить клинически значимые различия в кардиоваскулярных событиях, обусловленных применением ИПП (табл. 3).
Сформулированные выводы были восприняты медицинской общественностью с большой настороженностью – всего лишь год перед этим FDA настоятельно рекомендовало применение пантопразола. Еще одним объяснением данному факту может стать досрочное завершение исследования: в соответствии с планами авторов проекта в этом трайле должны были принять 5 тыс. больных, но медленный набор пациентов и небольшое число кардиоваскулярных событий явились поводом для прекращения финансирования и закрытия исследования COGENT. Однако спустя 6 лет результаты исследования COGENT были проанализированы и перепроверены другой группой ученых, не принимавших непосредственного участия в его проведении.
М. Vaduganathan и соавт. (2016) полностью подтвердили выводы, сформулированные D. Bhatt и соавт.: у пациентов, перенесших чрескожное коронарное вмешательство (n=2676), омепразол значительно уменьшал вероятность развития гастроинтестинальных событий без значимого повышения риска кардиоваскулярных событий по сравнению с плацебо (5,4 vs 6,3%, соответственно; ОР 1,0; 95% ДИ 0,67-1,50; р=1,00). Аналогично в когорте больных острым коронарным синдромом (n=1573) омепразол предупреждал появление значимых гастроинтестинальных событий, не провоцируя возрастание вероятности появления кардиоваскулярных событий по сравнению с плацебо (5,6 vs 4,5% соответственно; ОР 1,4; 95% ДИ 0,77-2,53; р=0,27).
Вторым, не менее серьезным ударом по кардиологическому образу пантопразола стала публикация в авторитетном журнале Американской кардиологической ассоциации систематического обзора, подготовленная под руководством М. Sherwood (2015).
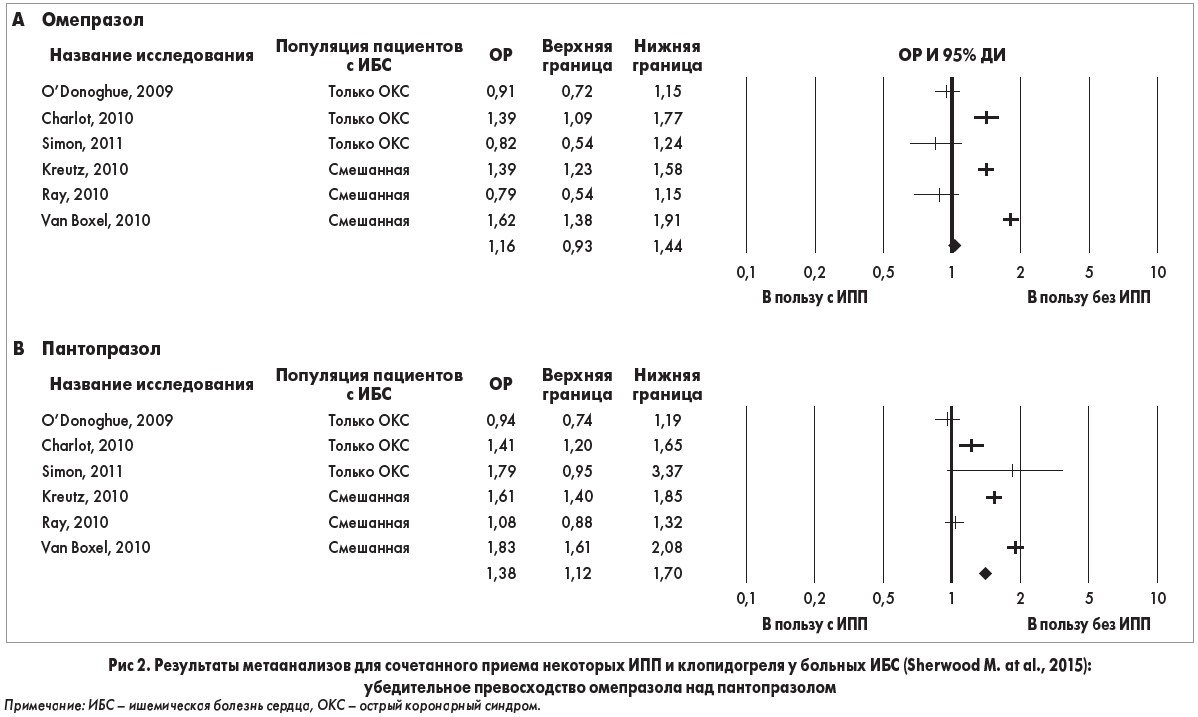
Метаанализ 6 отобранных исследований выявил повышение риска возникновения нежелательных кардиоваскулярных событий у пациентов, принимавших пантопразол (ОР 1,38; 95% ДИ 1,12-1,70), лансопразол (ОР 1,29; 95% ДИ 1,09-1,52) или эзомепразол (ОР 1,27; 95% ДИ 1,02-1,58) по сравнению с больными, не получающими ИПП. Ученые особо подчеркнули тот факт, что упомянутая связь не была значимой для омепразола (ОР 1,16; 95% ДИ 0,93-1,44), т. е. омепразол может использоваться при проведении ДАТТ, т. к. не оказывает негативного влияния на cердечно-сосудистый риск (рис. 2).
Комментируя полученные данные, М. Sherwood и соавт. высказали предположение, что анализ показателей относительно безопасности приема ИПП при проведении ДАТТ следует проводить для каждого представителя этой группы в отдельности, не обобщая все данные в одну группу и не рассматривая вопрос с позиции «польза / вред всех ИПП».
Чрезвычайно интересны результаты обсервационного исследования, выполненного под руководством А. Guérin (2016). Исследователи постарались установить, как повлияла рекомендация FDA по предпочтительному назначению пантопразола при проведении ДАТТ.
Ученые констатировали два важных факта: публикация рекомендации FDA привела к уменьшению общего количества пациентов, которым была назначена комбинация клопидогреля – ИПП; однако, несмотря на снижение доли больных, получавших комбинацию клопидогрела и ИПП, омепразол оставался наиболее часто используемым препаратом, назначаемым совместно с клопидогрелем.
Третий удар нанесли Т. Shamliyan и соавт. (2017), авторы широкомасштабной работы, в основу которой легли результаты 17 систематических обзоров и метаанализов, 16 рандомизированных контролированных исследований и 16 обсервационных исследований.
Команда ученых анализировала особенности сочетанного приема ИПП с 10 различными классами лекарственных средств. Изучив полученные данные, Т. Shamliyan и соавт. резюмировали: «В отношении конкретных ИПП одновременный прием пантопразола или эзомепразола, но не омепразола и лансопразола, ассоциирован с повышением риска общей летальности, нефатального инфаркта миокарда и инсульта».
Цирроз печени и ИПП – все совсем не просто
Еще одним камнем преткновения в проблеме безопасного применения ИПП стал цирроз печени. Больным циррозом печени, вне зависимости от этиологической причины заболевания, свойственен высокий риск развития портальной гипертензивной гастропатии, появления вариксов в пищеводе и желудке, а также возникновения кровотечения из варикозно-расширенных вен. Для лечения и профилактики указанных осложнений используются ИПП.
Однако оказалось, что эта простая на первый взгляд рекомендация влечет за собой ряд серьезных проблем: применение ИПП у больных циррозом печени ассоциируется с резким возрастанием риска возникновения инфекционных осложнений и печеночной энцефалопатии. Незамедлительно последовала реакция медицинской общественности: одни ученые рекомендовали значительно ограничить показания к назначению ИПП в данной категории больных, другие высказали более радикальное мнение: считать цирроз печени противопоказанием к назначению этих лекарственных средств.
Сгустившиеся тучи над ИПП развеяла статья R. Weersink и соавт., опубликованная в апреле 2018 г. в авторитетном журнале British Journal of Clinical Pharmacology. Эта группа ученых последовала рекомендациям М. Sherwood и проанализировала безопасность применения ИПП, не объединяя все препараты в одну группу. Основываясь на результатах анализа 69 исследований, авторы метаанализа доказали, что применение только трех ИПП не ассоциировано с появлением «дополнительных известных рисков».
В данную категорию вошли омепразол, эзомепразол и рабепразол. R. Weersink и соавт. установили, что безопасность приема перечисленных ИПП зависит от степени тяжести цирроза, определенной по шкале Чайлд-Пью: больным циррозом печени, состояние которых соответствует классу А и В, можно назначать омепразол и рабепразол, но желательно уменьшить максимальную суточную дозу перечисленных лекарственных средств.
Пациентам, находящимся в крайне тяжелом состоянии (класс С), следует рекомендовать только эзомепразол в максимальной суточной дозе 20 мг. Пантопразол и лансопразол признаны «небезопасными препаратами», т. к. их прием ассоциирован с 4-8-кратным увеличением риска различных осложнений.
Заключение, или Продолжение следует?
В настоящее время вопрос безопасности одновременного применения ИПП и клопидогреля в составе ДАТТ продолжает оставаться открытым. По мнению ряда ведущих международных экспертов, следует ожидать обновления рекомендаций различных кардиологических обществ по выбору ИПП при проведении ДАТТ.
Ремарка. Омез®
Среди множества генерических омепразолов, представленных на отечественном рынке, наибольшей известностью пользуется препарат Омез®, представляемый фирмой «Dr. Reddy’s Laboratories Limited». За спиной у Омеза – клинический опыт его активного применения во многих странах мира, равный нескольким десятилетиям. За это время Омез® успел доказать свою терапевтическую эквивалентность оригинальному омепразолу.
Небрендированный омепразол производства «Др. Реддис Лабораторис» занял достойное место в известной Orange Book, публикуемой FDA. Применение Омеза обсуждалось международной экспертной группой Gastrosphere 1.0 и 2.0 для профилактики и лечения НПВП-индуцированных поражений верхних отделов желудочно-кишечного тракта. Омез® в дозе 10-20 мг может использоваться для проведения безопасной кислотосупрессивной терапии у больных циррозом печени класса А-В по шкале Чайлд-Пью.
Выводы
На основании вышеизложенного можно утверждать, что в настоящее время омепразол является одним из наиболее изученных препаратов в своем классе. Важно также отметить, что омепразол является одним из наиболее часто назначаемых ИПП и как ИПП входит в стандарты лечения КЗЗ в США и странах Европы. На украинском фармацевтическом рынке среди генерических омепразолов наибольшую популярность получил препарат Омез®.
Литература
1. Miner PJr, Katz PO, Chen Y, et al. Gastric acid control with esomeprazole, lansoprazole, omeprazole, pantoprazole, and rabeprazole: A five-way crossover study. Am J Gastroenterol 2003;98:2616-20. DOI: 10.1111/j.1572-0241.2003.08783.x.
2. Food and Drug Administration. Follow-Up to the January 26, 2009, Early Communication about an Ongoing Safety Review of Clopidogrel Bisulfate (marketed as Plavix) and Omeprazole (marketed as Prilosec and Prilosec OTC) [Internet]. U. S. Food and Drug Administration; 2009 [cited 1 Jan 2015]. Available: http://www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPatientsand
Providers/DrugSafetyInformationforHeathcareProfessionals/ucm190784.htm.
3. Holmes DR, Dehmer GJ, Kaul S, Leifer D, O’Gara PT, Stein CM. ACCF/AHA clopidogrel clinical alert: approaches to the FDA “boxed warning”: a report of the American College of Cardiology Foundation Task Force on clinical expert consensus documents and the American Heart Association endorsed by the Society for Cardiova. J Am Coll Cardiol. 2010; 56: 321-41. doi: 10.1016/j.jacc.2010.05.013 PMID:20633831.
4. Bhatt DL, Cryer BL, Contant CF, Cohen M, Lanas A, Schnitzer TJ, et al. Clopidogrel with or without omeprazole in coronary artery disease. N Engl J Med. 2010; 363: 1909-17. doi: 10.1056/NEJMoa1007964 PMID: 20925534.
5. Vaduganathan M. Efficacy and Safety of Proton-Pump Inhibitors in High-Risk Cardiovascular Subsets of the COGENT Trial. Am J Med. 2016 Sep;129(9):1002-5. doi: 10.1016/j.amjmed.2016.03.042. Epub 2016 Apr 30.
6. Roffi М. 2015 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Task Force for the Management of Acute Coronary Syndromes in Patients Presenting without Persistent ST-Segment Elevation of the European Society of Cardiology (ESC). European Heart Journal (2016) 37, 267-315. doi:10.1093/eurheartj/ehv320.
7. Guérin A, Mody R, Carter V, Ayas C, Patel H, Lasch K, et al. (2016) Changes in Practice Patterns of Clopidogrel in Combination with Proton Pump Inhibitors after an FDA Safety Communication. PLoS ONE11(1): e0145504. doi:10.1371/journal. pone.0145504.
8. Shamliyan TA. Patient-centered Outcomes with Concomitant Use of Proton Pump Inhibitors and Other Drugs. Clin Ther. 2017 Feb;39(2):404-427.e36. doi: 10.1016/j.clinthera.2017.01.011. Epub 2017 Feb 9.
9. Российские стандарты по лечению инфаркта миокарда (2015).
10. Matthew W. Sherwood. Individual Proton Pump Inhibitors and Outcomes in Patients With Coronary Artery Disease on Dual Antiplatelet Therapy: A Systematic Review. J Am Heart Assoc. 2015;
4: e002245 doi: 10.1161/JAHA.115.002245.
11. Weersink RA. Safe use of proton pump inhibitors in patients with cirrhosis. Br J Clin Pharmacol. 2018 Apr 24. doi: 10.1111/bcp.13615.
Медична газета «Здоров’я України 21 сторіччя» № 13-14 (434-435), липень 2018 р.
СТАТТІ ЗА ТЕМОЮ Терапія та сімейна медицина
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Серед препаратів, які мають велику доказову базу щодо лікування пацієнтів із захворюваннями дихальних шляхів з алергічним компонентом, особливий інтерес становлять антагоністи лейкотрієнових рецепторів (АЛТР). Ці препарати мають хорошу переносимість у дорослих та дітей, а також, на відміну від інгаляційних кортикостероїдів (ІКС), характеризуються високим комплаєнсом, тому посідають чільне місце в лікуванні пацієнтів із респіраторною патологією. У лютому відбувся міждисциплінарний конгрес із міжнародною участю «Життя без алергії International» за участю провідних вітчизняних міжнародних експертів. Слово мав президент Асоціації алергологів України, професор кафедри фтизіатрії та пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук Сергій Вікторович Зайков із доповіддю «Місце АЛТР у лікуванні пацієнтів із респіраторною патологією». ...
Розбір клінічного випадку...