Можливості хондропротекторної терапії при остеоартриті
За матеріалами науково-практичної конференції з міжнародною участю «Сімейна медицина – майбутнє охорони здоров’я України» (17-18 травня, м. Київ)
Остеоартрит (ОА) – одне з найпоширеніших захворювань у світі, на яке страждають близько 6,5% населення планети. За даними літератури, ознаки ОА спостерігають у 97% осіб у віці старше 60 років.
 Про особливості патогенезу ОА та сучасні підходи до терапії цієї патології, зокрема про потенціал деяких хондропротекторів, розповіла керівник центру ревматології Клінічної лікарні «Феофанія» Державного управління справами (м. Київ), доктор медичних наук, професор Ірина Юріївна Головач.
Про особливості патогенезу ОА та сучасні підходи до терапії цієї патології, зокрема про потенціал деяких хондропротекторів, розповіла керівник центру ревматології Клінічної лікарні «Феофанія» Державного управління справами (м. Київ), доктор медичних наук, професор Ірина Юріївна Головач.
Лектор нагадала, що до патологічного процесу при ОА залучається не тільки хрящ, а й усі структурні компоненти суглоба: зв’язки, кістка, синовіальна оболонка, нервові закінчення, м’язова та жирова тканини. Отже, ОА слід розглядати не тільки як дегенеративний процес у хрящі, а й як патологічне ремоделювання всіх тканин суглоба, що ініціюється та визначається прозапальними медіаторами з розвитком метаболічних, а згодом і функціональних порушень у суглобі (R.F. Loeser et al., 2012). Саме з цієї точки зору слід оцінювати методи, які планується використовувати в лікуванні ОА.
Серед медикаментозних засобів лікування ОА слід виділити такі основні групи:
- симптом-модифікувальні лікарські засоби, що впливають на симптоми хвороби (біль, функціональна недостатність);
- структурно-модифікувальні лікарські засоби, що впливають на прогресію патологічних змін і можуть впливати чи не впливати на симптоми ОА.
Як симптом-модифікувальні засоби найчастіше використовують нестероїдні протизапальні препарати (НПЗП), які відіграють важливу роль на початковому етапі лікування та в періоди загострень. Однак після усунення больового синдрому необхідно зосередитися на тому, щоб загальмувати патологічне ремоделювання суглобів. Із цією метою вже понад 20 років у лікуванні ОА застосовують структурно-модифікувальні препарати сповільненої дії, відомі також як хондропротектори (рекомендації Європейської протиревматичної ліги, 2003; Міжнародного товариства з вивчення ОА, 2010). До таких препаратів належать, зокрема, хондроїтину сульфат, глюкозаміну сульфат, препарати гіалуронової кислоти, діацереїн, неомилювані похідні сої й авокадо (avocado-soybean unsaponifiables – ASU).
Остання група – ASU – представлена в Україні оригінальним препаратом Піаскледин 300 (Laboratoires Expanscience, Франція), до складу якого входить комплекс неомилюваних фітостеролів і жирних кислот з олій авокадо та сої у співвідношенні 1:2. Піаскледин 300 – високотехнологічний продукт, запатентована формула якого не має аналогів. Здатність препарату ефективно усувати симптоми ОА та відновлювати структуру хряща доведена в численних клінічних випробуваннях.
Біологічні ефекти ASU полягають насамперед у впливі на молекули, які визначають метаболічну активність суглобового хряща: ASU підвищує експресію трансформувальних факторів росту (TGF) та інгібітора активатора плазміногена, стимулює синтез протеогліканів і утворення колагенових волокон, інгібує та блокує інтерлейкін‑1 (IL‑1) тощо.
Встановлено, що ASU знижує експресію прозапальних сполук – фактора некрозу пухлини-α, IL‑1β, циклооксигенази‑2 та індуцибельної NO-синтази – в культурах бичачих хондроцитів, активованих ліпополісахаридами (R.Y. Au et al., 2007).
Y. Henrotin і співавт. (1998) показали, що ASU зменшують у культурах хондроцитів людини продукцію металопротеаз, цитокінів та простагландину Е2, які підтримують запальний і дегенеративний процеси в хрящі. З іншого боку, ASU підвищує рівень факторів росту TGF-β1 та TGF-β2 в синовіальній рідині колінних суглобів собак (L. Altinel et al., 2007), що свідчить про посилення репаративних процесів у хрящі.
У клінічних дослідженнях доведено, що застосування ASU забезпечує подвійний ефект – симптом-модифікувальний і структурно-модифікувальний: призводить до зменшення болю в суглобах, відновлення функції уражених суглобів, зниження дози чи відміни НПЗП, сповільнення прогресування ОА. Крім того, ASU демонструє прийнятний профіль безпеки при тривалому прийомі.
У 6-місячному дослідженні E. Maheu та співавт. (1998), в якому взяли участь пацієнти з ОА колінного й кульшового суглобів, було показано, що на тлі прийому ASU достовірно зменшуються загальний біль (>50% за аналоговою шкалою), функціональний індекс Лекена (покращання >30%) та індекс загальної функціональної неспроможності порівняно з групою плацебо. Терапевтичний ефект відзначався з 2-го місяця застосування ASU та зберігався після завершення курсу лікування.
Зниження потреби в НПЗП при застосуванні ASU в лікуванні ОА колінного та кульшового суглобів було доведено в дослідженні F. Blotman і співавт. (1997). Одна група отримувала протягом 3 міс препарат ASU, друга – плацебо. Завдяки симптом-модифікувальному ефекту ASU на 90-й день лікування 6 із 10 пацієнтів, які отримували активний препарат, знизили дозу чи відмінили НПЗП. Також відзначено поліпшення функціонального індексу в групі ASU порівняно з групою плацебо.
Вплив препарату Піаскледин на больовий синдром при ОА було продемонстровано в метааналізі R. Christensen і співавт. (2008). До метааналізу увійшли чотири дослідження (E. Maheu et al., 1998; F. Blotman et al., 1997; T. Appelboom et al., 2001; M. Lequesne et al., 2002). Доведено, що прийом Піаскледину достовірно зменшує біль (величина ефекту, ES 0,39; 95% довірчий інтервал, ДІ 0,01- 0,76; р=0,04) та індекс Лекена (ES 0,45; 95% ДІ 0,21-0,70; р=0,0003) (рис. 1).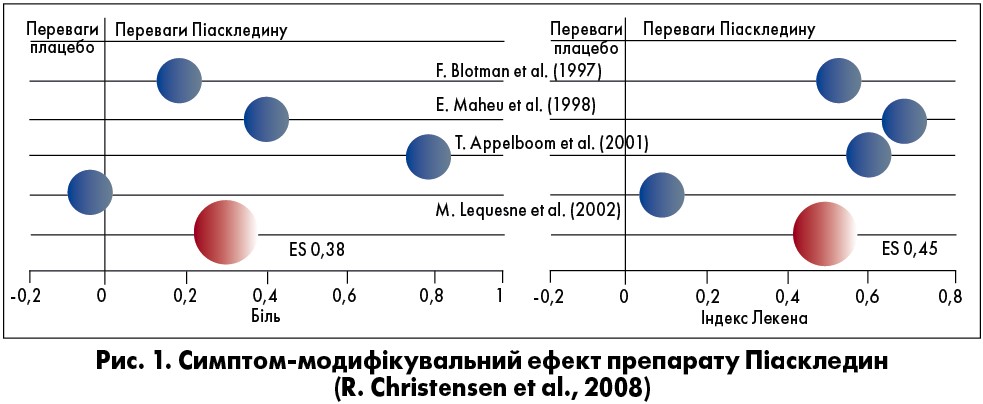
Дуже важливо, що для ASU доведений структурно-модифікувальний ефект. Так, Lequesne та співавт. (2002) показали, що прийом ASU забезпечує дворазове сповільнення звуження щілини кульшового суглоба порівняно з плацебо в пацієнтів з ОА.
У 2013 р. було опубліковано результати проспективного рандомізованого подвійного сліпого плацебо-контрольованого дослідження в паралельних групах ERADIAS, яке тривало три роки (E. Maheu et al., 2013). У дослідженні взяли участь 399 пацієнтів (середній вік – 62 роки) з ОА кульшового суглоба, що тривав не менш як чотири роки за критеріями Американської колегії ревматологів. Ширина суглобової щілини в ураженому суглобі в цих хворих становила 1-4 мм. Хворі були розподілені в дві групи, одна з яких отримувала препарат ASU Піаскледин 300 в дозі 300 мг на добу, а друга – плацебо. Спостереження показало, що через три роки лікування відносний ризик подальшого звуження суглобової щілини (>0,5 мм) зменшився на 20% порівняно з плацебо (р=0,039) (рис. 2).
Отже, в пацієнтів з ОА та схильністю до запальних реакцій препаратом вибору є Піаскледин 300, який достовірно уповільнює прогресування ОА, чинить знеболювальну та протизапальну дію, зменшує тривалість прийому та дозу НПЗП, добре переноситься й має зручну схему прийому – 1 капсула на добу. Крім того, препарат Піаскледин 300 відповідає сучасним вимогам до структурно-модифікувальних препаратів, які необхідно приймати довгостроково, а саме – має прийнятний профіль безпеки, що є вкрай актуальним для пацієнтів із коморбідними захворюваннями.
Підготувала Катерина Ткаченко
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (59) вересень-жовтень 2018 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...




