Як проводять антигелікобактерну терапію в Україні
За даними аналізу Українського реєстру Hp-EuReg – UKRAINE
 Інфекція Helicobacter pylori протягом багатьох років є важливою медичною та соціально-економічною проблемою. H. pylori інфіковано понад половину людства. Інфекція H. pylori – основна причина хронічного гастриту, виразкової хвороби шлунка та дванадцятипалої кишки, мальтоми шлунка та є визнаним чинником ризику розвитку раку шлунка.
Інфекція Helicobacter pylori протягом багатьох років є важливою медичною та соціально-економічною проблемою. H. pylori інфіковано понад половину людства. Інфекція H. pylori – основна причина хронічного гастриту, виразкової хвороби шлунка та дванадцятипалої кишки, мальтоми шлунка та є визнаним чинником ризику розвитку раку шлунка.
Основні принципи діагностики та лікування захворювань, пов’язаних з інфекцією H. pylori, регулярно переглядають та публікують у вітчизняних і міжнародних рекомендаціях.
Згідно з рекомендаціями Маастрихтського консенсусу IV антигелікобактерну терапію (АГБТ) строго рекомендовано пацієнтам із виразковою хворобою шлунка та дванадцятипалої кишки, атрофічним гастритом, MALT-лімфомою шлунка, після резекції шлунка з приводу раку шлунка чи при першому ступені спорідненості з хворим на рак шлунка, а також за бажанням інфікованого H. pylori пацієнта після консультації з лікарем. Рекомендована тривалість лікування становила 10-14 днів.
У Кіотському консенсусі і Маастрихтському консенсусі V містяться принципові доповнення щодо стратегії ведення хворих, інфікованих H. pylori. Зокрема у Маастрихтському консенсусі V зазначено, що H. pylori спричиняє хронічний активний гастрит (ХАГ) у всіх інфікованих осіб, тому було запропоновано новий термін – «бактеріальний гастрит». Звертається увага на те, що ХАГ може призвести до розвитку виразкової хвороби, атрофічного гастриту, аденокарциноми шлунка або MALT-лімфоми, тому успішна ерадикація H. pylori сприяє виліковуванню ХАГ і може запобігти прогресуванню захворювання, розвитку віддалених ускладнень або рецидивів хвороби. З цих причин захворювання, зумовлене H. pylori, вважають інфекційним незалежно від симптомів і стадії хвороби. Ерадикацію H. pylori слід рекомендувати всім інфікованим, оскільки вона усуває запалення слизової оболонки шлунка, запобігає розвитку атрофії та зменшує ризик розвитку раку шлунка.
Доведено, що ерадикація H. pylori зупиняє прогресування пошкодження слизової оболонки до розвитку атрофії, тому лікування інфекції найбільш ефективне з позиції канцеропревенції у пацієнтів з неатрофічним гастритом. Після ерадикації інфекції у хворих з розвиненою атрофією зберігається ризик виникнення раку шлунка, пропорційний ступеню і тяжкості атрофічного гастриту. Однак актуальність проведення АГБТ не зменшується. Вибір схеми АГБТ має ґрунтуватися на даних про ефективність режиму лікування в цій популяції, яка значною мірою визначається чутливістю H. pylori до антибіотиків. Як емпіричне лікування можна призначати схеми АГБТ, які достовірно забезпечують ефективність ерадикації не менше ніж 90%.
У Маастрихтському консенсусі V рекомендовано збільшення тривалості потрійної терапії з кларитроміцином і квадротерапії до 14 днів як один з варіантів оптимізації АГБТ.
В економічно розвинених країнах останніми десятиліттями спостерігається значне зниження частоти раку шлунка, що пояснюється зменшенням поширеності H. pylori внаслідок упровадження комплексу профілактичних заходів (профілактика гелікобактерної інфекції та її ерадикація) і поліпшення умов життя. Однак невпинне підвищення резистентності гелікобактера до раніше ефективних схем АГБТ викликає велике занепокоєння і потребує доопрацювання терапевтичних стратегій у країнах з високою поширеністю H. pylori. В Україні зберігається високий рівень як поширеності, так і захворюваності на H. pylori-асоційовані захворювання. Моніторинг скринінгу та ефективності ерадикаційної терапії в конкретних регіонах є важливим і актуальним.
Для оцінки ситуації з дотриманням сучасних рекомендацій у клінічній практиці проводять динамічні міжнародні дослідження. Одним з таких досліджень є проспективне багатоцентрове дослідження Європейський реєстр інфікування H. pylori (Європейський реєстр з питань лікування H. pylori, Нр-EuReg), розпочате у 2013 р. Європейською групою з вивчення H. pylori та мікробіоти (EHMSG; http://www.helicobacter.org). У цьому дослідженні беруть участь 27 країн, у кожній з яких задіяно не менше ніж 10 медичних закладів.
Метою реєстру Нр-EuReg є створення бази даних, яка дасть змогу систематизувати інформацію про реальну картину клінічної практики європейських гастроентерологів, котрі ведуть хворих, інфікованих H. pylori. За допомогою реєстру можна оцінити, наскільки реалізуються чинні клінічні рекомендації щодо діагностики та лікування хворих з інфекцією H. pylori в клінічній практиці в різних країнах та регіонах, а також ефективність різних схем АГБТ.
Аналіз даних щодо методів діагностики та лікування пацієнтів з H. pylori проводять на базі ДУ «Національний інститут терапії імені Л.Т. Малої НАМН України».
Мета – оцінити ситуацію з діагностикою інфекції H. pylori і лікуванням пацієнтів з нею в Україні та їх відповідність сучасним міжнародним рекомендаціям.
Матеріали та методи
Уся необхідна для аналізу інформація збирається та опрацьовується за допомогою науково-дослідної електронної бази даних Research Electronic Data Capture (REDCap), розміщеної на серверах Асоціації гастроентерологів Іспанії (Asociacion Espanola de Gastroenterologia – AEG, www.aegastro.es). AEG – некомерційна науково-медична асоціація гастроентерологів, метою якої є заохочення проведення незалежних міжнародних досліджень. Підтримка бази даних REDCap проводиться безкоштовно. В онлайн-базу даних на платформі AEG-REDCap вводять основні відомості про пацієнтів: стать, вік, етнічна належність, діагноз та клінічні симптоми, відомості про наявність раніше проведених курсів АГБТ, способи первинної діагностики H. pylori, вибір схеми та тривалості АГБТ, способи, застосовані для оцінки ефективності ерадикації, загальна ефективність та небажані ефекти АГБТ, прихильність пацієнтів до дотримання різних схем АГБТ.
Для проведення аналізу власних даних із REDCap Hp-EuReg – UKRAINE реєстру gfadeenko було взято дані пацієнтів, внесені з 2013 до 26.10.2018 р. Додатково проведено аналіз анкет обстежених хворих.
Результати та обговорення
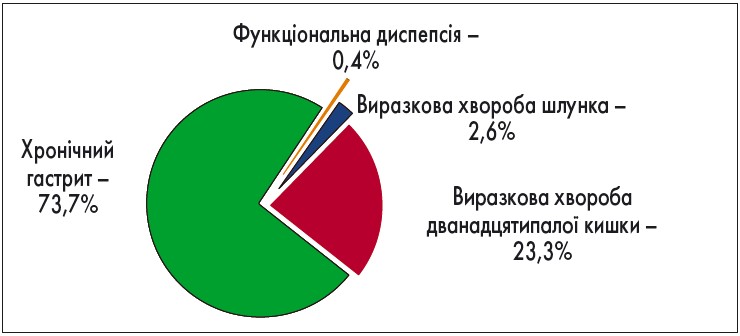
Проаналізовано дані 500 пацієнтів, інфікованих H. pylori, яким проводили АГБТ. Середній вік пацієнтів – 49,33±24,66 року. Серед хворих переважали жінки (54,2%). Терапію завершили 488 (97,6%) хворих. Показанням до лікування була патологія верхніх відділів шлунково-кишкового тракту, асоційована з інфекцією H. pylori. Переважали хворі з патологією, віднесеною до рубрики «інші захворювання», та пацієнти з виразковою хворобою дванадцятипалої кишки (рис. 1).
Рис. 1. Нозологічна характеристика хворих (власні дані)
Серед скарг переважали прояви диспепсії (78,4%) та віднесені до рубрики «інші скарги» (біль – 88,2%). Крім того, значна частина хворих скаржилась на печію (65,6%).
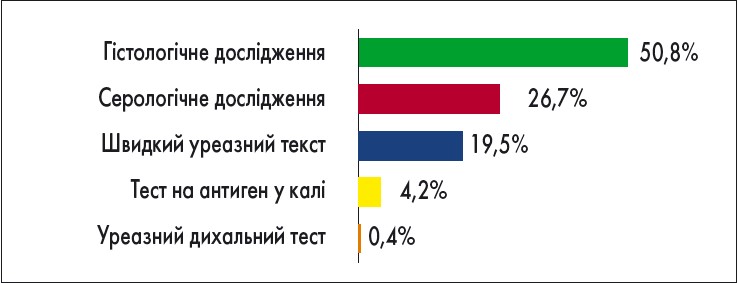
У всіх хворих до призначення лікування проводили діагностику інфекції H. pylori. Дані щодо методів первинної діагностики наведено на рис. 2.
Рис. 2. Методи діагностики інфекції H. pylori до лікування (власні дані). У деяких хворих використали кілька методів діагностики інфекції H. pylori
Переважали методи інвазивної діагностики, які потребували проведення відеоезофагогастродуоденоскопії: гістологічне дослідження і швидкий уреазний тест. Із неінвазивних методів найчастіше використовували серологічний із визначенням антитіл IgG до H. pylori у сироватці крові. Цей метод застосовували переважно у хворих, які вже приймали інгібітори протонної помпи (ІПП). Значно рідше використовували визначення антигену в калі та уреазний дихальний тест. У деяких хворих застосовували два методи первинної діагностики інфекції H. pylori: гістологічне дослідження та серологічний метод або гістологічне дослідження і швидкий уреазний тест.
Найчастіше (у 43,2% хворих) призначали потрійну терапію (ІПП, кларитроміцин, амоксицилін), а також потрійну терапію з додаванням вісмуту трикалію дицитрату (ВТД; 54,0% випадків). Стандартну квадротерапію (ІПП, тетрациклін, метронідазол, ВТД) використовували рідко (у 2,8% хворих).
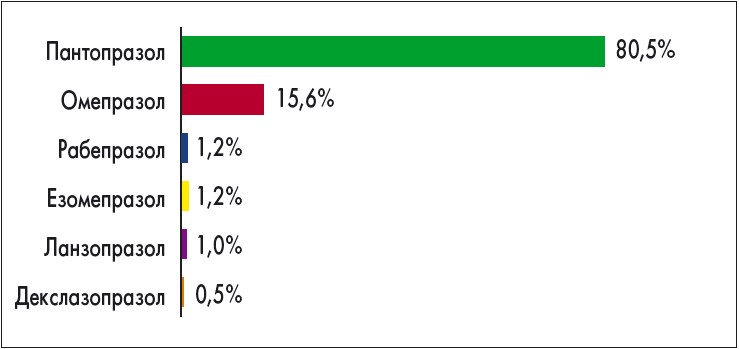
З ІПП у схемах АГБТ найчастіше призначали пантопразол (80,5%; рис. 3).
Рис. 3. Частота застосування інгібітора протонної помпи у схемах антигелікобактерної терапії (власні дані)
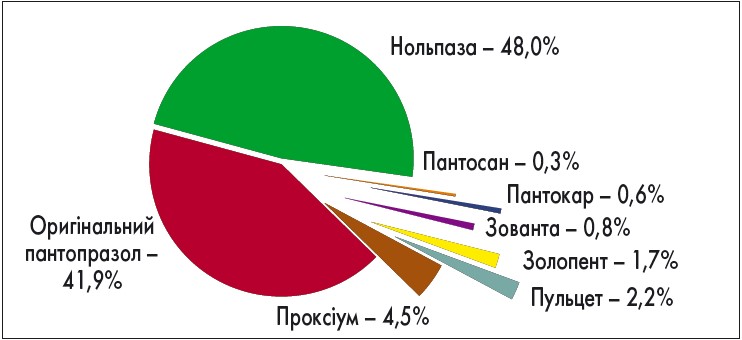
Переважне застосування пантопразолу як складника схеми АГБТ зумовлене частою поліморбідністю хворих, які приймали супутню терапію (96%) і потребували ефективного та безпечного щодо міжлікарських взаємодій ІПП. За аналізом анкет виявили, що із препаратів пантопразолу в схемах первинної лінії АГБТ переважно призначали оригінальний пантопразол та його якісний європейський генеричний препарат Нольпаза, значно рідше – інші препарати (рис. 4).
Рис. 4. Частота призначення препаратів пантопразолу (власні дані)
При призначенні потрійної терапії найчастіше рекомендували 10-денний курс АГБТ (у 40,7% випадків), при призначенні потрійної терапії з додаванням ВТД – 14-денну терапію (у 57,1%), при призначенні квадротерапії – 10- та 14-денну (у 37,5 і 62,5% відповідно). Незважаючи на низьку ефективність 7-денних схем АГБТ, лікарі використали їх у 26% випадків потрійної терапії та у 7,8% випадків потрійної терапії з додаванням ВТД (рис. 5).
 Рис. 5. Загальна тривалість антигелікобактерної терапії першої лінії за різними схемами (власні дані)
Рис. 5. Загальна тривалість антигелікобактерної терапії першої лінії за різними схемами (власні дані)
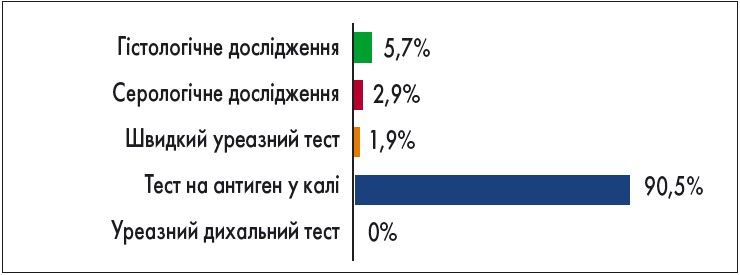
Контроль ерадикації проводили не раніше ніж через 30 днів після припинення прийому всіх препаратів схеми АГБТ, що відповідає рекомендаціям Маастрихтського консенсусу V та дає змогу запобігти отриманню хибнопозитивних результатів. Для контролю ерадикації використовували переважно неінвазивні методи (тест на виявлення антигену до H. pylori в калі; рис. 6). Однак у 2,9% пацієнтів для контролю ерадикації застосовано серологічний метод, що є суттєвою діагностичною помилкою. Позитивний результат серологічного тесту свідчить про наявність інфекції в минулому на підставі виявлення антитіл IgG до H. pylori та не може використовуватися для контролю ефективності ерадикаційної терапії. Ці антитіла з’являються через 3-4 тижні після інфікування H. pylori та можуть виявлятися ще протягом кількох місяців навіть після успішного лікування хворих. Саме тому серологічний метод є ефективним у первинній діагностиці інфекції H. pylori, але його не можна використовувати для контролю ерадикації.
Рис. 6. Методи контролю ерадикації інфекції H. pylori (власні дані).
У деяких хворих використали кілька методів контролю ерадикації
Незважаючи на високу доступність у нашому регіоні неінвазивних тестів, у 5,7% випадків контролю ерадикації лікарі використовували інвазивний метод (гістологічне дослідження біоптатів слизової оболонки).
Загальна тривалість АГБТ у 15,4% випадків становила 7 днів, у 37,6% – 10 днів, у 47,0% – 14 днів. Відзначено істотну зміну частоти призначення різних схем лікування з роками. Якщо у 2013, 2014 та 2015 рр. часто призначали 7-денну потрійну терапію (у 34, 23 та 18% випадків відповідно), то у 2016 р. таку терапію було призначено лише у 5% випадків, а у 2017 та 2018 р. не призначали взагалі. Аналогічну ситуацію виявлено і щодо призначення 10-денної потрійної терапії (25% – у 2013 р., 42% – 2014 р., 20% – у 2015 р., 10% – у 2016 р., 2% – у 2017 р.). Потрійну 14-денну терапію призначали до 2016 р. (у 20-32% випадків).
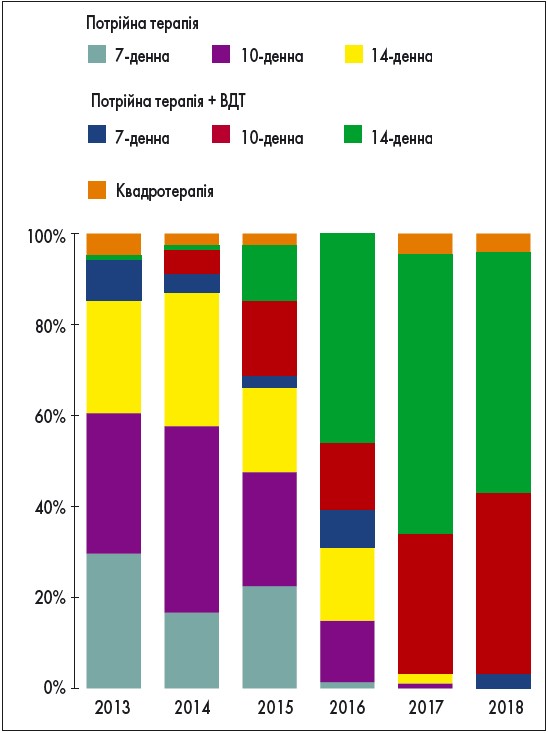
Частота призначення схем 10- та 14-денної потрійної терапії із додаванням ВТД істотно зросла з 2015 р. (рис. 7). Потрійна 14-денна АГБТ із додаванням ВТД є найпоширенішою терапією впродовж останніх 2 років (55 та 52% у 2017 та 2018 р. відповідно). Потрійну 7-денну терапію із додаванням ВТД призначали лише до 2016 р. Такий підхід до вибору схем АГБТ свідчить про відповідність призначень лікарів сучасним міжнародним рекомендаціям.
Рис. 7. Частота призначення різних схем ерадикації інфекції H. pylori (власні дані)
У Маастрихтському консенсусі V при виборі ІПП рекомендують віддавати перевагу езомепразолу та рабепразолу, що пояснюється поширеністю їх швидких метаболайзерів у Європі та Північній Америці. За даними реєстру Hp-EuReg – UKRAINE gfadeenko, найчастіше у схемах АГБТ призначали пантопразол (80,5%). Установлено високу ефективність та безпечність застосування отригінального пантопразолу та його якісного генеричного препарату (Нольпаза), особливо у поліморбідних хворих, які отримували супутню терапію та потребували безпечного щодо міжлікарських взаємодій ІПП. Відзначено зменшення частки хворих, які отримували у схемах АГБТ омепразол (15,6%), та низький рівень призначень у нашому регіоні рабепразолу та езомепразолу (по 1,2%).
При аналізі ефективності різних схем АГБТ залежно від тривалості лікування виявлено недостатню ефективність потрійної терапії та субоптимальну ефективність 10-денних схем АГБТ без призначення ВТД. Загальна ефективність 7-денної потрійної терапії становить 53,5%, 10-денної – 68,2%, 14-денної – 75,0% та не досягає рекомендованого міжнародними експертами рівня ефективності (90-95%). Ці дані свідчать про необхідність відмови від призначення схем потрійної терапії в нашому регіоні.
Дещо вищі показники ефективності відзначено при призначенні 7-денної потрійної терапії із додаванням ВТД (71,4%). Однак лише 10- та 14-денні схеми потрійної терапії із додаванням ВТД забезпечують ефективність лікування 92,6 та 94,1% відповідно.
Висновки
Аналіз даних пацієнтів, внесених до реєстру Hp-EuReg – UKRAINE, дає змогу оцінити клінічну практику та відповідність призначень міжнародним консенсусам і рекомендаціям. У деяких випадках відзначено недотримання рекомендацій експертів Маастрихтського консенсусу V щодо загальної тривалості АГБТ та контролю ефективності ерадикаційної терапії. Установлено недостатню ефективність потрійної терапії та субоптимальну ефективність 10- та 14-денних схем АГБТ без призначення ВТД. З ІПП найчастіше у схемах АГБТ призначали пантопразол. Доведено високу ефективність і безпечність застосування генеричного препарату пантопразолу (Нольпаза) порівняно з такими оригінального пантопразолу. Встановлено, що додавання ВТД до схем лікування забезпечує підвищення ефективності ерадикації (понад 90%), тому цей спосіб оптимізації АГБТ є актуальним в Україні.
У перспективі буде продовжено внесення даних до реєстру Hp-EuReg – UKRAINE з метою динамічного своєчасного аналізу клінічної практики та її відповідності міжнародним стандартам щодо ведення пацієнтів із захворюваннями, асоційованими з інфекцією H. pylori.
Література
1. Бордин Д.С., Янова О.Б., Абдулхаков Р.А. и др. Европейский регистр Helicobacter pylori (протокол Hp-EuReg): первые результаты Российских центров // Тер. архив. – 2016. – № 2. – С. 33-38.
2. Бордин Д.С., Эмбутниекс Ю.В., Вологжанина Л.Г. и др. Европейский регистр Helicobacter pylori (Hp-EuReg): анализ данных 2360 больных, получавших терапию первой линии в России // Тер. архив. – 2018. – № 2. – С. 35-42.
3. Никифорова Я.В., Черелюк Н.И., Толстова Т.Н. Основные положения Cогласительной конференции по диагностике и лечению инфекции Helicobacter pylori – Маастрихт V (2015) // Сучасна гастроентерол. – 2016. – № 6 (92). – С. 119-133.
4. Фадєєнко Г.Д., Нікіфорова Я.В. Хронічний гастрит та канцеропревенція. Роль препаратів колоїдного субцитрату вісмуту у профілактиці раку шлунка // Сучасна гастроентерол. – 2015. – № 5 (85) – С. 48-57.
5. Фадеенко Г.Д., Никифорова Я.В. Антихеликобактерная терапия. Роль препаратов висмута трикалия дицитрата в повышении эффективности стандартных схем терапии инфекции Н. p. // Новости медицины и фармации. Гастроэнтерология. – 2016 (тематический номер). – С. 36-41.
6. Chey W.D., Leontiadis G.I., Howden C.W., Moss S.F. ACG Clinical Guideline: Treatment of Helicobacter pylori Infection // Am. J. Gastroenterol. – 2017. – Vol. 112 (2). – P. 212-239.
7. Ferwana M., Abdulmajeed I., Alhajiahmed A. et al. Accuracy of urea breath test in Helicobacter pylori infection: meta-analysis // World J. Gastroenterol. – 2015. – Vol. 21. – P. 1305-1314.
8. Malfertheiner P., Megraud F., O’Morain C. A. et al. European Helicobacter and Microbiota Study Group and Consensus panel. Management of Helicobacter pylori infection – the Maastricht V/Florence Consensus Report // Gut. – 2017. – Vol. 66 (1). – P. 6-30.
9. Sugano K., Tack J., Kuipers E. J. et al. Faculty members of Kyoto Global Consensus Conference. Kyoto global consensus report on Helicobacter pylori gastritis // Gut. – 2015. – Vol. 64 (9). – P. 1353-1367. Doi: 10.1136/ gutjnl‑2015-309252.
10. Chey W., Leontiadis G., Howden C., Moss S. ACG Clinical Guideline: Treatment of Helicobacter pylori Infection // Am J. Gastroenterol. – 2017. – Vol. 112. – Р. 212-238. Doi: www.nature.com/ajg.
11. Zhang W., Chen Q., Liang X. et al. Bismuth, lansoprazole, amoxicillin and metronidazole or clarithromycin as first-line Helicobacter pylori therapy // Gut. – 2015. – Vol. 64. – P. 1715-1720.
Стаття друкується в скороченні. Сучасна гастроентерологія, № 5 (103), 2018 р.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 4 (50), грудень 2018 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...