Кардіоонкологія – новий напрямок в Україні: принципи мультидисциплінарного підходу
 На базі ННЦ «Інститут кардіології ім. М.Д. Стражеска» НАМН України (м. Київ) був створений Експертний консультативно-діагностичний центр із кардіоонкології (далі – Центр), фахівці якого можуть надавати всю необхідну кардіологічну допомогу онкологічним хворим (переважно амбулаторну, але за потреби й стаціонарну). Про те, як розвивається сьогодні в Україні нова галузь медицини – кардіоонкологія, наш кореспондент бесідувала з керівником відділу клінічної фармакології ННЦ «Інститут кардіології ім. М.Д. Стражеска» НАМН України, доктором медичних наук С.М. Кожуховим.
На базі ННЦ «Інститут кардіології ім. М.Д. Стражеска» НАМН України (м. Київ) був створений Експертний консультативно-діагностичний центр із кардіоонкології (далі – Центр), фахівці якого можуть надавати всю необхідну кардіологічну допомогу онкологічним хворим (переважно амбулаторну, але за потреби й стаціонарну). Про те, як розвивається сьогодні в Україні нова галузь медицини – кардіоонкологія, наш кореспондент бесідувала з керівником відділу клінічної фармакології ННЦ «Інститут кардіології ім. М.Д. Стражеска» НАМН України, доктором медичних наук С.М. Кожуховим.
? Сергію Миколайовичу, пропоную спочатку охарактеризувати в цілому проблему, що пов’язана з кардіотоксичним впливом протипухлинної терапії. Отже, що таке кардіотоксичність, які її основні прояви?
– Є декілька визначень кардіотоксичності, але всі вони відображають як прямий несприятливий вплив протиракового лікування на кардіоміоцити у вигляді серцевої недостатності (СН) та порушень ритму, так і непрямі ефекти, пов’язані зі зміною кардіогемодинаміки (клапанні порушення) чи тромбозами.
Розрізняють декілька типів кардіотоксичності:
- Гостра кардіотоксичність розвивається миттєво під час введення та/або до 2-3 днів після застосування хіміотерапії та може трансформуватися в ранню (від перших тижнів до 1 року). Частота виявлення – близько 11%. Клінічно гостра чи рання кардіотоксичність може проявлятися болем у грудях, серцебиттям, а з патофізіологічного погляду це міоперикардит – наслідок набряку міофібрил і перикардіального мезотелію. На електрокардіограмі розпізнається як синусова тахікардія, передсердні та шлуночкові екстрасистоли, надшлуночкові тахікардії. Гостра лівошлуночкова СН проявляється дуже рідко, й вона, як правило, зворотна.
- Пізня кардіотоксичність трапляється набагато рідше, іноді маніфестує через рік після застосування останньої дози протиракових лікарських засобів, але може виникнути навіть через 6-10 років після введення препаратів. Факторами ризику є інші кардіотоксичні впливи, медіастинальна променева терапія, старший вік, анамнез кардіоваскулярних захворювань.
? Які серцево-судинні ускладнення найчастіше виникають при проведенні протиракової терапії?
– Виділяють такі основні серцево-судинні ускладнення, що виникають унаслідок дії протипухлинної терапії: дисфункція міокарда лівого шлуночка та СН; захворювання коронарних артерій, ішемічна хвороба серця (зокрема гострий коронарний синдром); ураження клапанів серця; аритмії, особливо у разі застосування препаратів, які подовжують інтервал QT; артеріальна гіпертензія; тромбоемболічні ускладнення; пошкодження периферичних артерій та інсульт; легенева гіпертензія; захворювання перикарда.
Це далеко не повний перелік, оскільки в реальну клінічну практику впроваджуються протипухлинні препарати з новими механізмами дії, та ми ще не маємо досвіду їхнього тривалого використання та спостереження.
? Які ускладнення при проведенні поліхіміотерапії трапляються найчастіше?
– Найчастіше виявляються дисфункція міокарда лівого шлуночка та СН. Клінічні прояви можуть з’явитися одразу ж після експозиції, але іноді маніфестують через роки.
Пацієнти, котрі в дитячому віці перенесли рак і отримували лікування антрациклінами та/або медіастинальну променеву терапію, мають у 15 разів вищу ймовірність виникнення СН. У дорослих пацієнтів із серйозними серцево-судинними факторами ризику наявний несприятливий короткотривалий прогноз щодо розвитку СН. За даними клінічних досліджень, реальна поширеність дисфункції міокарда лівого шлуночка становить 9% протягом перших 12 міс.
Також слід зазначити негативний вплив променевої терапії на розвиток СН. Наприклад, у пацієнтів із раком грудної залози ризик кардіотоксичності є найвищим при поєднанні лівобічного променевого лікування та протипухлинних препаратів із потенційно кардіотоксичною дією, що свідчить про їхній несприятливий синергічний ефект на міокард. Із патофізіологічної точки зору це – значний інтерстиційний фіброз міокарда. Систолічна дисфункція зазвичай спостерігається при поєднанні радіотерапії з антрациклінами. Крім того, СН може посилюватися/прогресувати за рахунок супутнього впливу променевого лікування на клапанний апарат серця та розвиток захворювання коронарних судин.
Окремо слід зупинитися на тромбоемболічних ускладненнях. Якщо у хворих на рак внутрішньоартеріальні тромбоутворення трапляються рідко (близько 1%) у вигляді гострого коронарного синдрому, порушень мозкового кровообігу, то венозні тромбози та тромбоемболії діагностують у 20% госпіталізованих пацієнтів з онкологічними захворюваннями. Часто венозні тромбоемболії діагностують випадково при застосуванні візуалізаційних методів досліджень, адже з клінічної точки зору майже 50% венозних тромбоемболій є асимптомними.
? Цілком логічно присвятити частину нашої бесіди історії розвитку кардіоонкології у світі. Як усе починалося?
– Перші кардіологічні відділи в онкологічних центрах з’явилися в США приблизно 15-20 років тому. Це було зумовлено проблемою токсичного впливу на міокард препаратів анти-HER2+ у пацієнток із раком грудної залози та застосуванням інгібіторів тирозинкінази. Вдалося досягти таких результатів: хворі почали отримувати протиракову терапію в повному обсязі, покращилась якість життя. Досвід почав швидко поширюватися. У 2007 р. відбулася перша конференція з кардіоонкології (Houston, США), а 2009 р. було засноване Міжнародне кардіоонкологічне товариство. У 2016 р. Європейським товариством кардіологів було видане перше керівництво «Position Paper on cancer treatments and cardiovascular toxicity developed under the auspices of the ESC Committee for Practice Guidelines: The Task Force for cancer treatments and cardiovascular toxicity of the European Society of Cardiology».
На сьогодні взірцем кардіоонкології є США. У кожному штаті функціонують кардіоонкологічні відділення, також наявні декілька великих регіональних центрів при університетських клініках та інститутах. Запроваджено цільові державні програми для вивчення питань кардіотоксичності при проведенні протипухлинного лікування.
У Західній Європі ситуація від країни до країни відрізняється. Найбільший досвід отриманий в Італії, Швейцарії, Іспанії. Є окремі центри та відділення при великих клініках і шпиталях. У Східній Європі питання кардіоонкологічної допомоги називати пріоритетним поки що рано.
На сучасному етапі кардіоонкологія стає ще актуальнішою, оскільки технології лікування раку значно розвинулися, виживаність пацієнтів покращилася, й це збільшує потребу в підтримувальній терапії. Слід зауважити, що при виявленні та лікуванні окремих локалізацій раку на ранніх стадіях рівень виліковності наближається до 100%, і вкрай важливо, щоб хворі, яким вдалося врятувати життя, могли насолоджуватися ним повною мірою, а не боротися надалі з наслідками протипухлинної терапії. Крім того, збільшується частка осіб із супутніми захворюваннями, тож проблема кардіотоксичності може виходити на перший план.
? Чи є керівництва, які регламентували б роботу кардіоонкологічних відділень?
– У серпні 2018 р. вийшло перше керівництво Європейського товариства кардіологів «Cardio-Oncology Services: rationale, organization, and implementation: A report from the ESC Cardio-Oncology council», в якому на основі досвіду США й окремих країн Європи наведені головні принципи організації кардіоонкологічної допомоги: для чого це потрібно, що для цього необхідно, структура, штат, обладнання, принципи мультидисциплінарного підходу тощо.
? Як розвивається кардіоонкологія в Україні?
– Ідея розвитку цього напряму в Україні належить співробітникам відділу клінічної фармакології ННЦ «Інститут кардіології ім. М.Д. Стражеска» НАМН України, й ця діяльність почалася 2016 р. із планування наукової тематики відділу, адже питання кардіоонкології тісно пов’язані з клінічною фармакологією. Оскільки кардіоонкологія – це нова субспеціалізація, то для здобуття досвіду співробітники відділу проходили стажування в Національному інституті раку МОЗ України, отримували другу спеціалізацію із клінічної онкології та, нарешті, стажувалися у передових центрах – Європейському інституті онкології (Мілан, Італія), університетській клініці «Інзельшпиталь» (Берн, Швейцарія).
Необхідність концентрування уваги на проблемах, що пов’язані з токсичним впливом протипухлинних засобів, зумовлена сумною статистикою: в Україні щороку лікарі реєструють близько 130 тис. пацієнтів з онкологічними захворюваннями (торік – 143 тис.). За даними МОЗ, нині у країні є понад мільйон хворих на рак. При цьому онкологічна патологія посідає друге місце серед причин смертності населення.
Україна друга в Європі за темпами поширення раку. За останні 10 років у нашій країні відзначають невпинну тенденцію до зростання рівня захворюваності на злоякісні новоутворення з щорічним підвищенням приблизно на 3%.
Протипухлинні препарати одночасно з основною антинеопластичною дією часто чинять токсичний вплив на серце. Тому сьогодні клінічна фармакологія, крім дослідження основних властивостей нових лікарських засобів, також займається вивченням їхніх негативних ефектів, зокрема кардіотоксичності як у короткі, так і віддалені терміни.
Цьогоріч у межах XIX Національного конгресу кардіологів України було проведено секцію «Кардіоонкологія в реальній клінічній практиці: стратегії профілактики та лікування серцево-судинних ускладнень у онкологічних хворих», в якій брали участь кардіологи, онкологи та спеціалісти з функціональної діагностики. Зі вступним словом на секції виступив директор ННЦ «Інститут кардіології ім. М.Д. Стражеска» НАМН України, академік В.М. Коваленко, який зазначив важливість розвитку кардіоонкології, необхідність співпраці у цьому напрямі з Європейським товариством кардіологів та імплементації рекомендацій товариства з кардіоонкології. Володимир Миколайович підкреслив, що це перший захід у сфері кардіоонкології в Україні, й увага лікарів до нього підтвердила актуальність проблеми.
? Які завдання стоять наразі перед спеціалістами у галузі кардіоонкології? Які хворі отримують консультації в Центрі?
– Кардіоонколог – це лікар, який виявляє, лікує та запобігає серцево-судинним подіям у хворих на рак до, під час та після протипухлинного лікування. Його головне завдання – корекція кардіоваскулярних захворювань і кардіотоксичних ускладнень, що є бар’єром для проведення протиракової терапії в повному обсязі. Ще один важливий пункт – консультація пацієнта кардіологом перед виконанням комплексних протипухлинних заходів: оперативного втручання, поліхіміотерапії та променевого лікування. Це дає можливість виявити фактори ризику серцево-судинних ускладнень, провести відповідну профілактику, а в осіб із кардіоваскулярними захворюваннями – призначити або переглянути терапію, тобто максимально підготувати до неї.
Не менш важливе завдання кардіоонкології полягає в моніторингу кардіотоксичності у процесі та після проведення протипухлинної терапії, насамперед у пацієнтів високого ризику, оскільки ускладнення можуть виникати як негайно після введення першої дози протипухлинного препарату, так і через тривалий час (рання та пізня кардіотоксичність відповідно). Довгочасне спостереження є необхідним для хворих, які отримали поліхіміотерапію та/або променеве лікування, адже в деяких випадках кардіотоксичність може проявитися через 5 і 10 років після завершення усіх терапевтичних заходів.
Протягом останніх двох років ми надаємо консультативну допомогу онкологічним хворим зі всієї України. Передусім консультуємо та спостерігаємо за станом пацієнтів, у яких під час проведення поліхіміотерапії, таргетного та променевого лікування виникли серцево-судинні ускладнення. Крім того, перед онкологом/хіміотерапевтом могло постати питання: призупинити життєво важливу терапію, перейти на прийом препаратів, які є менш кардіотоксичними (але також можуть бути недостатньо ефективними), або взагалі використовувати паліативне лікування? Результати нашої роботи нещодавно були опубліковані в журналі OncoReview (Kozhukhov S., Dovganych N., Smolanka I., Lyhyrda O. Cardio-oncology in Ukraine: experience at Strazhesko Institute of Cardiology, 2018; 8 (3): 65-69).
? Як розвивається співпраця Центру з українськими онкологами?
– Цей напрям роботи активізувався, зацікавленість обох сторін є очевидною. Ми почали тісно співпрацювати з Національним інститутом раку МОЗ України, а також іншими профільними установами. Більшість онкологів, які вже об’єднали зусилля з кардіологами, зрозуміли важливість і необхідність цієї співпраці, що є важливою умовою забезпечення онкологічних пацієнтів адекватною супроводжувальною терапією. Ми плануємо проведення спільних з онкологами науково-практичних заходів.
Звичайно, якщо аналізувати в історичному аспекті, то були часи, коли співпраці кардіологів та онкологів заважали непорозуміння. І навіть відбувалося протистояння. На сьогодні всі суперечності успішно вирішуються, й ми маємо надію, що знаходимося на шляху до втілення командного підходу у веденні онкологічних хворих із високим ризиком серцево-судинних ускладнень.
? Як має здійснюватися командний підхід у лікуванні онкологічних хворих у реальній практиці?
– Командний підхід передбачає співпрацю онколога не тільки з кардіологом, але й із гематологом, психіатром, психотерапевтом та іншими спеціалістами. Після встановлення діагнозу онкологічного захворювання й до проведення протипухлинного лікування пацієнт має бути оглянутий кардіологом на предмет виявлення та модифікації серцево-судинних факторів ризику, а за наявності таких захворювань – їхньої медикаментозної корекції. Онколог/хіміотерапевт призначає поліхіміотерапію (у разі потреби разом із радіологом – променеве лікування), а за наявності факторів ризику кардіотоксичності спрямовує до кардіолога. У процесі проведення поліхіміотерапії в певні проміжки часу виконують моніторинг показників серцево-судинної системи (електро-, ехокардіографія), за потреби – профілактику чи лікування серцево-судинних ускладнень. Відомо, що під час протипухлинного лікування можуть виникати значні зрушення з боку показників крові (лейкоцитопенія, анемія, тромбоцитопенія), тоді необхідною може бути консультація гематолога.
Часто пацієнти з онкозахворюваннями потребують психологічної допомоги та соціальної адаптації. Після закінчення протипухлинного лікування вони мають спостерігатися лікарем первинної ланки для моніторингу рецидиву раку чи виникнення проявів кардіотоксичності. Це ідеальний варіант мультидисциплінарної командної роботи, й до цього потрібно прагнути (рис.).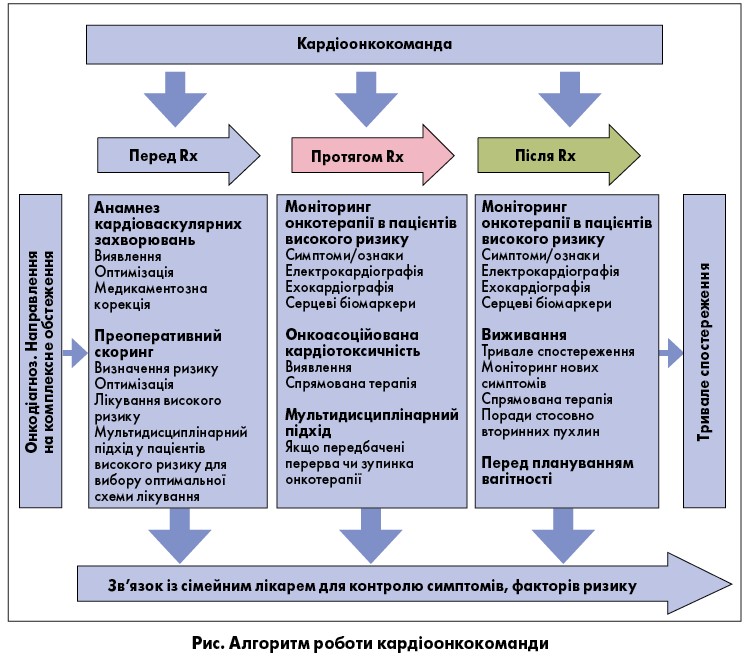
Наприкінці бесіди хочу зазначити, що на базі нашого інституту є абсолютно всі інструменти для надання якісної високоспеціалізованої допомоги онкологічним хворим. І головне – є розуміння необхідності міждисциплінарної взаємодії для покращення якості життя та підвищення виживання онкологічних хворих, що нами й демонструється на прикладі тісної співпраці ННЦ «Інститут кардіології ім. М.Д. Стражеска» НАМН України та Національного інституту раку МОЗ України.
Підготувала Наталя Очеретяна
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 5 (60) листопад 2018 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....




