Выбор альтернативного препарата для антибактериальной терапии негоспитальной пневмонии
 Пневмония и в XXI веке остается важной медико-социальной проблемой. Это обусловлено в первую очередь ее значительной распространенностью, достаточно высокими показателями инвалидизации и смертности, а также значительными экономическими потерями вследствие этого заболевания.
Пневмония и в XXI веке остается важной медико-социальной проблемой. Это обусловлено в первую очередь ее значительной распространенностью, достаточно высокими показателями инвалидизации и смертности, а также значительными экономическими потерями вследствие этого заболевания.
Негоспитальная пневмония (НП) – это острое заболевание, которое возникает во внебольничных условиях (за пределами стационара, либо позднее 4 нед после выписки из него, либо диагностировано в первые 48 ч от момента госпитализации). Процесс сопровождается симптомами инфекции нижних дыхательных путей (лихорадка, кашель, выделение мокроты, возможно, гнойного характера, боль в груди и одышка), а также рентгенологическими признаками вновь возникших очагово-инфильтративных изменений в легочной ткани при отсутствии очевидной диагностической альтернативы.
Современные алгоритмы антибактериальной терапии пневмонии изложены в отечественных рекомендациях, которые учитывают опыт европейских систем здравоохранения. Однако до сих пор допускается достаточное количество ошибок в выборе антибиотика для лечения этого заболевания. Неправильное назначение антибактериальных препаратов (АБП) оказывает решающее влияние на исход заболевания, снижает экономическую эффективность лечения и ведет к селекции резистентных штаммов возбудителей. Адекватно и своевременно начатая антибактериальная терапия является необходимым условием эффективного лечения и, следовательно, благоприятного исхода пневмонии. Участковый терапевт часто бывает первым медицинским работником, к которому обращается больной. Поэтому знание современных аспектов антибактериальной терапии необходимо для правильного выбора препарата. Принципы лечения НП достаточно хорошо изучены и представлены во многих международных и региональных рекомендациях, однако проблема рациональной антибактериальной терапии больных НП не теряет актуальности и в настоящее время.
Для адекватного выбора антибактериальной терапии в настоящее время предлагается разделять всех взрослых пациентов на четыре группы [2].
К I группе относят больных НП легкой степени, которые не требуют госпитализации, без сопутствующей патологии, и тех, которые в последние 3 мес не принимали АБП. Наиболее часто возбудителями НП у таких пациентов являются S. pneumoniae, M. pneumoniae, C. pneumoniae, H. influenzae (как правило, у курильщиков) и респираторные вирусы. У 30-50% пациентов возбудителя не определяют вообще, так как проводить рутинную микробиологическую диагностику нецелесообразно. Определенную ценность могут иметь данные эпидемиологических исследований (групповая заболеваемость лиц молодого возраста в организованных коллективах характерна для инфекции, вызванной S. pneumoniae или M. pneumoniae).
Ко II группе относят больных НП легкой степени, которые не требуют госпитализации, с наличием сопутствующей патологии (хроническое обструктивное заболевание легких, почечная и сердечная недостаточность, цереброваскулярная патология, опухоли, сахарный диабет, хронические заболевания печени разной этиологии, психические расстройства, алкоголизм) и/или тех, которые принимали в последние 3 мес АБП. Возбудителями НП у этих пациентов являются S. pneumoniae (в том числе антибиотикорезистентные штаммы), H. influenzae, S. aureus, респираторные вирусы. Следует учитывать и возможность грамотрицательной инфекции (семейство Enterobacteriaceae: E. coli, Klebsiella spp.), особенно у людей пожилого возраста. Необходимо предвидеть также вероятность анаэробной инфекции при наличии НП у лиц с несанированной полостью рта, клинико-анамнестическими данными наличия неврологических заболеваний и/или нарушением акта глотания. Рутинная микробиологическая диагностика у этих больных также малоинформативна и практически не влияет на выбор антибиотиков. Однако примерно у 20% больных этой группы может возникнуть потребность в госпитализации из-за неэффективного амбулаторного лечения и/или обострения/декомпенсации сопутствующих заболеваний.
К III группе относят больных НП средней степени тяжести, которые требуют госпитализации в терапевтическое (пульмонологическое) отделение по медицинским показаниям (наличие неблагоприятных прогностических факторов). У пациентов этой группы НП может быть обусловлена S. pneumoniae, H. influenzae, атипичными возбудителями, грамотрицательными энтеробактериями, респираторными вирусами. У 10-40% больных III группы нередко выявляют «смешанную» инфекцию (то есть наличие типичных и атипичных бактериальных возбудителей). Такая разница в частоте выявления возбудителей обусловлена особенностями микробиологических методов диагностики, которые используют разные исследователи.
К IV группе относят больных НП с тяжелым течением, которые требуют госпитализации в отделение реанимации и интенсивной терапии (ОРИТ). Спектр микробной флоры у таких пациентов включает S. pneumoniae, Legionella spp., H. influenzae, грамотрицательные энтеробактерии, S. aureus и M. pneumoniae (достаточно редко).
Антибактериальная терапия больным НП назначается в зависимости от группы, к которой относится пациент (табл.).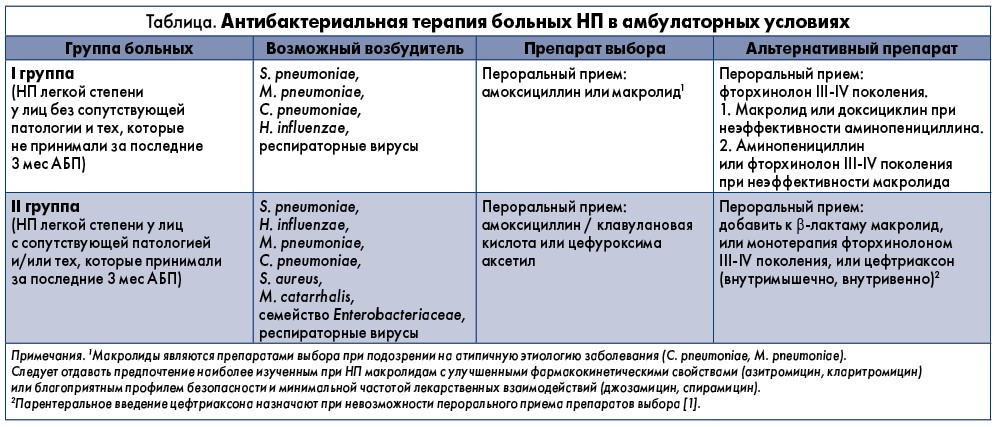
При наблюдении пациентов с НП необходимо:
- оценить степень тяжести и прогноз заболевания;
- решить вопрос о месте лечения (амбулаторно, стационарно);
- выбрать стартовую эмпирическую терапию.
Выбор места лечения определяет объем лечебно-диагностических процедур и финансовых затрат. Согласно современным принципам ведения взрослых пациентов с НП, значительное их количество (80%) может лечиться амбулаторно [2]. От 30 до 50% пациентов, госпитализированных по поводу НП, с успехом могут лечиться в домашних условиях. В связи с этим особое значение придается определению критериев или показаний для госпитализации, которые базируются на ряде известных клинико-лабораторных шкал. Наиболее простой и доступной для рутинного использования в амбулаторных условиях является прогностическая шкала CRB‑65. В ее основе лежит модифицированная шкала Британского торакального общества, в которой учитывается оценка четырех параметров:
- нарушение сознания (Confusion);
- частота дыхания ≥30/мин (Respiratory rate);
- систолическое артериальное давление (АД) <90 мм рт. ст. или диастолическое АД ≤60 мм рт. ст. (Blood pressure);
- возраст >65 лет (65).
В зависимости от вероятности летального исхода пациенты разделяются на три группы, каждая из которых отвечает определенной степени тяжести заболевания и для каждой из которых рекомендуется преимущественное место лечения (рис.). Минимальное количество баллов по этой шкале – 0, максимальное – 4:
- 0 баллов – течение болезни оценивается как легкое (риск летальности – 1,2%), лечение проводится амбулаторно;
- 1 (2*) балла (где * означает, что пациент старше 65 лет) – НП средней тяжести (риск летальности – 8,15%), лечение рекомендуется проводить в стационаре;
- 2-3 (3-4*) балла – состояние оценивается как тяжелое (риск летальности – 31%), требуется срочная госпитализация в ОРИТ.

Антибактериальную терапию назначают эмпирически, то есть учитывается чувствительность наиболее вероятных возбудителей. Для проведения эмпирической антибактериальной терапии необходимо применять АБП, которые:
- имеют направленный спектр антимикробного действия – высокую активность в отношении вероятных возбудителей НП;
- имеют оптимальный профиль безопасности (низкая частота развития побочных эффектов);
- способны создавать высокие концентрации в тканях и биологических жидкостях органов дыхания;
- имеют оптимальное соотношение стоимость/эффективность;
- удобно применять, что способствует приверженности пациента к лечению (комплаенсу). Это особенно важно при амбулаторном лечении социально активных пациентов, которые нарушают режим приема препаратов. Комплаенс в значительной мере зависит от необходимой частоты приема лекарственного средства на протяжении суток, а также от длительности курса лечения. В таких случаях преимущество отдают препаратам, которые назначают 1-2 раза в сутки и/или короткими курсами.
Выбор АБП для этиотропной терапии больных НП осуществляется с учетом их природной активности к основным возбудителям заболевания. Стартовая антибактериальная терапия выстраивается так, чтобы бороться с пневмококками и гемофильной палочкой. Если есть основания подозревать внутриклеточные патогены, терапия должна быть направлена и против них.
У больных НП I группы адекватный клинический эффект возможен при пероральном приеме АБП в виде монотерапии. В качестве препарата выбора рекомендованы амоксициллин или макролид (азитромицин, кларитромицин, спирамицин). In vitro амоксициллин не перекрывает весь спектр потенциальных патогенов, однако, по данным контролированных исследований, не выявлено достоверных различий в эффективности терапии с использованием антибиотиков этих групп, а также отдельных классов представителей макролидов. При использовании препаратов, в спектр действия которых входят только пневмококки и гемофильная палочка, эмпирическая антибиотикотерапия НП может быть эффективной примерно у 70-80% пациентов [1, 3]. В случае неэффективности амоксициллина через 48-72 ч лечения в качестве альтернативного препарата назначают макролид или доксициклин. Это обусловлено их высокой активностью в отношении атипичных возбудителей, которые могут быть наиболее вероятной причиной неудачного лечения аминопенициллином. В случае неэффективности стартовой антибиотикотерапии макролидом альтернативным препаратом может быть амоксициллин или фторхинолон III-IV поколения. Возможными причинами неэффективности лечения макролидом могут быть наличие резистентных к этой группе антибиотиков штаммов пневмококка или то, что заболевание вызвано грамотрицательными возбудителями.
У больных II группы выраженный клинический эффект также возможен в случае перорального приема антибиотиков. Однако, поскольку увеличивается вероятность этиологической роли грамотрицательных микроорганизмов (в том числе имеющих механизм развития резистентности к антибиотикам), в качестве препарата выбора рекомендуется защищенный аминопенициллин или цефалоспорин II поколения. В качестве альтернативной терапии могут быть назначены фторхинолоны III-IV поколения. При невозможности перорального приема препарата или низкого комплаенса назначается парентеральный антибиотик. У пациентов II группы отсутствие эффекта при лечении препаратами выбора может быть связано с тем, что этиопатогенами НП являются атипичные возбудители. Поэтому на втором этапе антибиотикотерапии следует добавлять макролид к β-лактаму или же вместо комбинированной терапии назначить монотерапию фторхинолоном III-IV поколения. Фторхинолоны III-IV поколения (их еще называют «новыми», или «респираторными») характеризуются повышенной активностью в отношении S. pneumoniae и внутриклеточных патогенов, устраняют, помимо пневмококков, всех типичных возбудителей внебольничных инфекций нижних дыхательных путей – стафилококки, гемофильную палочку, моракселлы и другую внебольничную грамотрицательную микрофлору, а также внутриклеточные патогенны и анаэробы [1]. Новые фторхинолоны сохраняют активность и в отношении штаммов S. pneumoniae, устойчивых к пенициллину, макролидам и фторхинолонам первых поколений. Они обладают также более высокой активностью в отношении стафилококков и умеренной – метициллинрезистентных стафилококков. Все фторхинолоны активны против хламидий и микоплазм: ранние – в умеренной степени, новые – в высокой.
Таким образом, в последнее время основными моментами, требующими коррекции в схемах терапии НП, являются:
- растущая резистентность пневмококка к стандартно применяемым АБП (у незащищенных β-лактамных АБП и макролидов);
- необходимость воздействия также на атипичную (внутриклеточную) флору (этой способности лишены все β-лактамные АБП).
Моксифлоксацин и гемифлоксацин проявляют наиболее высокую активность против респираторных патогенов in vitro. Резистентность штаммов внебольничных респираторных патогенов к новым фторхинолонам развивается медленно или вообще не развивается. Фторхинолоны оказывают бактерицидный эффект, ингибируя два жизненно важных фермента микробной клетки – ДНК‑гиразу и топоизомеразу IV, нарушают синтез ДНК патогенного микроорганизма.
Фторхинолоны III-IV поколения получили название «респираторных» в связи с высокой активностью в отношении бактериальных инфекций верхних и нижних дыхательных путей. Они быстро абсорбируются и распределяются в тканях организма. Все новые фторхинолоны имеют бактерицидную активность и постантибиотический эффект, большой период полувыведения, что позволяет применять их 1 раз в сутки. Вследствие угнетения топоизомераз II и IV они оказывают бактерицидное действие и демонстрируют высокую активность in vivo, поскольку обладают высоким уровнем распределения и пенетрации, накапливаясь в тканях и клетках-мишенях в количествах, значительно превышающих необходимую минимальную подавляющую концентрацию. В частности, отмечают высокую степень накопления препаратов в респираторных путях – слизистой оболочке бронхов, бронхиальном секрете, альвеолярных макрофагах. Высокие внутриклеточные концентрации являются предиктором эффективной эрадикации атипичных (внутриклеточных) микроорганизмов [4]. В механизмах действия хинолонов относительно грамположительных и грамотрицательных микроорганизмов имеются некоторые отличия. Основной мишенью действия хинолонов у грамотрицательных микроорганизмов является ДНК‑гираза (топоизомераза IV менее значима), у грамположительных – наоборот. Большинство нефторированных и фторированных хинолонов обладают большим сродством с ДНК‑гиразой, с чем и связана их преимущественная активность относительно грамотрицательных микроорганизмов. Причем степень аффинности (сродства) к ДНК‑гиразе, а следовательно, и антибактериальная активность против грамотрицательных бактерий у всех препаратов этой группы примерно одинаковы. Однако ряд новых фторхинолонов обладают высокой активностью в отношении грамположительных микроорганизмов, что, вероятно, объясняется их повышенным сродством к топоизомеразе IV. По результатам одних исследований, моксифлоксацин, гемифлоксацин, спарфлоксацин и гатифлоксацин обладают активностью в отношении ДНК‑гиразы, по результатам других – к топоизомеразе IV. Имеются также предположения, что их активность, особенно моксифлоксацина и гемифлоксацина, распространяется на оба фермента [7].
При высокой эффективности препараты этой группы достаточно безопасны. Побочные эффекты связаны в основном с реакциями со стороны желудочно-кишечного тракта и сравнимы с таковыми при использовании препаратов для стандартной терапии инфекционных заболеваний нижних дыхательных путей.
Среди препаратов последнего поколения фторхинолонов, имеющихся на фармацевтическом рынке Украины, наибольшей активностью против грамположительных бактерий (пневмококков и стафилококков) обладает моксифлоксацин – препарат IV поколения. Он характеризуется повышенной антибактериальной активностью в отношении патогенов, устойчивых к действию фторхинолонов предыдущих поколений, и расширенным спектром действия в отношении грамположительных микроорганизмов. Левофлоксацин и гатифлоксацин уступают ему по активности влияния на грамположительные бактерии и анаэробы. Моксифлоксацин – наиболее активен среди указанных антибиотиков в отношении пенициллинрезистентных пневмококков, стафилококков, гемофильной палочки, клебсиеллы, легионеллы in vitro; как и защищенные аминопенициллины, наиболее активен против анаэробов [5].
Результаты многочисленных многоцентровых сравнительных клинических исследований, клинический опыт медицинской практики свидетельствуют о преимуществах моксифлоксацина в отношении как эффективности и безопасности, так и экономической выгоды при лечении НП, в том числе вызванной атипичными патогенами и пенициллинрезистентными S. pneumoniae.
В исследовании Finch R. и соавт. сравнивали эффективность ступенчатой терапии у 538 пациентов со среднетяжелой и тяжелой НП, применяя моксифлоксацин внутривенно/перорально в дозе 400 мг 1 раз в сутки (n=258), амоксициллин/клавуланат 1,2 г внутривенно / 625 мг по 3 раза в сутки с кларитромицином (n=193) либо без него (n=87) внутривенно/перорально – 50 мг 2 раза в сутки. Лечение проводили в течение 7-14 дней под контролем клинико-лабораторных показателей. Преимущества лечения моксифлоксацином были очевидны по всем основным показателям. Так, клинический успех терапии, который оценивали на 5-7-й день, был статистически достоверно выше при использовании моксифлоксацина (93,4%), чем амоксициллина/клавуланата ± кларитромицина (85,4%). Более чем в 2 раза чаще наблюдались клинические неудачи при назначении последней схемы лечения (6,6 и 14,6% соответственно).
Микробиологическая эффективность (эрадикация и предполагаемая эрадикация инфекционных возбудителей) была также достоверно выше в группе больных, получающих моксифлоксацин (94%), чем в группе сравнения (82%). Причем эрадикация S. pneumoniae, H. influenzae (в мокроте и крови), M. pneumoniae, C. pneumoniae, L. pneumophila, обнаруженных в группе больных пневмонией, которые получали моксифлоксацин, отмечена в 100% случаев. В то же время в группе сравнения эрадикация S. pneumoniae в мокроте составляла 81,3%, в крови – 100%; H. influenzae в мокроте – 88,9%, в крови – 100%; M. pneumoniae – 94,1%; С. pneumoniae – 80%; L. pneumophila – 75%. То есть, несмотря на введение в схему комбинированной терапии макролида, проникающего внутриклеточно и теоретически эффективного в отношении атипичных патогенов, эрадикация их при сочетанной терапии с амоксициллином/клавуланатом была значительно ниже [5].
Моксифлоксацин зарекомендовал себя как эффективный препарат, превосходящий другие применяемые для лечения больных НП лекарственные средства. В многоцентровом двойном слепом исследовании оценивали клиническую и бактериологическую эффективность 10-дневного применения моксифлоксацина (по 400 мг 1 раз в сутки) при сравнении с кларитромицином (по 500 мг 2 раза в сутки). Лечили соответственно 194 и 188 больных НП, вызванной в 15 и 18% случаев S. pneumoniae, в 46 и 47% – C. pneumoniae, в 22 и 19% – M. pneumoniae, в 21 и 15% – H. influenzae; остальные микроорганизмы (K. pneumoniae, P. aeruginosa, M. catarrhalis, S. aureus) встречались реже (2-6%). После лечения клинический эффект моксифлоксацина и кларитромицина составил 97 и 95% соответственно. При последующем обследовании эти показатели составляли 98 и 99%. При инфекциях, вызванных атипичными микробами, эффективность равнялась 96 и 99%, а при инфекциях, вызванных только типичными микробами, – 100 и 97%. Бактериологический эффект моксифлоксацина и кларитромицина (подлежали оценке соответственно 110 и 104 пациента) составил 97 и 98%, при этом при инфекциях, вызванных C. pneumoniae, эрадикация микроорганизмов равнялась 92 и 98%, M. pneumoniae – 96 и 100%, H. influenzae – 96 и 88%, M. catarrhalis – 100 и 100%, K. pneumoniae – 100 и 100%, S. pneumoniae – 100 и 95%, S. aureus – 100 и 100% соответственно. Установлена высокая корреляция между клиническим эффектом и эрадикацией микробов. Существенных различий в эффективности моксифлоксацина и кларитромицина не выявлено, что говорит о высокой эффективности моксифлоксацина не только при наличии типичных возбудителей, но и при атипичной флоре [12].
Высокая клиническая и бактериологическая эффективность моксифлоксацина позволили включить его в перечень АБП, которые можно рекомендовать пациентам с НП в качестве альтернативных препаратов.
Широкий спектр действия моксифлоксацина дает лечащему врачу возможность назначить его эмпирически в случае неэффективности первоначально назначенного антибиотика.
Высокая биодоступность моксифлоксацина позволяет использовать на амбулаторном этапе таблетированные формы, а не внутримышечные инъекции, которые не удобны для больного и требуют дополнительных расходов.
Возможность применения короткого курса терапии (5 дней) и режим приема 1 раз в сутки повышают приверженность пациентов к лечению.
Появление на рынке Украины достойных генерических препаратов моксифлоксацина (Мофлакса) способствует получению пациентами качественного лечения при умеренных финансовых затратах.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 22 (443), листопад 2018 р.
СТАТТІ ЗА ТЕМОЮ Пульмонологія та оториноларингологія
Риносинусит (РС) незмінно потрапляє до десятки найпоширеніших діагнозів в амбулаторній лікарській практиці та посідає 5-те місце серед захворювань, щодо яких призначається антибактеріальна терапія [1]. Симптоми гострих РС маніфестують тоді, коли уражаються слизові оболонки приносових пазух і порожнини носа. Оскільки слизова оболонка носа та приносових пазух – єдине ціле, гострий запальний процес уражатиме ці слизові оболонки, а ізольоване запалення слизової оболонки порожнини носа чи будь-якої з приносових пазух може визначатися при хронічних захворюваннях [2]. Це обґрунтовує доцільність використання терміна «РС». ...
Застуда та інші інфекції дихальних шляхів – актуальна проблема охорони здоров’я через високий рівень захворюваності, що перевищує такий інших інфекційних патологій. З метою підвищення кваліфікації лікарів загальної практики та обміну досвідом з актуальних питань лікування інфекційних захворювань у лютому була проведена науково-практична конференція «Академія сімейного лікаря. Для кого небезпечні сезонні інфекції? Загроза сезонних інфекцій. Погляд пульмонолога, інфекціоніста, алерголога, ендокринолога, кардіолога, педіатра» за участю провідних вітчизняних спеціалістів-практиків....
Хворі на хронічний фарингіт (ХФ) і хронічний тонзиліт (ХТ) складають вагому частку пацієнтів у щоденній практиці оториноларингологів та лікарів сімейної медицини в усьому світі. Симптоми ХФ і ХТ досить суттєво впливають на якість життя хворих (дискомфорт, відчуття стороннього тіла в глотці, сухий кашель від подразнення в горлі, неприємний запах із рота), змушують пацієнтів звертатися до спеціалістів у галузі патології верхніх дихальних шляхів, гастроентерологів, психотерапевтів, психологів....
Пацієнти з риносинуситами (РС) складають ≈30% усіх хворих оториноларингологічного профілю, причому їхня кількість продовжує зростати через тенденцію до ослаблення місцевого та системного імунітету популяції світу, збільшення кількості випадків алергічних реакцій та наростання резистентності мікроорганізмів. Основними клінічними ознаками РС є утруднене носове дихання, виділення з носа та головний біль, які значно знижують якість життя пацієнтів. Окрім того, РС може спричиняти орбітальні та внутрішньочерепні ускладнення, погіршувати функцію нижніх відділів дихальної системи та несприятливо впливати на стан серцево-судинної системи....




