Артеріальна гіпертензія у дітей та підлітків (закінчення)
 Закінчення. Початок у № 4 (47), стор. 53-58.
Закінчення. Початок у № 4 (47), стор. 53-58.
Медикаментозне лікування
Метою антигіпертензивної терапії, крім зниження АТ до цільового рівня, є запобігання і профілактика прогресування та регресія ураження органів-мішеней. Цільовий рівень АТ становить <90-го перцентилю. Проте при хронічних захворюваннях нирок цільовий рівень АТ нижчий: <75-го перцентилю у пацієнтів без протеїнурії та <50-го перцентилю у пацієнтів із протеїнурією.
Слід враховувати те, що терапевтичний ефект у випадку уражень органів-мішеней досягається у різні строки. Так, відповідних змін з боку гіпертрофованого ЛШ слід очікувати не раніше ніж через 6 міс, показники ШКФ при гіпертензивній нефропатії можуть покращитися через кілька років лікування, зменшення протеїнурії відбувається впродовж кількох тижнів або місяців, регрес потовщення комплексу інтима-медіа загальних сонних артерій спостерігається як мінімум через рік терапії. Наприклад, у дослідженні М. Litwin та співавт. (2010) показано, що частка пацієнтів із гіпертрофією ЛШ у результаті лікування тривалістю 12 міс зменшилася з 46,5% до 31,4%.
Загальним положенням при ініціюванні антигіпертензивної фармакотерапії є початкове призначення мінімальної дози одного препарату із поступовим її титруванням до досягнення необхідного терапевтичного ефекту або виникнення непереносимості. Перевагу віддають лікарським засобам із тривалою дією, які при одноразовому прийомі можуть забезпечити контроль АТ протягом 24 год. У разі непереносимості лікарського засобу його замінюють на препарат іншої групи.
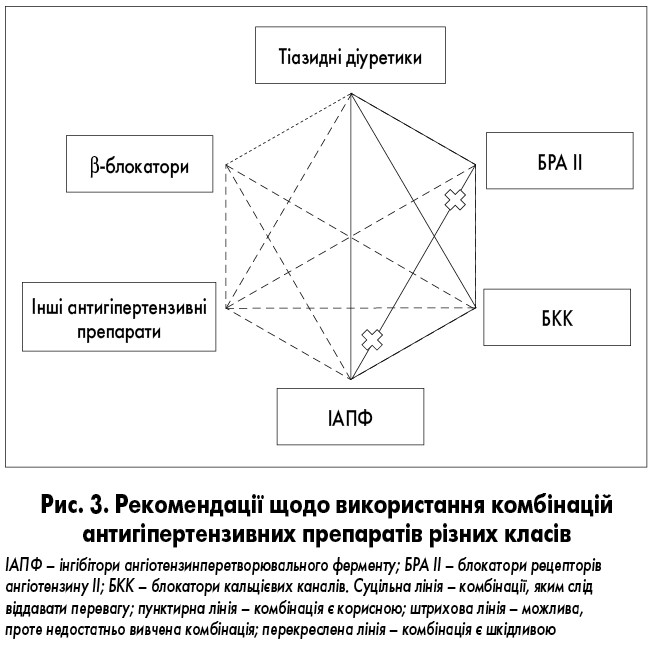 Якщо монотерапія є неефективною, призначають комбінацію лікарських засобів різних груп, їх дози також підбирають методом титрування з визначенням мінімально ефективних. Рекомендації щодо використання комбінацій препаратів різних груп схематично представлені на рисунку 3.
Якщо монотерапія є неефективною, призначають комбінацію лікарських засобів різних груп, їх дози також підбирають методом титрування з визначенням мінімально ефективних. Рекомендації щодо використання комбінацій препаратів різних груп схематично представлені на рисунку 3.
Оцінка ефективності антигіпертензивного лікування проводиться через 8-12 тижнів від його початку. Оптимальна тривалість медикаментозної терапії визначається індивідуально залежно від динаміки захворювання, проте мінімально необхідним вважається курс 3 міс, бажано – 6-12 міс. За умови правильно підібраної терапії тільки після 3 міс безперервного медикаментозного та немедикаментозного лікування при стабільно нормальному АТ розглядають можливість поступового зниження дози антигіпертензивних препаратів аж до повної їх відміни та питання щодо подальшого продовження немедикаментозної терапії.
За останні 15 років проведено випробування близько 20 нових антигіпертензивних препаратів у дітей, проте всі вони показують подібні результати ефективності застосування щодо нормалізації АТ та відрізняються іншими системними, у тому числі побічними, ефектами.
На сьогодні найкращий препарат першої лінії терапії для дітей поки що не визначений, а клінічна практика характеризується значною варіативністю.
У таблиці 14 наведено рекомендовані дози антигіпертензивних лікарських засобів (для перорального прийому та внутрішньовенного введення), які застосовуються для лікування педіатричних пацієнтів з АГ та ГК.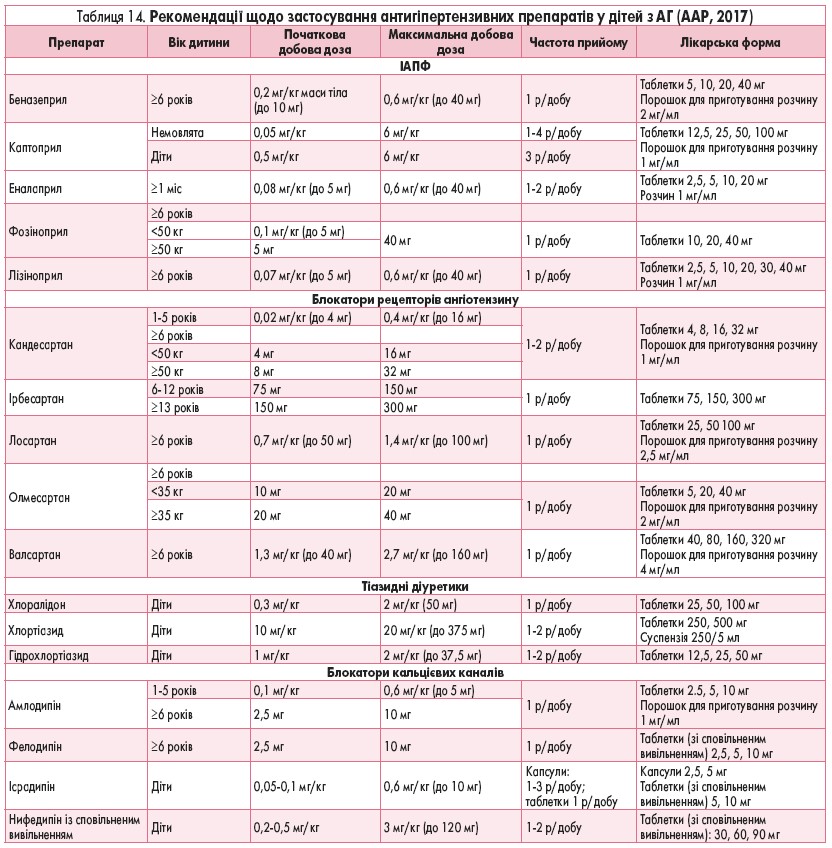
Інгібітори АПФ
Останнім часом дедалі більшу увагу лікарів-клініцистів і науковців привертає група інгібіторів АПФ (ІАПФ) завдяки їх здатності не тільки ефективно знижувати АТ, а й сприяти регресу ураження органів-мішеней. Так, доведено, що препарати цієї групи забезпечують регресію гіпертрофії ЛШ і зменшення проявів ендотеліальної дисфункції. Позитивним ефектом застосування ІАПФ також є збільшення ниркового кровотоку і покращення функції нирок.
Окрім гіпотензивного ефекту, ІАПФ чинять протисклеротичну, протизапальну, антипроліферативну, трофічну та мембраностабілізуючу дію, знижують оксидативний стрес і підвищують інсулінорезистентність, активують адаптаційні процеси. Як наслідок, у пацієнтів молодого та середнього віку з ПАГ покращуються когнітивні функції.
Встановлено, що ІАПФ позитивно впливають на ремоделювання міокарда, сприяють нормалізації об’ємних показників серця і покращують діастолічну функцію ЛШ за рахунок ефекту релаксації.
Антигіпертензивна дія ІАПФ насамперед пов’язана з гальмуванням перетворення ангіотензину І на ангіотензин ІІ. Крім зменшення концентрації ангіотензину ІІ, препарати цієї групи знижують рівень альдостерону, підвищують рівень реніну та ендотеліального релаксуючого фактора (оксиду азоту), перешкоджають розпаду брадикініну.
Виявлено, що ІАПФ пригнічують пресорну (симпатоадреналову) та активують депресорну (калікреїн-кінінову і простагландинову) системи організму. У результаті їх застосування поступово знижується АТ практично без зміни частоти серцевих скорочень, зменшуються загальний периферичний опір судин і післянавантаження на серце, знижується тиск у правому передсерді та малому колі кровообігу.
ІАПФ не впливають на метаболізм глюкози та ліпопротеїдів, що робить цю групу лікарських засобів препаратами вибору для лікування дітей із метаболічним синдромом. Навпаки, ІАПФ, які блокують РАС в ендотелії та гладеньких м’язових волокнах судинної стінки, сприяють зменшенню впливу інсуліну та інсуліноподібного фактора росту I на ріст і гіпертрофію судинних елементів.
Доведено, що у корі надниркових залоз, особливо в пучковій та гломерулярній зоні, концентрація ангіотензину II є однією з найвищих порівняно з іншими органами. У наднирниках ангіотензин ІІ бере участь у синтезі кортикостероїдів та альдостерону. Тому ІАПФ можна застосовувати з метою зниження рівня глюко- і мінералокортикоїдів у дітей з АГ.
У дорослих пацієнтів із прийомом ІАПФ пов’язані такі побічні ефекти: гіперкаліємія, хронічний кашель та ангіодистрофія. Що стосується досліджень за участю педіатричних пацієнтів, то повідомлялося про кашель, що вказує на нижчу частоту побічних ефектів у дітей порівняно з дорослими.
Одне з найбільш масштабних клінічних досліджень з оцінки ефективності застосування еналаприлу у лікуванні АГ у дітей (подвійне плацебо-контрольоване) провели у 2002 р. T.A. Wells та співавт. [28]. На підставі отриманих результатів автори зробили висновок про те, що порівняно з плацебо лікування еналаприлом у дозах – від 2,5 до 20 мг у дітей із масою тіла <50 кг і 5-40 мг для дітей із масою тіла >50 кг – забезпечує ефективне зниження САТ і ДАТ. Дози від 0,625 до 1,25 мг не впливають на АТ у дітей. Не виявлено істотних відмінностей гіпотензивного ефекту еналаприлу у дітей різного віку, статі та стадії статевого дозрівання. У дослідженні показано хорошу переносимість препарату протягом 4 тижнів лікування. Протягом цього періоду найчастішими побічними явищами були запаморочення (3,6%) і головний біль (1,8%). Тільки в одному випадку (<1%) прийом препарату припинено через побічну дію.
Згідно з класифікацією виділяють три класи ІАПФ, які відрізняються переважно шляхом екскреції з організму (табл. 15).
Ліпофільні властивості ІАПФ зумовлюють їх схильність до кумуляції в жировій тканині, тому вони мають низьку ефективність у дітей із надмірною масою тіла.
ІАПФ ІІІ класу лізиноприл завдяки гідрофільним властивостям не метаболізується в організмі, а виділяється нирками у незміненому вигляді, тому він безпечний для застосування у пацієнтів з АГ та ураженням печінки. Крім того, цей препарат має такі переваги: низька здатність до зв’язування з білками плазми крові, не змінює фармакокінетику інших препаратів і може застосовуватись у комбінації з серцевими глікозидами, антикоагулянтами, антиаритмічними та іншими препаратами. Різні представники групи ІАПФ мають різну тканинну чутливість, що схематично представлено на рисунку 4.
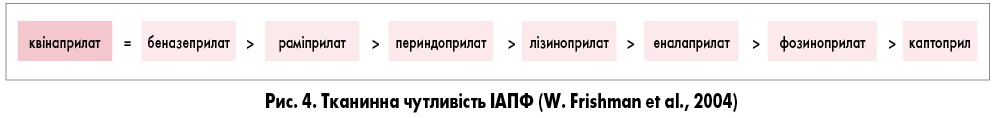 Експерти Європейського товариства кардіологів (ESC) у консенсусі з лікування АГ про застосування ІАПФ зазначили: «По суті, всі доступні ІАПФ можна розглядати як однаково ефективні для зниження АТ».
Експерти Європейського товариства кардіологів (ESC) у консенсусі з лікування АГ про застосування ІАПФ зазначили: «По суті, всі доступні ІАПФ можна розглядати як однаково ефективні для зниження АТ».
Найбільш поширеним побічним ефектом ІАПФ є сухий нав’язливий кашель, що може потребувати заміни препарату, наприклад, на блокатор рецепторів ангіотензину ІІ.
Наш власний досвід застосування ІАПФ еналаприлу свідчить, що при індивідуальному підборі дози цього препарату слід враховувати середньодобовий рівень АТ за даними ДМАТ. Орієнтовно вважають, що 1 мг еналаприлу знижує рівень середньодобового САТ на 1 мм рт. ст. Відповідно, для досягнення цільового рівня САТ, наприклад, 130 мм рт. ст. у дитини з початковими показниками середньодобового САТ 140 мм рт. ст. достатньо застосування добової дози препарату 10 мг. Водночас у дитини з середньодобовим рівнем САТ >150 мм рт. ст. ця доза буде неефективною. Така дитина потребує для контролю гіпертензії добової дози >20 мг. При недостатньому ступені нічного зниження АТ добову дозу еналаприлу доцільно розділити на 2 прийоми.
Блокатори рецепторів ангіотензину ІІ
Блокатори рецепторів ангіотензину ІІ (БРА) показані для застосування у дітей із непереносимістю ІАПФ. Ці препарати використовують переважно у підлітків, враховуючи вікові обмеження, що містять інструкції для медичного застосування лікарських засобів, зареєстрованих в Україні.
БРА, так само як попередня група препаратів, блокують каскад РААС, проте шляхом дії на рецептори ангіотензину ІІ. Загалом показання для застосування та ефекти БРА подібні до таких ІАПФ, проте препарати цієї групи мають більш виражений церебральний ангіопротекторний ефект та дуже низьку частоту побічних явищ у вигляді кашлю.
У разі недостатньої ефективності монотерапії ІАПФ або БРА у схему терапію, як правило, включають сечогінні препарати, переважно тіазидні діуретики.
Тіазидні діуретики
Препарати цієї групи протягом перших 1-2 тижнів лікування зменшують об’єм циркулюючої крові за рахунок зниження реабсорбції натрію та води нирками. Це приводить до зменшення серцевого викиду та розвитку рефлекторної вазодилатації і, як наслідок, до зниження АТ. Через кілька тижнів лікування діуретиками показники об’єму циркулюючої крові та серцевого викиду нормалізуються, тоді як периферична вазодилатація залишається основним механізмом антигіпертензивної дії діуретиків у разі тривалої терапії. Препарати цієї групи показані для застосування у пацієнтів з АГ, спричиненою затримкою натрію та води. Діуретики (крім калійзберігаючих – спіронолактону і триамтерену) є ідеальною опцією для комбінації з ІАПФ/БРА у пацієнтів з АГ, патогенетичним механізмом якої є дисфункція РААС та об’ємно-сольове перевантаження. Слід зазначити, що одночасне застосування калійзберігаючих діуретиків та ІАПФ/БРА знижує ризик розвитку гіпокаліємії через гіперкаліємічний ефект останніх. І, навпаки, комбінація ІАПФ/БРА з антагоністами альдостерону не рекомендована через взаємопотенціювання гіперкаліємічного ефекту.
Блокатори кальцієвих каналів
 Якщо у дитини з АГ комбінація ІАПФ/БРА з діуретиком є малоефективною, то схему лікування доповнюють третім антигіпертензивним препаратом. При цьому перевагу віддають блокаторам кальцієвих каналів (БКК).
Якщо у дитини з АГ комбінація ІАПФ/БРА з діуретиком є малоефективною, то схему лікування доповнюють третім антигіпертензивним препаратом. При цьому перевагу віддають блокаторам кальцієвих каналів (БКК).
Механізм дії БКК полягає у блокаді повільних кальцієвих каналів у кардіоміоцитах та гладеньком’язових волокнах медії периферичних судин. Зменшення току кальцію приводить до зниження скоротливості міокарда та периферичної вазодилатації. Згідно з результатами досліджень за участю дорослих пацієнтів з АГ БКК знижують ризик розвитку інфаркту міокарда та інсульту, проте підвищують ризик виникнення застійної серцевої недостатності.
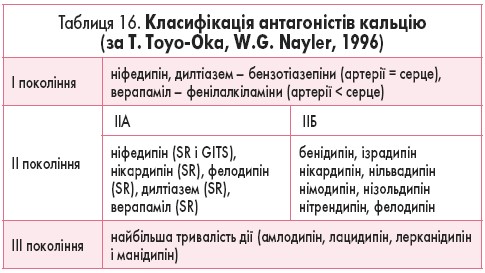
Розрізняють три покоління БКК (табл. 16), які відрізняються переважно тривалістю дії.
Бета-блокатори
У деяких випадках замість БКК можна використовувати β-блокатори. Проте слід враховувати, що більшість кардіоселективних β-блокаторів, зареєстрованих в Україні, мають вікові обмеження щодо їх застосування.
Антигіпертензивний ефект β-адреноблокаторів зумовлений блокуванням впливу симпатичного відділу ВНС та циркулюючих катехоламінів на серце (кардіоселективні – метопролол, бісопролол, атенолол) або одночасно на серце та судини (кардіонеселективні – пропранолол). Призначення β-блокаторів є обґрунтованим у випадках АГ на фоні гіперсимпатикотонії (супроводжується синусовою тахікардією, переважанням підвищення САТ над підвищенням ДАТ, високим пульсовим тиском, гіперкінетичним типом кровообігу, відповідними ознаками за даними аналізу варіабельності серцевого ритму), тривожно-фобічних розладів (психогенна гіперсимпатикотонія) та гіпертиреозу (підвищення чутливості серця до дії катехоламінів). Застосування β-блокаторів може зашкодити пацієнту з АГ на фоні ожиріння, метаболічного синдрому та ЦД 2 типу, оскільки, за даними деяких досліджень, вони підвищують інсулінорезистентність тканин та у поодиноких випадках у разі тривалого прийому можуть сприяти розвитку ЦД 2 типу у схильних до цього осіб. Винятком є карведілол та небіволол. Лікування β-блокаторами потребує регулярного моніторингу ЕКГ для своєчасного виявлення побічних ефектів (синусової брадикардії та АВ-блокади), корекції дози препарату чи його відміни.
Окрім β-блокаторів, препаратом четвертої лінії терапії також може бути α-блокатор або ще один діуретик.
Медикаментозна терапія із застосуванням препаратів інших фармакологічних груп
У лікуванні пацієнта з ПАГ слід враховувати поєднання у нього підвищеного АТ із вегетативними розладами, а також із такими станами, як тривожність і астенічний синдром. Своєчасна корекція цих розладів із проведенням терапії седативними, ноотропними, метаболітними препаратами дозволяє зупинити прогресування захворювання на ранній стадії. Препарати цих груп мають особливе значення у дітей з лабільною ПАГ, у яких відсутні показання для застосування антигіпертензивних препаратів. Спектр лікувальних заходів при лабільній ПАГ подібний до такого при синдромі вегетативної дисфункції. Такі препарати, як, наприклад, вінпоцетин і цинаризин, покращують кровотік у церебральних венах, мають помірний спазмолітичний ефект.
Цинаризин покращує мозковий, периферичний та коронарний кровообіг, має високу тропність до судин головного мозку. Препарат інгібує надходження до клітини іонів кальцію і зменшує вміст у депо її плазмолеми, що значною мірою пов’язано з блокуванням мембранних кальцієвих каналів. Цинаризин знижує тонус гладенької мускулатури артеріол, безпосередньо впливає на гладеньку мускулатуру судин, зменшує реакції на біогенні судинозвужувальні речовини (адреналін, норадреналін, брадикінін), посилює стійкість тканин до гіпоксії. Препарат має помірну антигістамінну активність, зменшує збудливість вестибулярного апарату. У пацієнтів із порушенням периферичного кровообігу він покращує кровопостачання та потенціює постішемічну гіперемію. У дітей цинаризин застосовують у початковій дозі 6,25 мг (1/4 таблетки), яку потім підвищують до 25 мг (1 таблетка), тричі на добу курсом 1 міс.
Кавінтон має комплексний механізм терапевтичної дії: покращує мозковий кровообіг та церебральний метаболізм, а також реологічні властивості крові. Препарат чинить нейропротективний ефект за рахунок зменшення цитотоксичних реакцій, спричинених стимулюючими амінокислотами; інгібує функціональну активність як клітинних трансмембранних натрієвих та кальцієвих канальців, так і рецепторів NMDA і AMPA; потенціює нейропротективний ефект аденозину; стимулює церебральний метаболізм (посилює поглинання та засвоєння мозком глюкози та кисню); підвищує стійкість нейронів до гіпоксії (стимулює транспорт глюкози через гематоенцефалічний бар’єр); сприяє зсуву метаболізму глюкози убік більш енергетично вигідного аеробного; вибірково інгібує Са2+-калмодулін-залежну цГМФ-фосфодіестеразу, підвищує концентрацію цАМФ і цГМФ у тканинах мозку, а також концентрацію АТФ та співвідношення АТФ/АМФ; покращує церебральний метаболізм норадреналіну та серотоніну; стимулює висхідну норадренергічну систему; чинить антиоксидантну дію.
Вказаний механізм дії забезпечує також церебропротективний ефект кавінтону. Препарат покращує мікроциркуляцію у тканинах мозку (блокує агрегацію тромбоцитів); зменшує патологічно підвищену в’язкість крові; збільшує здатність еритроцитів до деформації та гальмує поглинання ними аденозину; стимулює внутрішньотканинний транспорт кисню, зменшуючи спорідненість до нього еритроцитів. Кавінтон вибірково підсилює мозковий кровоток: збільшує мозкову фракцію хвилинного об’єму; зменшує опір мозкових судин без зміни параметрів загального кровообігу, практично не впливає на хвилинний об’єм, частоту пульсу, загальний периферичний опір; не спричиняє феномен «обкрадання». Навпаки, у разі застосування цього препарату передусім посилюється кровопостачання ішемізованої, але ще життєздатної ділянки з низьким рівнем перфузії – феномен «зворотного обкрадання».
Вінпоцетин застосовують у формі таблеток 5 мг тричі на добу протягом місяця, переважно у підлітків, враховуючи вікові обмеження щодо його застосування у дітей.
Застосування препаратів пірацетаму покращує енергетичний метаболізм у головному мозку, зменшує цереброастенічні прояви. Пірацетам, який являє собою циклічне похідне ГАМК, є ноотропним лікарським засобом, який позитивно діє на функцію головного мозку, покращуючи когнітивні функції (здатність до навчання, пам’ять, увагу), а також розумову працездатність. Припускають, що існує кілька механізмів позитивної дії пірацетаму на ЦНС: зміна швидкості поширення збудження у головному мозку; посилення метаболізму у нервових клітинах; покращення мікроциркуляції за рахунок зміни реологічних характеристик крові. При цьому препарат не чинить судинорозширювальну дію. Пірацетам покращує зв’язки між півкулями головного мозку і синаптичну провідність у неокортикальних структурах; пригнічує агрегацію тромбоцитів і відновлює еластичність мембрани еритроцитів, зменшує адгезію еритроцитів; чинить протективну і відновлювальну дію при порушенні функції головного мозку внаслідок гіпоксії або інтоксикації. Препарат позитивно впливає на метаболічні процеси у ЦНС, стимулює обмін макроергічних з’єднань, регулює споживання глюкози та кисню тканинами мозку, покращує кровопостачання головного мозку, процес міжнейрональної передачі імпульсів, стимулює регенерацію пошкоджених нейронів. Пірацетам активує асоціативні процеси, інтегративну діяльність мозку, процеси мислення та пам’яті, покращує здатність до концентрації уваги та навчання. Препарат не чинить седативної дії та не спричиняє ейфорії. У дітей з АГ пірацетам застосовують у дозі 400 мг (1 таблетка) 2-3 р/добу курсом тривалістю 1 міс.
Фенібут – фенільне похідне γ-аміномасляної кислоти та фенілетиламіну. Препарат чинить насамперед антигіпоксичну та антиамнестичну дію. Він усуває напруження, тривожність, страх, поліпшує сон; подовжує та підсилює дію снодійних, наркотичних, нейролептичних та протисудомних лікарських засобів. Фенібут – ноотропний препарат, який полегшує ГАМК-опосередковану передачу нервових імпульсів у ЦНС (шляхом прямої дії на ГАМК-ергічні рецептори), має також транквілізуючий, психостимулювальний, антиагрегантний та антиоксидантний ефекти. Препарат покращує функціональний стан мозку за рахунок нормалізації метаболізму у його тканинах та впливу на мозковий кровообіг (збільшує об’ємну та лінійну швидкість мозкового кровотоку, зменшує опір мозкових судин, поліпшує мікроциркуляцію); позитивно впливає на холіно- та адренорецептори; зменшує прояви астенії та вазовегетативні симптоми (головний біль, відчуття важкості в голові, порушення сну, дратівливість, емоційну лабільність тощо), підвищує розумову працездатність, покращує психологічні показники (увагу, пам’ять, швидкість і точність сенсорно-моторних реакцій). У пацієнтів з астенією з перших днів терапії фенібутом покращується суб’єктивне самопочуття, підвищуються зацікавленість та ініціативність (мотивація діяльності) без небажаної седації та збудження. Після тяжких черепно-мозкових травм препарат стимулює біоенергетичні процеси у головному мозку. Він також покращує мікроциркуляцію у тканинах ока. У дітей з АГ фенібут застосовують у дозі 250 мг (1 таблетка) тричі на добу протягом 1 міс.
На підставі результатів досліджень з оцінки ефективності лікування дітей із ПАГ, проведених на кафедрі педіатрії післядипломної освіти НМУ імені О.О. Богомольця у 2004-2016 рр., розроблено алгоритм, згідно з яким додавання до гіпотензивних препаратів медикаментозних засобів інших груп у схемах терапії АГ потенціює дію антигіпертензивних препаратів та зменшує строки нормалізації АТ, а також сприяє більш швидкому регресу ураження органів-мішеней [29]. До таких препаратів належать комбіновані препарати магнію і вітаміну В6, а також ГАМК-ергічні препарати та кардіометаболітні засоби [30, 31].
На рисунку 5 схематично представлена ступінчаста терапія ПАГ. На початкових стадіях захворювання, коли показники АТ не досягають високих значень, проте формується фаза первинної дезадаптації, для якої характерна виражена симптоматика та недостатня активність стрес-лімітуючих систем, ефективним є короткий курс ноотропної та седативної терапії із застосуванням фенібуту і комбінованого препарату магнію та вітаміну В6 у поєднанні з немедикаментозними методами лікування, зокрема фізіотерапевтичними методами седативної спрямованості, необхідними для нормалізації режиму праці та відпочинку дитини. У таких випадках обов’язковими є контроль рівня магнію у сироватці крові та своєчасна корекція його дефіциту, що значно зменшує астенічні прояви та активізує стрес-лімітуючі системи організму.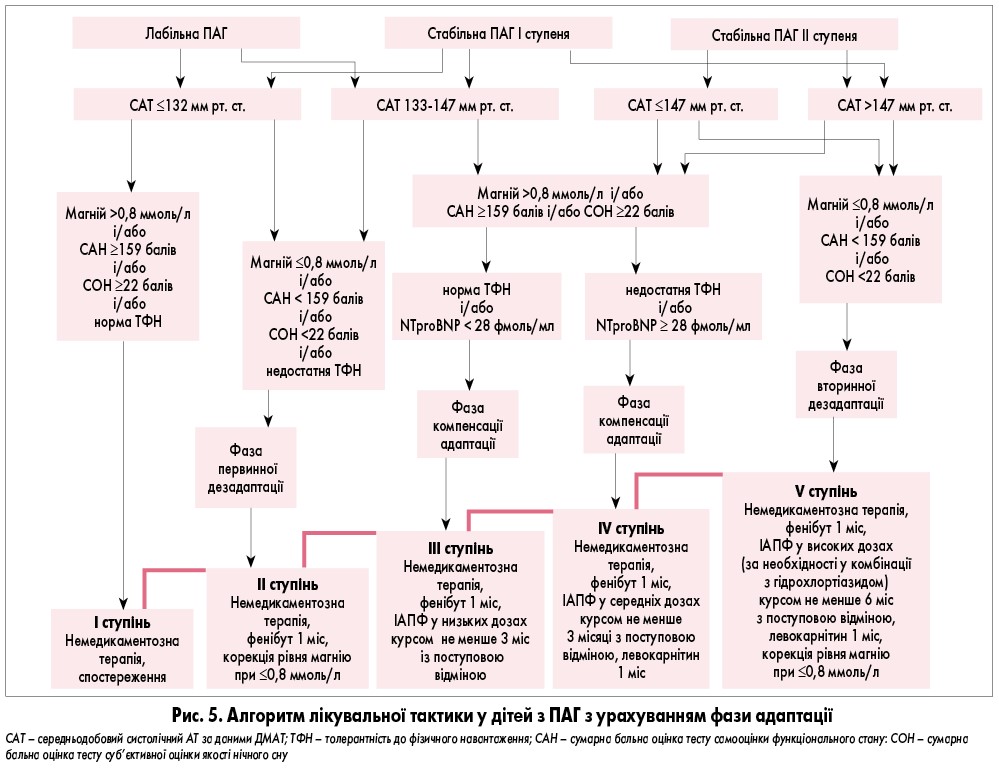
Застосування цієї схеми лікування у дітей із лабільною ПАГ дозволяє запобігти прогресуванню захворювання та його переходу у стабільну форму.
Якщо ПАГ у дитини з часом прогресує, відбувається стабілізація гіпертензії – захворювання переходить у фазу компенсації адаптації, організм пристосовується до функціонування за умов високого АТ. У таких пацієнтів, незважаючи на малосимптомний перебіг, прогресує ураження органів-мішеней, що потребує обов’язкового застосування антигіпертензивних препаратів та проведення кардіометаболітної терапії.
На тлі вторинної дезадаптації, коли відбувається виснаження стрес-лімітуючих систем організму, скарги хворих поновлюються, спостерігається дисбаланс регуляції АТ на всіх рівнях, прогресує ураження органів-мішеней. Такі зміни важко піддаються зворотному розвитку, потребують тривалої антигіпертензивної терапії та застосування високих доз антигіпертензивних препаратів. У дітей з ПАГ у фазі вторинної дезадаптації у схеми комплексної терапії необхідно включати поряд з немедикаментозними заходами повторні курси нейро- і кардіотропної терапії, а також своєчасно коригувати дефіцит магнію.
Література
- Whelton P.K., Carey R.M., Aronow W.S., Casey D.E. Jr, Collins K.J., Dennison Himmelfarb C., DePalma S.M., Gidding S., Jamerson K.A., Jones D.W., MacLaughlin E.J., Muntner P., Ovbiagele B., Smith S.C. Jr, Spencer C.C., Stafford R.S., Taler S.J., Thomas R.J., Williams K.A. Sr, Williamson J.D., Wright J.T. Jr. 2017 ACC/AHA/AAPA/ABC/ACPM/AGS/APhA/ASH/ASPC/NMA/PCNA Guideline for the Prevention, Detection, Evaluation, and Management of High Blood Pressure in Adults: Executive Summary: A Report оf the American College of Cardiology / American Heart Association Task Force on Clinical Practice Guidelines. J Am Soc Hypertens. 2018 Aug; 12(8): 579.
- Марушко Ю.В. Аналіз та перспективи нових клінічних рекомендацій ААР (2017) щодо скринінгу та контролю високого артеріального тиску у дітей та підлітків / Ю.В. Марушко, Т.В. Гищак // Современная педиатрия. – 2018. – № 4(92). – С. 27-39.
- Flynn J.T. Clinical Practice Guideline for Screening and Management of High Blood Pressure in Children and Adolescents / J.T. Flynn, D.C. Kaelber, C.M. Baker-Smi et al. Pediatrics. 2017; 140(3).
- Lurbе E. 2016 European Society of Hypertension guidelines for the management of high blood pressure in children and adolescents / Lurbe E., Agabiti-Rosei E., Cruickshank J.K. et al. J Hypertens. 2016. Oct; 34(10): 1887-1920.
- Brady T.M., Stefani-Glucksberg A., Simonetti G.D. Manаgement of high blood pressure in children: similarities and differences between US and European guidelines. Pediatr Nephrol. 2018 Mar 28.
- Antza C., Doundoulakis I., Stabouli S., Kotsis V. Cоmparison Among Recommendations for the Management of Arterial Hypertension Issued by Last US, Canadian, British and European Guidelines.High Blood Press Cardiovasc Prev. 2018 Mar; 25(1): 9-16.
- Badi M.A. Overweight/obesity and hypertension in schoolchildren aged 6-16 years, Aden Governorate, Yemen, 2009 / M.A. Badi, B.E. Garcia-Triana, R. Suarez-Martinez. East Mediterr Health J. 2012; 18(7): 718-722.
- Chirita-Emandi A. Arterial hypertension in school-aged children in western Romania / A. Chirita-Emandi, M. Puiu, M. Gafencu, C. Pienar. Cardiol Young. 2013; 23(2): 189-196.
- Litwin M. Pediatric hypertension – definition, normative values, epidemiology, screening and treatment / M. Litwin, K. Zbigniew. Postepy Nauk Medycznych. – 2015. – Т. XXVIII. – № 11. – p. 134-145.
- Menghetti E. Hypertension and obesity in Italian school children: The role of diet, lifestyle and family history / E. Menghetti, P. Strisciuglio, A. Spagnolo et al. Nutr Metab Cardiovasc Dis. 2015; 25 (6): 602-607.
- Майданник В.Г. Особливості артеріального тиску у дітей із надлишковою масою тіла (за даними добового моніторування) / В.Г. Майданник, М.В. Хайтович, Л.І. Місюра, О.М. Кужель // Международный журнал педиатрии, акушерства и гинекологии. – 2014. – Т. 5. – № 3. – С. 18-23.
- Коренєв М.М. Артеріальна гіпертензія та ожиріння в підлітків / М.М. Коренєв, Л.Ф. Богмат, О.М. Носова // Український журнал дитячої ендокринології. – 2014. – № 2. – С. 79-80.
- Погодина А.В. Мочевая кислота и факторы кардиометаболического риска при артериальной гипертензии у подростков / А.В. Погодина, В.В. Долгих, Л.В. Рычкова // Кардиология. – 2014. – № 7. – С. 36-42.
- Feig D.I. The role of uric acid in the pathogenesis of hypertension in the young / D.I. Feig. J Clin Hypertens (Greenwich). 2012; 14: 346-352.
- Ровда Ю.И. Метаболические нарушения как факторы риска прогрессирования артериальной гипертензии у детей и подростков / Ю.И. Ровда, Н.Н. Миняйлова, Е.Г. Бунина [и др.] // Педиатрия. – 2010. – № 3. – С. 6-9.
- Долгих В.В. Особенности коагуляционного гемостаза и фибринолиза при эссенциальной артериальной гипертензии у детей / В.В. Долгих, М.В. Гомелля, Е.С. Филиппов, Л.В. Рычкова // Кардиология. – 2016. – № 11. – С. 69-72.
- Peotta V. Neonatal growth restriction-related leptin deficiency enhances leptin-triggered sympathetic activation and central angiotensin II receptor-dependent stress-evoked hypertension / V. Peotta, K. Rahmouni, J.L. Segar [et al.]. Pediatr Res. 2016; 80(2): 244-251.
- Bertagnolli M. Activation of the Cardiac Renin-Angiotensin System in High Oxygen-Exposed Newborn Rats: Angiotensin Receptor Blockade Prevents the Developmental Programming of Cardiac Dysfunction / M. Bertagnolli, A. Dios, S. Beland-Bonenfant [et al.]. Hypertension. 2016; 67 (4): 74-82.
- Favero G. Melatonin and its atheroprotective effects: a review / G. Favero, L.F. Rodella, R.J. Reiter, R. Rezzani. Mol Cell Endocrinol. – 2014. – V. 15. – № 382 (2). – p. 926-937.
- Хомазюк Т.А. Когнітивні порушення у хворих на артеріальну гіпертензію в реальній лікарській практиці / Т.А. Хомазюк [та ін.] // Медичні перспективи. – 2015. – Т. 20. – № 2. – С. 42-47.
- Шлімкевич І.В. Особливості психоемоційного статусу та когнітивні функції в дітей із первинною артеріальною гіпертензією / І.В. Шлімкевич // Клінічна та експериментальна патологія. – 2015. – Т. 14. – № 1. – С. 197-199.
- Bijlsma M.W. Why pediatricians fail to diagnose hypertension: a multicenter survey / M.W. Bijlsma, H.N. Blufpand, G.J. Kaspers, A. Bokenkamp. J Pediatr. 2014; 164: 173-177.
- Ewald D.R. Risk Factors in Adolescent Hypertension / D.R. Ewald, L.A. Haldeman. Glob Pediatr Health. 2016; 16: 3-12.
- Postel-Vinay N., Bobrie G., Savard S., Persu A., Amar L., Azizi M., Parati G.Hоme bloоd pressure measurement and digital health: communication technologies create a new context. J Hypertens. 2018 Nov; 36(11): 2125-2131.
- Khoury P.R., Mitsnefes M., Daniels St.R., Kimball T.R. Age-Specific Reference Intervals for Indexed Left Ventricular Mass in Children // Journal of the American Society of Echocardiography. – 2009. – Vol. 22. – p. 709-714.
- Lang R.M. Recommendations for chamber quantification: a report from the American Society of Echocardiography’s Guidelines and Standards Committee and the Chamber Quantification Writing Group, developed in conjunction with the European Association of Echocardiography, a branch of the European Society of Cardiology / R.M. Lang, M. Bierig, R.B. Devereux [et al.]/ J Am Soc Echocardi. 2005; 18 (12): 1440-1463.
- Wong T.Y., Mitchell P.N. Hypertensive retinopathy // The New England Journal of Medicine. – 2004. – Vol. 351. – № 22. – p. 2310-2317.
- Wells T. A double-blind, placebo-controlled, dose-response study of the effectiveness and safety of enalapril for children with hypertension / T. Wells, V. Frame, B. Soffer [et al.]. J Clin Pharmacol. 2002; 42: 870-880.
- Марушко Ю.В. Фази адаптації у дітей з первинною артеріальною гіпертензією / Ю.В. Марушко, Т.В. Гищак // Современная педиатрия. – 2016. – № 7(79). – С. 88-93.
- Марушко Ю.В. Ефективність застосування препарату ноофен у дітей із стабільною первинною артеріально гіпертензією / Ю.В. Марушко, Т.В. Гищак // Современная педиатрия. – 2016. – № 8(80). – С. 94-102.
- Марушко Ю.В., Гищак Т.В., Злобинец А.С., Марушко Е.Ю. Опыт применения левокарнитина в клинической педиатрии // Педиатрия. Восточная Европа. – 2018. – Т. 6. – № 1. – С. 155-164.
- Марушко Ю.В. Обґрунтування застосування препаратів магнію в педіатричній практиці / Ю.В. Марушко, Т.В. Гищак // Современная педиатрия. – 2016. – № 6. – С. 27-32.
Тематичний номер «Педіатрія» №1 (48), березень 2019 р.
СТАТТІ ЗА ТЕМОЮ Педіатрія
Вроджена дисфункція кори надниркових залоз (ВДКНЗ) – це захворювання з автосомно-рецесивним типом успадкування, в основі якого лежить дефект чи дефіцит ферментів або транспортних білків, що беруть участь у біосинтезі кортизолу. Рання діагностика і початок лікування пацієнтів з ВДКНЗ сприяє покращенню показників виживаності та якості життя пацієнтів....
Алергічний риніт (АР) є поширеним запальним захворюванням верхніх дихальних шляхів (ВДШ), особливо серед педіатричних пацієнтів. Ця патологія може знижувати якість життя, погіршувати сон та щоденну продуктивність. Метою наведеного огляду є надання оновленої інформації щодо епідеміології АР та його діагностики, з урахуванням зв’язку з бронхіальною астмою (БА). ...
Американська академія педіатрії (AAP) оновила рекомендації щодо контролю грипу серед дитячого населення під час сезону 2023-2024 рр. Згідно з оновленим керівництвом, для профілактики та лікування грипу в дітей необхідно проводити планову вакцинацію з 6-місячного віку, а також своєчасно застосовувати противірусні препарати за наявності показань. ...
Поширеність і вплив алергічних захворювань часто недооцінюють [1]. Ключовим фактором алергічної відповіді є імуноглобулін (Ig) Е, присутній на поверхні тучних клітин і базофілів. Взаємодія алергену з IgЕ та його рецепторним комплексом призводить до активації цих клітин і вивільнення речовин, у тому числі гістаміну, які викликають симптоми алергії [2]. Враховуючи ключову роль гістаміну в розвитку алергічних реакцій, при багатьох алергічних станах, включаючи алергічний риніт і кропив’янку, пацієнту призначають антигістамінні препарати [3, 4]....




