Роль бенфотіаміну в комплексному лікуванні цукрового діабету
Кожен ендокринолог знає, що першочерговим завданням у лікуванні цукрового діабету (ЦД) є досягнення адекватного глікемічного контролю. Але не менш важливим питанням є запобігання цьому захворюванню та лікування його ускладнень, у тому числі полінейропатії. Традиційно в терапії нейропатій різного ґенезу застосовують вітаміни групи B. На особливу увагу клініцистів заслуговує бенфотіамін – жиророзчинна форма вітаміну B1, яку вважають набагато ефективнішою, ніж водорозчинна, що доведено в ході багатьох клінічних досліджень.
В Одесі пройшла науково-практична конференція для лікарів-ендокринологів, у рамках програми роботи якої було заслухано доповідь професора, завідувача відділенням внутрішньої медицини Клініки Шон (м. Нюрнберг Фюрт, Німеччина) Аліна Штірбана. На прикладі двох клінічних випадків доктор Штірбан розповів про використання α-ліпоєвої кислоти (АЛК) та бенфотіаміну в терапії сенсомоторної діабетичної нейропатії (ДН).
У першому випадку пацієнт звернувся до відділення швидкої допомоги з виразками на нозі. Під час збору анамнезу було встановлено, що пацієнт грів ногу пляшкою з гарячою водою, при цьому ніякого дискомфорту він не відчував. Уже наступного дня він побачив рани на стопі, які насправді були опіками. У ході обстеження виявлено відсутність больової чутливості нижніх кінцівок.
У другому випадку пацієнт звернувся до лікувального закладу, де працює доктор А. Штірбан. Пацієнт скаржився на поколювання в стопах і біль при дотику до них. Ці симптоми частіше виникали ввечері та вночі, що призводило до порушення сну, втоми та розвитку депресії. Під час клінічного обстеження чутливість стоп виявилася нормальною, але виникав спонтанний біль.
Симптоми в обох пацієнтів є типовими проявами сенсорно-моторної ДН. Зазвичай пацієнти з цим ускладненням ЦД скаржаться на постійний пекучий тупий чи пароксизмальний стріляючий біль, дизестезії (болючі парестезії), гіпералгезію, аллодинію чи оніміння кінцівок. При клінічному огляді виявляється зменшення больової, температурної та вібраційної чутливості, зниження рефлексів.
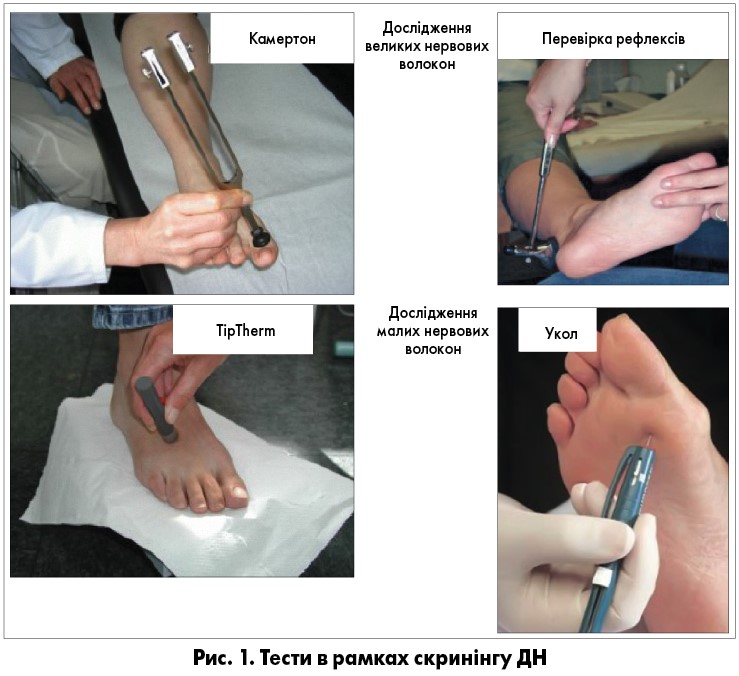
Для діагностики нейропатії скринінг у пацієнтів із ЦД 1 типу проводять щонайбільше через 5 років після встановлення діагнозу, а потім – не рідше 1 разу на півроку. При ЦД 2 типу обстеження проводять після встановлення діагнозу, а потім – не менше як 1 раз на рік. Скринінг ДН триває менше 5 хвилин, він складається з простих тестів (рис. 1) і може проводитися як лікарем (у тому числі – загальної практики), так і медичною сестрою.
У Німеччині нещодавно проводилося дослідження, яке включало 1100 осіб, 154 (14%) з яких мали ДН. При цьому виявилося, що 91% учасників із предіабетом та 77% хворих на діабет не знали про наявність у них нейропатії. Серед пацієнтів із ДН 32% ніколи раніше не обстежували нижні кінцівки.
Дуже важливим завданням лікаря є запобігання розвитку ДН. Для цього слід дотримуватися таких рекомендацій: уникати гіпо- і гіпертермії нижніх кінцівок, регулярно оглядати стопи і носити спеціальне взуття, призначене для хворих на діабет (таке, що не стискає та не обмежує кровообіг).
Лікування ДН
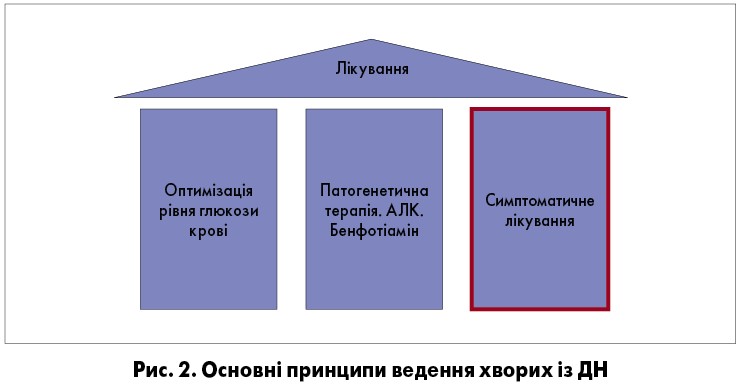
Основні принципи лікування ДН відображено на рисунку 2. Це – адекватний глікемічний контроль, патогенетична терапія, що покращує чутливість нервів та кровообіг, симптоматичне лікування.
Для патогенетичного лікування ДН в Європі використовують наступні препарати з доведеною ефективністю:
- АЛК;
- бенфотіамін;
- інгібітор альдозоредуктази.
Ще у 80-х роках АЛК було визнано сильним антиоксидантом. Вона утворюється в організмі як тварин, так і людини. АЛК – це єдиний жиро- й водорозчинний антиоксидант. Джерелом АЛК є картопля, капуста броколі, м’ясо, печінка. Дуже важливо, що ефективність цього засобу в лікуванні ДН є доведеною. Так, багатоцентрове рандомізоване подвійне сліпе плацебо-контрольоване дослідження SYDNEY2 (Ziegler D., Ametov A., Barinov A. et al.) включало 181 пацієнта з ЦД 2 типу, які приймали АЛК перорально в дозі 600, 1200 та 1800 мг на добу. Після 5 тиж лікування показники по шкалі загальних симптомів (ШЗС) достовірно покращилися в усіх досліджуваних групах (рис. 3).
Показники шкали невропатичного дефіциту NIS (Neuropathy Impairment Score) суттєво покращилися в групі, учасники якої приймали препарат у дозі 1200 мг/добу.
Дослідження NATHAN1 (Ziegler D., Low P.A., Litchy W.J., 2011) показало, що прийом АЛК у дозі 600 мг/добу сприяв достовірному покращенню невропатичного дефіциту (NIS), але це не супроводжувалося покращенням швидкості проведення по нервових волокнах.
У наступному дослідженні (Ruessmann H.J., 2009) 443 пацієнти з ЦД і хронічною нейропатією та больовим синдромом лікувалися АЛК у дозі 600 мг/добу перорально у середньому протягом 5 років. Після закінчення курсу терапії 293 особи було переведено на габапентин (600-2400 мг/добу), а 150 залишилися без лікування через відсутність гострих симптомів. Виявилося, що перехід від тривалого лікування АЛК до таких центральних аналгетичних препаратів, як габапентин, супроводжувався вищим рівнем побічних ефектів, частішим рівнем амбулаторних викликів і щоденними витратами на лікування. Тому варіант патогенетичного лікування становить для клінічного діабетолога ефективний, безпечний та економічно вигідний для більшості пацієнтів із ДН.
Бенфотіамін – жиророзчинна форма тіаміну (вітаміну B1). Його біодоступність перевищує таку тіаміну гідрохлориду в 5-6 разів.
У рандомізованому плацебо-контрольованому дослідженні H. Ledermann і K.D. Wiedey (1989) пацієнти отримували 320 мг бенфотіаміну (+ вітамін B6 + вітамін B12). У результаті визначалося покращення больової (з 1,7 до 0,9; p<0,01), тактильної (з 1,5 до 1,0; p<0,05) та вібраційної чутливості (з 0,84 до 2,22; p<0,05).
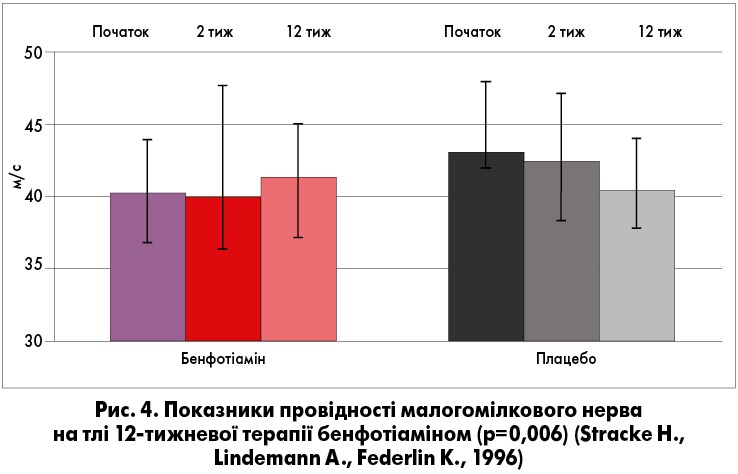
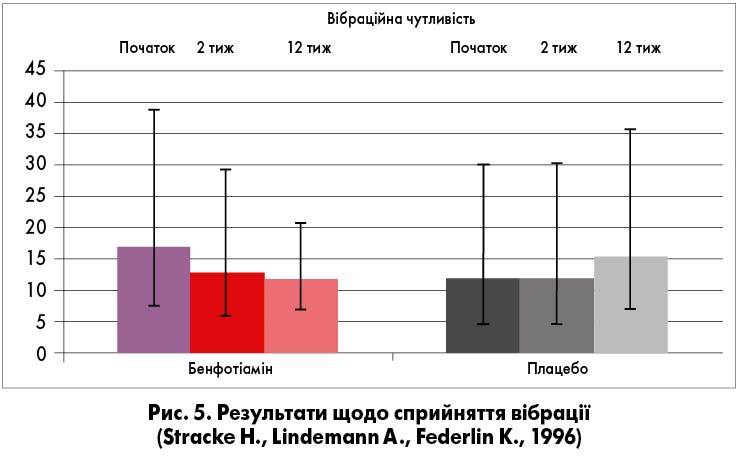
У дослідженні Н. Stracke, А. Lindemann, К. Federlin (1996) протягом 12 тиж оцінювали застосування бенфотіаміну (+ піридоксин + ціанокобаламін). Перші 2 тиж (початкова терапія) бенфотіамін призначався в дозі 320 мг, а наступні 10 тиж – 120 мг. Згідно з отриманими даними, у досліджуваній групі покращувалася провідність нервового імпульсу, знижувався поріг вібраційної чутливості стопи (рис. 4-5).
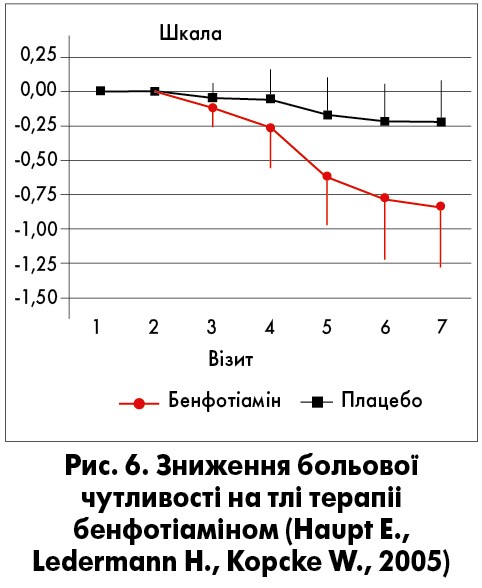 У дослідженні BEDIP (Haupt E., Ledermann H., Kоpcke W., 2005) пацієнти протягом 3 тиж приймали бенфотіамін 400 мг на добу протягом 3 тижнів. Згідно з отриманими результатами в пацієнтів значуще знижувався больовий синдром (рис. 6).
У дослідженні BEDIP (Haupt E., Ledermann H., Kоpcke W., 2005) пацієнти протягом 3 тиж приймали бенфотіамін 400 мг на добу протягом 3 тижнів. Згідно з отриманими результатами в пацієнтів значуще знижувався больовий синдром (рис. 6).
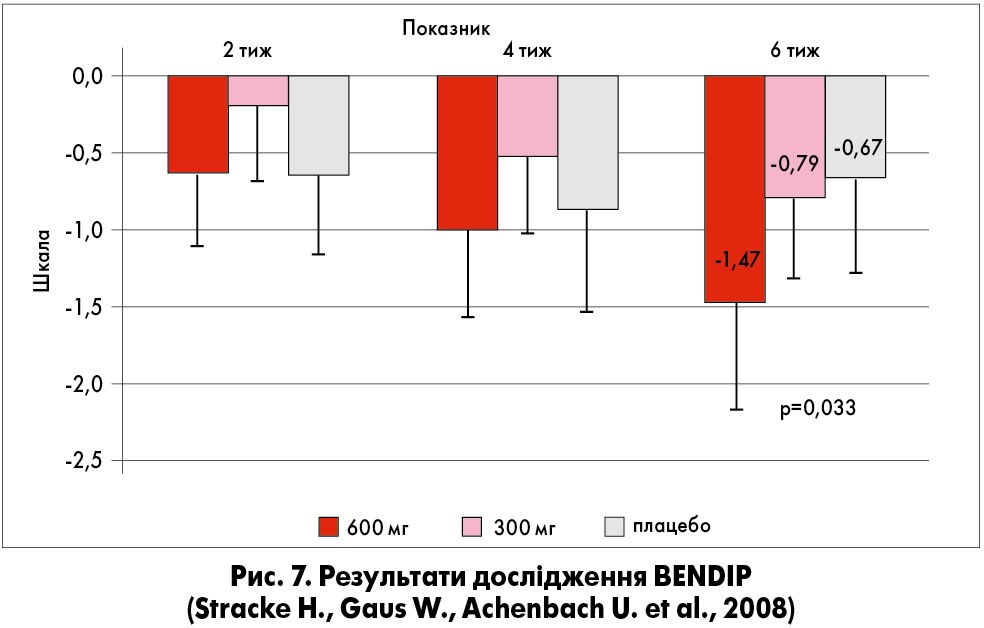
Дослідження BENDIP (Stracke Н., Gaus W. et al., 2008) порівнювало використання бенфотіаміну в дозі 300 мг, 600 мг з плацебо у хворих на ДН. Симптоми захворювання оцінювалися за шкалами NSS (шкала невропатичних симптомів Young) і TSS (загальна шкала неврологічних симптомів, модіфікована за Ziegler). Після курсу лікування кількість балів по шкалі NSS суттєво зменшилася (рис. 7).
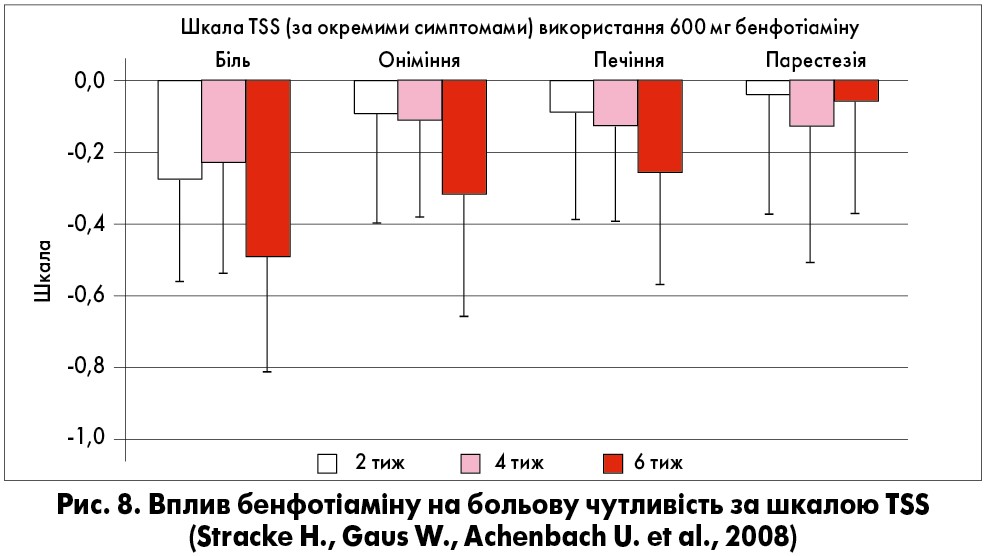
Під час оцінки симптомів за шкалою TSS було виявлено, що хворі з групи бенфотіаміну відчували більш значуще поліпшення стану, ніж учасники групи плацебо, при цьому досліджуваний препарат найбільше впливав на показник «біль» (рис. 8).
Тривалість терапії бенфотіаміном допоки залишається не до кінця вирішеним питанням. Було проведено подвійне сліпе рандомізоване плацебо-контрольоване паралельне дослідження, яке включало 22 пацієнти з ЦД 1 та 2 типу. Критеріями включення були: наявність діабетичної сенсомоторної полінейропатії (кількість балів за опитувальником MNSI (Michigan Neuropathy Screening Instrument) ≥4 або кількість балів при огляді MNSI ≥2,5); вік – від 18 до 75 років; рівень глікозильованого гемоглобіну (HbA1c) ≤9,5%. Досліджувана група отримувала бенфотіамін у дозі 600 мг/добу протягом 3 міс, а потім – 300 мг/добу до 9 місяців. У пацієнтів симптоми ДН оцінювали за шкалою Лікерта та MNSI, а якість життя – за шкалою Neuro-QOL. Результати показали, що після періоду лікування в досліджуваній групі вираженість симптомів, оцінена за шкалою MNSI, значуще зменшувалася.
У пацієнтів, які отримували бенфотіамін, також спостерігалося значне зменшення больового синдрому. Під час огляду пацієнтів основної групи зазначалося суттєве покращення всіх видів чутливості нижніх кінцівок, особливо виражене в період 6-9 міс лікування. Важливо, що на тлі використання бенфотіаміну не було виявлено значного впливу на рівень HbA1c та якості життя, розрахованої за шкалою QOL. За результатом дослідження авторами був зроблений висновок, що терапія бенфотіаміном протягом 6-12 міс у хворих на ДН:
- є безпечною;
- значуще покращує симптоми ДН, передусім знижується відчуття болю;
- має тривати не менше як 6 місяців.
В іще одному дослідженні (Du Х., 2008) вивчалося комбіноване застосування бенфотіаміну та АЛК для лікування ускладнень ЦД 1 типу. Вже через 2 тиж спостерігалося значне зменшення токсичних метаболітів, що спричиняють розвиток ускладнень діабету.
Наприкінці своєї доповіді професор А. Штірбан перелічив основні тези свого виступу:
- ДН часто не діагностується або діагностується несвоєчасно.
- За технологією скринінг ДН є легким і швидким.
- Патогенетичне лікування ДН має включати використання АЛК та/або бенфотіаміну як безпечних препаратів.
- АЛК і бенфотіамін можуть використовуватися для довготривалої терапії (є дані про використання АЛК протягом 4 років, а бенфотіаміну – протягом 1 року).
Отже, використання бенфотіаміну та АЛК має беззаперечні переваги в лікуванні ДН. В Україні бенфотіамін представлений препаратом Бенфогама® 300, АЛК – препаратами Тіогама® таблетки та Тіогама® Турбо (компанія «Вьорваг Фарма», Німеччина). Бенфогаму рекомендовано використовувати по 1 таблетці (300 мг) 1 раз на добу тривало, а Тіогаму Турбо – по 600 мг внутрішньовенно крапельно 1 раз на добу протягом 2-4 тижнів, а далі – по 1 таблетці Тіогами 600 мг 1 раз на добу 2-4 місяці.
Підготував Валерій Палько
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 1 (45) березень 2019 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....
Метформін – протидіабетичний препарат першої лінії, який пригнічує глюконеогенез у печінці і в такий спосіб знижує рівні глюкози в крові. Крім того, він знижує ризик кардіоваскулярних подій, чинить нефропротекторний ефект і здатен подовжувати тривалість життя. Завдяки цим властивостям метформін нині розглядають як мультифункціональний препарат і дедалі частіше застосовують для лікування та профілактики різноманітних захворювань....
Сучасне лікування хворих на цукровий діабет (ЦД) 2 типу включає зміну способу життя і медикаментозну терапію для контролю глікемії та профілактики ускладнень. Проте дослідження показують, що на практиці небагато хворих досягають контролю захворювання (частково через погану прихильність до лікування). Частка пацієнтів, які дотримуються протидіабетичної терапії, коливається від 33 до 93% (упродовж 6-24 міс) [1, 2]....