Новые механизмы развития неалкогольной жировой болезни печени и стратегия патогенетической терапии
 Неалкогольная жировая болезнь печени (НАЖБП) является наиболее распространенным заболеванием, от которого страдает около 25% взрослого населения во всем мире. НАЖБП – серьезная проблема общественного здравоохранения, связанная с эпидемией ожирения, нездоровыми диетическими моделями и распространением малоподвижного образа жизни.
Неалкогольная жировая болезнь печени (НАЖБП) является наиболее распространенным заболеванием, от которого страдает около 25% взрослого населения во всем мире. НАЖБП – серьезная проблема общественного здравоохранения, связанная с эпидемией ожирения, нездоровыми диетическими моделями и распространением малоподвижного образа жизни.
Быстро повышающаяся распространенность заболевания и его агрессивной формы – неалкогольного стеатогепатита (НАСГ) – требует новых терапевтических подходов, основанных на глубоком понимании факторов риска и патогенетических механизмов развития заболевания, с целью прекращения прогрессирования болезни до стадии фиброза или цирроза и рака печени. Новые данные свидетельствуют о том, что наблюдаемое в последнее время увеличение заболеваемости гепатоцеллюлярной карциномой обусловлено НАЖБП, особенно за рубежом [24]. Риск развития НАЖБП у женщин в репродуктивный период ниже по сравнению с мужчинами, однако с возрастом защитный эффект теряется, и распространенность НАЖБП сопоставима с таковой у мужчин.
Несмотря на то что в последние десятилетия были достигнуты значимые прорывы в отношении изучения патогенеза НАЖБП, заболевание по-прежнему остается сложным и мультисистемным, и понимание его механизмов все еще не полно.
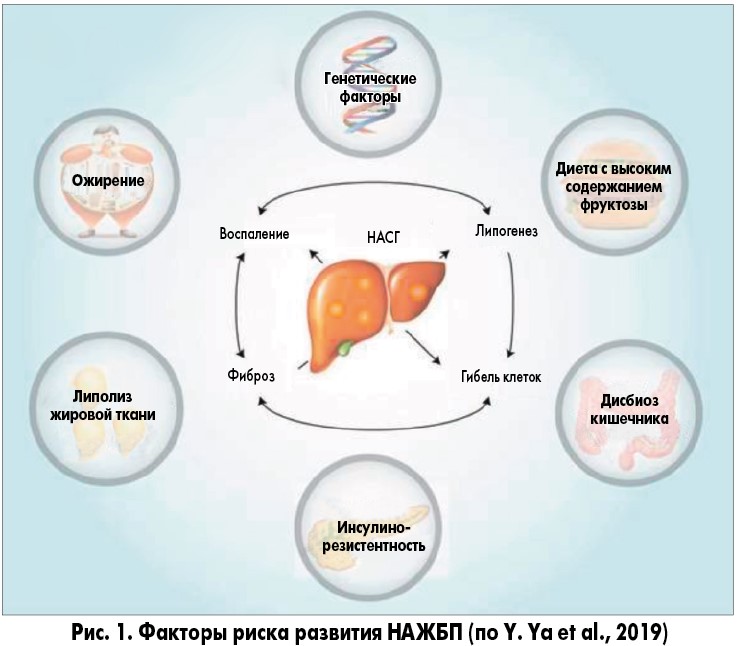
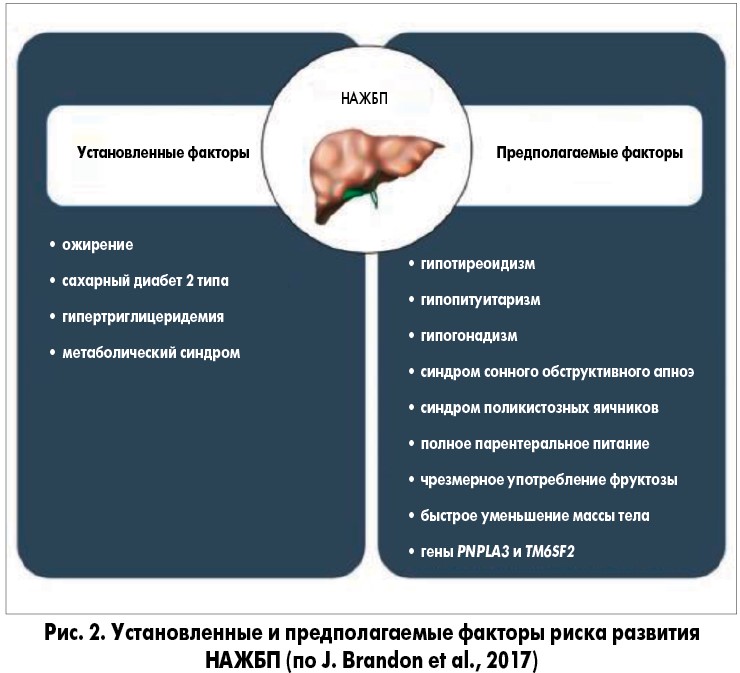
В 2018 году были достигнуты существенные успехи в изучении факторов риска прогрессирующего заболевания печени при НАЖБП, включая генетические варианты и микробиоту кишечника (рис. 1, 2). Получены также обнадеживающие результаты применения лекарственных средств, воздействующих на метаболические пути, вовлеченные в прогрессирование повреждения печени.
В настоящее время гипотеза «множественных ударов», которая подразумевает множество факторов, действующих параллельно и синергически у лиц с генетической предрасположенностью, является общепринятой точкой зрения для объяснения разных стадий развития НАЖБП, наблюдаемых клинически (рис. 3).
Новые концепции патогенеза, подтвержденные результатами клинических исследований, свидетельствуют о том, что стеатоз печени и НАСГ могут считаться изолированными, совершенно самостоятельными заболеваниями и не рассматриваться как последовательный процесс трансформации стеатоза в стеатогепатит. Однако эта точка зрения не является общепризнанной и требует дальнейшего изучения [2, 13].
Наследственные факторы и отличительные признаки некоторых этнических групп позволяют предположить, что генетические факторы могут играть важную роль в определении фенотипического проявления и общего риска развития НАЖБП [2]. В эпидемиологических и генетических исследованиях показана связь морфологической стадии НАЖБП и наследственных факторов. В настоящее время выделяют три гена, ассоциированных с НАЖБП: PNPLA3, TM6SF2 и GCKR. Вместе с генами, отвечающими за инсулинорезистентность, депонирование липидов, воспаление и фиброгенез в гепатоцитах, они определяют фенотип жировой болезни печени. Участие генетических факторов в развитии НАЖБП было доказано у лиц с инсулинорезистентностью и избыточной массой тела.
Кластеры НАЖБП в семьях с определенными генетическими вариациями генов TM6SF2, PNPLA3, NCAN и PPP1R3B или изменениями рядом с ними увеличивают наследуемость НАЖБП до 27%. Одним из генетических вариантов, связанных с НАЖБП, является миссенс-мутация в гене 3, содержащем палатиноподобный фосфолипазный домен (PNPLA3). PNPLA3 оказывает сильное влияние не только в отношении накопления жира в печени, но также и на склонность к развитию более тяжелого гистологического поражения печени, независимо от степени ожирения или наличия диабета [2].
Установлена возможность быстрого прогрессирования НАЖБП при наличии аллеля адипонутрина rs738409 и отсутствии ожирения, сахарного диабета, дислипидемии и других компонентов метаболического синдрома. Изменения в генах, регулирующих процессинг и синтез липопротеинов очень низкой плотности, были сопряжены с частотой выявления НАЖБП [2].
Белок-переносчик эфиров холестерина играет ключевую роль в обратном транспорте холестерина, посредством которого последний проникает из периферических тканей обратно в печень – место его синтеза. L. Adams и соавт. (2012) описали два однонуклеотидных полиморфизма кодирующего гена – rs12447924 и rs12597002, ассоциированные с повышенным риском стеатоза печени; при этом степень риска у лиц с НАЖБП без ожирения была выше [10].
Стеролрегулирующий элементсвязывающий фактор‑2 (SREBF‑2) – ген SREBF‑2 кодирует стеролрегулирующий элементсвязывающий протеин, контролирующий его клеточный синтез, захват и экскрецию: повышение продукции SREBF‑2 в печени коррелирует с тяжестью НАЖБП [2].
Эпигенетические модификации определяются как наследственное, но обратимое явление, влияющее на экспрессию генов без изменения последовательности ДНК. Они включают метилирование ДНК, модификации гистонов и микро-РНК, а также могут играть роль в патогенезе НАЖБП. Эпигенетические модификации, как полагают, являются ключевым детерминантом НАЖБП, и их изучение предоставляет новые возможности для управления заболеваемостью и смертностью от гепатоцеллюлярной карциномы, хотя имеющиеся данные весьма скудны. Необходимы всесторонние исследования относительно применения эпигенетических факторов с целью диагностики и терапии НАЖБП [2].
Согласно данным исследования GWAS Xu et al. (2019), во время прогрессирования НАЖБП активность генов, связанных с биосинтезом липидов, клеточным апоптозом и воспалением, увеличивалась, тогда как генов, связанных с реакцией повреждения ДНК, биосинтезом холестерина и углеводным обменом, снижалась. В других исследованиях была показана корреляция между статусом метилирования или ацетилирования различных гистонов и митохондриальных белков и воспалительной активностью при НАСГ. Кроме того, печеночная экспрессия различных микро-РНК, таких как miR‑122, miR‑335, miR‑29c, miR‑34a, miR‑155 и miR‑200b, участвует в патогенезе НАЖБП, их можно использовать в качестве биомаркеров заболевания [27].
По данным NHANES III, общая тенденция к увеличению распространенности заболевания наблюдается с возрастом. Так, распространенность НАЖБП у мужчин в возрасте от 30 до 40 лет составляет 16,1%, от 41 до 50 лет – 22,3%, старше 60 лет – 27,6%; при этом максимальная распространенность заболевания отмечается в возрасте от 51 до 60 лет – 29,3% [13].
Связь ожирения и НАЖБП обусловлена следующим. Жировая ткань является одним из основных чувствительных к инсулину органов, и процесс дифференциации преадипоцитов в адипоциты индуцируется инсулином [25]. Внутри жировой ткани инсулин стимулирует синтез триглицеридов и ингибирует липолиз, усиливая активность липопротеинлипазы. Она является наиболее чувствительным путем действия инсулина, облегчая поглощение свободных жирных кислот и транспорт глюкозы, ингибируя гормоночувствительную липазу и увеличивая экспрессию генов липогенных ферментов.
Ожирение и нарушение действия инсулина в адипоцитах приводят к неспособности подавления липолиза, стрессу адипоцитов, рекрутингу и инфильтрации макрофагами жировой ткани с последующим высвобождением провоспалительных адипоцитокинов, главным образом фактора некроза опухоли (TNF), интерлейкина (IL)‑6, моноцитарного хемоаттрактантного белка‑1, резистина и ингибитора активатора плазминогена‑1. Эти адипоцитокины способствуют нарушению передачи сигналов инсулина через ядерный фактор-κB (NF-κB) и c-Jun N-терминальную киназу (JNK), созданию порочного круга в жировой ткани и формированию инсулинорезистентности (ИР) в других чувствительных к инсулину тканях, в то время как уровень защитных адипокинов (снижающих ИР), таких как адипонектин, у пациентов с НАЖБП снижается. Уровень адипонектина в сыворотке крови при НАЖБП обычно снижается, тогда как уровень лептина повышается, что способствует возникновению профибротической среды при фиброзе.
Цитокиновые сигналы макрофагов, активные формы кислорода (АФК) и изменение соотношения адипонектин/лептин в пользу последнего ведут к активации звездчатых клеток печени и гиперпродукции экстрацеллюлярного матрикса, т.е. к фиброгенезу при НАЖБП [1].
В прогрессировании НАЖБП и развитии фиброза печени принимают участие разные факторы роста, стимулирующие процессы фиброгенеза путем усиления образования коллагена и соединительной ткани в органе: трансформирующий фактор роста-b (TGF-b), инсулиноподобный фактор роста, тромбоцитарный фактор роста (PDGF).
В последние годы в нескольких когортных исследованиях продемонстрирована связь между изменением массы тела и заболеваемостью НАЖБП. Было показано, что даже незначительное увеличение массы тела на 2 кг в пределах нормы повышает риск развития НАЖБП. Общая распространенность ожирения при НАЖБП в мире составляет 51% [2].
Следует отметить, что существует тип «худой» НАЖБП, который отмечается у пациентов без ожирения. Механизм нежировой неалкогольной болезни печени является сложным, связан с генетическими факторами и обусловлен диетой с высоким содержанием жиров и фруктозы. Пациенты с «мышечной» НАЖБП всегда молодого возраста, часто ведут малоподвижный образ жизни и имеют сниженную чувствительность к инсулину, высокий уровень триглицеридов и высокий риск развития сердечно-сосудистых заболеваний. Тем не менее механизмы прогрессирования стеатоза в фиброз при «худой» неалкогольной болезни печени и НАЖБП одинаковы [3].
Калорийность рациона и специфическое потребление питательных веществ имеют решающее значение для развития НАЖБП, в частности стеатоза печени. Диета, содержащая высокий уровень холестерина, большое количество фруктозы (диета быстрого питания, или фаст-фуд) и насыщенных жиров вызывает ожирение, ИР, развитие стеатоза печени с минимальным воспалением без фиброза. У подростков большее потребление фруктозы связано с множественными маркерами кардиометаболического риска, но, по-видимому, эти отношения опосредованы висцеральным ожирением [10]. Диета с высоким содержанием жиров приводит к подавлению воспалительных процессов в кишечнике и усилению этого механизма в печени.
Cреди диетических факторов фруктоза имеет первостепенное значение, поскольку она является одновременно субстратом и мощным индуктором печеночного синтеза жирных кислот и триглицеридов (липогенез de novo – DNL) из-за активации ключевых факторов транскрипции, таких как SREBP‑1c и ChREBP. Предполагается, что сахара стимулируют DNL и запускают воспалительный ответ, приводящий к апоптозу гепатоцитов через c-Jun-N-терминальный путь. Следует отметить, что гепатоциты подвергаются воздействию более высоких концентраций фруктозы, чем клетки других тканей, поскольку после абсорбции фруктоза напрямую поступает в печень через воротную вену.
Фруктоза, которая истощает внутриклеточный аденозинтрифосфат, при отсутствии инсулина трансформируется в липид, увеличивая таким образом жировые отложения, и вносит свой вклад в развитие НАЖБП и НАСГ. Об этом также свидетельствует сильная связь сахарного диабета 2 типа и НАСГ у лиц, потребляющих много фруктозы, содержащейся в безалкогольных напитках. Истощение печеночного аденозинтрифосфата обусловливает митохондриальную дисфункцию, образование АФК и развитие воспаления, а также усиливает стресс эндоплазматического ретикулума с последующей активацией связанной со стрессом JNK, способствующей апоптозу гепатоцитов, что является отличительным признаком НАСГ.
Фруктоза и определенные специфические рецепторы (например, связанный с G-белком рецептор хемокинов – CX3CR1) могут регулировать кишечную проницаемость при НАЖБП, приводя к прогрессированию заболевания. Фруктоза безалкогольных напитков способствует развитию жировой дистрофии печени и повышению уровня С-реактивного белка [12].
Реализация ИР осуществляется, прежде всего, на уровне гепатоцитов. При нарушении функционального состояния гепатоцитов, развитии воспаления значительно снижается активность многих белков-транспортеров, в первую очередь происходят нарушения в мембранных белках – транспортерах глюкозы. Это приводит к формированию ИР, провоцирующей развитие системной сосудистой воспалительной реакции.
Липидный гомеостаз печени жестко контролируется сложной системой сигнальных/транскрипционных путей, регулируемых гормонами, факторами транскрипции и ядерными рецепторами, при этом передача сигналов инсулина играет ключевую роль. Нарушение передачи сигналов инсулина на уровне жировой ткани и печени способствует тому, что у пациентов с ожирением или сахарным диабетом 2 типа развитие ИР приводит к неингибированному липолизу в жировой ткани. Это вызывает чрезмерный приток неэтерифицированных жирных кислот в печень, где они поглощаются гепатоцитами при помощи транспорта жирных кислот через белок 2 (FATP2), FATP5 и другие транспортные белки, такие как белок, связывающий жирные кислоты (FA), и кавеолин‑1.
Роль железа в прогрессировании НАСГ остается спорной, но есть предположения, что железо может принимать определенное участие в патогенезе НАСГ. В мышиной модели db/db (особи с дефицитом рецептора лептина и генетическим ожирением) перегрузка железом обусловливала окислительный стресс в печени, активацию иммунных клеток и повреждение везикул гепатоцитов, что приводило к НАСГ. Сообщалось, что у пациентов с НАСГ повышена абсорбция железа в двенадцатиперстной кишке за счет активации транспортера двухвалентного металла 1, и что отложение железа в гепатоцитах при НАСГ способствует прогрессированию заболевания за счет увеличения выработки АФК и более высокой частоты апоптоза гепатоцитов. Отложение железа в гепатоцитах также ассоциировано с повышенным риском фиброза печени [13].
Недавно несколько исследовательских групп выявили, что липотоксичность в гепатоцитах связана с усилением воспалительного ответа из-за высвобождения внеклеточных пузырьков – экстрацеллюлярных везикул, происходящих из клеток (EVs). Эти EVs содержат несколько биоактивных молекул (включая белки, липиды и нуклеиновые кислоты), которые служат межклеточными мессенджерами и могут модулировать прогрессирование резидентных мононуклеарных клеток, активирующих НАСГ. Экстрацеллюлярные везикулы также могут передавать сигналы другим клеткам: эндотелиальным клеткам, активирующим ангиогенез, и звездчатым, индуцирующим профиброгенный фенотип. Высвобождение EVs из гепатоцитов представляет собой сложный процесс, вызванный токсической перегрузкой липидами и опосредованный сигнальным каскадом TNF-подобного апоптоз-индуцирующего лиганда (TRAIL) рецептора 2 (TRAIL-R2) и Rho-ассоциированной протеинкиназой 1. EVs были предложены в качестве биомаркеров НАСГ, но необходимы дальнейшие исследования для определения того, можно ли путем выявления EVs в сыворотке крови отличать НАСГ от простого стеатоза [13].
Нарушение сна является независимым фактором риска развития НАЖБП и связано с воспалительными цитокинами (IL‑6 и TNF). Эти цитокины активируются при нарушениях сна и принимают участие в патогенезе НАЖБП за счет повышения липолиза адипоцитов, вызвающего избыточное накопление в печени свободных жирных кислот. Нарушение сна может влиять на ось надпочечники – гипофиз, что, в свою очередь, сказывается на метаболизме кортизола, приводящем к накоплению жира в печени.
Определенное значение в патогенезе НАЖБП имеет снижение синтеза и нарушение транспорта желчных кислот, связанное с повреждением мембран гепатоцитов, ингибированием ферментных систем и воспалением.
В настоящее время активно изучается так называемая энтерогепатическая ось патогенеза НАЖБП. На уровне энтероцитов также происходят метаболические нарушения, связанные с активностью так называемых toll-подобных рецепторов (TLR) 3 типа, CD28. TLR3 – мембранный белок, относится к группе toll-подобных рецепторов, обеспечивающих функционирование врожденного иммунитета. TLR3 играет важную роль в реализации хронического системного воспаления и патогенезе НАЖБП.
По данным проведенных исследований, у пациентов с НАЖБП выявляют более высокие титры антител (IgG) к ряду кишечных бактерий, в частности, Escherichia coli HA116, Bacteroides fragilis, Bifidobacterium thermophilium и Klebsiella oxytoca.
У пациентов с НАЖБП чаще, чем у здоровых лиц, отмечается повышенная проницаемость кишечной стенки, при этом риск ее формирования увеличивается в 30 раз и более на стадии НАСГ. Проницаемость кишечного эпителиального барьера ассоциирована с уровнем липополисахаридсвязывающего белка, гиперпродукция которого характерна для пациентов с НАЖБП [1].
У людей с ожирением чаще развивается синдром избыточного бактериального роста в кишечнике. Клеточные стенки грамотрицательных бактерий содержат липополисахарид (ЛПС) или эндотоксин, который может активировать каскад воспаления через 4-зависимые и TLR4-независимые пути toll-подобного рецептора. Это приводит к повышенной активности генов для некоторых цитокинов – TNF и IL‑6, индуцибельной синтазы оксида азота, NF-κB, ингибитора NF-κB. Данные медиаторы воспаления вызывают ИР. У лиц с НАЖБП повышены кишечная проницаемость и уровень сывороточного эндотоксина, что приводит к бактериальной транслокации и эндотоксемии. В нормальных условиях эта эндотоксемия быстро «очищается» ретикуло-эндотелиальной системой печени. Однако на фоне патологии печени или при длительном воздействии ЛПС, которые являются гепатотоксинами, в органе запускается каскад морфологических и функциональных изменений, вызывая острый воспалительный ответ и увеличение количества полиморфно-ядерных клеток, выделяющих реактивные кислородные метаболиты, протеазы и другие ферменты, с прогрессирующим повреждением печени и формированием НАСГ.
В печени имеется большое количество клеток врожденной иммунной системы. Эти клетки могут распознавать экзогенные молекулы, которые несут специфические патогенассоциированные молекулярные паттерны, и эндогенные вещества с ассоциированными с опасностью молекулярными паттернами через их рецепторы распознавания паттернов, в том числе TLR и нуклеотидсвязывающие белковые рецепторы, содержащие домен олигомеризации. Взаимодействие этих рецепторов с бактериальными продуктами приводит к активации нескольких путей воспаления, включая воспалительные процессы, которые, в свою очередь, активируют каспазу‑1, расщепляющую про-IL‑1β и про-IL‑18 в провоспалительные цитокины.
Повышенное поступление эндотоксинов кишечных бактерий в портальную систему вызывает активацию клеток Купфера, которые индуцируют выработку TGF-β и последующую активацию звездчатых клеток, приводя к формированию фиброза печени. Кроме того, будучи основными прекурсорами миофибробластов, звездчатые клетки также являются преобладающими мишенями, через которые TLR4-лиганды способствуют фиброгенезу. Звездчатые клетки могут также играть важную роль в создании воспалительного каскада в печени, связанного с эндотоксемией. TLR4 активирует не только клетки Купфера, но и звездчатые клетки; в то время как клетки Купфера участвуют в фиброгенезе посредством продуцирования провоспалительных и профиброгенных медиаторов, звездчатые клетки, как указано, являются основным источником внеклеточной матрицы в фиброзном процессе. Активированные звездчатые клетки очень чувствительны к ЛПС через TLR4-зависимый путь.
Под влиянием генетических (полиморфизмы адипонутрина, белка – переносчика эфиров холестерина, SREBF‑2) и пищевых факторов (холестерин, фруктоза), а также нарушений передачи инсулинового сигнала формируется ключевое патогенетическое звено НАЖБП – ИР. Последняя способствует как липолизу, так и липогенезу, обусловливающим перегрузку печени свободными жирными кислотами. Последствиями этой перегрузки являются инициация дополнительной «печеночной» ИР, стресс эндоплазматического ретикулума, активация NF-κB, жировая дистрофия гепатоцитов и окисление свободных жирных кислот, ведущее к гиперпродукции АФК. Стресс эндоплазматического ретикулума усиливает синтез триглицеридов, способствует апоптозу гепатоцитов и активирует JNK и макрофаги. NF-κB стимулирует продукцию TNF, блокирующего инсулиновые рецепторы и нарушающего продукцию адипонектина. Цитокиновые сигналы макрофагов, АФК и изменение соотношения адипонектин/лептин в пользу последнего ведут к активации звездчатых клеток печени и гиперпродукции экстрацеллюлярного матрикса, т.е. фиброгенезу (рис. 4).
В настоящее время, несмотря на прогресс в понимании патогенеза, клинического течения и прогноза НАЖБП, существуют сложности в выборе оптимального препарата для лечения пациентов с данным заболеванием. Причина, в первую очередь, заключается в том, что это мультифакторное заболевание, а пациент с НАЖБП – это пациент с коморбидной патологией. Этиология НАЖБП сложна, связана с множеством факторов, а клинические проявления и особенности прогрессирования на разных стадиях заболевания и у разных пациентов не совпадают, что увеличивает сложность лечения.
Важной составляющей патогенетического лечения при НАЖБП является предупреждение прогрессирования заболевания от простого стеатоза до фиброза, поэтому предпочтение отдается препаратам природного происхождения с выраженными антифибротическими свойствами. Гепаризин® – единственный гепатопротектор с доказанным прямым антифибротическим и антиканцерогенным действием, который позиционируется как средство для патогенетической терапии при НАЖБП.
Гепаризин® имеет две формы выпуска: ампулы для внутривенного введения и капсулы для перорального применения. Недавно компания «Валартин Фарма» представила Гепаризин® в капсулах с повышенной в 2 раза концентрацией ингредиентов – Гепаризин форте. Он содержит 50 мг глицирризина, 50 мг глицина и 50 мг метионина. Такая дозировка способствует повышению пациентами комплайенса, так как суточная доза будет достигнута при приеме 3 капсул в день (против 6 капсул в день при применении препарата Гепаризин®). Гепаризин форте принимают по 1 капсуле 3 раза в день, длительность курса подбирают индивидуально, минимальный курс – 1 мес.
Прямое антифибротическое действие глицирризина основано на снижении концентрации TNF и TGF-β1 (цитокинов, приводящих к индукции фиброгенеза), подавлении активации звездчатых клеток, угнетении избыточного синтеза коллагена I и III типа, активации коллагеназы (ММРs), что приводит к дегрануляции избыточных отложений коллагена в экстрацеллюлярном матриксе, ингибированию каспазы‑3, -8, снижению процессов апоптоза гепатоцитов [6]. Супрессивное воздействие препарата Гепаризин® на TNF и каспазу‑3 обусловливает его противовоспалительный и гепатопротекторный эффект.
Антивирусное действие глицирризина заключается в ингибировании вирусной репликации и регуляции иммунных реакций. Механизмом действия глицирризина при лечении вирусного гепатита С является дозозависимое ингибирование первичных частиц вируса, а также подавление экспрессии и функции основного ядерного белка, который оказывает провоспалительное и цитопатическое действие на гепатоциты.
Глицирризин способен усиливать некоторые иммунные функции, такие как продукция интерферонов и активность натуральных киллеров, а также модулировать реакции роста лимфоцитов путем повышения выработки IL‑2 (активация врожденного иммунитета).
Аминокислота глицин, входящая в состав препарата Гепаризин®, способствует снижению окислительного стресса, уменьшает воспаление и повреждение гепатоцитов свободными радикалами за счет увеличения синтеза глутатиона, нейтрализует токсическое воздействие этанола на организм, участвует в детоксикации аммиака, хелатообразовании, оказывает антиастеническое, антифибротическое, иммуномодулирующее, антиапоптотическое, энергосберегающее, противовирусное действие, препятствует возникновению побочных эффектов при длительном применении глицирризина.
Цистеин/метионин – серосодержащие аминокислоты, выступающие в роли антиоксиданта и детоксиканта (SH-группы инактивируют свободные радикалы), являются предшественниками глутатиона и метионина, оказывают антигипоксическое, антиоксидантное, детоксикационное, липотропное действие [6, 7]. Предотвращают возникновение побочных эффектов при длительном применении глицирризина.
Глицирризин (главный компонент препарата Гепаризин®) представляет собой соединение калиевой и кальциевой соли глицирризиновой кислоты, которое является тритерпеновым гликозидом, образованным одной молекулой глицирретовой кислоты и двумя молекулами глюкуроновой кислоты. Наличие агликана (глицирретовой кислоты), по своей структуре сходного с глюкокортикоидами, обусловливает гормоноподобное действие глицирризина.
Противовоспалительное действие препарата связано с псевдокортикостероидным (гормоноподобным) эффектом: глицирризин ингибирует 11-β-оксистероиддегидрогеназу, которая превращает глюкокортикоид кортизол в его неактивную форму кортизон, что приводит к увеличению концентрации эндогенного кортизола в крови и одновременной активации минералокортикоидных рецепторов.
Гепаризин® является синергистом синтетических глюкокортикоидных препаратов за счет блокирования расщепляющих их ферментов, угнетает провоспалительные цитокины: TNF, IL‑6, NF-κB в макрофагах, стимулирует синтез противовоспалительных цитокинов (IL‑2, -10, -12), селективно блокирует фосфолипазу А – метаболический фермент синтеза арахидоновой кислоты, в связи с чем блокируется образование простагландинов, лейкотриенов и других факторов воспаления.
Гепаризин® может ослаблять воспалительные реакции и модулировать врожденный иммунный ответ. В зависимости от исходного состояния иммунной системы реализуются два пути действия препарата – либо иммуностимуляция, либо иммуносупрессия. Иммунорегулирующее действие препарата Гепаризин® обусловлено регуляцией активации Т-лимфоцитов, индукцией интерферона-γ, активацией натуральных киллеров, дифференциацией Т-лимфоцитов тимуса.
Tingting Yan и соавт. (2018) показали, что глицирризин посредством восстановления гомеостаза желчных кислот и ингибирования воспалительного повреждения может быть терапевтической опцией для лечения пациентов с НАСГ. По данным этих авторов, глицирризин значительно ослабил экспрессию мРНК фиброгенетического гена, включая TGF-β1, тканевые ингибиторы металлопротеиназ 1 и 2, коллагена 1 и 2 и матриксных металлопротеиназ 2 и 9. Эти результаты свидетельствуют, что введение глицирризина способствует значительному уменьшению фиброгенеза печени, связанного с НАСГ [23].
Европейская исследовательская группа SNMC (M.P. Manns, H. Wedemeyer, A. Singer et al., 2012) cообщила о проведении III фазы исследования, направленного на подтверждение эффективности и безопасности применения глицирризина у пациентов, которым раньше не проводили терапию на основе интерферона + рибавирина, с оценкой биохимических и гистологических эффектов через 52 недели. Исследование было проведено в 73 центрах 11 европейских стран. После рандомизированного двойного слепого плацебо-контролируемого сравнения глицирризина, вводимого внутривенно 5 или 3 раза в неделю, и плацебо 5 раз в неделю в течение 12 недель 379 пациентам, последовало рандомизированное открытое сравнение. Глицирризин применяли внутривенно 5 и 3 раза в неделю в течение 40 недель. Первичными конечными точками были: доля пациентов со снижением уровня аланинаминотрансферазы ≥50% после 12 недель двойной слепой фазы и доля пациентов с уменьшением некровоспаления через 52 недели по сравнению с исходным уровнем. Доля пациентов с уменьшением некровоспаления через 52 недели при введении глицирризина 5 раз в неделю составила 44,9%, 3 раза в неделю – 46,0% соответственно. Глицирризин обеспечивал значительно более высокое снижение уровня аланинаминотрансферазы по сравнению с плацебо через 12 недель терапии, уменьшение некровоспаления и фиброза после 52-недельного лечения. Авторы отмечали хорошую переносимость глицирризина [18].
Результаты многочисленных рандомизированных контролируемых исследований свидетельствуют о том, что препарат SNMС (глицирризин + глицин + цистеин) значительно улучшает функцию печени у пациентов с циррозом печени: 252 пациента с циррозом печени получали SNMС по 2 капсулы 3-4 раза в день в течение 3 месяцев. У 80 (32%) пациентов выявлена нормализация биохимических показателей, у 167 (66%) – улучшение показателей в 2 раза и более, у 5 (2%) эффект не достигнут. Общая эффективность терапии составила 98% (Yue Sihong, 1998) [26].
Гепаризин® является полным аналогом японского препарата SNMC. Гепаризин® способствует уменьшению выраженности стеатоза, липотоксичности и фиброза печени; оказывает метаболический эффект, обеспечивая нормализацию липидного спектра, снижает ИР, что дает основание считать его патогенетическим средством с доказанным антифибротическими свойствами для лечения пациентов с НАЖБП.
Собственные наблюдения у больных с алкогольным фиброзом печени и НАЖБП также подтверждают антифибротическое, противовоспалительное действие препарата Гепаризин® [6-8].
Cписок литературы находится в редакции.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 2 (52), травень 2019 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...