Міждисциплінарний консенсус Швейцарії щодо ведення пацієнток із передменструальними розладами
Передменструальний синдром (ПМС) і передменструальний дисфоричний розлад (ПМДР) виявляють у жінок упродовж усього репродуктивного періоду життя. Оскільки симптоматика таких розладів є доволі широкою, до лікування іноді залучають лікарів різних спеціальностей: сімейних, гінекологів і психіатрів. У 2016 році у Швейцарії відбулася міждисциплінарна експертна зустріч, де було представлено алгоритм із ведення ПМС/ПМДР. Цей огляд присвячений методам діагностики та лікування передменструальних розладів у жінок.
Передменструальні розлади: визначення та епідеміологія
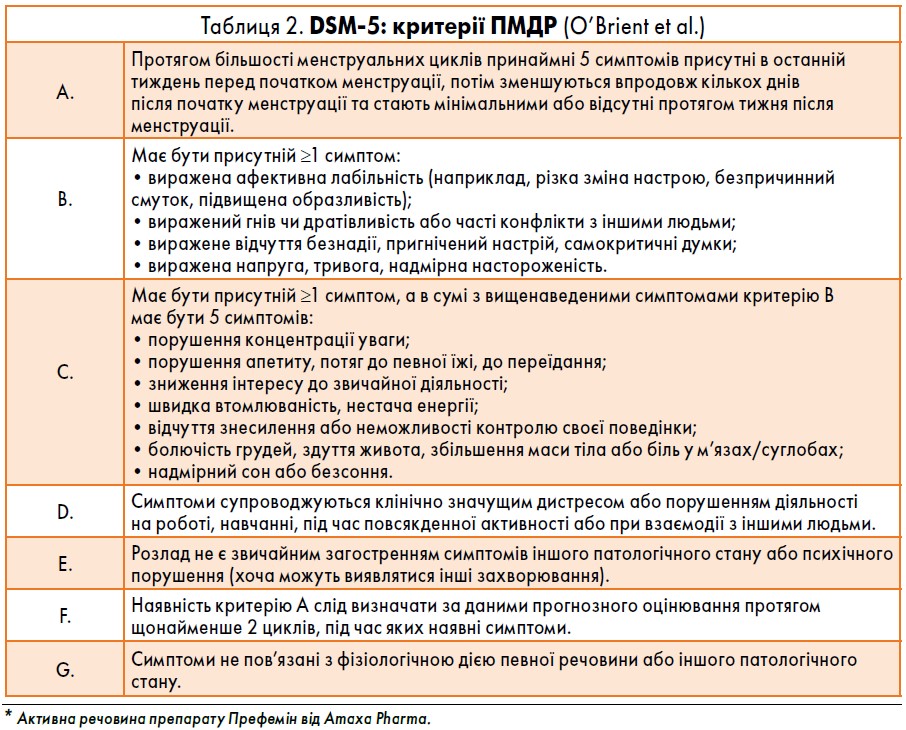
Міжнародне товариство з питань передменструальних розладів (ISPD) опублікувало оновлений консенсус щодо передменструальних розладів (ПМР). Відповідно до цього консенсусу, класичний ПМР слід відрізняти від варіантів ПМР (табл. 1). Класичний ПМР можна додатково класифікувати на (1) ПМР з переважно соматичними симптомами, (2) ПМР з переважно психологічними симптомами або (3) змішану форму із соматичними та психологічними симптомами. Найбільш поширеними психологічними симптомами є різка зміна настрою, дратівливість, тривога і депресія. При обстеженні жінок із переважно психологічними симптомами можна використовувати критерії Діагностичних та статистичних настанов із психічних захворювань (DSM‑5) щодо ПМДР (табл. 2). Приблизно у 30-40% жінок реєструють симптоми ПМС, а 3-8% жінок репродуктивного віку мають ПМДР (Ryu et al.). Тривалість цих симптомів може бути різною: від кількох днів до двох тижнів упродовж одного менструального циклу. Симптоми зазвичай наростають за тиждень до початку менструації і є максимально вираженими за два дні до неї. Перед овуляцією, як правило, симптоми відсутні.
Діагностичні дослідження
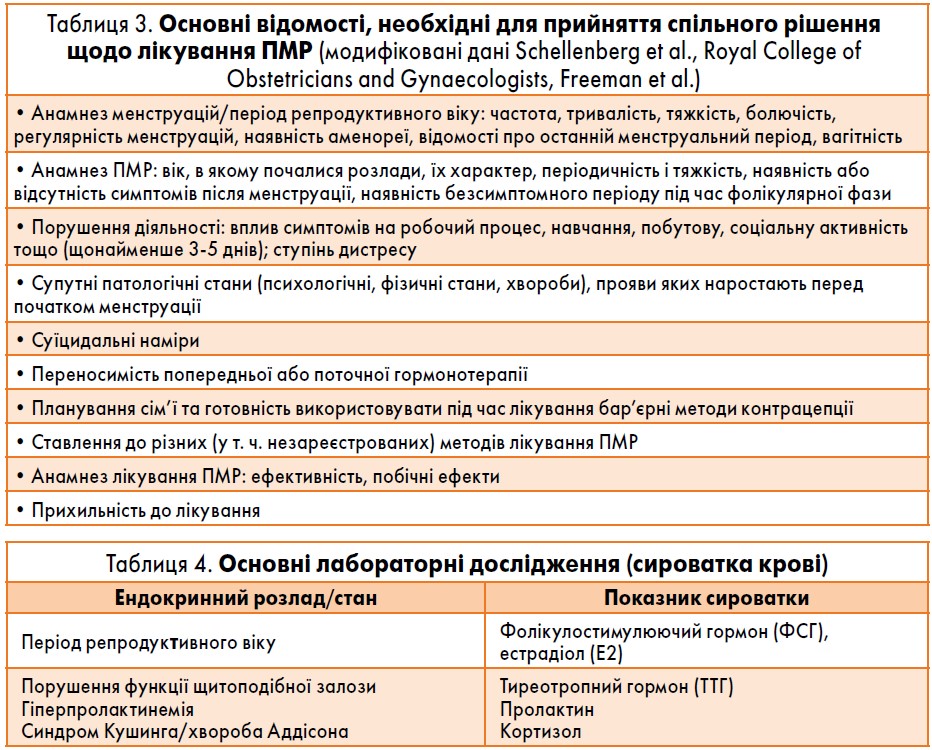
Для складання оптимального плану лікування під час першої консультації слід розглянути нижченаведені аспекти/питання (табл. 3), надалі – виконати основні лабораторні дослідження (бажано на 2-5-й день циклу, натще, між 8.00 та 9.00 годинами ранку) (табл. 4) та здійснювати систематичне оцінювання симптомів. Оскільки симптоми ПМС та ПМДР неспецифічні й мають схожість із симптомами інших патологічних станів, для підтвердження діагнозу необхідно виявити достовірні й надійні проспективні симптоми.
Зокрема, ПМДР часто супроводжуються порушеннями психіки, наприклад депресією (23%), біполярним розладом (8%) і тривожністю (7%) (Pearlstein et al.), тому важливо зібрати в пацієнтки анамнез про будь-які супутні психічні хвороби та схильність до суїциду. ПМДР можна відрізнити від ПМС за допомогою критеріїв DSM‑5 (табл. 2), тоді як диференційна діагностика ПМС є більш складною. Виділяють кілька інструментів збору даних, серед яких найчастіше використовують (принаймні в англомовних країнах) Анкету щоденного обліку тяжкості симптомів (DRSP). Це валідований опитувальник для самостійного заповнення.
Незалежно від обраного виду анкети, мінімальна тривалість записів має охоплювати два послідовні цикли. Актуальною проблемою усіх анкет є відсутність у них нормативних значень, що свідчать про наявність ПМС. На противагу цьому під час досліджень необхідне дотримання строгих критеріїв ПМС, встановлених Національним інститутом охорони здоров’я США (NIH). До цих критеріїв відносяться наростання симптомів ПМС щонайменше на 30% у період між фолікулярною (5-10-й дні менструального циклу) та лютеїновою фазами (за 6 днів до менструації). Крім того, ПМДР чітко визначений критеріями DSM‑5.
Огляд методів лікування ПМР
До методів лікування належать такі, як когнітивно-поведінкова терапія (особливо при ПМДР), альтернативні методи лікування, застосування психотропних препаратів, гормонотерапії, діуретиків та хірургічні втручання. Слід зазначити, що у Швейцарії, крім застосування прутняку звичайного (Vitex agnus-castus L.)* та прогестерону, не схвалено жодного з нижченаведених методів терапії ПМР.
Альтернативні методи лікування
До альтернативних методів лікування відносяться дієта, фізичні вправи, вживання мікроелементів (кальцію, піридоксину, магнію, вітаміну Е, міо-інозитолу), терапія лікарськими рослинами (прутняком звичайним (Vitex agnus-castus L.)*, звіробоєм (Hypericum perforatum L.), олією примули вечірньої (Oenothera biennis L.), шафраном (Crocus sativus L.), Ginkgo biloba L.), і немедикаментозне лікування, а саме – когнітивно-поведінкова терапія та голкотерапія. Слід зазначити, що лікувальні рослини можуть бути зареєстровані як харчові добавки або препарати, які реєструє Орган контролю за медичними препаратами та приладами Швейцарії (Swissmedic). В останньому випадку вони мають відповідати вимогам ефективності, безпеки та виробничого контролю.
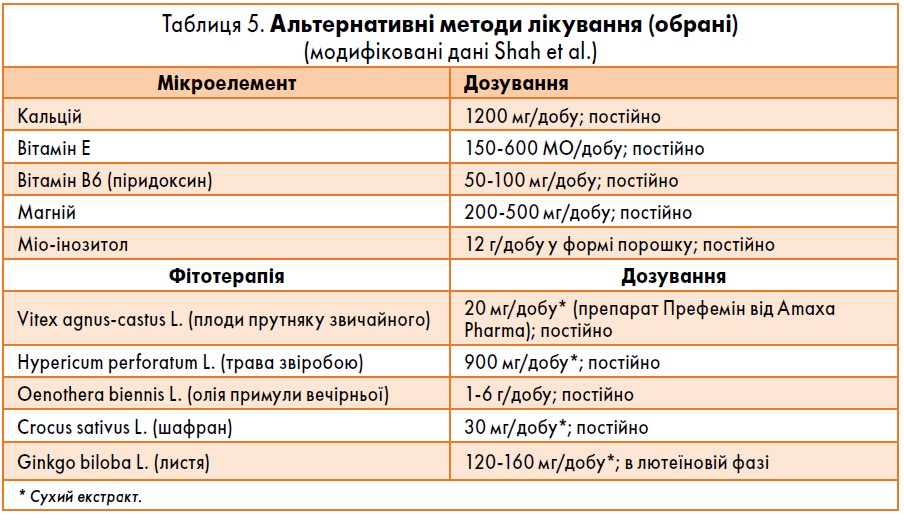
! Найбільш значущі докази ефективності альтернативного лікування ПМР виявлено при застосуванні кальцію, прутняку звичайного (Vitex agnus-castus L.)* і когнітивно-поведінкової терапії (табл. 5) (Nevatte et al.; Maharaj et al.).
За даними систематичного огляду, терапія екстрактом прутняку звичайного має переваги порівняно із застосуванням плацебо, піридоксину й оксиду магнію у жінок з ПМС (van Die et al.). У жінок із ПМДР, за даними одного дослідження, дія прутняку звичайного така сама, як у флуоксетину (Atmaca et al.), а в іншому дослідженні флуоксетин виявився більш ефективним (Ciotta et al.). Ефективність Vitex agnus-castus встановлено при лікуванні й соматичних, і психічних симптомів (van Die et al.). Загальний показник відповіді на лікування Vitex agnus-castus L. (препарат Префемін) у пацієнток із ПМР становив 52-81% (van Die et al.; Schellenberg et al.). Рекомендована тривалість лікування – не менше 3 місяців. Проте слід мати на увазі, що прутняк звичайний має допамінергічну дію, а отже, може взаємодіяти з антипсихотичними препаратами (це припущення на сьогодні не досліджено).
Психотропні препарати
До психотропних препаратів відносяться антидепресанти та анксіолітики. Антидепресанти можна застосовувати постійно або тільки протягом лютеїнової фази (початок – за 14 днів до передбачуваної менструальної кровотечі; завершення – день настання менструальної кровотечі або через кілька днів після цього). Загальний показник відповіді на лікування селективними інгібіторами зворотного захоплення серотоніну (СІЗЗС) у пацієнток із ПМР становить 50-90% (Shah et al.; Marjoribanks et al.). Ефект від лікування зазвичай спостерігають протягом 48 год від його початку. Незважаючи на те, що постійні та періодичні схеми лікування СІЗЗС однаково ефективно усувають дратівливість та різкі зміни настрою, постійна терапія СІЗЗС більш ефективна за наявності пригніченого настрою та соматичних симптомів (Freeman et al.; Landen et al.). Якщо відповідь на лікування в першому терапевтичному циклі є недостатньою, в наступному циклі можна збільшити дозу, а також змінити СІЗЗС. Побічні ефекти, наприклад нудоту, безсоння, головний біль, загальну слабкість, діарею і запаморочення, часто реєструють на початку застосування СІЗЗС (частота – 15%), але ці явища зазвичай зменшуються протягом кількох днів терапії. Навпаки, статеві розлади, приміром зниження лібідо або затримка оргазму, можуть зберігатися довго (частота – 9-30%), але швидко зникають після відміни СІЗЗС. На сьогодні серед жінок з ПМР, що приймають СІЗЗС та селективні інгібітори зворотного захоплення норадреналіну (СІЗЗН), не було зареєстровано жодних випадків спроб самогубства. Хоча синдром відміни при застосуванні СІЗЗС виникає рідко, їх дозу можна поступово зменшувати, особливо коли пацієнтці призначено постійну терапію. Протягом 6-8 міс після припинення лікування приблизно у 50% пацієнток реєструють рецидив розладу, проте він можливий навіть під час прийому медикаментів. Систематично не досліджувалося поєднання СІЗЗС з іншими препаратами (наприклад, кількома антидепресантами) під час лікування ПМР.
Доведено, що для усунення симптомів ПМР, крім СІЗЗС, можна застосовувати СІЗЗН, трициклічні антидепресанти та анксіолітики. Однак доказова база для цих препаратів є значно меншою.
Жінкам із симптомами одного з варіантів ПМР, наприклад передменструального загострення супутнього психічного розладу, слід призначати терапію антидепресантами, постійно консультуючись із психіатром. Це зумовлено тим, що у деяких пацієнток, наприклад із передпсихотичними станами, СІЗЗС можуть погіршити перебіг супутнього психічного захворювання. Крім того, при лікуванні класичного ПМР у жінок фертильного віку рекомендовано призначати препарат, який можна приймати під час вагітності (зокрема, сертралін, циталопрам).
Пригнічення овуляції
Для пригнічення овуляції можна застосовувати комбіновані оральні контрацептиви (КОК), агоністи гонадотропін-рилізинг-гормону (аГнРГ), естрогени та даназол. За даними попередніх досліджень встановлено, що КОК негативно впливають на афективні симптоми у жінок з ПМР. Тим не менше доведено, що інші препарати цієї групи, особливо з прогестагеном дроспіреноном у складі та/або коротшим періодом між прийомами таблеток, ефективні при лікуванні афективних і соматичних симптомів відповідно (Nevatte et al.; Maharaj et al.; Lopez et al.). Однак, оскільки застосування КОК підвищує ризик венозних тромбоемболій, під час їх прийому необхідне належне спостереження лікарем.
Отже, аГнРГ пригнічують функцію системи «гіпоталамус – гіпофіз – яєчник», викликаючи псевдоменопаузальний стан. Встановлено, що у жінок із ПМР показник відповіді на лікування становить 60-75%, при лікуванні й фізичних, і поведінкових симптомів (Wyatt et al.). Разом із аГнРГ, як правило, призначають «зворотну» менопаузальну гормонотерапію (МГТ): естрогени в поєднанні з прогестагенами, тиболон. Метою цієї терапії є запобігання негативним наслідкам дефіциту естрогену, зокрема припливам жару і остеопорозу. Проте на теперішній час не отримано даних про довгострокову безпеку такого лікування. Тому рекомендовано проводити денситометрію кісток при застосуванні аГнРГ(±МГТ) довше 6 міс і щонайменше кожні 2 роки після припинення терапії або, в окремих випадках, з іншою періодичністю. Лікування слід припинити, якщо на рентгенограмах, отриманих з інтервалом в 1 рік, виявлене значне зменшення щільності кісткової тканини.
Трансдермальні та ін’єкційні (але не пероральні) естрогени пригнічують овуляцію й суттєво зменшують симптоми ПМР порівняно з плацебо. Щоб забезпечити захист ендометрію, прогестаген слід поєднувати, наприклад, із дидрогестероном (не діє на центральну нервову систему) або додатково встановити внутрішньоматкову систему з левоноргестрелом. При застосуванні останньої виявляють всмоктування гормону у системний кровообіг протягом перших 3-4 міс, що може викликати наступні симптоми: депресію, загальну слабкість і здуття живота. Ці явища спостерігають у 10% жінок із непереносимістю прогестагену (Elovainio et al.). Як правило, через деякий час ці симптоми зникають.
Очевидно, що терапією відчаю при ПМР може бути проведення двобічної оваріектомії (ОЕ) та гістеректомії (ГЕ). Доведено, що таке втручання ефективно усуває і порушення настрою, і фізичні симптоми при ПМР, але ефект від нього зберігається лише за умови призначення МГТ естрогенами (монотерапії). Перш ніж рекомендувати хірургічне втручання, слід призначити аГнРГ і, таким чином, визначити потенційну ефективність оваріектомії.
Прогестагени
Ефективність застосування прогестагенів і прогестерону у жінок з ПМР не доведена, тому їх, як правило, не рекомендують застосовувати. Проте, за даними Кокранівського огляду (2012), неефективність прогестерону при ПМС не доведена (Ford et al.).
Діуретики
Доведено, що застосування спіронолактону, антагоніста рецепторів альдостерону, в дозі 100 мг/добу протягом лютеїнової фази зменшує й фізичні, й афективні симптоми (Vellacott et al.; Wang et al.). Оскільки спіронолактон є калійзберігаючим діуретиком, пацієнток слід періодично обстежувати для виключення гіперкаліємії.
Швейцарський алгоритм ведення ПМР
Швейцарський алгоритм ведення пацієнток із ПМР включає різні рівні надання медичної допомоги (первинної/вторинної) і проведення діагностичних та лікувальних заходів з урахуванням періоду репродуктивного віку жінки (репродуктивна фаза, перехідний період перед менопаузою).
Відповідно до багаторівневої схеми сімейні лікарі й гінекологи загального профілю відповідають за надання первинної медичної допомоги при ПМР, тоді як гінекологи-ендокринологи (провідні клініцисти), психіатри та психологи забезпечують надання вторинної допомоги при ПМР. Разом із пацієнткою вони утворюють «терапевтичний трикутник», у який, за наявності показань, можна додати фахівців із альтернативного лікування та хірургів. Первинний клінічний діагноз (що передбачає збір анамнезу, прогнозне оцінювання симптомів) має встановлювати лікар, що надає первинну медичну допомогу при ПМР.
! Міждисциплінарна експертна група рекомендує записувати симптоми під час ПМС щодня або щонайменше двічі в одному менструальному циклі (наприклад, під час фолікулярної (5-7-й день циклу) та лютеїнової фази (за 14 або за 6 днів до наступної менструації)) протягом двох послідовних циклів.
Якщо терапія першої та другої ліній (рис. 1, 2) неефективна, пацієнтку з ПМР слід направити до фахівця з вторинної медичної допомоги, бажано – до гінеколога-ендокринолога. Психіатр є необхідним спеціалістом для надання вторинної медичної допомоги жінкам із варіантом ПМР та супутнім психічним захворюванням. Комплексна клінічна діагностика передбачає також виконання лабораторних досліджень сироватки крові та прогнозне оцінювання симптомів упродовж двох послідовних циклів.
Слід зазначити, що запропонований алгоритм лікування є неоднаковим у жінок репродуктивного періоду та в пацієнток у пременопаузі.
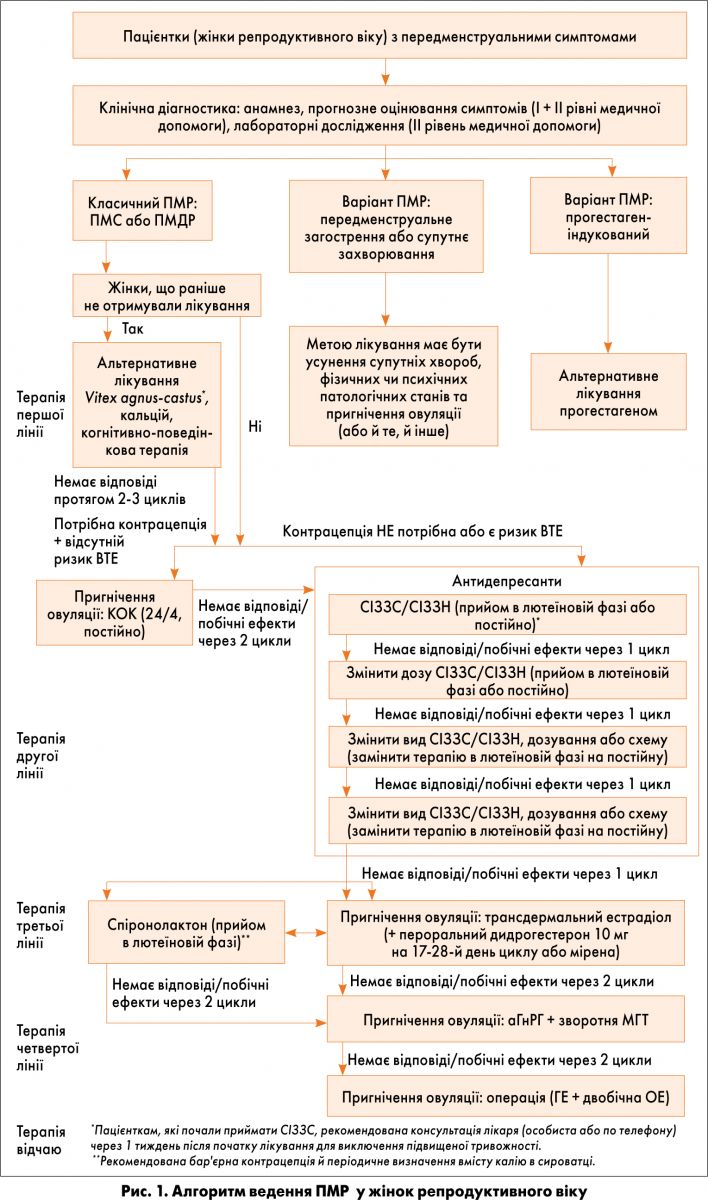
Основою для всіх наведених методів лікування має бути психологічне навчання пацієнтів. Для лікування жінок репродуктивного віку, що раніше не отримували лікування (рис. 1), використовують терапію першої лінії, а саме – альтернативне лікування (не менше 2-3 міс). У осіб, що не відповідали на терапію першої лінії або попередньо отримували лікування, застосовують терапію другої лінії: 2-місячний курс КОК, якщо необхідна контрацепція і немає ризику венозної тромбоемболії (ВТЕ); антидепресанти (СІЗЗС, СІЗЗН), якщо контрацепція не потрібна або є ризик ВТЕ. Пацієнткам, які почали приймати СІЗЗС, рекомендована консультація лікаря (особиста або по телефону) через 1 тиждень після початку лікування для виключення підвищеної тривожності. Для жінок, які планують вагітність, оптимальними препаратами СІЗЗС є циталопрам і сертралін. Трициклічні антидепресанти та анксіолитики мають призначатися виключно психіатром і лише у жінок із тяжкою формою ПМДР.
У пацієнток, які не відповідають на терапію, або в жінок із побічними ефектами від лікування можна розпочати терапію третьої лінії (застосування спіронолактону або пригнічення овуляції трансдермальними естрогенами, до яких додають прогестаген, щоб забезпечити захист ендометрію). Жінок, які обирають лікування спіронолактоном, слід попередити про необхідність бар’єрної контрацепції. Їм також рекомендують періодично визначати вміст калію в сироватці.
Пацієнткам, які не відповідають на будь-який варіант терапії третьої лінії, можна запропонувати пригнічення овуляції за допомогою аГнРГ в поєднанні зі зворотною МГТ (терапія четвертої лінії). У осіб, що відповідають на лікування, слід виконувати кісткову денситометрію принаймні через 6 міс від початку лікування та щонайменше кожні 2 роки після припинення терапії або, в окремих випадках, з іншою періодичністю. Хірургічне втручання у формі гістеректомії та двобічної оваріектомії є терапією відчаю, якої в більшості випадків можна уникнути.
Жінкам репродуктивного віку з класичною формою ПМДР слід повідомити, що вони мають підвищений ризик розвитку депресії, яка може виникнути під час вагітності, після пологів та в пременопаузальному періоді. Ця інформація пришвидшить звернення пацієнток до лікарів різного фаху у різні періоди життя.
У жінок під час пременопаузи можуть з’являтися нові передменструальні симптоми або посилюватися вже існуючі. Для початкового періоду пременопаузи характерна неоднакова тривалість менструального циклу, що перевищує 7 днів, часте підвищення рівнів ФСГ сироватки і зменшення резерву яйцеклітин. Для пізнього етапу властиві нерегулярні менструальні цикли з незначними кровотечами і, з високою ймовірністю, низький рівень естрогену в сироватці, часті загальні симптоми менопаузи.
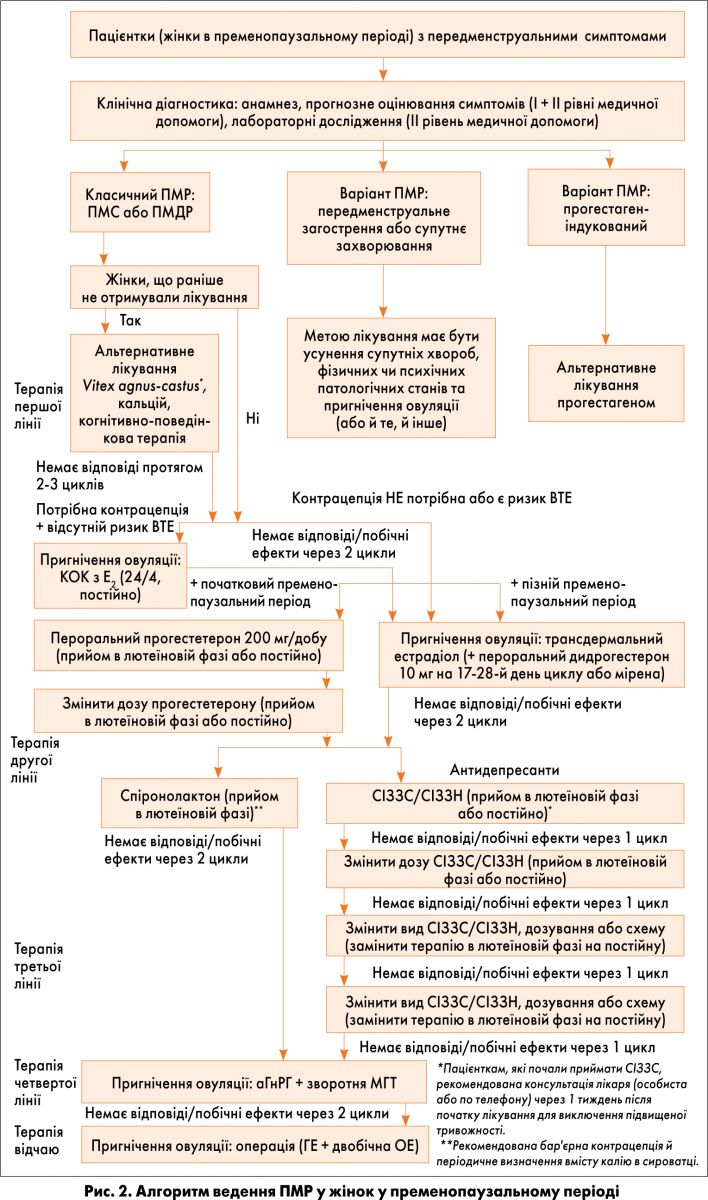
Жінки під час пременопаузи, що раніше не отримували лікування, як і жінки репродуктивного віку з ПМР (рис. 2), можуть спробувати альтернативне лікування в якості терапії першої лінії (2-3 міс). У осіб, що не відповідали на терапію першої лінії або попередньо отримували лікування, застосовують терапію другої лінії, яка передбачає 2-місячний курс КОК з Е2 (якщо необхідна контрацепція і відсутній ризик ВТЕ), застосування перорального прогестерону (початок пременопаузи, якщо контрацепція не потрібна або є ризик ВТЕ) чи супресію овуляції трансдермальними естрогенами, які поєднують із прогестагеном для захисту ендометрію (пізня пременопауза, якщо контрацепція не потрібна або є ризик ВТЕ). Пацієнткам, які не відповідають на терапію або в яких виникли побічні ефекти, призначають інші види лікування, наприклад прийом антидепресантів, спіронолактону (терапію третьої лінії), аГнРГ у поєднанні зі зворотною МГТ (четверту лінію) та хірургічне втручання у формі гістеректомії і двобічної оваріектомії (терапію відчаю).
Таким чином, Швейцарський алгоритм ведення пацієнток із ПМР, розроблений для надання багаторівневої медичної допомоги, з урахуванням періоду репродуктивного віку та залученням лікарів різного фаху, передбачає п’ять рівнів лікування.
За матеріалами P. Stute, C. Bodmer, U. Ehlert, R. Eltbogen, A. Ging, I. Streuli & Michael von Wolff (2017): Interdisciplinary consensus on management of premenstrual disorders in Switzerland, Gynecological Endocrinology.
Підготувала Анна Сакалош
Тематичний номер «Гінекологія, Акушерство, Репродуктологія» № 1 (33), березень 2019 р.
СТАТТІ ЗА ТЕМОЮ Акушерство/гінекологія
Чи варто змінювати свої харчові звички під час вагітності? Довкола цієї теми є багато суперечностей і рекомендацій, у яких легко заплутатися. Команда платформи доказової інформації про здоров’я «Бережи себе» спільно з лікарем-дієтологом Тетяною Лакустою з’ясували, чим раціон жінки в цей період особливий та на що слід звернути увагу. ...
Хронічний тазовий біль (ХТБ) є поширеним патологічним станом, який відзначається у жінок будь-якого віку і супроводжується сексуальною дисфункцією, емоційною лабільністю, аномальними матковими кровотечами, порушенням сечовипускання, розладами з боку кишечника тощо. Пацієнтки, які страждають на ХТБ, часто скаржаться на симптоми тривоги та депресії, що негативно позначається на їхній повсякденній активності, включаючи зниження працездатності та погіршення якості життя [1]. Сьогодні проблема ХТБ є економічним тягарем, пов’язаним із прямими або непрямими медичними витратами, які в середньому в різних країнах світу оцінюються у 4,9 млрд доларів на рік [2]. Раціональна фармакотерапія,спрямована на полегшення та контроль симптомів болю, є ключовою стратегією боротьби із ХТБ...
Дефіцит заліза є найпоширенішим патологічним станом у світі та однією з п’яти основних причин інвалідності. У той час як низький показник феритину у сироватці крові є діагностичною ознакою залізодефіциту, підвищений його рівень визначається як гострофазовий маркер, що може реєструватися при запальних станах уже в І триместрі вагітності. Відповідно до сучасних настанов, проведення рутинного скринінгу на залізодефіцит у невагітних та вагітних жінок за відсутності ознак анемії не рекомендоване. З огляду на останні літературні дані ця рекомендація має бути переглянута...
Наказ Міністерства охорони здоров’я України від 25.08.2023 № 1533 ...