Атопический дерматит: четыре составляющие эффективной топической терапии
 Атопический дерматит (АтД) – одно из самых распространенных дерматологических заболеваний, которому последние несколько десятилетий медики уделяют пристальное внимание, стремясь подобрать наиболее эффективное и безопасное лечение. Современные особенности диагностики и лечения АтД в странах Европейского региона регламентирует недавно опубликованный консенсус по лечению атопической экземы (атопического дерматита) у взрослых и детей (Wollenberg А. et al., 2018). В этом согласительном документе подчеркивается высокая распространенность АтД в мире: по данным экспертов, в глобальном масштабе этой патологией страдает 20% детского и 2-8% взрослого населения.
Атопический дерматит (АтД) – одно из самых распространенных дерматологических заболеваний, которому последние несколько десятилетий медики уделяют пристальное внимание, стремясь подобрать наиболее эффективное и безопасное лечение. Современные особенности диагностики и лечения АтД в странах Европейского региона регламентирует недавно опубликованный консенсус по лечению атопической экземы (атопического дерматита) у взрослых и детей (Wollenberg А. et al., 2018). В этом согласительном документе подчеркивается высокая распространенность АтД в мире: по данным экспертов, в глобальном масштабе этой патологией страдает 20% детского и 2-8% взрослого населения.
Первоначально АтД считался исключительно педиатрической проблемой, которая возникает почти у 50% детей первого года жизни и в 95% случаев манифестирует до достижения 5-летнего возраста. Следует отметить, что некоторые педиатры все еще используют в клинической практике такие устаревшие термины, как «аллергический диатез», «экссудативно-катаральный диатез», «детская экзема», «аллергический дерматит». Вместе с тем нынешняя действительность диктует необходимость отказа от подобного обилия синонимов АтД, большей частью имеющих историческую, а не диагностическую ценность, как не соответствующих ни современным знаниям об этиопатогенетической сущности заболевания, ни насущным потребностям практической педиатрии и официальной медицинской статистики. Для устранения терминологической путаницы в настоящее время в качестве основного нозологического диагноза рекомендован термин «атопический дерматит», поскольку именно этот термин используется в отечественных нормативных документах («Уніфікований клінічний протокол первинної, вторинної, третинної медичної допомоги. Атопічний дерматит», 2016).
В настоящее время терапию АтД условно подразделяют на базисную, направленную на очищение и увлажнение кожных покровов (проведение гигиенических процедур и применение эмолентов); топическую и системную противовоспалительную. Успешность каждого вида лечения определяет эффективность терапии АтД в целом, при этом результативность топического вмешательства, по мнению европейских экспертов, обусловлена соблюдением нескольких фундаментальных принципов. Рассмотрим их подробнее.
Диагностика АтД
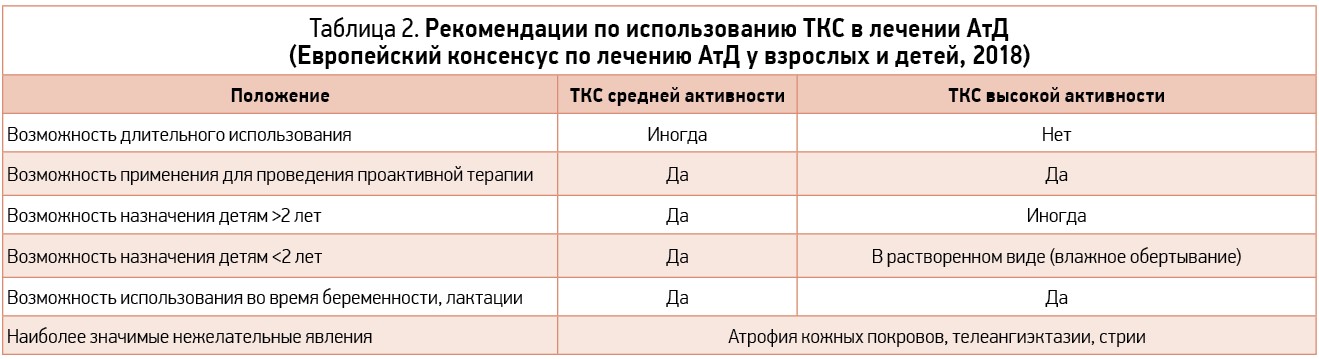
 В настоящее время не существует специфического теста для диагностики АтД, поэтому диагноз основывается на анализе имеющихся клинических проявлений и анамнестических данных. Согласно диагностическим критериям, сформулированным экспертами Американской академии дерматологии (AAD; Eichenfield L. et al., 2014), Американской академии аллергии, астмы и иммунологии (AAAAI; Schneider L. et al., 2013), основными признаками АтД являются зуд и хронические/рецидивирующие экзематозные поражения, которые имеют возрастные особенности морфологии и локализации кожных поражений (рис. 1).
В настоящее время не существует специфического теста для диагностики АтД, поэтому диагноз основывается на анализе имеющихся клинических проявлений и анамнестических данных. Согласно диагностическим критериям, сформулированным экспертами Американской академии дерматологии (AAD; Eichenfield L. et al., 2014), Американской академии аллергии, астмы и иммунологии (AAAAI; Schneider L. et al., 2013), основными признаками АтД являются зуд и хронические/рецидивирующие экзематозные поражения, которые имеют возрастные особенности морфологии и локализации кожных поражений (рис. 1).
У самых маленьких пациентов (в возрасте 3 мес – 2 года) высыпания на коже носят острый характер и локализуются преимущественно на лице, разгибательных поверхностях нижних конечностей, туловище. АтД у детей 2-12 лет характеризуется острыми и хроническими поражениями кожных покровов, которые, как правило, локализуются в сгибательных поверхностях и на коже периоральной и периорбикулярной областей. В старшей возрастной подгруппе – у подростков и взрослых (12-60 лет) – поражения кожи имеют выраженный и распространенный характер, сопровождаются лихенификацией (утолщением), экскориациями, имеют типичную локализацию (область лица, особенно периорбитальная зона, задняя поверхность шеи, сгибательные поверхности (складки), а также на кистях рук). Течение АтД у пожилых (>60 лет) сопряжено с выраженным кожным зудом, а обширные поражения кожных покровов чаще локализуются на сгибательных поверхностях.
Современная терапия АтД
Характерной особенностью двух недавно опубликованных руководств, представленных авторитетными международными обществами – AAD (2014) и Японским обществом аллергологии (2018), – а также вышеупомянутого Европейского консенсуса (2018) является полное согласие экспертов в отношении дефиниции заболевания: специалисты единодушно подчеркивают воспалительный характер повреждения кожных покровов, наличие интенсивного зуда и острых, подострых или хронических экзематозных поражений кожи. Это единодушие в определении АтД определяет сопоставимость рекомендаций относительно назначения базисной и местной противовоспалительной терапии в виде применения топических кортикостероидов (ТКС) и топических ингибиторов кальциневрина (ТИК).
Базисная терапия АтД предполагает активное использование гигиенических процедур и применение увлажняющих средств с целью улучшения защитной функции и восстановления целостности кожных покровов; при недостаточной эффективности базисных мероприятий необходимо назначение топических противовоспалительных средств – ТКС/ТИК. ТКС, препятствующие представлению антигена и высвобождению провоспалительных цитокинов в иммунных клетках, являются первой линией противовоспалительной терапии. Препаратами второй линии считаются ТИК, которые тормозят кальциневрин-зависимую активацию Т‑клеток. При неэффективности топических средств, а также при резистентном или тяжелом течении заболевания предусматривается назначение системных препаратов (иммунодепрессантов, пероральных кортикостероидов).
Положения относительно использования ТКС (Европейский консенсус по лечению АтД у взрослых и детей, 2018)
- ТКС являются важными противовоспалительными препаратами, которые используются в лечении АтД, особенно в острой фазе.
- В лечении АтД рекомендуется использовать ТКС с улучшенным профилем «польза/риск».
- Разбавленные ТКС могут использоваться для кратковременных влажных обертываний при остром АтД с целью повышения эффективности терапии.
- Проактивная терапия или двукратная аппликация противовоспалительных препаратов на протяжении 1 нед в условиях длительного динамического наблюдения может уменьшить вероятность рецидивов.
- Проактивная терапия ТКС может быть безопасной на протяжении как минимум 20 нед, что соответствует самому продолжительному периоду наблюдения в клинических исследованиях.
- Следует своевременно выявлять страх пациентов перед побочными действиями кортикостероидов (кортикофобия), адекватно корригировать его с целью повышения приверженности к лечению и предотвращения отказа от терапии.
Топическая терапия: три условия успеха
Согласно положениям Европейского консенсуса, залогом эффективности топической терапии является одновременное использование трех фундаментальных принципов: достаточная сила, достаточная доза и корректное нанесение медикаментов. Эксперты подчеркивают, что препаратами первой линии в лечении острого АтД являются ТКС.
 Характеризуя спектр ТКС, применяемых при АтД в качестве терапии первой линии, специалисты рекомендуют отдавать предпочтение препаратам средней активности в лечении АтД легкой степени тяжести и кортикостероидам высокой активности для купирования проявлений заболевания средней степени тяжести (табл. 1).
Характеризуя спектр ТКС, применяемых при АтД в качестве терапии первой линии, специалисты рекомендуют отдавать предпочтение препаратам средней активности в лечении АтД легкой степени тяжести и кортикостероидам высокой активности для купирования проявлений заболевания средней степени тяжести (табл. 1).
Следующим важным условием успеха в ведении больных АтД является достаточная доза топического препарата, которая определяется согласно правилу фаланги пальца (finger tip unit (FTU) – единица, равная кончику пальца). Количество FTU зависит от возраста пациента, тяжести течения АтД. Одна доза FTU – это такое количество мази, которое выдавливается из тубы диаметром 5 мм на дистальную ладонную поверхность указательного пальца взрослого (приблизительно 0,5 г). Одна доза FTU может покрыть две ладони взрослого (2% площади поверхности тела). Чтобы покрыть мазью все тело, необходимо 50 FTU, или 25 г.
Третьей составляющей успеха считается корректное нанесение препарата на пораженные участки кожи. Здесь подразумевается использование традиционной и проактивной терапии. Под традиционным (реактивным) способом применения топических противовоспалительных средств понимают нанесение препарата исключительно в острой фазе и только на поврежденные кожные покровы; терапию прекращают либо уменьшают частоту нанесения медикамента по мере исчезновения видимых элементов сыпи. Обновленные положения Европейского консенсуса рекомендуют отказаться от реактивного подхода, заменив его на альтернативную терапию, получившую известность под названием «проактивное лечение».
Европейские специалисты дают следующее определение проактивной терапии: «Это комбинация предварительно определенного длительного противовоспалительного лечения, при котором аппликация препаратов на ранее пораженные области кожи осуществляется, как правило, 2 раза в неделю, в сочетании с обильным использованием эмолентов на всю поверхность тела и обязательным посещением врача для клинического осмотра согласно четкому графику». Проактивный режим нанесения медикаментов стартует непосредственно после заживления всех повреждений кожи, достигнутого благодаря ежедневному применению ТКС или ТИК. Для проактивной терапии могут использоваться как ТКС, так и ТИК.
Для эффективной терапии АтД не менее важна приверженность пациентов к проводимому лечению. В ряде случаев причиной неудовлетворительного комплайенса являются некорректное применение препаратов, ограниченный доступ к необходимым медикаментам (в силу разных обстоятельств, в том числе экономических), гиперчувствительность к топической терапии, появление местных побочных действий (жжение, покалывание, зуд, боль). Поэтому критической составляющей успеха, к сожалению, не нашедшей отражения в европейских рекомендациях, является переносимость топических препаратов (Zoe D. et al., 2019).
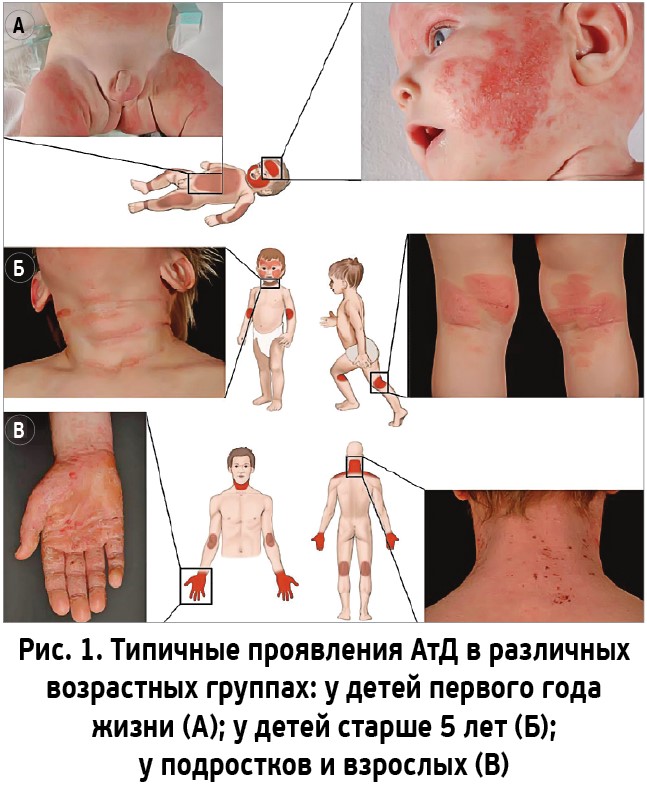
Однако европейские эксперты подчеркивают, что аппликации ТКС могут сопровождаться появлением как локальных, так и системных побочных действий. Наиболее распространенными местными побочными действиями ТКС, по данным А. Wollenberg и соавт. (2018), являются атрофия кожных покровов, телеангиэктазии, экхимозы, стрии, гипертрихоз. Использование ТКС у детей раннего возраста в области, закрываемой памперсом, может осложниться развитием гранулемы ягодичных мышц, а в ряде случаев – возникновением ятрогенного синдрома Кушинга; риск появления ТКС-индуцированных офтальмологических осложнений очень низок (табл. 2).
Ожидать возникновения системных побочных действий следует только при использовании сильных ТКС без учета возраста пациента, при превышении дозировки и частоты аппликации стероидных препаратов, длительном применении этих средств. Авторы Европейского консенсуса подчеркивают, что сильные и очень сильные кортикостероиды не рекомендуются для лечения АтД, особенно у детей. Корректное использование ТКС при условии назначения стероида адекватной силы и при четком соблюдении схемы, длительности его нанесения практически никогда не осложняется развитием системных побочных эффектов. Эксперты допускают возможность аппликации ТКС в зонах с очень тонкой, чувствительной кожей (лицо, периорбитальные участки), подчеркивая при этом, что с этой целью должны использоваться только ТКС низкой и средней активности (Wollenberg A. et al., 2018).
Ярким примером ТКС средней активности является гидрокортизона бутират, характеризующийся оптимальной переносимостью. В инструкциях к лекарственным средствам, содержащим гидрокортизона бутират, подчеркивается, что он разрешен для применения у детей старше 3 мес.
В обзоре D. Zoe и соавт. (2019) большое внимание уделяется сравнительной переносимости ТКС. Ученые приводят результаты двух исследований, выполненных под руководством Reitamo (2002, 2005). В первой работе оценивалась переносимость 3-недельной терапии 0,1% гидрокортизона бутиратом, 0,03% и 0,1% такролимусом; показан сопоставимый параметр таковой для 0,1% мази гидрокортизона бутирата и 0,1% такролимуса. Однако в более поздней работе, предполагавшей 6-месячное наблюдение за больными АтД, эти же авторы изменили свою точку зрения, сравнив частоту возникновения локальных побочных действий при использовании 0,1% гидрокортизона бутирата, 0,1% такролимуса и 1% гидрокортизона ацетата. Оказалось, что разнообразные нежелательные явления возникали чаще при аппликации ТИК, чем при нанесении ТКС, в том числе покалывание (ТКС – 0,6%; ТИК – 2,7%; р=0,02) и жжение (ТКС – 13,8%, ТИК – 52,4%; р<0,001).
В этом контексте весьма интересны результаты исследования J. Fowler и соавт. (2005), представивших мнение пациентов о переносимости различных ТКС. Особенностью этого многоцентрового рандомизированного двойного слепого исследования является нетривиальная аппликация лекарственных средств. Распределив пациентов на три группы, ученые рекомендовали участникам парную топическую терапию: на одну сторону тела наносить 0,1% мазь гидрокортизона бутирата, на другую – препарат сравнения, различный для каждой группы (0,05% крем флутиказона пропионата, 0,1% крем предникарбата, 0,1% крем мометазона фуроата). Больные получали два препарата, один из них имел маркировку «правая сторона», другой – «левая сторона»; для предотвращения перемешивания лекарственных средств во время аппликации второго препарата пациентов просили надевать новые виниловые перчатки. По истечении 2 нед терапии исследователи оценили клиническую эффективность и переносимость препаратов по мнению лечащих врачей и самих больных. Для этого на финальном визите пациентов просили заполнить опросник, в котором они сравнивали два использованных медикамента, отмечая, какой из применявшихся кремов оказывал более выраженное успокаивающее и увлажняющее действие, а также указывая лекарственное средство, оптимальное для клинического применения. По мнению врачей, все использованные ТКС имели примерно одинаковую эффективность в нивелировании кожных проявлений АтД (эритемы, трещин, чешуек, папул/везикул, зуда, жжения и уменьшения площади поражения рук), за исключением одного показателя: заживление трещин происходило значительно быстрее в группе гидрокортизона бутирата по сравнению с предникарбатом (р<0,05). Подобного мнения придерживались пациенты с АтД, считая все использованные препараты примерно одинаковыми по способности купировать симптомы заболевания (р>0,08). Однако, сравнив показатели косметической приемлемости, авторы исследования зафиксировали интересный факт: больные АтД предпочитали пользоваться кремом гидрокортизона бутирата, а не флутиказона пропионатом, предникарбатом, мометазона фуроатом. Свое мнение пациенты объясняли лучшей способностью гидрокортизона бутирата увлажнять и успокаивать кожу в месте аппликации по сравнению с другими препаратами (рис. 2). Нежелательные явления при использовании указанных ТКС развивались редко и, по мнению исследователей, не были связаны с указанной терапией.
Гидрокортизона бутират, помимо сопоставимой эффективности с другими ТКС и превосходной переносимости, обладает еще несколькими важными дополнительными преимуществами. Нанесение этого ТКС не сопровождается подавлением функциональной активности надпочечников (Eichenfield L. et al., 2007), редко ассоциируется с развитием нежелательных явлений (Abramovits W. et al., 2010), имеет оптимальный профиль «польза/риск» по сравнению с другими препаратами (Fowler J. et al., 2005).
На фармацевтическом рынке Украины гидрокортизона бутират представлен препаратом Бутикорт (ПАО «Химфармзавод «Червона Зірка»). Препарат выпускается в форме мази в тубах по 30 г. Доза гидрокортизона бутирата составляет 1 мг/г.
Принимая во внимание то, что АтД – хроническое воспалительное заболевание кожи, манифестирующее в детском возрасте, необходима эффективная топическая терапия, которая определяется тремя фундаментальными принципами:
- достаточной силой;
- достаточной дозой;
- корректным нанесением.
Оптимальным по переносимости и эффективности ТКС является 0,1% мазь гидрокортизона 17-бутирата.
Гидрокортизона бутират – препарат, характеризующийся благоприятными косметическими свойствами, комфортный и приятный для нанесения, что обеспечивает высокую приверженность к лечению и позволяет добиться оптимальных результатов терапии.
Медична газета «Здоров’я України 21 сторіччя» № 11 (456), червень 2019 р.
СТАТТІ ЗА ТЕМОЮ Дерматологія
У лютому відбувся онлайн-майстер-клас «Персоніфікація сучасної медицини. Важливі питання гендерних особливостей перебігу захворювань внутрішніх органів. Вплив психоемоційних та інших складових», організований кафедрою терапії, інфекційних хвороб і дерматовенерології Інституту післядипломної освіти Національного медичного університету ім. О.О. Богомольця (м. Київ), а також ГО «Українська академія функціональної медицини та гастропсихології» (м. Київ). ...
Щорічна захворюваність на злоякісну меланому шкіри (МШ) коливається в межах від 3-5 на 100 тисяч населення (країни Середземномор’я) до 12-35 на 100 тисяч (північні країни), тоді як в Австралії та Новій Зеландії може сягати 50 на 100 тисяч населення. Захворюваність на меланому постійно зростає впродовж останніх 40 років з тенденцією до стабілізації смертності, окрім чоловіків похилого віку. ...
Пов’язки із препаратами на основі срібла є однією з основних груп засобів, що застосовуються під час лікування інфікованих ран і ран із високим ризиком інфікування, в т. ч. опікових. Іони срібла каталізують окислення генетичного матеріалу бактеріальної клітини, що є основним механізмом їхньої бактеріостатичної та бактерицидної дії на грампозитивні й грамнегативні бактерії, а також фунгіцидного ефекту. Широкий вибір препаратів срібла, доступних на сьогодні, надає можливість підібрати засіб відповідно до потреб і вподобань пацієнта. В рекомендаціях Асоціації з науково обґрунтованого лікування ран (2020) згадуються засоби на основі іонного, металевого та нанокристалічного срібла, а також сульфату срібла й інших його солей....
Під час розгляду принципів терапії дерматологічних хворих зазвичай мається на увазі системне та зовнішнє лікування. Саме так і за таким порядком ми відзначили напрями підходу до курації хворих на дерматози з огляду на ухвалений у нас принцип послідовності терапії. Але! В європейських стандартах лікування, європейських монографіях і довідниках спочатку щодо терапії захворювань шкіри надається опис топічної терапії, а вже потім висвітлюються сучасні напрями системного підходу....