Нові можливості лікування пацієнтів з метастатичним недрібноклітинним раком легені
Останніми роками впровадження у клінічну практику таргетних та імунотерапевтичних препаратів дозволило істотно покращити результати лікування пацієнтів з метастатичним неплоскоклітинним недрібноклітинним раком легені (НДРЛ). Проте залишаються категорії хворих на НДРЛ, лікувальні можливості яких є обмеженими, – це пацієнти з мутаціями гена EGFR (кодує рецептор епідермального фактора росту), а також хворі з метастазами у печінці. Так, у пацієнтів з мутаціями EGFR застосування у 1-й лінії терапії інгібіторів тирозинкінази EGFR (ерлотиніб, гефітиніб, афатиніб) забезпечує медіану виживаності без прогресування (ВБП) 8-11 міс, проте ВБП після 2-ї і наступних ліній терапії є значно нижчою. У хворих з метастазами у печінці прогноз є значно гіршим, ніж у пацієнтів з метастазами інших локалізацій, а також відзначається погана відповідь на хіміотерапію (ХТ).
Атезолізумаб (Тецентрик®, Roche) – імунотерапевтичний препарат, що інгібує зв’язування ліганду білка програмованої клітинної смерті 1 (PD-L1) з його рецепторами PD‑1/B7.1 та відновлює пухлиноспецифічний Т-клітинний імунітет. У раніше лікованих пацієнтів з НДРЛ атезолізумаб порівняно з доцетакселом покращив загальну виживаність незалежно від експресії PD-L1. Сьогодні триває низка досліджень ефективності застосування атезолізумабу в 1-й лінії терапії НДРЛ, зокрема в комбінаціях зі стандартними схемами: карбоплатин + паклітаксел + бевацизумаб. Бевацизумаб (Авастин®, Roche) – рекомбінантне гуманізоване антитіло, яке блокує ангіогенез шляхом пригнічення судинного ендотеліального фактора росту А (VEGFA). Комбіноване застосування атезолізумабу та бевацизумабу може посилити потенціал імунної системи для боротьби з широким спектром онкологічних захворювань, включно з НДРЛ. Крім відомих антиангіогенних ефектів, бевацизумаб може потенціювати здатність атезолізумабу відновлювати протираковий імунітет, пригнічуючи VEGF-залежну імуносупресію, сприяючи інфільтрації пухлини Т-лімфоцитами й забезпечуючи первинну сенсибілізацію та активацію T-клітинної відповіді, спрямованої проти пухлинних клітин.
IMpower150 – рандомізоване клінічне дослідження III фази, метою якого було вивчити ефективність комбінації ХТ, бевацизумабу та імунотерапії в 1-й лінії лікування пацієнтів з НДРЛ. Критеріями включення були неплоскоклітинний НДРЛ IV стадії або метастатичний рецидивний НДРЛ, відсутність ХТ в анамнезі (пацієнти з активуючими мутаціями EGFR повинні були мати прогресування захворювання на тлі застосування таргетних препаратів або непереносимість одного чи кількох із них), статус експресії PD-L1 міг бути будь-яким.
У дослідженні IMpower150 пацієнтів (n=1202) рандомізували у співвідношенні 1:1:1 на три групи для лікування за схемами ABCP (атезолізумаб, бевацизумаб, карбоплатин, паклітаксел), ACP (атезолізумаб, карбоплатин, паклітаксел) або BCP (бевацизумаб, карбоплатин, паклітаксел). Індукційна терапія складалася з 4 або 6 (дослідники визначали їх кількість до рандомізації) 21-денних циклів; лікування призначали у 1-й день кожного циклу. Атезолізумаб застосовували у дозі 1200 мг, бевацизумаб – 15 мг/кг маси тіла, паклітаксел – 200 мг/м2 площі поверхні тіла (175 мг/м2 для пацієнтів азіатського походження), карбоплатин – з AUC (площа під кривою «концентрація-час») 6 мг/мл за 1 хв. Після індукційної фази пацієнти продовжували отримувати атезолізумаб, бевацизумаб або їх комбінацію до появи токсичних ефектів, які не піддалися корекції, або до прогресування захворювання.
Виявлено значне покращення ВБП і загальної виживаності (ЗВ) при додаванні атезолізумабу до бевацизумабу та ХТ незалежно від експресії PD-L1 та статусу EGFR/ALK (M.A. Socinski et al., 2018).
Нещодавно був представлений аналіз результатів лікування у підгрупах пацієнтів з мутаціями EGFR та метастазами у печінці на момент включення (M. Reck et al., 2019).
У групах ABCP, ACP та BCP позитивний статус за EGFR мали 9, 11 та 11% пацієнтів відповідно, метастази в печінці на момент включення – 13, 13 та 14% хворих.
Початкові характеристики пацієнтів з мутаціями EGFR були в цілому подібними до таких у загальній популяції дослідження. Найчастішими типами мутації були делеція екзону 19 та мутація Leu858Arg (сенситизуючі мутації); у 3 пацієнтів виявили мутацію Thr790Met.
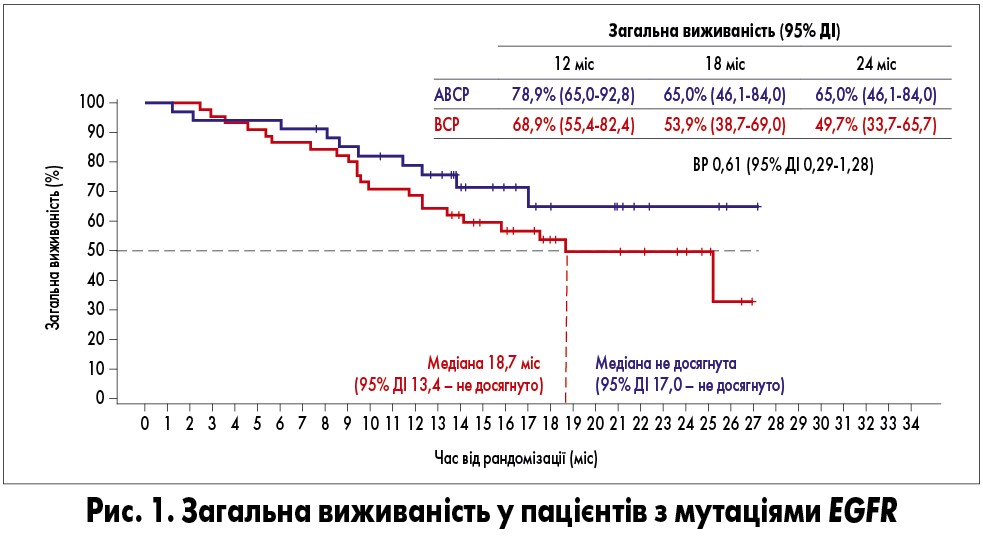
У пацієнтів з мутаціями EGFR додавання атезолізумабу до бевацизумабу та ХТ (схема ABCP) зменшувало ризик смерті на 39%. Медіана ЗВ у разі використання схеми ABCP не була досягнута, натомість при застосуванні схеми ВСР вона становила 18,7 міс (рис. 1).
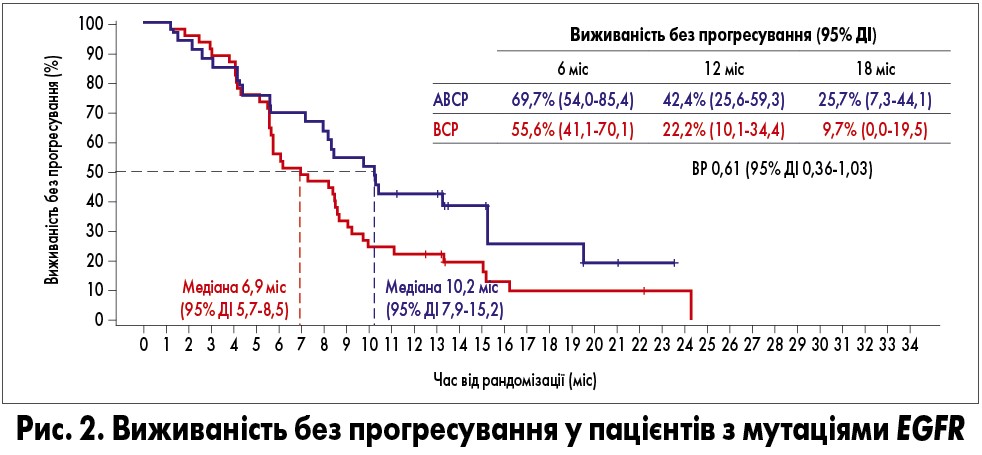
Ризик прогресування або смерті при лікуванні за схемою АВСР порівняно з ВСР знижувався на 39% в усіх EGFR-позитивних хворих, на 59% – у пацієнтів із сенситизуючими мутаціями EGFR та на 58% – у пацієнтів, які раніше отримували інгібітори тирозинкінази. Медіана ВБП становила 10,2 та 6,9 міс при використанні АВСР та ВСР відповідно (рис. 2).
Об’єктивна відповідь в EGFR-позитивній популяції була досягнута у 71% пацієнтів, яких лікували за схемою АВСР, та 42% – ВСР, медіана тривалості відповіді становила 11,1 та 4,7 міс відповідно. На момент запланованого аналізу відповідь зберігалася у 38% пацієнтів групи АВСР та у 0% хворих групи ВСР. Варто зазначити, що результати застосування схеми АВСР у пацієнтів з мутаціями EGFR не були зумовлені високою експресію PD-L1.
Медіана ЗВ для EGFR-позитивних пацієнтів у групах ACP та BCP становила 21,4 vs 18,7 міс, медіана ВБП в обох групах – 6,9 міс.
Покращення ЗВ при застосуванні схеми АВСР порівняно з ВСР спостерігалося у пацієнтів з різними демографічними та початковими клінічними характеристиками, зокрема у чоловіків (відносний ризик – ВР – 0,73) та у пацієнтів віком від 65 до 74 років (ВР 0,69).
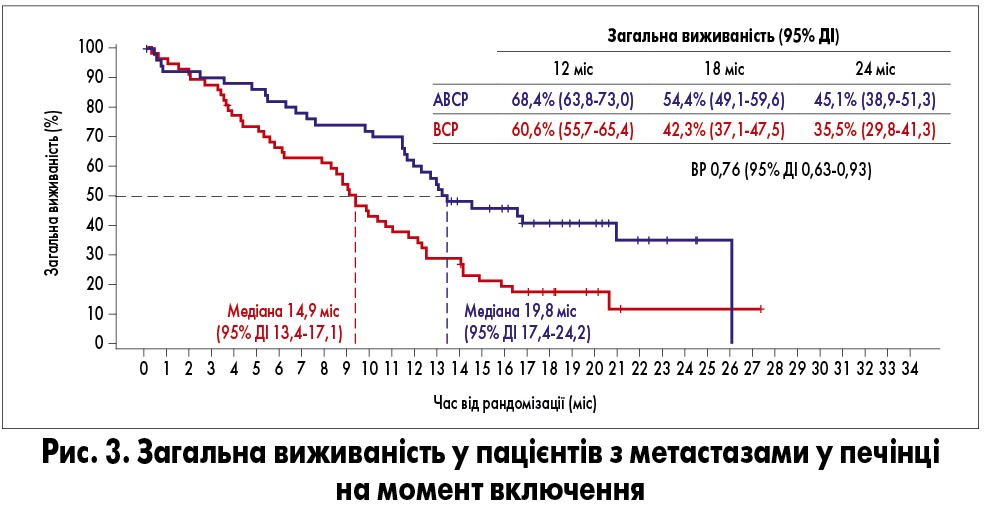
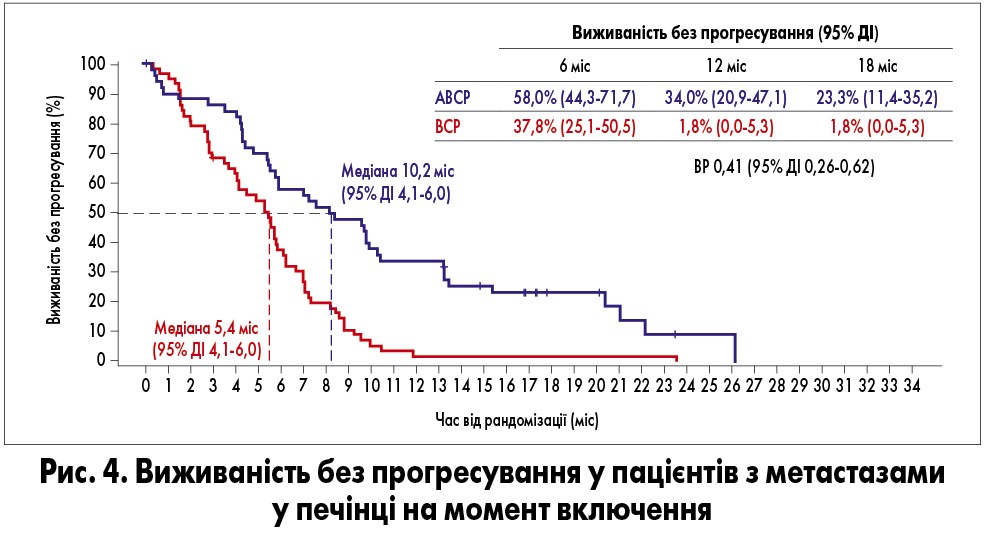
Метастази в печінці на момент включення були присутні у 52 з 400 пацієнтів групи АВСР та у 57 з 400 хворих групи ВСР. У цій популяції застосування схеми АВСР значно покращило ЗВ (медіана 13,3 vs 9,4 міс для ВСР; ВР 0,52) та ВБП (медіана 8,2 vs 5,4 міс для ВСР; ВР 0,41), а також частоту об’єктивної відповіді (61 vs 41%) та її тривалість (10,7 vs 4,6 міс). Як і в EGFR-позитивній популяції, у пацієнтів з метастазами в печінці вища ефективність схеми АВСР відзначалася в усіх демографічних і клінічних групах, зокрема в усіх підгрупах з експресією PD-L1 (рис. 3, 4).
Застосування схеми АСР порівняно з ВСР у пацієнтів з метастазами в печінці не покращувало ЗВ та ВБП.
***
Таким чином, у пацієнтів з метастатичним неплоскоклітинним НДРЛ, які мають мутації EGFR та/або метастази у печінці, додавання атезолізумабу до бевацизумабу та ХТ (схема АВСР) значно покращувало ЗВ, ВБП, частоту і тривалість об’єктивної відповіді. Порівняно із загальною популяцією дослідження у цих категорій хворих рідше визначалася експресія PD‑L1, отже, переваги схеми АВСР щодо виживаності не були зумовлені високою експресією PD-L1.
Відомо, що у пацієнтів зі змінами EGFR/ALK відзначається знижена інфільтрація пухлини CD8+ Т-лімфоцитами до і після лікування інгібіторами тирозинкінази. Бевацизумаб нормалізує судинну сітку пухлини і збільшує інфільтрацію пухлини Т-лімфоцитами, тому лікування EGFR‑позитивних пацієнтів бевацизумабом може підвищувати їх чутливість до інгібіторів контрольних точок (атезолізумабу). Крім того, оскільки сигнальний шлях EGFR стимулює експресію VEGF у пухлинах, пацієнти з мутаціями EGFR можуть бути більш чутливими до лікування бевацизумабом.
Гепатоцелюлярна карцинома асоціюється із гіпоксичним станом пухлини, високою експресією VEGF і посиленим ангіогенезом, що може сприяти індукції імуносупресивних клітин і розвитку імунотолерантності. Відповідь на лікування метастазів раку легені у печінці більше схожа на таку гепатоцелюлярної карциноми. У попередніх дослідженнях додавання бевацизумабу до карбоплатину й паклітакселу покращувало ЗВ у пацієнтів з метастазами в печінці. Однак у пацієнтів з метастазами НДРЛ у печінці візначається погана відповідь на монотерапію інгібіторами контрольних точок. Висока ефективність схеми АВСР в учасників дослідження IMpower150 з метастазами в печінці свідчить, що бевацизумаб може сприяти відновленню чутливості печінкових метастазів НДРЛ до імунотерапії.
За матеріалами статті: Reck M., Mok T.S.K., Nishio M. et al. Atezolizumab plus bevacizumab and chemotherapy in non-small-cell lung cancer (IMpower150): key subgroup analyses of patients with EGFR mutations or baseline liver metastases in a randomised, open-label phase 3 trial. Lancet Respir Med 2019. Published Online March 25, 2019.
Підготував Олексій Терещенко
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 2 (58), 2019 р
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...