Ефективність препарату Новірин у дітей із вірусними діареями

У світі щороку серед дітей перших 5 років життя реєструється близько 1,4 мільярда випадків гострих кишкових інфекцій (ГКІ), серед яких 1,87 мільйонів закінчується летально [3, 19]. В Європі на кожну дитину раннього віку припадає 0,5-1,9 епізодів інфекційних діарей [7]. В Україні щорічно реєструється 50-60 тисяч випадків гострих інфекційних діарей у дітей [21].
Більшість (понад 65%) гострих кишкових інфекцій у країнах Європи мають вірусну етіологію. До найбільш поширених збудників кишкових інфекцій належать ротавіруси, які спричинюють гострі кишкові інфекції у 10-35% випадків, норовіруси (у 2-20%), аденовіруси (у 2-10%) [7,16, 19].
Основними напрямами лікування гострих кишкових інфекцій вірусної етіології є застосування регідратації та засобів симптоматичної терапії [7]. Проте існує багато публікацій щодо позитивного впливу препаратів із противірусною активністю на перебіг вірусних діарей. Зокрема відзначено скорочення тривалості діареї на фоні застосування таких препаратів, як комплексний імуноглобуліновий препарат (КІП), кіпферон (КІП та інтерферон), арбідол (уміфеновір), циклоферон, гепон та інші [22].
Останніми роками при лікуванні захворювань вірусної етіології у дітей успішно використовується інозин пранобекс, противірусний засіб із імуномодулювальними властивостями.
Інозин пранобекс стимулює диференціювання Т-лімфоцитів у популяції цитотоксичних Т-клітин (CD8+) та Т-хелперів (CD4). Водночас препарат сприяє дозріванню плазматичних клітин, які продукують антитіла, і, таким чином, активує гуморальний імунітет [2, 17]. Окрім того, що інозин активує імунокомпетентні клітини, він має пряму противірусну дію. Внаслідок вбудовування інозиноротової кислоти до рибосом ураженої вірусом клітини порушується реплікація вірусної нуклеїнової кислоти [15]. Так, у дослідах in vitro було продемонстровано ефективність препарату при лікуванні ротавірусної інфекції [14]. Окрім того, інозин проявляє протизапальну дію, блокуючи продукцію таких прозапальних цитокінів, як фактор некрозу пухлин α та інтерлейкін 1β [20].
Натепер накопичено значний досвід використання інозину пранобексу при різних захворюваннях вірусної природи. Зокрема, препарат проявив свою ефективність як засіб для профілактики та лікування при гострих респіраторних інфекціях, при терапії підгострого склерозуючого паненцефаліту, цервікальних кондилом, гострого міозиту, вогнищевої алопеції, герпетичної та ВІЛ-інфекції [1, 4-6, 8-13, 18].
Мета клінічного спостереження: оцінка ефективності препарату Новірин (інозин пранобекс) при лікуванні вірусних діарей у дітей.
Матеріал та методи
До клінічного спостереження залучалися діти віком від 1 до 18 років, які проходили стаціонарне лікування на клінічній базі кафедри дитячих інфекційних хвороб Національного медичного університету імені О.О. Богомольця.
Критерії включення:
- гостра кишкова інфекція з підтвердженою вірусною етіологією;
- згода пацієнта та батьків на участь у спостереженні.
Критерії виключення:
- тривалість діареї більше 3 діб до моменту госпіталізації;
- наявність хронічної патології, яка може вплинути на тривалість клінічних симптомів, що вивчаються;
- непереносимість інозину пранобексу.
До спостереження було залучено 60 дітей: 30 пацієнтів увійшли до групи А, в якій отримували стандартну терапію та препарат Новірин; 30 хворих, які отримували тільки стандартну терапію, становили групу Б. Вікову та гендерну структуру груп пацієнтів представлено в таблиці 1.
Таблиця 1. Вікова та гендерна структура груп пацієнтів
|
Група |
Стать, абсолютна кількість пацієнтів (%) |
Вік (роки), медіана (мінімум-максимум) |
|
|
Чоловіча |
Жіноча |
||
|
А (n = 30) |
19 (63,3) |
11 (36,7) |
1,10 (1,0-14,0) |
|
Б (n = 30) |
17 (56,7) |
13 (43,3) |
1,11 (1,02-11,0) |
|
Всього |
36 (60,0) |
24 (40,0) |
1,11 (1,0-14,0) |
|
Примітка. n – кількість пацієнтів у групах. |
|||
Серед обстежених пацієнтів в обох групах переважали хлопчики. Вік хворих був від 12 місяців до 14 років. За віком та статтю різниця між групами А та Б недостовірна (p > 0,05 за критерієм хі-квадрат Пірсона).
До спостереження залучалися пацієнти, тривалість захворювання яких на момент госпіталізації не перевищувала 3 діб. Більшість хворих була госпіталізована протягом першої доби захворювання (73,3%). Діти, госпіталізовані протягом третьої доби, становили всього 3,3%. Суттєвої різниці між групами з різними методами терапії за кількістю днів госпіталізації не відзначалося (p > 0,05 за критерієм хі-квадрат Пірсона).
Результати та їх обговорення
У всіх хворих (100%), які були залучені до спостереження, тяжкість захворювання оцінювалася як середня.
Етіологічну розшифровку проведено за допомогою експрес-тестів CITO TEST ROTA-ADENO для визначення антигенів рота- і аденовірусної інфекцій (фекалії), виробництва ТОВ «Фармаско» (табл. 2). В етіологічній структурі переважав ротавірус (63,3%), дещо рідше – норовірус (25%) та аденовірус (5%). У 6,7% дітей спостерігалася мікст-інфекція. Суттєвої різниці за етіологічною структурою захворювань між групами А та Б не відзначалося (p > 0,05 за критерієм хі-квадрат Пірсона).
Таблиця 2. Етіологічна структура захворювань
|
Етіологічний чинник |
Група А |
Група Б |
Всього |
|
Абсолютна кількість пацієнтів (%) |
|||
|
Ротавірус |
20 (66,7) |
18 (60,0) |
38 (63,3) |
|
Аденовірус |
2 (6,7) |
1 (3,3) |
3 (5,0) |
|
Норовірус |
7 (23,3) |
8 (26,7) |
15 (25,0) |
|
Ротавірус + аденовірус |
1 (3,3) |
0 (0) |
1 (1,7) |
|
Ротавірус + норовірус |
0 (0) |
3 (10,0) |
3 (5,0) |
|
Всього |
30 (100) |
30 (100) |
60 (100) |
Основні клінічні симптоми захворювання представлено в таблиці 3. Прояви інтоксикації спостерігалися у всіх пацієнтів на початку спостереження. Симптоми включали зміни поведінки (млявість, вередливість) та зниження апетиту.
Таблиця 3. Частота основних клінічних симптомів в різних етіологічних групах хворих
|
Етіологія |
Симптоми інтоксикації |
Лихоманка |
Блювання |
Діарея |
|
Абсолютна кількість пацієнтів (%) |
||||
|
Ротавірус (n = 38) |
38 (100,0) |
32 (84,2)* |
14 (36,8)* |
38 (100,0) |
|
Аденовірус (n = 3) |
3 (100,0) |
3 (100,0) |
3 (100,0) |
3 (100,0) |
|
Норовірус (n = 15) |
15 (100,0) |
6 (40,0)* |
13 (86,7)* |
15 (100,0) |
|
Ротавірус + аденовірус (n = 1) |
1 (100,0) |
1 (100,0) |
0 (0) |
1 (100,0) |
|
Ротавірус + норовірус (n = 3) |
3 (100,0) |
3 (100,0) |
0 (0) |
3 (100,0) |
|
Всього (n = 60) |
60 (100) |
44 (73,3) |
28 (46,7) |
60 (100) |
|
Примітки: n – кількість пацієнтів у групах. * Різниця достовірна між групами «Ротавірус» та «Норовірус» (p < 0,05 за точним критерієм Фішера). |
||||
Діарея у всіх пацієнтів мала секреторний характер. Випорожнення були водянистими, інколи з домішками прозорого слизу. Домішки крові в жодному випадку не виявлялися. Частота випорожнень майже в половині випадків (49,3%) не перевищувала 5 епізодів на добу; у 37,1% становила 6-10 епізодів на добу, у 13,6% – понад 10 дефекацій на добу.
Лихоманка спостерігалася у 73,3% хворих. Серед хворих з лихоманкою у більшості пацієнтів (65,9%) температура тіла коливалася в межах субфебрильних цифр (37,0-38,5 °С); у 34,1% дітей спостерігалося підвищення до фебрильних цифр (> 38,5 °С). Частіше цей симптом спостерігався при ротавірусній та аденовірусній етіології захворювання (у 84,2 і 100% випадків відповідно) і лише у 40,0% пацієнтів із норовірусною етіологією (різниця між групами з ротавірусною та норовірусною інфекціями достовірна, p < 0,05).
Блювання відзначалося майже у половини (46,7%) обстежених хворих. У більшості випадків (60,6%) це було одно-дворазове блювання. У 27,3% випадків блювання було повторним, з кількістю епізодів 3-5 на добу; у 12,1% – понад 5 епізодів на добу. Симптом виявлявся в усіх етіологічних групах хворих, окрім груп змішаної етіології з незначною кількістю пацієнтів (ротавірус + аденовірус, ротавірус + норовірус). Достовірно частіше блювання спостерігалося у пацієнтів із норовірусною етіологією захворювання (86,7%), ніж при ротавірусній етіології (36,8%) (p < 0,05 за точним критерієм Фішера). Між іншими групами достовірної різниці не відзначалося.
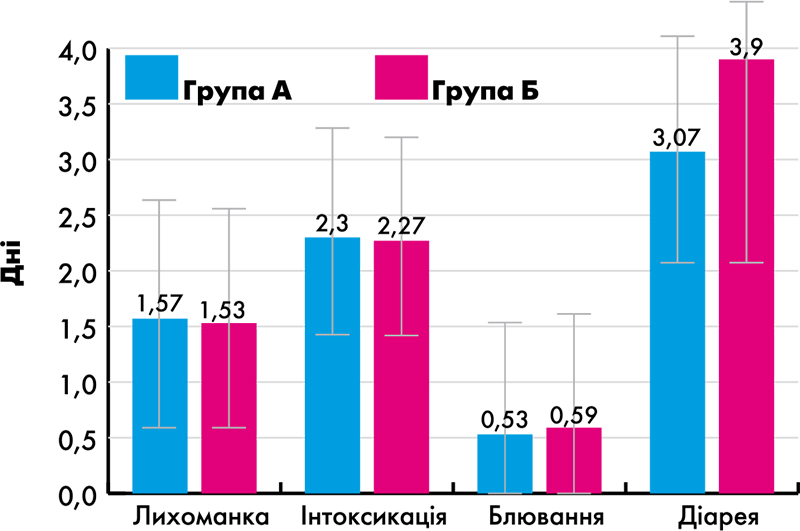
У всіх (100%) пацієнтів, які були залучені до спостереження, на фоні лікування спостерігалася позитивна динаміка захворювання і всі були виписані зі стаціонару у задовільному стані. Тривалість основних симптомів захворювання представлено на рисунку 1.
Тривалість лихоманки в середньому становила 1,55 дня. Вона суттєво не відрізнялася у групах з різними методами терапії (p > 0,05 за критерієм Манна-Вітні). Інтоксикаційні прояви тривали в середньому 2,28 доби і суттєво не відрізнялися між групами з різними методами терапії (p > 0,05). Середня тривалість блювання для загальної сукупності хворих становила 0,55 дня. Суттєвої різниці між групами з різними методами терапії не відзначалося (p > 0,05). Діарейний синдром у середньому спостерігався протягом 3,58 дня. На 0,83 доби меншою була тривалість діареї у групі дітей, які отримували в комплексній терапії препарат Новірин (p = 0,008 за критерієм Манна-Вітні).
Динаміку основних клінічних симптомів захворювання при різних методах терапії представлено в таблиці 4.
Таблиця 4. Динаміка частоти клінічних симптомів у групах з різними методами терапії
|
Група |
День спостереження |
||||
|
1 |
2 |
3 |
4 |
5 |
|
|
Абсолютна кількість пацієнтів (%) |
|||||
|
Лихоманка |
|||||
|
А |
21 (70,0) |
14 (46,7) |
6 (20,0) |
4 (13,3) |
0 (0) |
|
Б |
18 (60,0) |
19 (63,3) |
5 (16,7) |
1 (3,3) |
0 (0) |
|
Блювання |
|||||
|
А |
14 (46,7) |
2 (6,7) |
0 (0) |
0 (0) |
0 (0) |
|
Б |
12 (40,0) |
3 (10,0) |
2 (6,7) |
0 (0) |
0 (0) |
|
Діарея |
|||||
|
А |
30 (100) |
29 (96,7) |
23 (76,7) |
15 (50,0) |
6 (20,0)* |
|
Б |
30 (100) |
28 (93,3) |
27 (90,0) |
21 (70,0) |
17 (56, )* |
|
Примітки: кількість пацієнтів у групі А = 30, у групі Б = 30. * Різниця достовірна між групами A та Б (p < 0,05 за критерієм хі-квадрат). |
|||||
Лихоманка на момент госпіталізації спостерігалася у 70% дітей групи А та у 60% – групи Б (p > 0,05 за критерієм хі-квадрат Пірсона). Динаміка нормалізації температури тіла в обох групах була схожою. Вже на третю добу перебування у стаціонарі підвищена температура тіла відзначалася лише у 20% хворих групи А та у 16,7% групи Б (p > 0,05 за критерієм хі-квадрат Пірсона). На 5-у добу спостереження у всіх пацієнтів реєструвалася нормальна температура тіла.
Блювання на момент госпіталізації спостерігалося у 46,7% дітей групи А та у 40% групи Б (p > 0,05 за критерієм хі-квадрат Пірсона). На третю добу спостереження в жодного пацієнта групи А блювання не повторювалося, в групі Б у двох дітей були наявні епізоди блювання. Після третього дня в обох групах цей симптом не спостерігався.
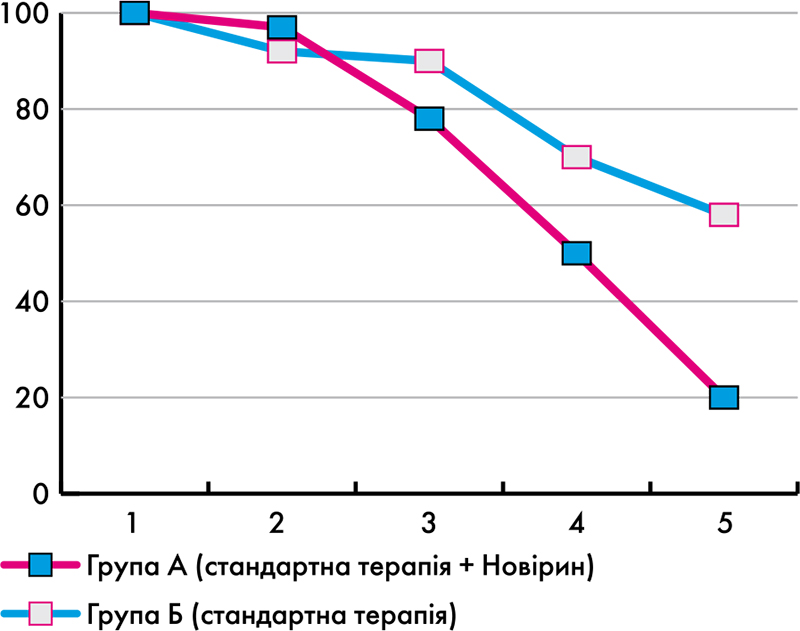
Діарея на момент госпіталізації спостерігалася у всіх (100%) пацієнтів, які були залучені до спостереження (див. табл. 3, рис. 2). З часом зменшення відсотку пацієнтів з діареєю інтенсивніше відбувалося у групі А. Так, на 3-й день спостереження їх частка у групі А становила 76,7%, у групі Б – 90%; на 4-й день 50 та 70% відповідно; на 5-й день 20 та 56,7% відповідно. Різниця на 5-й день спостереження була достовірною (p < 0,05 за критерієм хі-квадрат).
При застосуванні препарату Новірин у комплексній терапії жодного побічного явища виявлено не було. За результатами дослідження, препарат Новірин переносився добре.
Висновки
1. У рамках дослідження в етіологічній структурі вірусних діарей у дітей переважали рота- та норовірус (63,3 та 25,0% випадків відповідно).
2. Призначення препарату Новірин дало змогу припинити діарею в перші 5 днів від початку лікування у достовірно більшої кількості дітей (80%), ніж у контрольній групі (43%).
3. Препарат Новірин добре переносився хворими, жодних побічних реакцій при його застосуванні не було зареєстровано.
4. Експрес-тести на вірусні антигени збудників кишкових інфекцій дали змогу швидко встановити етіологічний діагноз та визначити оптимальну лікувальну тактику.
Література
1. Anlar B. Subacute sclerosing panencephalitis and chronic viral encephalitis. Handb Clin Neurol. 2013; 112: 1183-9. doi:10.1016/B978-0-444-52910-7.00039-8
2. Aronson J.K. Meyler’s. Side Effects of Antimicrobial Drugs. Elsevier; 2010. Available at: https://books.google.com.ua/books?id=aYh5NwAACAAJ
3. Black R.E., Cousens S., Johnson H.L. et al. Global, regional, and national causes of child mortality in 2008: a systematic analysis. Lancet. 2010; 375 (9730): 1969-87. doi:10.1016/S0140-6736(10)60549-1
4. Georgala S., Katoulis A.C., Befon A., Georgala C., Rigopoulos D. Oral inosiplex in the treatment of cervical condylomata acuminata: a randomised placebo-controlled trial. BJOG. 2006; 113 (9): 1088-91. doi:10.1111/j.1471-0528.2006.01041.x
5. Georgala S., Katoulis A.C., Befon A., Georgala K., Stavropoulos P.G. Inosiplex for treatment of alopecia areata: a randomized placebo-controlled study. Acta Derm Venereol. 2006; 86 (5): 422-4. doi:10.2340/00015555-0138
6. Golebiowska-Wawrzyniak M., Markiewicz K., Kozar A., et al. Immunological and clinical study on therapeutic efficacy of inosine pranobex. Pol Merkur Lekarski. 2005; 19 (111): 379-382.
7. Guarino A., Ashkenazi S., Gendrel D., Lo Vecchio A., Shamir R., Szajewska H. ESPGHAN/ESPID Evidence-based Guidelines for the Management of Acute Gastroenteritis in Children in Europe: Update 2014. J Pediatr Gastroenterol Nutr. 2014; 39 (1): 132-152. doi:10.1097/MPG.0000000000000375
8. Gutierrez J., Issacson R.S., Koppel B.S. Subacute sclerosing panencephalitis: an update. Dev Med Child Neurol. 2010; 52 (10): 901-7. doi:10.1111/j.1469-8749.2010.03717.x
9. Harukawa H., Yuasa T. Progress of the therapy for virus related neurological disorders. Nihon Rinsho. 1997; 55 (4): 959-66. Available at: http://www.ncbi.nlm.nih.gov/pubmed/9103902. Accessed February 8, 2015.
10. Hosoya M. Anti SSPE drugs. Nihon Rinsho. 2012; 70 (4): 625-8. Available at: http://www.ncbi.nlm.nih.gov/pubmed/22568144. Accessed February 8, 2015.
11. Hosoya M. Subacute sclerosing panencephalitis (SSPE). Rinsho Shinkeigaku. 2011; 51 (11): 1047-50. Available at: http://www.ncbi.nlm.nih.gov/pubmed/22277474. Accessed February 8, 2015.
12. Hozyasz K.K., Gryglicka H, Radomyska B. Benign acute childhood myositis (BACM)-cases report. Pol Merkur Lekarski. 2009; 27 (158): 129-31. Available at: http://www.ncbi.nlm.nih.gov/pubmed/19856879. Accessed February 8, 2015.
13. Iakupova R.S., Skachkova M.A., Choloian S.B., Karpova E.G. Efficacy of immunomodulators in children with respiratory diseases in environmentally poor areas. Gig Sanit. 2012; (3): 33-4. Available at: http://www.ncbi.nlm.nih.gov/pubmed/23088120. Accessed February 8, 2015.
14. Linhares R.E.C., Rebelle M.A., Nozawa C.M. Effect of isoprinosine on rotavirus replication in vitro. Brazilian J Med Biol Res. 1996; 29: 219-222.
15. Ohnishi H., Kosuzume H., Inaba H., Ohkura M., Shimada S., Suzuki Y. The immunomodulatory action of inosiplex in relation to its effects in experimental viral infections. Int J Immunopharmacol. 1983; 5 (3): 181-96. Available at: http://www.ncbi.nlm.nih.gov/pubmed/6194125. Accessed February 8, 2015.
16. Orbuch M. Diarrheal Diseases. Gastroenterol Nurs. 1992; 14: 316. doi:10.1097/00001610-199206000-00011
17. Stenzel T., Tykalowski B., Smialek M., Koncicki A., Kwiatkowska-Stenzel A. The effect of different doses of methisoprinol on the percentage of CD4+ and CD8+ T lymphocyte subpopulation and the antibody titers in pigeons immunised against PPMV-1. Pol J Vet Sci. 2011; 14 (3): 367-71. Available at: http://www.ncbi.nlm.nih.gov/pubmed/21957729. Accessed February 8, 2015.
18. Thorsen S., Pedersen C., Sandstrоm E. et al. [Controlled, clinical trial of isoprinosine administration to HIV-infected patients. Results of a Danish/Swedish multicenter study. The Scandinavian Isoprinosine Study Group]. Ugeskr Laeger. 1994;156(22):3314-8. Available at: http://www.ncbi.nlm.nih.gov/pubmed/7520643. Accessed February 8, 2015.
19. WHO. Diarrhoeal disease. Available at: http://www.who.int/mediacentre/factsheets/fs330/en/. Accessed December 28, 2014.
20. Леваков С.А., Кедрова А.Г., Кажурина Е.В, Ванке Н.С. Синтетические аналоги инозина в современном лечении фоновых и предраковых заболеваний шейки матки // Клиническая практика. – 2010 – № 3. – С. 43-50.
21. Підручник: Інфекційні хвороби в дітей / С.О. Крамарьова, О.Б. Надрага, Л.В. Пипа [та ін.] / За ред. проф. С.О. Крамарьова, О.Б. Надраги. – К.: Медицина. – 2010, С. 392.
22. Учайкин В.Ф., Новокшонов А.А., Соколова Н.В. Этиопатогенетическая терапия острых кишечных инфекций у детей на современном этапе / Лечащий врач. – 2010. – № 1. – С. 7-13.




