Билиарный сладж и УДХК: грани патогенетической сопряженности и терапии
 Билиарный сладж (БС) среди лиц с наличием жалоб со стороны органов желудочно-кишечного тракта встречается у 7,5%, при билиарной диспепсии частота его достигает 24-74%, чаще встречается у женщин (59%), чем у мужчин (41%). При естественном течении БС в 8-20% случаев происходит формирование конкрементов в желчном пузыре (ЖП), а в 18-70% их спонтанное исчезновение [5, 6, 9, 16].
Билиарный сладж (БС) среди лиц с наличием жалоб со стороны органов желудочно-кишечного тракта встречается у 7,5%, при билиарной диспепсии частота его достигает 24-74%, чаще встречается у женщин (59%), чем у мужчин (41%). При естественном течении БС в 8-20% случаев происходит формирование конкрементов в желчном пузыре (ЖП), а в 18-70% их спонтанное исчезновение [5, 6, 9, 16].
Следует отметить, что в повседневной работе врачи не всегда своевременно и адекватно оценивают значение БС как начальной стадии желчнокаменной болезни (ЖКБ) и не рекомендуют пациентам соответствующий превентивный алгоритм обследования и лечения, что приводит к прогрессированию заболевания. Отсутствие четкой оценки БС обусловливает неоднозначность его клинической интерпретации – от транзиторного состояния, не требующего патогенетического лечения (о чем свидетельствует самостоятельное исчезновение сладжа у 70% больных), до трансформации в желчные конкременты у 32% пациентов как начальной стадии ЖКБ [1].
БС представляет собой суспензию жидких кристаллов моногидрата холестерина и/или гранул кальция билирубината в смеси муцина и белка. Суспензия сладжа включает различные по ультразвуковой и физико-химической характеристике структуры размером от 0,01 до 5 мм, при этом химический состав сладжа варьируется в различных клинических ситуациях. При различных физиологических и патофизиологических отклонениях в организме человека частота встречаемости БС вариабельна. Во время беременности из-за увеличения уровня эстрогенов и прогестинов сладж обнаруживается у 31% женщин, при быстром снижении массы тела, из-за повышения уровня холестерина в желчи и снижения скорости опорожнения ЖП БС наблюдается в 25% случаев.
Возможны 3 варианта течения БС: спонтанное разрешение (исчезновение), персистирование и эволюция в желчные камни. У больных с абдоминальной болью БС исчезал и не рецидивировал (по крайней мере в течение 2 лет) в 17,7% случаев, исчезал и рецидивировал в 60,4% случаев, а у 8,3% наблюдалась эволюция в бессимптомную ЖКБ. P. Janowitz и соавт. (1994) при наблюдении за пациентами с БС в течение 20 мес отмечали полное исчезновение сладжа в 71,0% случаев, формирование желчных камней в 12,5% случаев, у остальных пациентов наблюдалось персистирование БС, в 9,1% случаев у пациентов наблюдались эпизоды желчной колики [21].
Среди причин, способствующих формированию БС, выделяют основные группы факторов риска, которые встречаются и при ЖКБ. Генетические факторы включают семейную предрасположенность, аномалии развития ЖП и билиарного тракта, ферментативные дефекты синтеза солюбилизаторов желчи. Фундаментальные исследования молекулярной биологии синтеза желчных кислот в последнее десятилетие привели к недавнему выявлению рецепторов желчных кислот и мутаций ключевых генов биосинтеза желчных кислот у пациентов с заболеваниями печени и сердечно-сосудистыми заболеваниями. Исследования последних лет убедительно доказывают, что формирование осадка в ЖП является процессом, генетически детерминированным.
В настоящее время точно установлено, что FXR (фарнезоидный рецептор) и LXRα координируют синтез желчных кислот и гомеостаз холестерина в печени, кишечнике, периферических тканях и макрофагах. FXR функционирует для поддержания низких концентраций желчных кислот в гепатоцитах. Возможно, что дефицит синтеза желчных кислот нарушит гомеостаз холестерина и приведет к гиперхолестеринемии и сердечно-сосудистым заболеваниям.
Демографические факторы – женский пол, возраст, географическая зона проживания. Диетические факторы включают пищу, обедненную растительными волокнами, с избыточным содержанием углеводов и жиров, низкокалорийные диеты с редукцией массы тела. Медицинские факторы развития БС более многочисленны, наиболее значимыми являются ожирение, сахарный диабет, заболевания печени, воспалительные заболевания кишечника, парентеральное питание, нарушение моторики тонкой кишки, инфекции билиарного тракта, прием некоторых медикаментов (цефтриаксон, октреотид, клофибрат, препараты кальция, диуретики, контрацептивные средства), а также оперативные вмешательства – гастрэктомия, приводящая к нарушению иннервации ЖП и, как следствие, к снижению его сократительной функции, папиллосфинктеротомия, правосторонняя гемиколэктомия.
При беременности и приеме гормональных контрацептивов повышенный уровень эстрогенов крови приводит к увеличению секреции холестерина, нарушению биохимического состава желчи. Повышение уровня прогестерона вызывает релаксацию гладких мышц и гипотонию ЖП. После родов БС спонтанно исчезает у 60-80% женщин в течение 5-6 мес.
Голодание, соблюдение низкокалорийных диет, парентеральное питание способствуют снижению моторики ЖП, стазу желчи, повышению тонуса сфинктера Одди (СО). В связи с этим ограничивается поступление желчи в двенадцатиперстную кишку (ДПК) и нарушается пищеварение (преимущественно переваривание жиров). После восстановления нормального приема пищи сладж исчезает практически у всех пациентов через 4 нед.
Основные этапы патогенеза БС включают образование везикул с избыточным содержанием холестерина на фоне увеличения концентрации литогенных желчных кислот и снижения уровня хенодезоксихолевой кислоты. Одной из причин развития БС является нуклеация перенасыщенной желчи, которая стимулируется повышением концентрации кальция, меди, марганца, железа, магния, калия.
В развитии БС большое значение имеют увеличение содержания в желчи сиаловых кислот, гексоз и накопление продуктов перекисного окисления липидов. Персистенция БC обусловлена снижением клиренса из-за подавления сократительной способности ЖП, что провоцируется уже имеющимся сладжем в ЖП.
Важным патогенетическим фактором является перенасыщение желчи холестерином в результате нарушения сложных биохимических процессов, главным из которых является повышение активности ГМГ-КоА‑редуктазы, ведущее к увеличению синтеза холестерина, или снижение активности холестерин‑7α-гидроксилазы, сопровождающееся уменьшением синтеза желчных кислот. Эти два фактора являются ключевыми в пусковом механизме формирования холестериновых камней. При сохраненной сократительной активности ЖП агломерировавшие частицы эвакуируются в ДПК.
Гипотония ЖП, как и гипертонус СО, способствуют формированию и прогрессированию БС. Этому же способствует дисфункция СО и ЖП, в основе которой лежат воспалительные процессы в желудке и ДПК, нередко сопровождающиеся дуоденостазом. Имеются данные о прямом воздействии холестерина на сакролемму миоцита, приводящем к снижению сократительной функции ЖП [2]. Важную роль в развитии БС играет нарушение энтерогепатической циркуляции желчных кислот.
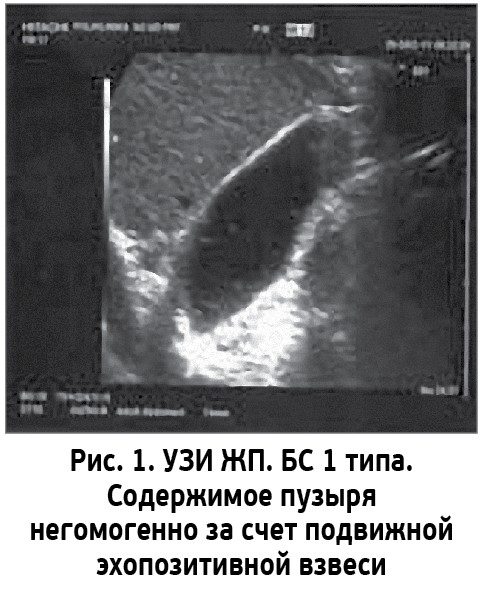 В связи с внедрением в клинику ультразвукового метода исследования выделяют 3 основных типа БС, которые имеют наиболее характерную эхографическую картину (рис. 1-4) [2]:
В связи с внедрением в клинику ультразвукового метода исследования выделяют 3 основных типа БС, которые имеют наиболее характерную эхографическую картину (рис. 1-4) [2]:
- 1 тип (микролитиаз) – взвесь гиперэхогенных частиц в виде точечных, единичных или множественных смещаемых образований размером до 4-5 мм, не дающих акустической тени, выявляемых после изменения положения тела пациента;
- 2 тип – наличие слабоподвижного уровня замазкообразной (эхопозитивной) желчи: расслоение желчи на эхонегативную и эхопозитивную (замазкообразную) фракции с наличием сгустков различной плотности, смещаемых, не дающих акустической тени или, в редких случаях, с эффектом ослабления за сгустком;
- 3 тип – замазкообразная желчь в виде подвижных и/или фиксированных сгустков без акустической тени в сочетании с микролитами.
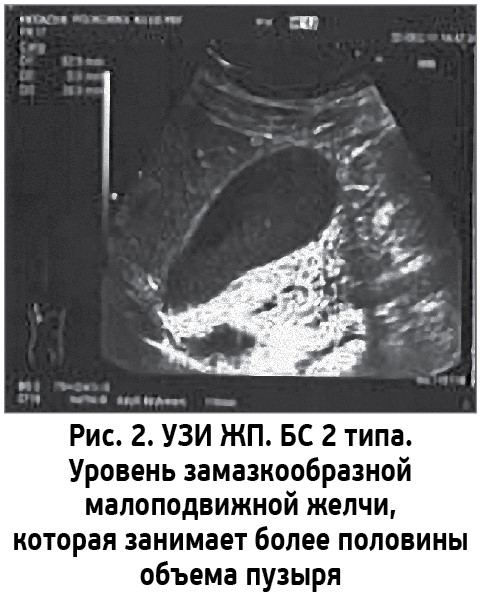 Эти типы определяют давность и динамику образования осадка. Самостоятельной клинической картины БС не имеет. Основное число случаев выявления БС приходится на случайные ультразвуковые находки у бессимптомных пациентов. В клинической практике чаще всего встречается 1 тип БС в виде взвеси гиперэхогенных частиц (около 70%), тогда как частота обнаружения двух других составляет около 10-12% [9].
Эти типы определяют давность и динамику образования осадка. Самостоятельной клинической картины БС не имеет. Основное число случаев выявления БС приходится на случайные ультразвуковые находки у бессимптомных пациентов. В клинической практике чаще всего встречается 1 тип БС в виде взвеси гиперэхогенных частиц (около 70%), тогда как частота обнаружения двух других составляет около 10-12% [9].
Из причисляемых для данного состояния симптомов – боли, горечи во рту, тошноты и ряда других – только боль является относительно специфическим симптомом. Боли обусловлены спазмом гладкой мускулатуры билиарного тракта вследствие раздражения рецепторов слизистой оболочки при миграции элементов БС. Миграция БС возникает чаще, чем при холецистолитиазе, в связи с более легким прохождением сладжа по сравнению с конкрементами. Кроме того, причиной билиарной боли может быть дисфункция ЖП и сфинктерного аппарата желчных путей, которые могут привести к формированию БС. Частота боли в области правого подреберья возрастает по мере изменения типа БС и становится более выраженной при БС 3 типа. Симптомы билиарной диспепсии также усиливаются при трансформации БС от 1 к 3 стадии. Спазм СО при БС проявляется в 50-93% случаев, часто сопровождается развитием билиарной гипертензии.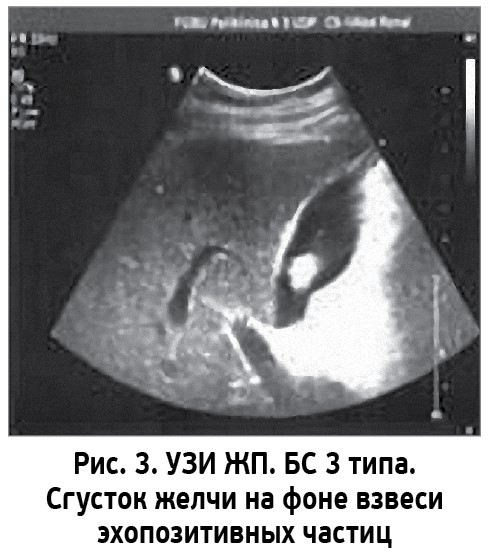
Изучение естественного течения БС демонстрирует, что до 20% случаев заканчивается формированием конкрементов в ЖП, в то время как спонтанный полный регресс наступает в 70% случаев. У 30-60% пациентов с БС динамическое ультразвуковое наблюдение выявляет эпизоды безмедикаментозного исчезновения и формирования его вновь.
К вероятным осложнениям БС относятся острый и хронический панкреатит, дисфункция СО, острый и хронический холецистит, холедохолитиаз и «отключенный» ЖП. Длительная персистенция БС и постоянный пассаж его в ДПК может осложняться развитием стриктур терминального отдела общего желчного протока и/или стенозирующего папиллита.
Ретроспективное наблюдение Р. А. Hill и R. D. Harris (2016) в течение 21 мес за 104 пациентами с БС продемонстрировало развитие осложнений у 24% больных [1].
Основным методом диагностики БС является ультразвуковое исследование (УЗИ) ЖП, в том числе с определением его сократительной функции и CО. По показаниям проводится эндоскопическая ультрасонография для дифференциальной диагностики, например между фиксированным к стенке ЖП сгустком и пристеночными образованиями, в первую очередь опухолевого генеза.
В последние годы для уточнения характера БС применяется компьютерная томография (КТ) с оценкой денситометрических показателей желчи, что позволяет сократить сроки лечения, вовремя назначив адекватную терапию. Денситометрия является дополняющим УЗИ методом. Для оценки плотности желчи используют шкалу Хаунсфилда (Hounsfield units, HU).
В ряде случаев используют динамическую гепатобилисцинтиграфию – способ радионуклидной диагностики заболеваний печени и желчных протоков, основанный на использовании меченого 99mTc радиофармпрепарата, избирательно накапливающегося в гепатоцитах и экскретируемого в желчь. Данное исследование позволяет получить информацию об анатомии и физиологии желчевыводящей системы, включая двигательную функцию ЖП и желчных протоков.
Предприняты многочисленные попытки, направленные на раннюю диагностику БС как предкаменной стадии развития ЖКБ, что открывает широкие перспективы по первичной профилактике холелитиаза.
По последним данным японских исследователей, БС является маркером раннего рака ЖП. В связи с этим рекомендуется эндоскопическая катетеризация ЖП с цитологическим исследованием билиарного осадка на наличие атипичных клеток [9].
Не вызывает сомнения, что больные с БС нуждаются в динамическом наблюдении и лечении. Терапия должна быть направлена на патогенетические звенья формирования БС, что предполагает:
- возможное устранение модифицируемых факторов риска данного состояния (при исчезновении причин, способствующих образованию сладжа, последний исчезает спонтанно);
- коррекцию дисхолии;
- нормализацию моторики ЖП, СО с восстановлением градиента давления и тока желчи по билиарному тракту;
- коррекцию кишечной микрофлоры, устранение синдрома избыточного бактериального роста;
- коррекцию симптомов нарушенного пищеварения и всасывания благодаря нормализации энтерогепатической циркуляции желчных кислот.
Диетические рекомендации включают частое дробное питание. Адекватный режим питания с частыми приемами пищи (5-6-разовое питание) способствует нормализации давления в ДПК и регуляции опорожнения ЖП и протоковой системы. Диетический рацион должен учитывать тип дисфункции ЖП (гиперкинетический или гипокинетический), сопутствующие заболевания органов желудочно-кишечного тракта.
Тактика ведения больных определялась эхографическим типом БС и наличием факторов риска.
На современном этапе основным лекарственным средством с доказанной эффективностью воздействия на различные звенья билиарного литогенеза является урсодезоксихолевая кислота (УДХК) [6, 7, 11, 13]. Урсодезоксихолевая кислота обладает широким спектром терапевтических эффектов, в связи с этим в клинической практике с лечебной целью все большее распространение получает применение препаратов УДХК.
Широко известны биологические функции и терапевтические эффекты УДХК, проявляющиеся ингибированием индуцированного дезоксихолевой кислотой апоптоза посредством модуляции продуцирования митохондриальных трансмембранных потенциальных и реакционноспособных форм кислорода, блокированием индуцирования синтазы оксида азота в кишечных эпителиальных клетках человека. Гидрофильная природа УДХК обеспечивает цитопротекцию при воспалительных заболеваниях печени, применяется в качестве иммуномоделирующего агента, значительно понижает уровень трансаминаз и холестатические ферментативные индексы повреждения печени при хроническом гепатите, значительно ингибирует рост Helicobacter pylori и пепсина. Высокий уровень УДХК блокирует пролиферацию вируса гепатита С, стабилизирует клеточные мембраны гепатоцитов, уменьшает алкогольную жировую инфильтрацию печени, оказывает сосудорасширяющее действие на системное сосудистое ложе, но не изменяет ни легочной васкулярной функции, ни сердечных функций.
УДХК оказывает цитопротекторный, антиоксидантный, антифибротический, литолитический, холеретический, иммуномодулирующий, гипохолестеринемический, антиапоптотический эффекты, среди которых существенное значение имеет выраженное литолитическое и гипохолестеринемичекое действие. Терапевтические свойства УДХК в отношении БС (т. н. диссолюционная терапия) обусловлены уменьшением синтеза холестерина в печени и его кишечной абсорбции, изменением структуры и состава мицелл в желчи, увеличением дисперсии холестерина с формированием жидкокристаллической фазы, а также усилением постпрандиальной сократимости ЖП.
Литолитический эффект УДХК объясняется снижением литогенности желчи вследствие формирования жидких кристаллов с молекулами холестерина, что способствует мицеллярной солюбилизации и предупреждению образования холестериновых камней. УДХК увеличивает удельный вес желчных кислот в желчи, снижая перенасыщение холестерина, и устраняет пузырный сладж. На фоне лечения доля этой гидрофильной желчной кислоты возрастает до 60%, а доля более токсичных гидрофобных желчных кислот, соответственно, падает, благодаря чему УДХК становится основным компонентом желчи [8].
Антихолестатический эффект УДХК заключается: в подавлении секреции токсических желчных кислот в желчь путем конкурентного захвата рецепторами в подвздошной кишке; в стимуляции экзоцитоза в гепатоцитах путем активизации Ca-зависимой α-протеинкиназы, что вызывает уменьшение концентрации гидрофобных желчных кислот; в индукции холереза, богатого бикарбонатами, что приводит к увеличению пассажа желчи рецепторами в подвздошной кишке; в модуляции структуры и состава богатых фосфолипидами смешанных мицелл в желчи.
Холеретический эффект УДХК заключается: в вытеснении пула токсичных гидрофобных ЖК посредством конкурентного захвата рецепторов в подвздошной кишке; в стимуляции экзоцитоза в гепатоцитах путем активации Са-зависимой L‑протеинкиназы, что уменьшает концентрацию гидрофобных ЖК; в индукции бикарбонатного холереза, что усиливает выведение гидрофобных ЖК в кишечник; в стимуляции различных белков холеретического транспорта (активирует экспрессию и интеграцию MRP2 и BSEP в канальцевых мембранах, стимулируя экскрецию желчных кислот с желчью; стимулирует базолатеральный MRP3, что повышает дисперсию солей ЖК в систему энтерогепатической циркуляции; активирует сложную сеть внутриклеточных сигнальных молекул).
Гипохолестеринемический эффект УДХК проявляется снижением всасывания холестерина в кишечнике, синтеза холестерина в печени и экскреции холестерина в желчь. УДХК, влияя на КоА‑редуктазу, уменьшает образование холестерина. Все это приводит к снижению литогенности желчи.
Доказательная база применения УДХК включает значительное количество исследований, свидетельствующих о различной эффективности (от 60 до 87,5%) и безопасности применения препаратов УДХК в лечении БС у различных групп пациентов. Вместе с тем отмечается разнородность данных исследований по продолжительности курса лечения, дозы УДХК, зависимости применения от выраженности клинической картины и ультразвуковой формы БС. Важными и не решенными для клинической практики остаются вопросы, касающиеся фармакоэкономических аспектов терапии БС и клинической эквивалентности различных препаратов УДХК [1].
Препарат Урсосан® (УДХК) является средством выбора и основным базисным патогенетическим препаратом, который используется для лечения и профилактики БС. Суточная доза Урсосана и продолжительность приема зависят от типа БС.
При 1 типе БС доза препарата составляет 10 мг/кг, при 2 типе – 10-15 мг/кг, при 3 типе – 15 мг/кг и более. Вся доза принимается однократно перед сном, срок лечения – от 3 мес при БС 1 типа до 12 мес при БС 3 типа. В случае резистентности БС 3 типа к литолитической терапии Урсосаном следует увеличить дозу до 15-20 мг на 1 кг массы тела и удлинить срок лечения до 6-12 мес. Контроль УЗИ в процессе лечения следует проводить ежемесячно.
В мире опубликовано значительное количество работ, отражающих результаты клинических испытаний УДХК, которые подтверждают эффективность и безопасность применения данной кислоты при более чем 45 нозологиях [2, 7, 12, 13].
Накопленные на сегодня экспериментальные и клинические данные свидетельствуют о том, что УДХК представляет собой лекарственный препарат плейотропного действия, что выражается в наличии многофакторного действия на состояние гепатобилиарной системы.
Л. С. Орешко и соавт. (2018) представили наблюдения (2016-2017) по изучению влияния терапии препаратом УДХК Гринтерол на клинико-биохимические параметры больных с гепатобилиарной патологией в условиях реальной поликлинической практики. Число участников составило 10 213 пациентов, среди которых 3625 пациентов были с хроническим холециститом и БС. В ходе проводимой терапии на конечном визите отмечалось снижение болевого синдрома у 90% пациентов, уменьшение горечи во рту – у 88%, нормализация стула наблюдалась у 95% пациентов. Проведенное на большом объеме наблюдений исследование продемонстрировало позитивное влияние УДХК на клиническую картину и сывороточные маркеры печеночного цитолиза и холестаза. Во всех группах прием Гринтерола приводил к уменьшению болей, а также симптомов желудочной, желчной и кишечной диспепсии. Улучшение клинического статуса сопровождалось уменьшением активности сывороточных маркеров внутрипеченочного холестаза. Целесообразно, по мнению авторов, опираясь на успешный опыт проведенного исследования, продолжить изучение результатов применения препаратов УДХК и включить пациентов старше 65 лет в группы с БС и хроническим холециститом [10].
О. А. Саблин и соавт. (2013) сообщают о наблюдении за 20 пациентами с наличием БС, верифицированного УЗИ, до и после лечения 500 мг/сут препаратом УДХК в течение 4 нед. На фоне лечения отмечено уменьшение частоты болевого абдоминального синдрома с 95 до 35% (р<0,01), горечи во рту – с 90 до 15% (р<0,001), тошноты – с 60 до 5% (р<0,05), запора – с 85 до 15% (р<0,001), вздутия живота – с 70 до 30% (р<0,05). Полная элиминация БС отмечена у 70%, у остальных пациентов зарегистрирована положительная динамика с 1,7 до 0,4 балла [12].
С. С. Бацков и соавт. (2015) наблюдали 150 больных с верифицированными БС и холелитиазом, получавших УДХК в дозе 15 мг/кг на один прием. Длительность лечения составила 8-14 мес при условии, что если по результатам УЗИ размеры конкрементов не уменьшались, то лечение прекращалось. К окончанию 10 мес лечения отмечено статистически достоверное уменьшение объема исходной желчи с 35,4±2,6 до 26,3±2,4 мл; объема остаточной желчи – с 15,5±1,4 до 8,2±1,7 мл; статистически достоверное увеличение объема выделенной желчи – с 17,5±1,8 до 21,6±3,2 мл; процента выделенной желчи – с 59,4±2,3 до 67,2±2,5; коэффициента тонуса – с 1,32±0,7 до 1,94±0,8. Улучшение функционального состояния билиарного тракта коррелировало со статистически достоверным снижением уровня АСТ, АЛТ, ГГТП, триглицеридов, общего холестерина, холестерина липопротеинов низкой плотности. Частота выявления БС в когорте больных снизилась с 37,5 до 15,4%, конкрементов размером от 3 до 5 мм – с 34,5 до 5,1%, от 5 до 10 мм – с 15,4 до 2,2%, 10 мм – с 12,5 до 4,4%. Соответственно, полный литолиз выявлялся у 65,9%, частичный – у 29,4%, отсутствие эффекта зарегистрировано у 4 пациентов (4,7%) с размером конкрементов 10 мм [3].
По данным ЦНИИ гастроэнтерологии, эффективность урсотерапии при дозе 10 мг/кг/сут в течение 3 мес при БС в виде мелких гиперэхогенных частиц составила 60%, а в виде эхонеоднородной желчи с наличием различной плотности сгустков – 85,7%, в виде замазкообразной желчи – 87,5% [6]. Согласно другим данным, применение УДХК в дозе 15 мг/кг/сут приводит к устранению БС у 85% больных в течение 6 мес, причем в ряде случаев требуется продолжение курса лечения до 12 мес и увеличение дозы до 20 мг/кг/сут. При успешном устранении БС авторы рекомендуют проведение поддерживающей терапии по 250-500 мг/сут в течение двух 3-месячных циклов продолжительностью до нескольких лет [8].
G. R. May и соавт. (1993) опубликовали результаты метаанализа исследований, выполненных в 1966-1992 гг. и охватывавших 819 пациентов. Указанный метаанализ продемонстрировал, что УДХК успешно растворяет рентгенонегативные камни в 37% случаев, а эффективность литолиза зависит от размера камня [18].
О. Н. Минушкин (2008) сообщает о 60 пациентах, из которых у 30 был БС, у 20 – множественные камни (3-5 мм), у 6 – множественные камни (6-10 мм) и у 4 – единичные камни (6-10 мм). Пациенты получали препарат УДХК в дозе 10 мг/кг/сут при наличии конкрементов и 5-7 мг/кг/сут – при БС. В результате лечения у 50 больных отмечено полное растворение камней и осадка, у 6 – уменьшение размеров камней, у 2 – динамика отсутствовала и у 2 – отмечено увеличение конкрементов. Шести больным, у которых отмечено уменьшение размеров камней, урсотерапия была продолжена в тех же или больших дозах при нормальной переносимости, средний срок растворения составил 1 год 3 мес [8].
Общеизвестно, что после резекции желудка с выключением из пассажа ДПК имеется высокий риск развития конкрементов вследствие гипомоторной дискинезии ЖП, сопровождающейся застоем и нарушением физико-химических свойств желчи.
А. Ю. Иоффе и соавт. (2005) опубликовали данные наблюдения за 22 больными, у которых после данного оперативного вмешательства развилась ЖКБ с наличием БС или небольших конкрементов. Назначение препарата УДХК в дозе 15 мг/кг/сут в течение одного месяца привело к полной элиминации конкрементов и БС у всех больных [7].
Отмечается высокий риск развития ЖКБ у больных, страдающих ожирением, после операции с целью быстрого снижения веса (с наложением желудочного обходного анастомоза).
H. J. Sugerman и соавт. (1995) сообщили об исследовании, включавшем 233 больных, перенесших подобную операцию; в группе плацебо у 32% пациентов отмечено образование желчных конкрементов. В то же время у пациентов, получавших препарат УДХК, камни формировались значительно реже – в 13, 2 и 6% случаев в группах, получавших 300, 600 и 1200 мг УДХК в день соответственно [19]. Также УДХК в дозе 600 мг/сут статистически достоверно предотвращает образование желчных камней у пациентов, находящихся на многонедельных разгрузочных диетах в связи с патологическим ожирением.
В 2007 г. Немецким обществом по изучению расстройств пищеварения и нарушений метаболизма и Немецким обществом хирургии желудочно-кишечного тракта на основании метаанализа семи рандомизированных плацебо-контролируемых исследований, включавших 897 пациентов, были приняты Рекомендации S‑3 по диагностике и лечению ЖКБ, в которых было зафиксировано, что УДХК в дозе 500 мг/сут и более в течение 3-6 мес статистически достоверно снижает риск развития ЖКБ, связанной со значительной потерей массы тела (более 1,5 кг в неделю), и должна назначаться до тех пор, пока вес пациента полностью не стабилизируется [8].
Отмечено, что профилактика с помощью УДХК является экономически эффективным решением, существенно снижающим затраты на лечение.
В 2017 г. D. E. Maqoulitios и соавт. опубликовали данные метаанализа 8 исследований (спланированных с позиций доказательной медицины), включившего результаты наблюдения за 1335 пациентами с ожирением после проведения бариатрической операции на желудке. Отмечена значительно меньшая частота развития конкрементов в ЖП в группах, в которых назначалась УДХК, по сравнению с контрольными группами: ОР через 6 мес после операции – 0,11 (95% ДИ 0,04, 0,26), через 12 мес после операции – 0,18 (95% ДИ 0,12, 0,29) [17].
В соответствии с рекомендациями Европейской ассоциации по изучению печени, опубликованными в 2016 г., сопутствующая терапия препаратами УДХК может назначаться пациентам, находящимся на длительной терапии соматостатином или его аналогами, для профилактики формирования холестериновых желчных камней [16].
При постхолецистэктомическом синдроме применение УДХК ликвидирует дефицит ЖК и билиарную недостаточность, снижает литогенность желчи. Д. И. Трухан и соавт. (2016) в качестве профилактического средства рекомендуют постоянный прием препаратов УДХК однократно от 250 до 500-750 мг/сут, в качестве альтернативной схемы предлагается назначение препарата месячными курсами каждый второй или третий месяц, а также проведение 2 курсов в год по 50 дней по 250 мг вечером [13].
Эффективность и безопасность УДХК подтверждены множеством клинических исследований и многолетним опытом применения.
S. Tamida и соавт. (1999) приводят данные 18-летнего наблюдения за 527 больными с ЖКБ, получавшими или не получавшими препараты УДХК. Продемонстрировано статистически достоверное уменьшение риска болевого абдоминального синдрома у больных с симптоматикой ЖКБ, получавших УДХК, по сравнению с контрольной группой (62 против 92% за 10 лет; р<0,01) и у бессимптомных пациентов (6 против 12% за 10 лет; р=0,037). Риск проведения холецистэктомии также был ниже у больных, принимавших УДХК (26 против 88% за 10 лет; р<0,001). Это не зависело от эффективности литолитической терапии, что позволило авторам рекомендовать назначение УДХК пациентам, имеющим значительный хирургический риск, т. к. длительная урсотерапия явно связана со снижением риска болевого абдоминального синдрома и атаки острого холецистита [20].
Этот эффект объясняется тем, что УДХК восстанавливает функции мышечного аппарата ЖП и снижает уровень биохимических маркеров окислительного стресса и воспаления [8].
Собственные наблюдения и проведенные исследования подтверждают высокую терапевтическую эффективность препарата Урсосан® при лечении пациентов с БС на фоне билиарной дисфункции, хронического холецистита, предкаменной стадии ЖКБ, что способствовало устранению билиарной и печеночно-клеточной дисхолии [5].
Таким образом, терапия БС должна быть комплексной, воздействующей на патогенетические механизмы развития заболевания.
Средством выбора для лечения БС является урсодезоксихолевая кислота (препарат Урсосан®).
По показаниям возможна комбинация с миотропными селективными спазмолитиками для купирования спазма СО и пробиотиками.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 13-14 (458-459), липень 2019 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...




