Скрининг и ранняя диагностика рака предстательной железы
Популяционный, или массовый, скрининг рака предстательной железы (РПЖ) – это определенная стратегия организации здравоохранения, включающая систематическое обследование мужчин группы риска без клинических симптомов. В отличие от него раннее выявление, или оппортунистический скрининг, состоит в проведении индивидуального обследования, которое инициируется самим пациентом и/или его врачом. Основными задачами обеих скрининговых программ являются снижение смертности вследствие РПЖ и поддержание качества жизни пациентов.
В большинстве стран с развитой экономикой смертность от РПЖ имеет тенденцию к снижению, но масштабы ее варьируются. Считается, что снижение этого показателя, наблюдаемое в последнее время в США, в какой-то мере обусловлено принятой политикой интенсивного скрининга РПЖ.
В настоящее время в литературе, посвященной проблемам урологии, вопрос о проведении скрининга РПЖ является одним из наиболее спорных. Некоторые авторы утверждают, что соблюдение рекомендаций Американской урологической ассоциации или Рабочей группы по профилактике заболеваний США (USPSTF) по проведению скрининга РПЖ может привести к тому, что у значительного количества мужчин агрессивные формы заболевания не будут выявлены. В 2017 г. USPSTF опубликовала обновленное положение о том, что мужчины в возрасте 55-69 лет должны быть проинформированы о преимуществах и рисках скринингового определения простатспецифического антигена (ПСА), поскольку таковое ассоциировано с незначительным положительным влиянием на выживаемость. Уровень данной рекомендации был повышен до «С» (ранее – «D»).
При сравнении программ систематического и оппортунистического скрининга (R. Arnsrud Godtman et al., 2015) обнаружено, что в случае организованного обследования отмечается гипердиагностика и снижение смертности. В то же время в когорте пациентов, прошедших оппортунистический скрининг, наблюдалась еще более высокая частота гипердиагностики при минимальном улучшении выживаемости.
Результаты Кокрановского обзора (2013) свидетельствуют о следующем:
- скрининг ассоциирован с повышением частоты диагностирования РПЖ;
- скрининг способствует выявлению в большей степени локализованных форм заболевания и в меньшей – распространенного РПЖ (T3-4N1M1);
- согласно результатам пяти рандомизированных клинических исследований (n=341 000), не обнаружено преимуществ в отношении показателя канцерспецифической выживаемости. По результатам четырех доступных исследований не наблюдалось положительного влияния скрининга на общую выживаемость.
Индивидуализированная тактика ранней диагностики РПЖ с учетом степени риска может быть предложена хорошо информированным мужчинам с прогнозируемой продолжительностью жизни от 10 до 15 лет. Однако этот подход может быть связан с существенным риском гипердиагностики. Поэтому следует тщательно определять когорты пациентов, для которых ранняя диагностика РПЖ наиболее полезна.
К группе повышенного риска развития РПЖ относятся мужчины:
- в возрасте старше 50 лет;
- старше 45 лет с семейным анамнезом РПЖ (по отцовской или материнской линии);
- афроамериканцы.
Кроме того, мужчины с уровнем ПСА >1 нг/мл в возрасте 40 лет и >2 нг/мл – 60 лет также подвержены повышенному риску метастатического РПЖ или смерти от этой патологии несколько десятилетий спустя.
Информированным мужчинам, подлежащим ранней диагностике РПЖ, следует провести тест на ПСА и пальцевое ректальное исследование. Стратегия наблюдения за этой категорией пациентов с учетом степени риска разрабатывается на основе исходного уровня ПСА. Оптимальные интервалы между обследованиями не установлены. Оно может проводиться каждые два года для лиц с изначально повышенным риском РПЖ или откладываться до восьми-десяти лет у тех, кто не подвергается таковому.
На основании данных, полученных Гетеборгской группой Европейского рандомизированного исследования скрининга РПЖ (European Randomized Study of Screening for Prostate Cancer, ERSPC, 2014), сделано предположение, что вопрос о возрасте, в котором следует прекратить раннюю диагностику, остается открытым. При этом должна быть принята во внимание ожидаемая продолжительность жизни пациента. Мужчинам, прогнозируемая продолжительность жизни у которых составляет <15 лет, скрининг вряд ли будет полезен. Кроме того, с учетом отсутствия простого инструмента оценки индивидуальной продолжительности жизни наличие коморбидных состояний столь же значимо, как и возраст.
Рекомендации относительно скрининга и ранней диагностики РПЖ
- Не следует предлагать определение уровня ПСА, не проконсультировав мужчину относительно потенциальных рисков и преимуществ такового (уровень доказательности – УД – 3, сила рекомендаций – СР – сильная).
- Разработать индивидуальную стратегию ранней диагностики с учетом степени риска для хорошо информированных пациентов без тяжелой соматической патологии и с ожидаемой продолжительностью жизни не менее 10-15 лет (УД 3; СР сильная).
- Следует предложить раннее обследование на ПСА хорошо информированным мужчинам группы повышенного риска развития РПЖ (возраст старше 50 лет; старше 45 лет с семейным анамнезом РПЖ; афроамериканцы в возрасте старше 45 лет; УД 2b; СР сильная).
- Предложить стратегию с учетом степени риска (на основе исходного уровня ПСА) с периодом наблюдения 2 года для лиц группы риска (УД 3; СР слабая):
- ПСА >1 нг/мл в возрасте 40 лет;
- ПСА >2 нг/мл в возрасте 60 лет.
- Отложить наблюдение до восьми лет у лиц с отсутствием риска.
- Не проводить раннюю диагностику РПЖ, исходя из короткой ожидаемой продолжительности жизни и неблагоприятного статуса здоровья пациента. Мужчинам с прогнозируемой продолжительностью жизни <15 лет скрининг вряд ли будет полезен (УД 3; СР сильная).
Клиническая диагностика
Подозрение на РПЖ обычно возникает на основании результатов пальцевого ректального исследования (ПРИ) и определения уровня ПСА. Окончательный диагноз устанавливают с учетом гистопатологической верификации аденокарциномы в биоптатах или образцах ткани простаты после трансуретральной резекции или простатэктомии, проведенных по поводу доброкачественной гиперплазии предстательной железы (ДГПЖ).
Пальцевое ректальное исследование
В большинстве случаев злокачественная опухоль локализуется в периферической зоне предстательной железы и может быть обнаружена методом ПРИ, если объем железы ≥0,2 мл. Положительная прогностическая значимость подозрительных результатов ПРИ у пациентов с уровнем ПСА ≤2 нг/мл составляет 5-30%. Выявление опухоли методом ПРИ связано с риском более высокой степени злокачественности по шкале Глисона и является показанием для биопсии.
Определение уровня ПСА
ПСА является органоспецифическим, но не канцерспецифическим биомаркером, поэтому его уровень может повышаться при ДГПЖ, простатите и других незлокачественных состояниях. Однако уровень ПСА является более достоверным прогностическим фактором рака, чем выявление подозрительных участков посредством ПРИ и трансректального ультразвукового исследования.
Для измерения ПСА не существует согласованных стандартов. Это непрерывный параметр, более высокие уровни которого свидетельствуют о более высокой вероятности наличия РПЖ. Вместе с тем установлено, что многие мужчины могут иметь РПЖ, несмотря на низкий уровень ПСА в сыворотке крови. В таблице приведены данные о риске возникновения агрессивного РПЖ (индекс Глисона ≥7 баллов) при низких уровнях ПСА.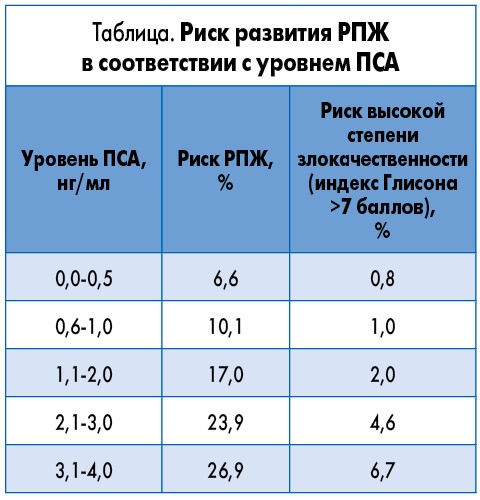
Плотность ПСА
Плотность ПСА (PSA density, PSA-D) определяется как количество общего ПСА сыворотки крови на единицу объема предстательной железы. Чем выше плотность ПСА, тем выше вероятность того, что РПЖ является клинически значимым.
Оценка скорости нарастания и времени удвоения уровня ПСА
Существует два способа измерения динамики уровня ПСА:
- скорость нарастания ПСА (PSA velosity, PSA-V) – это показатель абсолютного ежегодного повышения уровня ПСА в сыворотке крови (нг/мл в год);
- время удвоения уровня ПСА (PSA doubling time, PSA-DT), которое выражает экспоненциальное (величина переменной и скорость ее роста прямо пропорциональны) повышение уровня ПСА в сыворотке крови с течением времени.
Эти показатели имеют прогностическое значение при проведении лечения РПЖ. Вместе с тем их использование в диагностике РПЖ ограничено из-за влияния сопутствующих состояний (общий объем предстательной железы, ДГПЖ), разных интервалов между измерениями ПСА и повышения/снижения PSA-V и PSA-DT. Эти параметры не предоставляют дополнительной прогностической информации по сравнению с определением только уровня ПСА.
Соотношение свободный/общий ПСА
Соотношение свободный/общий ПСА (free/total PSA ratio, f/t PSA) следует использовать с осторожностью, поскольку на его значение могут влиять некоторые методологические и клинические факторы (например, нестабильность свободного ПСА при 4 °C и при комнатной температуре; вариабельность характеристик тестов; сопутствующая ДГПЖ).
Тем не менее соотношение f/t PSA имеет значение при стратификации риска РПЖ у мужчин с общим уровнем ПСА от 4 до 10 нг/мл и нормальным результатом ПРИ. Соотношение f/t PSA не имеет клинического значения при уровне общего ПСА в сыворотке крови >10 нг/мл или при наблюдении пациентов с диагностированным РПЖ.
Дополнительные методы лабораторной диагностики
В настоящее время для исследования доступны панель калликреинов в сыворотке или плазме крови, в том числе тест на определение индекса здоровья простаты (уровни свободного и общего ПСА и изоформы 2-про-ПСА), а также четыре маркера калликреина (уровни свободного, интактного, общего ПСА и калликреинподобной пептидазы 2). Проведение этих тестов может способствовать уменьшению количества ненужных процедур биопсии простаты у пациентов, прошедших исследование ПСА. В нескольких проспективных мультицентровых исследованиях продемонстрирована более высокая прогностическая значимость индекса здоровья простаты и панели четырех калликреинов в определении клинически значимого РПЖ у пациентов с уровнем ПСА
Генетический маркер рака простаты 3
Генетический маркер рака простаты 3 (Prostate cancer gene 3, PCA3) представляет собой простатспецифическую некодирующую мРНК и измеряется в осадке мочи, полученной после массажа предстательной железы.
На сегодняшний день для определения РСА3 разработана тест-система Progensa. Этот метод обладает большей по сравнению с исследованием ПСА специфичностью и чувствительностью в диагностике РПЖ у мужчин с повышенным уровнем такового.
Содержание PCA3 увеличивается в зависимости от объема предстательной железы, однако имеются противоречивые данные о его корреляции со степенью дифференциации опухоли (по шкале Глисона). Целесообразность его использования при активном наблюдении больных РПЖ пока не доказана. В настоящее время основным показанием для применения теста Progensa является определение необходимости проведения повторной биопсии после получения отрицательных результатов предыдущей (однако клиническая эффективность исследования с этой целью не установлена).
Тест SelectMDX также основан на выявлении мРНК в моче. Наличие мРНК генов HOXC6 и DLX1 оценивается с целью определения как риска обнаружения РПЖ при биопсии, так и наличия рака высокого риска.
Рекомендации по определению риска РПЖ у пациентов без симптомов
Во избежание ненужной биопсии пациентам без симптомов с нормальным результатом ПРИ и уровнем ПСА
- калькулятор риска;
- дополнительное исследование маркеров в сыворотке крови или моче:
- индекс здоровья простаты;
- панель четырех калликреинов;
- РСА3;
- HOXC6/DLX1;
- методы визуализации.
Исходя из имеющихся доказательств, некоторые биомаркеры могут способствовать дифференциальной диагностике агрессивных и неагрессивных опухолей в большей мере, чем прогностические параметры, которые в настоящее время используются клиницистами.
По материалам: Prostate Cancer. EAU Guidelines. Edn. presented at the EAU Annual Congress Copenhagen 2018. URL: http://uroweb.org/guideline/prostate-cancer/#11.
Подготовила Виктория Недвиженко
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 3 (59), 2019 р.
СТАТТІ ЗА ТЕМОЮ Діагностика
У лютому відбулася щорічна Всеукраїнська науково-практична конференція «Малоінвазивні технології в урології», присвячена актуальним проблемам сучасної урології. Пропонуємо огляд найцікавіших доповідей, що прозвучали в рамках заходу....
Інфекції сечовивідних шляхів (ІСШ) у всьому світі посідають провідне місце серед інфекційних захворювань дорослого населення. Поряд із тим серед фахівців зростає занепокоєння щодо триваючого зростання стійкості бактерій до більшості антибіотиків. Експерти провідних міжнародних товариств наголошують на необхідності розсудливого і виваженого призначення антимікробних препаратів. Про основні принципи раціональної антибіотикотерапії в урології, зокрема при проведенні діагностичних і хірургічних втручань, ми попросили розповісти завідувача відділу відновної урології та новітніх технологій ДУ «Інститут урології ім. акад. О.Ф. Возіанова НАМН України», доктора медичних наук, професора В’ячеслава Миколайовича Григоренка. ...
Процедура трансректальної біопсії простати супроводжується високим ризиком інфекційних ускладнень, тому проведення антимікробної профілактики при цьому втручанні є обов’язковим. Однак зростання антибіотикорезистентності, а також нещодавні рекомендації щодо обмеження призначень фторхінолонів значно звужують спектр можливих варіантів такої профілактики. Міжнародною мультидисциплінарною групою експертів на основі літературних джерел та клінічного досвіду було розроблено ряд настанов стосовно запобігання інфекційним ускладненням при біопсії простати та обґрунтовано доцільність і переваги призначення з цією метою фосфоміцину ...
Кількість людей, які страждають і помирають від вірусного гепатиту В (ВГВ), можна порівняти з кількістю хворих на коронавірусну хворобу 2019 року (COVID‑19), яка наразі викликає велике занепокоєння в усьому світі. Тому вкрай важливим залишається питання передачі вірусу, у тому числі через статеві клітини. Попередніми дослідженнями встановлено, що гени ВГВ, інтегровані в людські сперматозоїди, здатні до реплікації та експресії після передачі ембріонам. Однак досі це явище не було підтверджено клінічними дослідженнями у пацієнтів. Автори вивчали особливості інтеграції ВГВ у геном сперматозоїдів пацієнтів та аналізували можливі клінічні наслідки для потомства ...





