Аллергия на пенициллин
В 1928 г. сэр Александр Флеминг обнаружил, что активный компонент плесневого гриба пенициллина обладает способностью убивать бактерии в чашке Петри. Он назвал это вещество пенициллином. В 1945 г. А. Флемингу, Х.У. Флори и Э.Б. Чейну была присуждена Нобелевская премия по физиологии и медицине «За открытие пенициллина и его лечебный эффект при различной инфекционной патологии».
С начала 1950-х гг. пенициллин спас миллионы жизней, включая детей, беременных, больных сепсисом, менингитом, эндокардитом и другими жизнеугрожающими инфекционными заболеваниями. Пенициллин G остается единственным рекомендуемым методом профилактики трансмиссивной передачи сифилиса от матери к ребенку.
Первый случай анафилаксии, связанный с пенициллином, зарегистрирован в 1945 г.; в докладе Всемирной организации здравоохранения (1968) указано, что уровень смертности от анафилаксии составил 0,002%. Данные, свидетельствующие о возрастании частоты аллергических реакций на протяжении последних 60 лет, отсутствуют, однако имеются убедительные доказательства снижения сенсибилизации к пенициллину с течением времени. Анафилаксия, вызванная воздействием пенициллина, развивается при оральном, подкожном и внутривенном введении препарата. По данным национального американского исследования (1957), в котором приняли участие 827 больниц, в течение первых 10 лет клинического применения пенициллина зафиксировано 1000 пенициллин-ассоциированных смертей. Обзор клинических случаев (n=151), описывающих пенициллин-ассоциированные летальные исходы, отчеты о которых были опубликованы в медицинской литературе на протяжении 1951-1965 гг., продемонстрировал отсутствие гендерных отличий; возраст >50% погибших составил 25-65 лет, 44% имели инфекционные заболевания дыхательных путей, 28% – ранее диагностированную аллергию или бронхиальную астму, 69% ранее принимали пенициллин, у 36% их них развивались аллергические реакции на другие лекарственные средства. Средний интервал между приемом пенициллина и появлением симптомов составлял менее 15 мин в 85% случаях, большинство пациентов умерли в течение 1 ч после приема препарата.
Современная эпидемиология и географическая релевантность
Согласно медицинской документации, пенициллин является наиболее распространенным препаратом, вызывающим лекарственную аллергию; распространенность аллергии на пенициллин (АП) варьирует в пределах 6-25% в зависимости от географического региона и популяции больных. Доброкачественные кожные реакции, такие как крапивница и отсроченная макулопапулезная экзантема, являются самыми частыми. В 2007 г. в США зафиксировано 1,4% новых случаев АП у женщин и 1,1% у мужчин, согласно данным исследования, в котором анализировались данные электронных медицинских карт пациентов, получавших медицинскую помощь в больнице Kaiser Permanente (n=411 534). В исследовании (1966) встречаемость аллергических реакций составила 7,8%, при этом 22% подтвержденных случаев сопровождались положительными результатами кожных тестов; однако результаты одного одноцентрового американского исследования зафиксировали снижение доли положительных результатов кожных тестов на пенициллин с 15% в 1995 г. до 3% в 2007 г. и до 0,8% в 2013 г.
Пенициллины являются самой распространенной причиной лекарственно-индуцированных фатальных и нефатальных случаев анафилаксии в США и Великобритании. Минимальный уровень анафилаксии отмечен при применении пероральных пенициллинов; согласно одному сообщению из Великобритании, зафиксирован всего 1 случай фатальной анафилаксии при приеме перорального амоксициллина в течение 35 лет при назначении 100 млн курсов терапии этим препаратом. Аминопенициллины относятся к группе препаратов максимального риска, они вызывают появление отсроченной доброкачественной экзантемы, которая, как правило, развивается при острой вирусной инфекции Эпштейна-Барр. Аминопенициллины считаются наиболее частой причиной острого генерализованного экзантематозного пустулеза (ОГЭП). Пенициллины ассоциированы с другими тяжелыми кожными реакциями, такими как медикаментозно-индуцированная реакция с эозинофилией и системными проявлениями (МИРЭСП), синдромом Стивенса-Джонсона и токсическим эпидермальным некролизом (ССД-ТЭН).
Пенициллин и β-лактамы
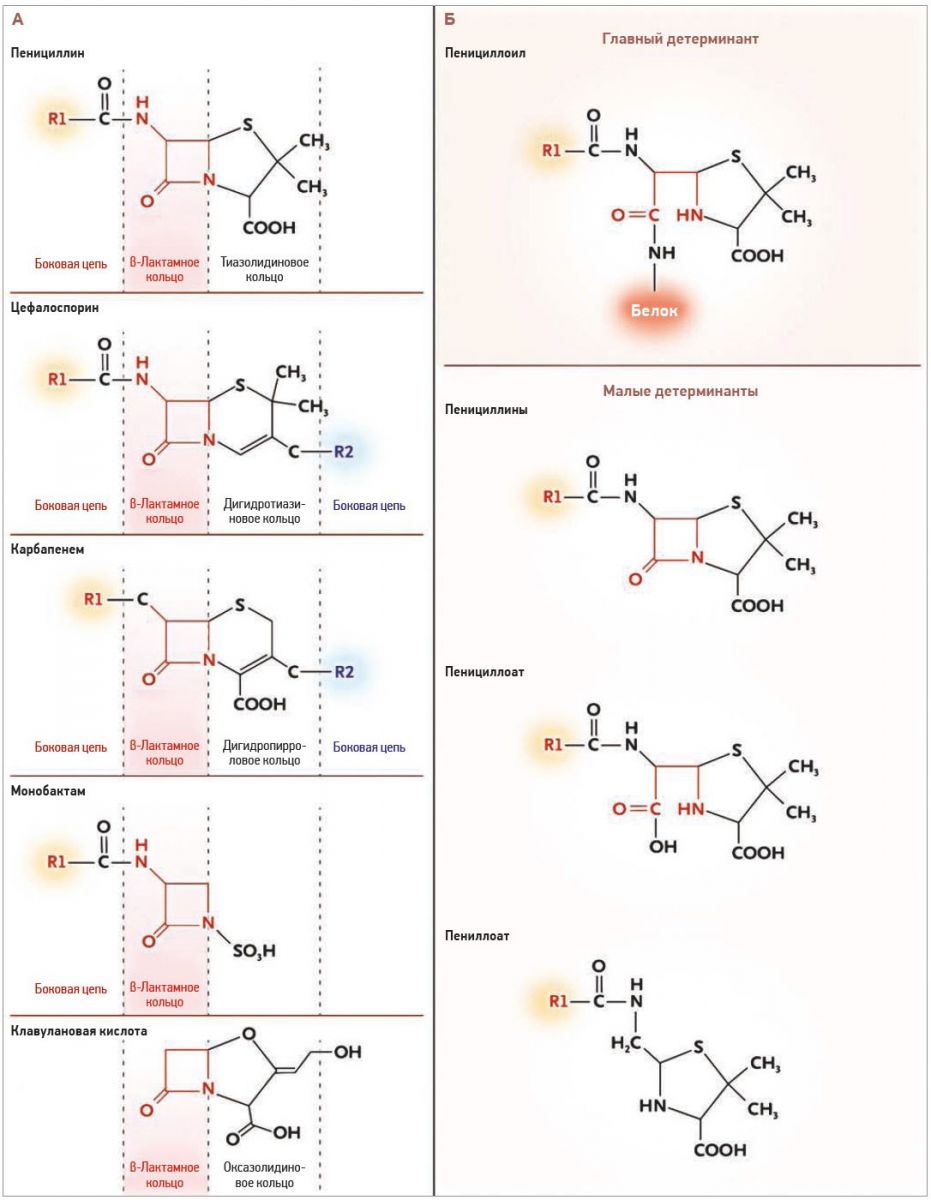
В отличие от других β-лактамов пенициллины имеют тиазолидиновое кольцо, а в отличие от цефалоспоринов и карбапенемов они лишены R2 или других дополнительных боковых цепей (рис. 1А). Боковые цепи пенициллинов и цефалоспоринов І поколения менее сложны, чем боковые цепи цефалоспоринов последних поколений; в первоначальных исследованиях зафиксировано >5% перекрестных реакций между пенициллинами и цефалоспоринами. Вероятным объяснением данного факта является контаминация ранних препаратов цефалоспоринов пенициллинами. В настоящее время не более 2% пациентов с положительными результатами кожных проб с многочисленными внутрикожными реагентами имеют аллергическую реакцию на цефалоспорины, за исключением лиц с аллергией на аминопенициллины, но не на бензилпенициллин, пенициллин VK, другие пенициллины. Такая селективная аллергия на аминопенициллины нечасто регистрируется в США, но, вероятно, имеет место в 1/3 случаев АП в Южной Европе, где 25-25% больных с селективной аллергией на аминопенициллин имеют перекрестную аллергию на аминоцефалоспорины. У 99% пациентов с отягощенным анамнезом в отношении АП кожные тесты и провокационная проба с карбапенемом ассоциируются с сопоставимым профилем побочных эффектов. По всей видимости, отсутствуют иммунологические или клинические перекрестные реакции между пенициллинами и монобактамом азтреонамом; однако зафиксированы реакции при приеме азтреонама у больных с аллергией на цефтазидим, что, вероятно, обусловлено наличием общей боковой цепи R1.
Рис. 1. Структура пенициллина и β-лактамов, главного и малых детерминантов пенициллина
Панель А демонстрирует, что пенициллин и β-лактамы имеют в структуре сходное β-лактамное кольцо (розовый цвет), отличаясь при этом соседними кольцами и боковыми цепями R-группы: цепью R1 (в положении C7
Механизмы аллергии на пенициллин
Пенициллины представляют собой небольшие молекулы; установлено, что они ковалентно связываются с белками в плазме крови, образуя комплексы гаптена с носителем (рис. 1Б). β-Лактамное кольцо связывается с остатками лизина в сывороточных белках, а при соединении с матриксом полилизина образуется главный антигенный детерминант – пенициллоил полилизин (рис. 1Б). Гаптенизация из ковалентной связи с карбоксилом и тиоловыми группами приводит к созданию нескольких малых детерминантов (рис. 1Б). Гаптен-прогаптеновая модель объясняет немедленную, или антитело-опосредованную, гиперчувствительность к пенициллину (реакции Гелла-Кумбса I, II и III типа; рис. 2). В IgE‑опосредованных реакциях дендритные клетки связываются и поглощают пенициллин-связанные белки для презентации наивным CD4+ T‑клеткам (Т‑клетки хелперы типа 0). В присутствии интерлейкина (ИЛ) 4 наивные Т‑клетки превращаются в пенициллин-специфические Т‑хелперы 2 типа (Th2), которые затем продуцируют ИЛ‑4 и ИЛ‑13, индуцирующие дифференцировку B‑клеток в плазматические клетки, секретирующие пенициллин-специфические IgE, связывающиеся, в свою очередь,
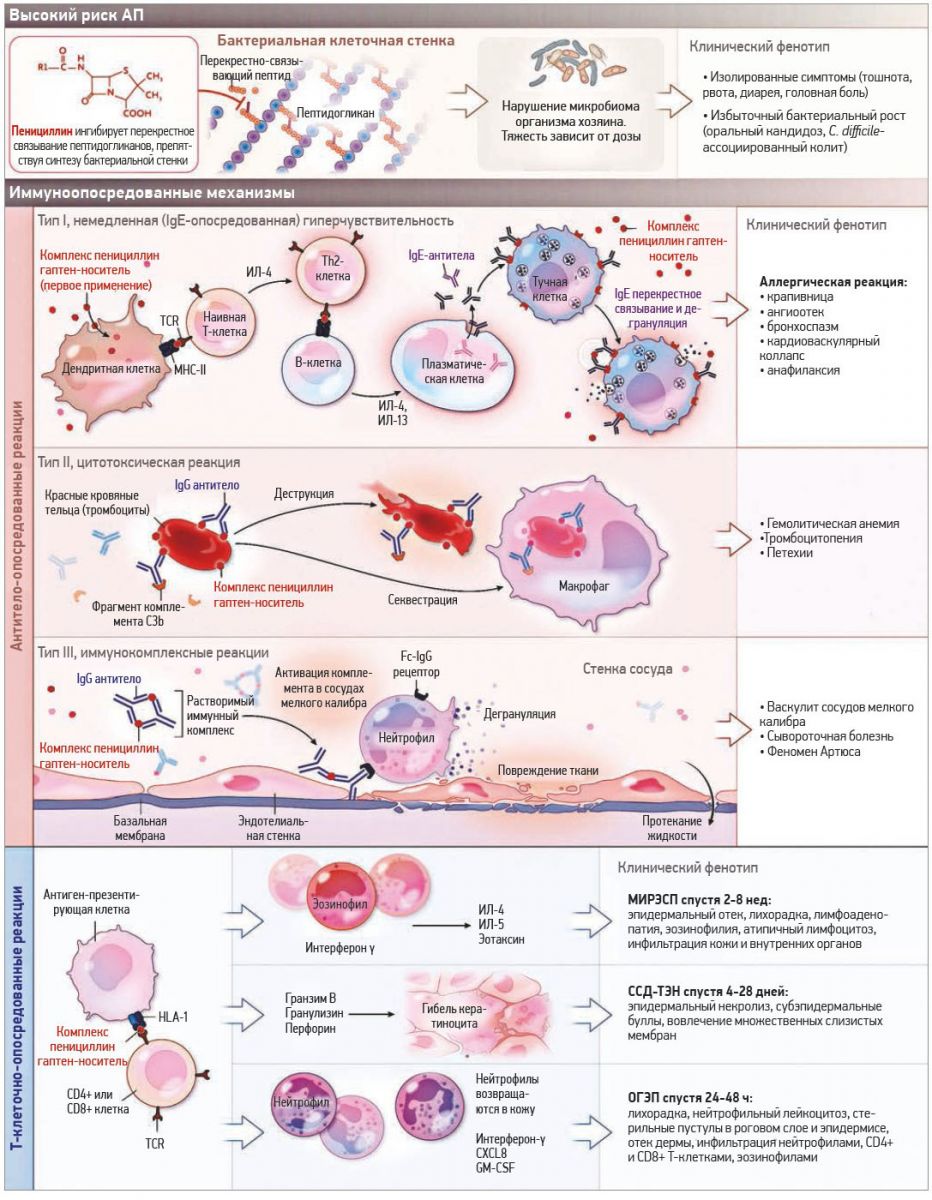
Рис. 2. Клинические проявления и механизмы развития побочных реакций при приеме пенициллинов
Пенициллин ингибирует синтез бактериальных клеток и специфических бактериальных мишеней; он воздействует на микробиом организма-хозяина и может спровоцировать избыточный бактериальный рост
Отсроченные реакции (рис. 2) часто объясняются моделями, предусматривающими нековалентное связывание, например моделью фармакологического взаимодействия/изменения специфичности пептида HLA. Общие фенотипы АП включают в себя реакции, развивающиеся в течение 1-6 ч после воздействия (крапивница, анафилаксия), и реакции, возникающие позже 6 ч от момента приема одной/нескольких доз препарата (макулопапулезная экзантема). К отсроченным Т‑клеточным опосредованным реакциям с системными проявлениями относят тяжелые кожные реакции: ОГЭП, МИРЭСП, ССД-ТЭН (рис. 2).
Диагноз IgE‑опосредованной АП
Спустя много лет широкого клинического применения антибиотиков пенициллинового ряда идентифицированы антигенные детерминанты пенициллина для определения популяции пациентов высокого риска развития аллергических реакций и анафилаксии. Первоначально в качестве диагностического средства использовался главный детерминант (пенициллоил полилизин), являющийся пенициллоилом, связанным с лизином для стабилизации; использование смеси малых детерминантов с этой целью началось в начале 1960-х гг. (рис. 1Б). В проспективном исследовании (1971) анализировали применение пенициллиновых кожных проб с пенициллоилом полизином и смесью малых детерминантов у непроизвольно отобранных стационарных больных, имевших показания для приема пенициллина. Идентифицировано 54 пациента с отягощенным анамнезом на гиперчувствительность к пенициллину, но с отрицательными кожными пробами; всем больным проводилась терапия пенициллином. Впоследствии только у 1 пациента развилась аллергическая реакция (крапивница и артралгии в течение 24 после введения препарата). На основании результатов этого и других исследований положительное прогностическое значение кожных проб с пенициллином с вышеуказанными реагентами составляет 50-75%, отрицательное прогностическое значение превышает 93%.
Пенициллиновые кожные пробы для IgE‑опосредованных реакций
Медикаментозная провокация с пенициллином считается эталонным тестом для оценки толерантности. Провокации могут проводиться посредством увеличения дозы препарата с течением времени (например, 1/10 дозы каждые 30 мин, через 1 ч – полная доза) или введением одной полной дозы с последующим наблюдением в течение 1 ч. В большинстве недавно опубликованных исследований, изучавших пенициллиновые кожные пробы, анализировали их отрицательное прогностическое значение. В настоящее время отрицательное прогностическое значение полного набора главного и малых детерминантов оценивается примерно в 98%, частота ложноотрицательных / легких кожных реакций после пенициллиновой провокации составляет 2-3%.
В Европе и Австралии селективная сенсибилизация к аминопенициллинам, клавулановой кислоте у пациентов с отрицательными результатами кожных проб с применением пенициллоила полизина и смеси малых детерминатов регистрируется несколько чаще (здесь все эти реагенты коммерчески доступны), чем в США. Реакции, обусловленные боковыми цепями, менее распространены в США. Однако при использовании панели малых детерминантов амоксициллина можно получить более достоверные результаты обследования пациентов высокого риска (рис. 1Б); набор для полного тестирования в настоящее время исследуется Управлением по контролю качества продуктов питания и лекарственных средств США (FDA). В отсутствие повсеместной доступности этих реагентов проведение провокационной пробы с амоксициллином после получения отрицательного результата кожной пробы с пенициллоилом полилизином и бензилпенициллином считается приемлемым методом изучения вероятности возникновения IgE‑опосредованной реакции на амоксициллин и другие пенициллины (пациенты с тяжелыми или недавними IgE‑опосредованными реакциями исключаются из тестирования).
Тестирование для обнаружения отсроченной АП
Кожные тесты для выявления отсроченных реакций на пенициллины включают проведение накожной пробы, отсроченной инъекции и внутрикожной пробы (рис. 3).
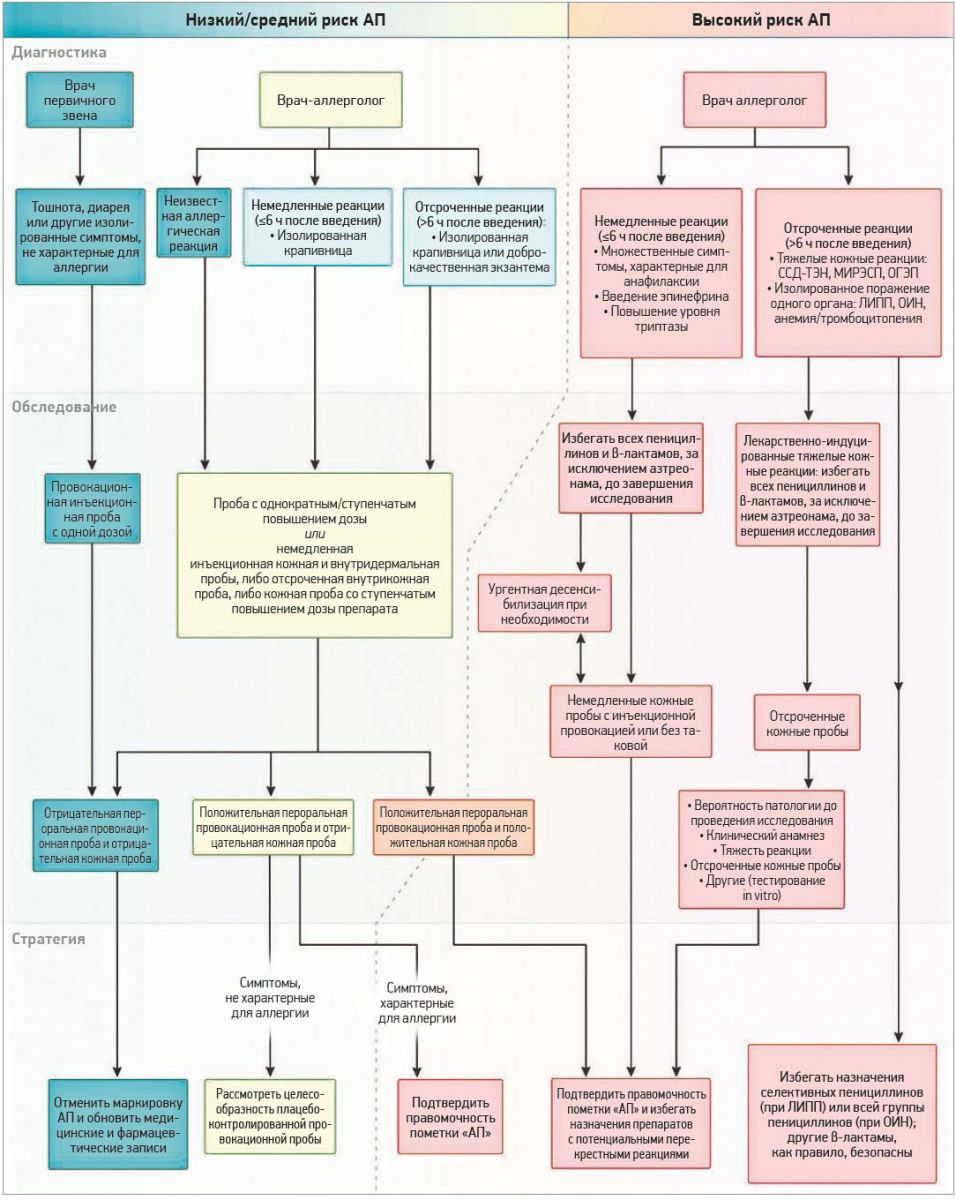
Рис. 3. Стратегия исключения АП и оценки риска безопасности препарата
Определение риска может облегчить обследование пациентов, в медицинских картах которых есть пометка «АП». Описаны нюансы ведения пациентов с низким (синий), средним (желтый) и высоким (красный) риском. Стратегия исключения АП у пациентов низкого и среднего риска: к пациентам низкого риска относят больных с отягощенным анамнезом по появлению изолированных жалоб после применения пенициллина (тошнота, понос, головная боль), а также больных с отдаленной реакцией / неуточненными анамнестическими данными в отношении АП. К пациентам низкого/среднего риска относят больных с изолированными симптомами (немедленная/отсроченная крапивница, легкая/среднетяжелая отсроченная экзантема). При получении отрицательных результатов кожных проб и пероральной провокационной пробы пометку об АП с медицинской карты можно удалить. Пациентов низкого риска с отрицательными кожными тестами и положительной пероральной провокационной пробой следует стратифицировать на основании результатов пероральной провокационной пробы. Стратегия безопасного приема лекарства у больных высокого риска с немедленными реакциями и множественными симптомами, которые свидетельствуют о тяжелой IgE-опосредованной реакции / анафилаксии (крапивница, ангионевротический отек, гиперемия, обструктивный синдром, гипотензия): к больным высокого риска относят пациентов с задокументированным повышением уровня триптазы и лиц, которым вводили эпинефрин. Если до формального завершения обследования на аллергию возникла необходимость использовать пенициллин или другой β-лактам как препарат выбора, следует провести десенсибилизацию. К отсроченным реакциям высокого риска относят тяжелые кожные реакции (МИРЭСП, ССД-ТЭН, ОГЭП) и реакции со стороны отдельных органов: ЛИПП, ОИН, гематологическую патологию (анемия/тромбоцитопения). В случае тяжелых лекарственно-индуцированных кожных реакций следует избегать применения всех β-лактамов, за исключением азтреонама. При изолированном поражении органов рекомендован персонифицированный подход, поскольку может иметь место селективная реакция на конкретный препарат или класс лекарственных средств (ЛИПП на флуклоксациллин, ОИН на полусинтетический пенициллин).
Пенициллин и его главный, малые антигенные детерминанты проникают в эпидермис (при проведении накожного теста, кожной инъекционной пробы) или дерму (внутрикожный тест) и взаимодействуют ковалентно/нековалентно с белками кожи, формируя антигенные конъюгаты, которые распознаются антиген-презентирующими клетками, представляющими основной комплекс гистосовместимости I или II типа. Впоследствии это приводит к пролиферации CD4+ Т‑клеток и/или CD8+ T-клеток, способствуя локальному высвобождению цитокинов и развитию воспалительной реакции.
В рамках проспективного 3-летнего многоцентрового исследования определяли чувствительность аппликационной кожной пробы в идентификации дефекта, вызвавшего тяжелые кожные лекарственно-индуцированные реакции; установлено, что чувствительность отсроченного внутрикожного теста может превосходить таковую аппликационной кожной пробы, особенно для макулопапулярной экзантемы, МИРЭСП, ОГЭП. Аппликационный тест имеет малую чувствительность для ССД-ТЭН (<40%), а отсроченное внутрикожное тестирование не рекомендовано в связи с наличием сообщений о развитии первоначальных аллергических реакций.
Изучение in vitro отсроченных реакций доступно только в научно-исследовательских или специализированных центрах, их чувствительность и специфичность зависят от использованного медикамента и выбранного теста. Данные исследования проводят, воздействуя исследуемым препаратом на лимфоциты пациента. К таким исследованиям относят тест трансформации лимфоцитов (в ходе которого измеряют пролиферацию Т‑клеток пациента в течение 5-7 дней), иммуносорбентный тест с иммобилизированными ферментами (ELISPOT; выявляют антиген-специфичные, цитокин-продуцирующие клетки после 24 ч инкубации с полиморфноядерными кровяными клетками). Оба теста проводятся в присутствии исследуемого препарата.
Оптимальная клиническая тактика для нивелирования АП
Различные методы использовались для преодоления АП как у стационарных, так и у амбулаторных больных (рис. 3). Они проводились с участием клинических фармацевтов, прошедших специальное обучение, и пациентов с отягощенным анамнезом в отношении АП и высокой вероятностью назначения антибиотиков, а также с применением специфических алгоритмов для обнаружения АП, пенициллиновых кожных тестов, телемедицинских консультаций (в связи с нехваткой аллергологов). Систематический обзор стационарного определения АП, в том числе в условиях отделений интенсивной терапии, подтвердил безопасность и эффективность данного подхода в преодолении АП; в 95% случаев получены отрицательные результаты кожных проб. Относительно недавно разработаны руководства для практикующих врачей (не аллергологов) по использованию антибиотиков у пациентов, в медицинских картах которых имеется пометка «АП». Эти рекомендации предусматривают оценку риска на основании данных клинического анамнеза, времени и фенотипа реакции, ассоциированных заболеваний.
Снятие маркировки «АП» проводится по результатам перорального/внутривенного введения тестовых доз, провокаций у пациентов низкого риска и по результатам кожных тестов у больных высокого риска. В когортном исследовании, сравнивавшем пенициллиновые кожные тесты, компьютеризованное ведение с обычной тактикой, показано, что использование обоих указанных подходов сопровождалось более частым применением цефалоспоринов III и IV поколения. Такие способы преодоления АП способствуют рационализации антибактериальной терапии, но не приводят к систематическому удалению пометки «АП».
Обследование на АП в амбулаторных клиниках и использование предупредительных пометок в электронных медицинских записях облегчают предоперационную оценку АП. Проведение провокации амоксициллином без предварительного выполнения пенициллиновых кожных тестов ассоциировалось с низкой заболеваемостью в когорте морских пехотинцев с отягощенным анамнезом по селективной АП, а также у детей с анамнестически низким риском АП. Необходимо проведение более масштабных исследований для оценки безопасности этого подхода в других популяциях.
Десенсибилизация к пенициллину
Пациенты с IgE‑зависимой АП (в том числе с анафилаксией), нуждающиеся в приеме пенициллина как препарата первой линии терапии, являются кандидатами для проведения быстрой десенсибилизации (рис. 3, табл.).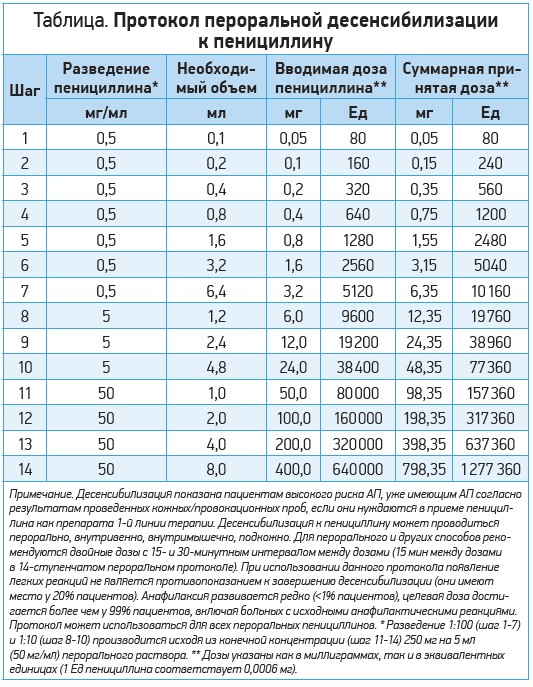
Первая десенсибилизация к пенициллину (приписываемая О’Доновану и осуществленная во время Второй мировой войны) проведена посредством добавления возрастающего количества перорального пенициллина в молоко до достижения целевой дозы без возникновения побочных эффектов у солдата, ранее имевшего анафилактическую реакцию на внутримышечное введение пенициллина. С тех пор внутримышечную, внутривенную и пероральную десенсибилизацию успешно проводили многим пациентам. Механизмы быстрой десенсибилизации изучались в экспериментальных исследованиях (в линиях клеток, у лабораторных животных), что привело к разработке клинических протоколов. В 2009 г. Legere и соавт. успешно десенсибилизировали 15 пациентов с муковисцидозом с объемом форсированного выдоха
Выводы
Распространенность как IgE‑опосредованных, так и не-IgE‑опосредованных реакций не возросла на протяжении последних 50 лет, а маркировка «АП» имеет серьезные последствия как для пациента, так и для общественного здравоохранения. Несмотря на то что многие пациенты имеют пометку «АП» в медицинских картах, более 95% из них могут безопасно принимать пенициллин при условии проведения надлежащего и безопасного обследования. АП сохраняется с течением времени; использование чувствительных и специфических методик для выявления пациентов с истинной АП должно стать приоритетом для органов здравоохранения, который может быть реализован посредством специальных десенсибилизирующих алгоритмов и программ. Со временем можно ожидать, что удаление маркировки у пациентов, не имеющих больше АП, позволит контролировать использование альтернативных дорогостоящих антибиотиков и уменьшить ассоциированную заболеваемость, смертность, снизить рост микроорганизмов, резистентных к пенициллину и β-лактамам. Защита пациентов, действительно имеющих АП, при помощи точной диагностики, правильной маркировки и, при необходимости, десенсибилизации должна стать следующим шагом на пути к повышению безопасности персонифицированной медицины и качества медицинской помощи. Тщательно анализируя данные анамнеза и определяя степень риска с целью выявления больных без IgE‑опосредованной аллергии, пациентов низкого риска, лица, оказывающие медицинские услуги, могут сыграть ключевую роль в смягчении последствий огромного индивидуального и общественного бремени, ассоциированного с АП.
Статья печатается в сокращении.
Castells M., Khan D. A., Phillips E. J. Penicillin Allergy. N Engl J Med 2019;381:2338-51.
Перевела с англ. Татьяна Можина
Медична газета «Здоров’я України 21 сторіччя» № 1 (470), січень 2020 р.
СТАТТІ ЗА ТЕМОЮ Алергія та імунологія
Серед препаратів, які мають велику доказову базу щодо лікування пацієнтів із захворюваннями дихальних шляхів з алергічним компонентом, особливий інтерес становлять антагоністи лейкотрієнових рецепторів (АЛТР). Ці препарати мають хорошу переносимість у дорослих та дітей, а також, на відміну від інгаляційних кортикостероїдів (ІКС), характеризуються високим комплаєнсом, тому посідають чільне місце в лікуванні пацієнтів із респіраторною патологією. У лютому відбувся міждисциплінарний конгрес із міжнародною участю «Життя без алергії International» за участю провідних вітчизняних міжнародних експертів. Слово мав президент Асоціації алергологів України, професор кафедри фтизіатрії та пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук Сергій Вікторович Зайков із доповіддю «Місце АЛТР у лікуванні пацієнтів із респіраторною патологією». ...
Розбір клінічного випадку...
Організм людини – це складна жива система, функціонування якої визначається безліччю змінних і задіює величезну кількість механізмів. Зовнішні і внутрішні чинники здатні порушувати регуляцію її діяльності. Однак є механізми, які допомагають ефективно усувати «поломки» в організмі і нормалізувати його стан. Така здатність має назву біорегуляції. Основою біорегуляційної медицини є комплексні біорегуляційні препарати, серед яких одним із найвідоміших є Ехінацея Композитум С. ...
Проблема гострих запальних захворювань верхніх дихальних шляхів (ВДШ), гострого риносинуситу (ГРС) зокрема, є однією з найактуальніших у сучасній клінічній медицині. Останніми роками спостерігають зростання частоти захворювань носа і приносових пазух, що проявляється збільшенням як абсолютних (захворюваності та поширеності), так і відносних (частка в структурі оториноларингологічної патології) показників. В Україні поширеність гострих ринітів, риносинуситів та ринофарингітів сягає 489,9 випадку на 10 тис. населення, а захворюваність – 5-15 випадків на 1 тис. населення залежно від сезону. Такі хворі становлять 60-65% амбулаторних пацієнтів лікарів-отоларингологів. Уніфікований клінічний протокол первинної та спеціалізованої медичної допомоги (УКПМД) призначений забезпечити організацію надання медичної допомоги пацієнтам із ГРС на всіх етапах медичної допомоги для своєчасного виявлення, профілактики та лікування ГРС. ...