Нові можливості лікування хронічного бактеріального простатиту у хворих, інфікованих Trichomonas vaginalis
 Простатит – найбільш поширене урологічне захворювання серед чоловіків віком до 50 років. При цьому значну роль в хронізації запального процесу в простаті відіграє інфікованість Trichomonas vaginalis.
Простатит – найбільш поширене урологічне захворювання серед чоловіків віком до 50 років. При цьому значну роль в хронізації запального процесу в простаті відіграє інфікованість Trichomonas vaginalis.
Хоча б один раз у житті 35‑50% чоловіків скаржились на симптоми нижніх сечових шляхів, що є характерними для простатиту. У 8‑11% європейців та 3‑16% американців простатит – це рецидивуюче захворювання. У даний час використовується класифікація простатиту, запропонована 1995 р. Американським Національним інститутом здоров’я та Національним інститутом діабету, травлення і хвороб нирок (NIDDK-NIH) (NIDDK Workshop Committee, 1995), що ґрунтується на розділенні всіх форм простатиту в залежності від наявності або відсутності бактеріального агента, лейкоцитів у секреті передміхурової залози (ПЗ) та клінічних проявів. Відповідно до цієї класифікації виділяють чотири категорії простатиту: гострий бактеріальний простатит, бактеріальний хронічний простатит (ХП), ХП/синдром хронічного тазового болю (СХТБ) та безсимптомний простатит [1, 19, 23, 26, 33].
Незважаючи на широку розповсюдженість використання класифікації NIDDK-NIH, вона не всюди є визнаною. Більш новий принцип класифікації, UPOINT, заснований на клінічному фенотипі ХП/СХТБ при прогнозах поліпшення стану пацієнтів внаслідок лікування та ведення хвороби. UPOINT розшифровується як сечовий (Urinary), психосоціальний (Psychosocial), органоцентричний (Organ-centric), інфекційний (Infection), неврогенний/системний (Neurogenic/systemic), больовий (Tenderness) [30, 34, 35]. Цю систему використовують для класифікації ХП/СХТБ задля визначення їхнього унікального клінічного фенотипу для подальшого вибору терапії. Виявлено, що кількість позитивних доменів UPOINT корелює із тяжкістю та тривалістю симптомів простатиту, оціненого за шкалою NIH-CPSI.
Застосування класифікації UPOINT та виділення клінічного фенотипу ХП/СХТБ пацієнтів дають можливість використовувати мультимодальну патогенетичну терапію для кожного із шести окремих доменів, яка, за даними декількох незалежних досліджень, приводить до значного зменшення вираженості клінічних симптомів у 75‑84% хворих [30, 32, 34]. «Незважаючи на те що золотого стандарту лікування не існує, міждисциплінарний підхід в мультимодальній терапії дає хворому на ХП/СХТБ шанс на полегшення симптомів», – С. Р. Smith [35].
Урогенітальний трихомоніаз (УТ) – широко розповсюджена інфекція, що передається статевим шляхом (ІПСШ), збудником якої є Trichomonas vaginalis, – найпростіший одноклітинний мікроорганізм, пристосований у процесі еволюції до паразитування в органах сечостатевої системи людини [18]. Трихомоніаз є поширеним захворюванням та посідає перше місце серед ІПСШ [7].
До всесвітньої бази даних щорічно надходять повідомлення про 170‑200 млн нових випадків зареєстрованого трихомоніазу [3‑5, 9]. Частота інфікування в економічно розвинених країнах становить 2‑10%, а в країнах, що розвиваються, – 15‑40%. Серед хворих зі змішаною урогенітальною інфекцією носії трихомонад складають 40‑50%, при тому що у 50% випадків захворювання мають безсимптомний перебіг. Слід мати на увазі, що носії трихомоніазу призводять до епідеміологічного розповсюдження збудника серед сексуальних партнерів [14, 37, 38]. В Україні офіційний показник захворюваності на УТ – 1263,7 випадку на 100 тис. чоловік, фактичний показник у 5 разів вище і становить близько 6% від загальної чисельності населення або 12% сексуально активного населення репродуктивного віку [10].
Чимало авторів звертають увагу на високу асоціацію трихомонадної інфекції з такими захворюваннями, як хламідіоз, міко-уреаплазмоз, бактеріальний вагіноз, ВІЛ-інфекція, СНІД, рак шийки матки [21, 24, 28].
Встановлена важлива роль феномена тропності трихомонад до ПЗ з облігатною колонізацією простатичних структур при хронічному процесі в уретрі, що має підтвердження їх наявності в біоптатах ПЗ. Останні зазвичай отримують під час гістологічної верифікації випадків доброякісної гіперплазії ПЗ (ДГПЗ) або раку ПЗ [27, 29]. В Україні були проведені інноваційні наукові дослідження, що були присвячені ролі трихомонадної інфекції в індукції і пролонгації хронічного запалення тканини ПЗ із формуванням гіперпластичного компонента та його можливого впливу на процеси ДГПЗ [17]. Підтвердження таких даних можна знайти в зарубіжній літературі, де також відмічено підвищенння рівня зустрічальності трихомонад у тканині ПЗ, за наявності ДГПЗ, з можливістю індукції запальної проліферації [27].
Згідно з D. Mitteregger et al. (2012), тканину ПЗ можна розглядати як екологічну нішу для T. vaginalis. Так, за результатами досліджень біоптатів у 86 чоловіків з ДГПЗ було встановлено, що у 34% з них ознаки неінфекційного запалення були асоційовані з позитивними результатами полімеразної ланцюгової реакції (ПЛР) на трихомоніаз [29].
Однією з особливостей T. vaginalis є їхня виняткова здатність до асоціації з іншими збудниками ІПСШ, тому УТ досить часто відзначається перебігом у складі мікст-інфекцій (разом із хламідійною, уреаплазмовою, мікоплазмовою інфекціями та гонореєю), що ускладнює його лікування і спричиняє виникнення посттрихомонадних ускладнень. Часто трихомонади виконують резервуарну функцію, зберігаючи цих збудників у незмінній формі (ендоцитобіоз), а деякі з них всередині T. vaginalis навіть активно розмножуються [12, 13, 15].
T. vaginalis уражає сечовипускний канал, сім’яні пухирці, передміхурову залозу. УТ призводить до таких ускладнень у чоловіків: баланіт, баланопостит, уретрит, парауретрит, куперит, епідидиміт, простатит, везикуліт, цистит [11]. Складність клініко-лабораторної діагностики бактеріальної інфекції полягає в наявності одночасно 2‑3 або більше патогенних збудників. Також складність виявлення захворювання у чоловіків пов’язана з особливостями будови статевої системи. При трихомонадному ураженні простатичного відділу уретри і ПЗ за рахунок бар’єрної функції мембранозного сфінктера не завжди вдається виявити збудника в екскретах [2].
Вибір методів досліджень при діагностиці ІПСШ залежить від багатьох факторів: даних анамнезу, результатів фізикальних досліджень, попередньо проведених досліджень (нативний мазок), переліку лабораторних досліджень, що були проведені в клініці, їх вартості, матеріальних можливостей хворого. Отже, вибір методів, алгоритм обстеження повинні не тільки відповідати чинній нормативній базі (протоколи, стандарти), а й також бути індивідуальними для кожного пацієнта. На якість діагностичного процесу звичайно впливає підготовка хворого та техніка забору матеріалу.
Для того щоб отримати більш достовірні та надійні дані, необхідно дотримуватися наступних правил:
- негативний результат будь-якого дослідження не виключає наявності трихомонад;
- дослідження отриманого матеріалу слід проводити одночасно всіма доступними методами;
- для оцінювання необхідно використовувати не тільки уретральні виділення та секрет ПЗ, але й осад свіжовипущеної сечі, секрет бульбоуретральних залоз, сперму [6, 8].
Відповідно до рекомендацій Європейської асоціації урології (EAU) при лікуванні ХП антибіотики рекомендовано приймати протягом 4‑6 тиж після встановлення діагнозу [23], а згідно з рекомендаціями Американської і Канадської урологічних асоціацій, – протягом 6‑12 тиж (рис. 1) [30]. При цьому необхідні відносно високі дози препаратів, і перевага надається пероральній формі прийому (GR: B). Фторхінолони, такі як ципрофлоксацин і левофлоксацин, вважаються препаратами вибору через їх сприятливі фармакокінетичні властивості (GR: В), безпечність та антибактеріальну активність у відношенні до грамнегативних збудників, у т.ч. Pseudomonas aeruginosa [1, 19, 26]. Крім того, левофлоксацин є активним щодо грампозитивних і атипових патогенів, таких як хламідії та генітальні мікоплазми (GR: B).
Останніми роками активно обговорюється проблема зростання резистентності уропатогенів до антибіотиків різних груп: частота мікробіологічної ерадикації при хронічній хворобі нирок для ципрофлоксацину становить 40‑70%, для поєднання азитроміцину та ципрофлоксацину – 62‑77%, для доксицикліну – 77% [20‑25, 36].
Навіть антибіотики однієї групи можуть мати різну ефективність. У порівняльному дослідженні за участю пацієнтів із хронічною хворобою нирок (n=408) було доведено, що левофлоксацин є більш ефективним, ніж ципрофлоксацин, із точки зору частоти бактеріальної ерадикації та клінічного поліпшення [39]. Ряд авторитетних джерел, у т.ч. EAU та Американська асоціація з антимікробної терапії, виступають проти широкого застосування фторхінолонів, пояснюючи це прогресуючим збільшенням числа резистентних штамів Escherichia coli, що також спостерігається в нашій країні [16].
Одним із шляхів вирішення проблеми є використання комбінацій фторхінілонів із протимікробними засобами інших груп, що зумовлює кумуляцію ефекту та розширення спектра протимікробної дії [20, 39].
Сучасні методи лікування хворих на трихомоніаз засновані на використанні специфічних протитрихомонадних засобів. Лікуванню підлягають усі пацієнти, у яких було виявлено T. vaginalis, незалежно від наявності або відсутності у них запальних явищ, а також особи із запальними процесами, у яких при обстеженні трихомонади не були виявлені, але найпростіші наявні у їхніх статевих партнерів або джерел інфікування.
Враховуючи зростаючу резистентність мікроорганізмів до сучасних протимікробних засобів, а також схильність T. vaginalis до ендоцитобіозу, чималий інтерес викликає препарат Макмірор. Активною речовиною препарату Макмірор є похідне нітрофурану – ніфуратель.
Дослідження in vivo/in vitro продемонстрували широкий спектр дії ніфурателю проти мікроорганізмів, включаючи інфекції сечостатевої системи, йому також властива антипротозойна та протигрибкова активність. Ніфуратель виступає як антибактеріальний засіб для грамнегативних і грампозитивних аеробних і анаеробних бактерій: Gardnerella vaginalis, E. coli, Shigella, Salmonella spp., Bacillus sp., Proteus spp., Klebsiella pneumoniae, T. vaginalis.
Ніфуратель не спричиняє перехресної резистентності мікроорганізмів до інших препаратів, що застосовують при лікуванні інфекцій. Вкрай важливим є те, що за 30 років не виявлено жодного випадку резистентності до ніфурателю.
Слід зауважити, що ніфуратель добре проникає в тканину ПЗ, що дає можливість для ефективного використання цього препарату в лікуванні ХП [19].
Варто зазначити, що Макмірор активно використовується в країнах ЄС (під назвою Nifuratel).
Враховуючи вищезазначене, метою проведеного дослідження було встановлення ефективності Макмірору в лікуванні хронічного бактеріального простатиту у хворих, інфікованих T. vaginalis. Для підвищення ефективності лікування і скорочення його тривалості було вирішено застосовувати ніфуратель (Макмірор) у комбінації з левофлоксацином у відповідності до рекомендацій EAU та Американської асоціації з антимікробної терапії.
Матеріали та методи
У дослідженні взяли участь 64 хворих на хронічний бактеріальний простатит, з яких 34 пацієнти основної групи (ОГ) як основний препарат отримували Макмірор, який комбінували з левофлоксацином; 30 хворих групи порівняння (ГП) – комбінацію левофлоксацину та препарату нітроімідазолової групи. Тривалість лікування – 15 днів.
Макмірор призначали дозою 400 мг (2 таблетки) 3 рази на добу у комбінації з левофлоксацином (500 мг/доб per os) протягом 15 днів. До і після лікування оцінювали загальний стан хворих, проводили мікроскопічне, бактеріологічне та ПЛР-дослідження секрету ПЗ, ультразвукове дослідження (УЗД) простати. Лабораторну діагностику трихомоніазу здійснювали за допомогою молекулярно-біологічного методу – ПЛР-дослідження секрету ПЗ на T. vaginalis та мікробіологічного дослідження уретрального секрету ПЗ на T. vaginalis (методика In Рouch TV). Обстеження проводили до лікування та через місяць після його завершення.
Лікування досліджуваним препаратом проводилося на фоні комплексної терапії, що включало імуномодулятори, біопептиди, системну ензимотерапію, індуктори інтерферону, фізіотерапію.
Переносимість Макмірору оцінювали в балах на підставі суб’єктивних відчуттів пацієнта та об’єктивних даних, отриманих дослідником у процесі лікування:
- 1 бал – дуже хороша переносимість (побічні ефекти не відзначаються);
- 2 бали – хороша (спостерігаються незначні побічні ефекти, що не заподіюють серйозних проблем пацієнту і не потребують відміни препарату);
- 3 бали – задовільна (мають місце побічні ефекти, що негативно впливають на стан пацієнта, але не вимагають відміни препарату);
- 4 бали – незадовільна (виникає небажаний побічний ефект, який має значний негативний вплив на стан хворого і вимагає відміни препарату);
- 5 балів – вкрай незадовільна (побічний ефект, що вимагає відміни препарату і надання невідкладної медичної допомоги).
Вік обстежених коливався в межах від 19 до 47 років, склавши в середньому 32±4,1 року. Тривалість захворювання становила від 1 до 13 років. У хворих обох груп мали місце такі клінічні прояви ХП (табл. 1):
- дизурія – у 57 (89%) осіб;
- больові відчуття в промежині і надлобковій ділянці – у 43 (67,2%);
- больові відчуття в поперековій і крижовій ділянці – у 36 (56,3%);
- больові відчуття в ділянці зовнішніх статевих органів, у паху – у 29 (45,3%);
- відчуття печіння в уретрі – у 34 (53,2%);
- нічна полакіурія – у 28 (43,8%);
- порушення статевої функції – у 19 (29,7%).
При пальцевому ректальному дослідженні ПЗ болючість відзначалася у 32 (94±4%) хворих ОГ і у 27 (90±6%) – ГП; неоднорідність структури залози відповідно – у 28 (82±7%) і 25 (83±7%); набряклість простати – у 16 (47±9%) та 11 (37±9%); болючість сім’яних міхурців – у 13 (44±9%) і 11 (37±9%) пацієнтів відповідно (р>0,05).
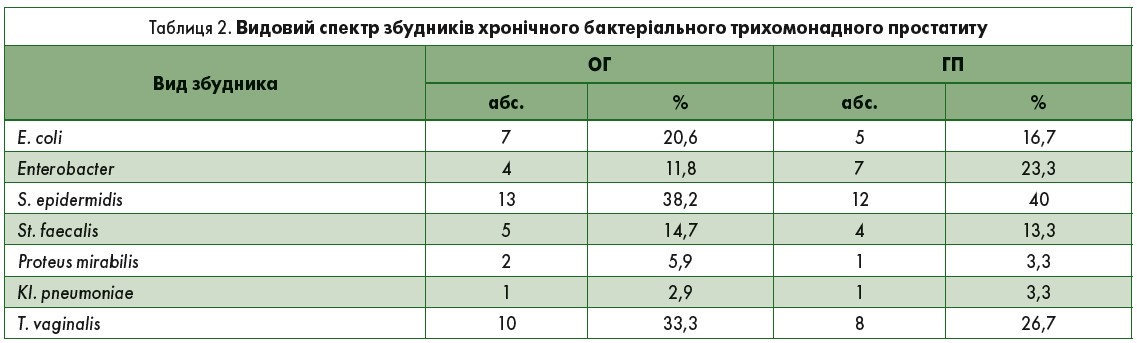
При бактеріологічному дослідженні секрету простати здебільшого виявлено зростання умовно-патогенної сфери, переважно Streptococcus faecalis, Staphylococcus epidermidis, Enterobacter, E. сoli, Proteus mirabilis, T. vaginalis (за методикою In Рouch TV) (табл. 2).
Аналіз результатів дослідження
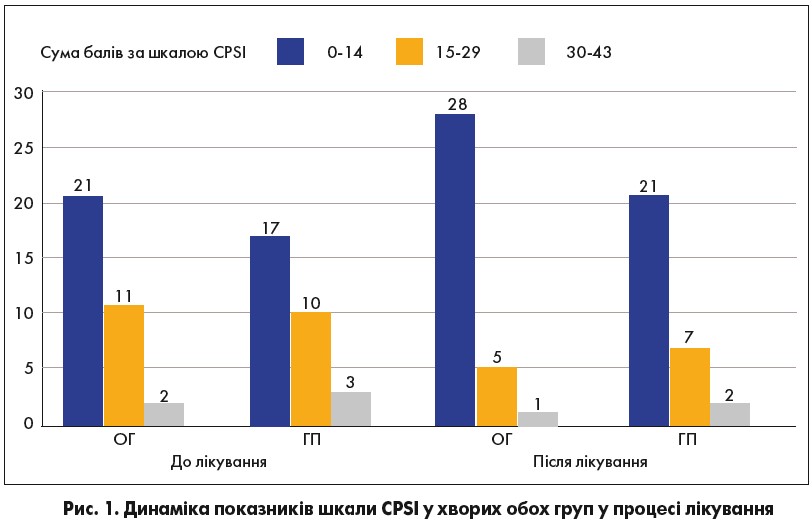
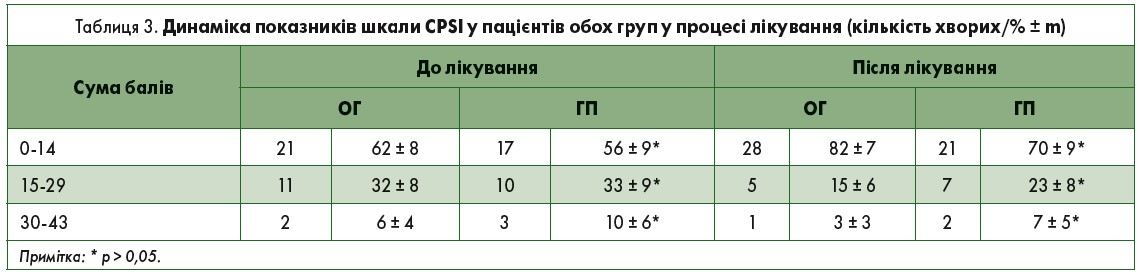
Комплексне лікування хворих обох груп дало позитивний результат у 33 (97,05%) осіб ОГ і 28 (93,3%) – ГП, що знайшло своє підтвердження в позитивній динаміці суми балів за шкалою CPSI (табл. 3).
При оцінюванні стану хворих на 7-му добу після початку лікування відмічено зменшення больових відчуттів у 9 (26±8%) хворих ОГ і у 6 (20±7%) – ГП; дизуричні явища зникли відповідно у 14 (41±9%) та 11 (37±9%); відчуття печіння в уретрі в 11 (32±8%) і 8 (27±8%); кількість нічних сечовипускань зменшилася у 8 (24±7%) і 7 (24±8%) пацієнтів відповідно (р>0,05) (рис. 1).
Після завершення курсу лікування у 30 (88±6%) хворих ОГ зникли всі больові відчуття, дискомфорт при сечовипусканні припинився у 23 (68±8%), а нічна полакіурія – у 15 (44±9%) пацієнтів ОГ. У ГП аналогічні зміни відбувались відповідно у 25 (83±7%), 11 (37±9%) та 6 (20±7%) осіб.
За результатами аналізу секрету ПЗ до лікування і на 7-й день після його початку відзначається достовірна зміна лейкоцитарної реакції в обох групах пацієнтів: із 75±5,1 до 14,2±3,7 лейкоцитів у полі зору в ОГ, з 82,2±4,2 до 18,9±3,6 – в ГП (p<0,05).
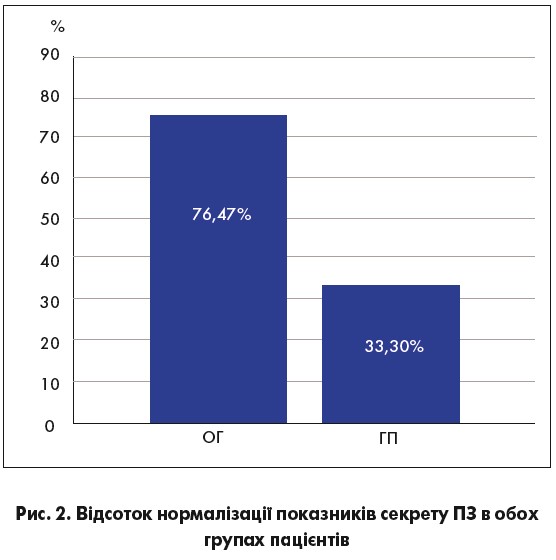
Після завершення лікування нормалізація простатичного секрету спостерігалась у 26 (76,47%) хворих ОГ і у 10 (33,3%) – ГП (p<0,05) (рис. 2).
Після проведеної антибактеріальної терапії було виявлено зростання в секреті ПЗ E. сoli у двох (6,7%) хворих ГП і St. faecalis – в одного пацієнта (2,9%) ОГ.
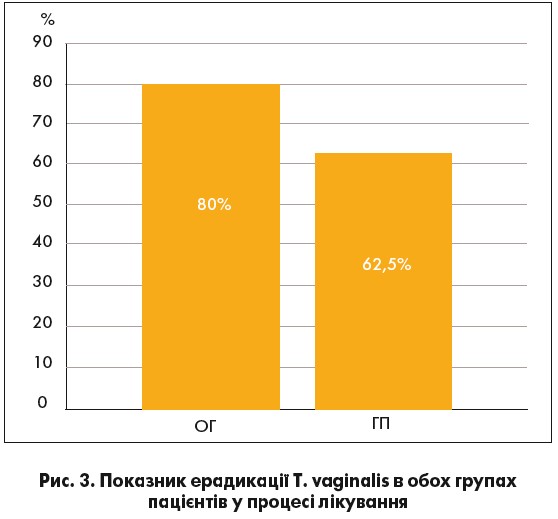
Ерадикація T. vaginalis відбулась у восьми пацієнтів ОГ, що становило 80%, і у п’яти – ГП, або 62,5% (рис. 3).
За даними УЗД ПЗ, істотних змін її обсягу і структури в процесі лікування у чоловіків обох груп не спостерігалося.
Макмірор відноситься до числа препаратів, які добре переносяться, що відмітили 32 (94,1%) пацієнти, вказавши середній бал оцінки 2,3. При більш ретельному аналізі побічних ефектів виявилося, що більшість з них були легкого або середнього ступеня тяжкості і зникали у процесі лікування без будь-якої корекції. При застосуванні Макмірору нудота спостерігалась у двох (6,1%) хворих, запаморочення або головний біль – у двох, шкірний висип у вигляді кропивниці – в одного (3,0%), тахікардія – в одного (3,0%) пацієнта (табл. 4). Інших побічних ефектів у процесі проведеного лікування не відзначалося. На фоні прийому препаратів у ГП диспепсія мала місце у восьми (26,7%) хворих, головний біль – у п’яти (16,7%), алергічний висип – у п’яти (16,7%), тахікардія – у двох (6,7%) чоловіків (р>0,05) (табл. 4). Середній бал оцінки в ГП становив 3,1 (задовільна переносимість).
Таким чином, згідно з вищенаведеними результатами комбінація левофлоксацину з ніфурателем (Макмірор) виявилась більш ефективною, ніж поєднання левофлоксацину з препаратом нітроімідазолового ряду, що підтверджується результатами проведеного клініко-лабораторного дослідження.
Аналізуючи ефективність лікування в обох групах, слід зазначити, що побічні дії медикаментів, які використовувалися в ГП, були більш вираженими та спостерігались у більшої кількості хворих, ніж в ОГ.
Висновки
1. Макмірор (ніфуратель) є високоефективним протимікробним препаратом для комбінованого лікування ХП, що зумовлено його значною (97,1%) клінічною ефективністю, успішною ерадикацією бактеріальної флори та T. vaginalis і доведеною здатністю до нормалізації показників секрету ПЗ.
2. Препарат зручний у застосуванні, має мінімальні побічні ефекти, високий рівень комплаєнтності і добре переноситься хворими.
3. Результати проведеного дослідження дозволяють рекомендувати Макмірор для комплексного лікування хронічного бактеріального простатиту у хворих, інфікованих T. vaginalis.
Література
- Аляев Ю. Г., Глыбочко П. В., Пушкарь Д. Ю. Урология. Российские клинические рекомендации. – М.: ГЭОТАР-Медиа, 2015. – 480 с.
- Беднова В. Н., Погорельский Л. В., Васильев М. М. и др. Тактика обследования и терапии больных инфекционными урогенитальными заболеваниями, осложненными дисбактериозом (пособие для врачей). – М.: Медицина, 1996. – С. 14‑32.
- Горпинченко И. И., Гурженко Ю. Н. Исследование эффективности применения препарата Орнизол у больных с хроническим урогенитальным трихомониазом // Здоровье мужчины. – 2010. – № 3. – С. 198‑200.
- Горпинченко И. И., Романюк М. Г., Корниенко А. М. Терапия метронидазол-резистентного трихомониаза комбинацией ципрофлоксацина и тинидазола // Здоровье мужчины. – 2014. – № 1. – С. 95‑98.
- Гоцуляк О. Л. Урогенитальный хламидиоз, асоциированный с трихомониазом // Новости медицины и фармации. – 2007. – № 1 (205). – С. 15‑17.
- Дерматовенерология: Учеб. пособие / Под ред. В. П. Федотова, А. Д. Дюдюна, В. И. Степаненко. Изд. 2-е, рус. – Днепропетровск; Киев: Изд. Свидлер А. Л., 2011. – 652 с.
- Дюдин А. Д. Полион Н. Н., Бюбюк И. А., Горбунцов В. В., Башмаков Д. Г. Эффективность, переносимость и комплайентность применения секнидазола в комплексном лечении больных урогенитальным трихомониазом // Український журнал дерматології, венерології, косметології. – 2013. – № 3 (50). – С. 144‑148.
- Каденко О. А., Болотюк М. В. Сравнительная характеристика эффективности методов лабораторной диагностики урогенитального трихомониаза (собственные исследования) // Журнал дерматовенерології та косметології ім. М. О. Торсуєва. – 2012. – № 1‑2. – С. 86‑94.
- Коган Б. Г. Урогенитальный трихомониаз: новое решение старой проблемы //Здоров’я України. – 2008. – № 11 (192). – С. 68.
- Корнацька А. Г., Вовк І. Б., Чубей Г. В. Запальні захворювання органів малого таза, спричинені інфекціями, що передаються статевим шляхом // Здоров’я України. – 2012. – № 4 (8). – С. 38, 39.
- Кубанова А. А. и др. Ведение больных с инфекциями, передаваемыми половым путем, и урогенитальные инфекции: Клинические рекомендации. – М.: Деловой экспресс, 2012. – 111 с.
- Кубанова А. А., Рахматулина М. Р. Урогенитальные инфекционные заболевания, вызванные генитальными микоплазмами // Вестник дерматолога и венеролога. – 2009. – № 3. – С. 78‑82.
- Леонтьев И. Г., Леонтьев Д. И. Современные комбинированные препараты при лечении урогенитального трихомониаза и ассоциированных уретрогенных инфекций у мужчин // Клиническая дерматология и венерология. – 2013. – № 3. – С. 63‑68.
- Мельников С. Н. Лечение хронических воспалительных заболеваний половых органов трихомонадно-бактериальной этиологии // Здоровье мужчины. – 2013. – № 1. – С. 162‑163.
- Молочков В. А. Урогенитальный трихомониаз, ассоциированные уретрогенные инфекции (эпидемиология, клиника, диагностика, лечение, профилактика) // Российский журнал кожных и венерических болезней. – 2000. – № 3. – С. 48‑56.
- Научный отчет о результатах многоцентрового исследования динамики антибиотикорезистентности возбудителей инфекций мочевых путей в различных субпопуляциях пациентов. – Смоленск: ДАРМИС, 2011. – 118 с.
- Пасечников С. П., Митченко Н. В., Грицай В. С. Инфицированность больных гиперплазией предстательной железы возбудителями заболеваний, передающихся половым путем // Здоровье мужчины. – 2006. – № 2 (17). – С. 203‑205.
- Рыжих П. Г., Гущин А. Е. К вопросу о лабораторной диагностике урогенитального трихомониаза с учетом концентрации Trichomonas vaginalis в биологическом материале // Клиническая дерматология и венерология. – 2013. – № 5. – С. 44‑48.
- Anothaisintawee T., Attia J., Nickel J. C. et al. Management of chronic prostatitis/ chronic pelvic pain syndrome: a systematic review and network meta-analysis. JAMA 2011; 305 (1): 78‑86.
- Cohen J. M., Fagin A. P., Hariton E. et al. Therapeutic intervention for chronic prostatitis/chronic pelvic pain syndrome (CP/CPPS): a systematic review and metaanalysis. PLoS One 2012; 7 (8): e41941.
- Dunne R. L., Dunn L. A., Upcroft P. et al. Drug resistance in the sexually transmited protozoan Trichomonas vaginalis. Cell Res. 2003, Aug; 13(4): 239‑49.
- FDA Drug Safety Communication: FDA advises restricting fluoroquinolone antibiotic use for certain uncomplicated infections; warns about disabling side effects that can occur together. May 12, 2016. Available at: http://www.fda.gov/Drugs/DrugSafety/ ucm500143. htm(дата обращения 27.05.2016).
- Grabe M., Bartoletti R., Bjerklund Johansen T. E. et al. Guidelines on urological infections. European Association of Urology, 2015. Pp. 42‑46.
- Innocente A. M., Vieira P. de B., Frasson A. P. еt al. AntiTrichomonas vaginalis activity from triterpenoid derivatives. Parasitol Res. 2014, Aug; 113(8): 2933‑40.
- Kelley K. J. FDA calls for more restriction on fluoroquinolone use. Medical news. Physicians first watch. Eds. by: S. Sadoughi, A. Sofair. May 16, 2016.
- Krieger J. N., Lee S. W., Jeon J. et al. Epidemiology of prostatitis. Int J Antimicrob Agents 2008; 31(Suppl 1): S85‑90.
- Lee J. J., Moon H. S., Lee T. Y. et al. PCR for diagnosis of male Trichomonas vaginalis infection with chronic prostatitis and urethritis. Korean J. Parasitol. 2012 Jun; 50(2): 157‑9.
- Meites E., Llata E., Braxton J. et al. Trichomonas vaginalis in selected U.S. sexually transmitted disease clinics: testing, screening, and prevalence. Sex Transm Dis. 2013 Nov; 40 (11): 865‑9.
- Mitteregger D., Aberle S. W., Makristathis A. et al. High detection rate of Trichomonas vaginalis in benign hyperplastic prostatic tissue. Med Microbiol Immunol. 2012 Feb; 201 (1): 113‑6.
- Nickel J. C. Prostatitis. Can Urol Assoc J 2011; 5(5): 306‑15.
- Perletti G., Marras E., Wagenlehner F. M., Magri V. Antimicrobial therapy for chronic bacterial prostatitis. Cochrane Database Syst Rev 2013; 8: CD009071.
- Polackwich A. S., Shoskes D. A. Chronic prostatitis/chronic pelvic pain syndrome: a review of evaluation and therapy. Prostate Cancer Prostatic Dis 2016; 19 (2): 132‑8.
- Rees J., Abrahams M., Doble A. et al. Diagnosis and treatment of chronic bacterial prostatitis and chronic prostatitis/chronic pelvic pain syndrome: a consensus guideline. BJU Int 2015; 116 (4): 509‑25.
- Shoskes D. A., Nickel J. C., Kattan M. W. Phenotypically directed multimodal therapy for chronic prostatitis/chronic pelvic pain syndrome: a prospective study using UPOINT. Urology 2010; 75 (6): 1249‑53.
- Smith C. P. Male chronic pelvic pain: An update. Indian J Urol 2016; 32 (1): 34‑9.
- Thakkinstian A., Attia J., Anothaisintawee T., Nickel J. C. α-blockers, antibiotics and anti-inflammatories have a role in the management of chronic prostatitis/ chronic pelvic pain syndrome. BJU Int 2012; 110 (7): 1014‑22.
- United Kingdom national guideline on the management of Trichomonas vaginalis (2007). Avilablle from: http // www. bashh. org / documents/87/87. рdf.
- Workowsri K. A., Berman S. Centers for Disease Control and Prevention (CDC). Sexually Transmitted Diseases Treatment Guidelines. 2010. MMWR Recomm Rep. 2010. 59 (RR‑12): 1‑10.
- Zhang Z. C., Jin F. S., Liu D. M. et al. Safety and efficacy of levofloxacin versus ciprofloxacin for the treatment of chronic bacterial prostatitis in Chinese patients. Asian J Androl 2012; 14 (6): 870‑4.
КНИЖКОВА ПОЛИЦЯ
 Невідкладна урологія в практиці лікарів хірургічного профілю / За ред. В.І. Горового, В.О. Шапринського, Г.В. Чайки, І.В. Барала, О.М. Капшука. – Вінниця: Твори, 2018. – 824 с.; іл.
Невідкладна урологія в практиці лікарів хірургічного профілю / За ред. В.І. Горового, В.О. Шапринського, Г.В. Чайки, І.В. Барала, О.М. Капшука. – Вінниця: Твори, 2018. – 824 с.; іл.
У навчальному посібнику висвітлено проблематику гострих урологічних захворювань і синдромів, уражень сечостатевих органів, із якими стикаються урологи та лікарі хірургічного профілю. Представлено причини цих станів і захворювань, їх симптоматологію та сучасні принципи лікування. Розглянуто клінічну анатомію сечостатевих органів і техніку виконання основних невідкладних операцій на них. Описано власні оригінальні класифікації, способи діагностики та лікування деяких невідкладних урологічних захворювань.
Видання пропонується для практичного використання урологам, хірургам, акушерам-гінеколoгам, судинним хірургам, онкологам, травматологам, анестезіологам, нейрохірургам, лікарям швидкої медичної допомоги, клінічним ординаторам, інтернам, а також студентам медичних вищих навчальних закладів III-IV рівнів акредитації.
Стосовно придбання посібника звертатися за тел.: (097) 751 81 53.
Тематичний номер «Урологія. Нефрологія. Андрологія» № 2-3 (16-17) 2019 р.
СТАТТІ ЗА ТЕМОЮ Урологія та андрологія
Кальцій є одним із найважливіших елементів в організмі людини, оскільки підтримує належний стан кісток і зубів, зменшує ризик остеопорозу, а також знижує імовірність розвитку серцево-судинних хвороб і ожиріння (Institute of Medicine, 2011; Zhang F. et al., 2019; Teegarden D., 2003). Значна кількість людей потребує кальцієвих добавок, але водночас боїться каменеутворення. Сечокам’яна хвороба (СКХ) – поширене в наш час захворювання; більшість каменів становлять кальцій-оксалатні (Wei L. et al., 2022)....
Рак передміхурової залози (РПЗ) – злоякісне новоутворення, що розвивається з епітелію передміхурової залози. РПЗ вважається одним із найпоширеніших видів раку у чоловіків та однією з головних причин смерті у чоловіків похилого віку в Україні і світі. Лікарі загальної практики – сімейної медицини, лікарі інших спеціальностей мають бути обізнані щодо основних факторів ризику та початкових клінічних проявів РПЗ з метою їх раннього виявлення та направлення пацієнта до закладу охорони здоров’я (ЗОЗ), що надає спеціалізовану медичну допомогу, а також сприяти виконанню усіх рекомендацій фахівців онкологічного профілю під час протипухлинного лікування та організації належної паліативної допомоги пацієнтам, які виявляють бажання перебувати вдома на термінальних стадіях захворювання. ...
У статті представлено коментарі до дослідження TRAVERSE* , яке оцінювало ризик виникнення довгострокових серцево-судинних подій у чоловіків із гіпогонадизмом, що застосовують тестостерон-замісну терапію....
Переважна більшість хворих урологічного профілю страждають від больового синдрому. Гострий біль, який може виникнути внаслідок перенесеного хірургічного втручання на передміхуровій залозі або сечовому міхурі, при гострих запальних захворюваннях сечовивідних шляхів або при нирковій кольці (НК), вимагає невідкладної аналгезії з використанням ефективного та безпечного препарату, який не викликає серйозних побічних явищ. Хронічний біль, який є основним симптомом хронічного простатиту (ХП) та синдрому хронічного тазового болю (СХТБ) у чоловіків, суттєво впливає на якість життя, сексуальну сферу та психоемоційний стан пацієнтів, що також потребує проведення раціональної знеболювальної терапії. Нестероїдні протизапальні препарати (НПЗП), зокрема диклофенак натрію, довели свою ефективність за рахунок вираженої знеболювальної й протизапальної дії при оперативних втручаннях в урології, у хворих урологічного профілю з хронічною патологією (ХП/СХТБ) або невідкладними станами. ...