Ефективність використання Неопрост-форте в лікуванні хронічного простатиту та доброякісної гіперплазії передміхурової залози
 Доброякісна гіперплазія передміхурової залози (ДГПЗ) та хронічний простатит (ХП) є одними з найбільш розповсюджених захворювань у чоловіків. Частота ДГПЗ широко відома. Так, якщо в 60-річному віці це захворювання спостерігається у 50% випадків, то у 80 років воно вражає понад 80% чоловіків.
Доброякісна гіперплазія передміхурової залози (ДГПЗ) та хронічний простатит (ХП) є одними з найбільш розповсюджених захворювань у чоловіків. Частота ДГПЗ широко відома. Так, якщо в 60-річному віці це захворювання спостерігається у 50% випадків, то у 80 років воно вражає понад 80% чоловіків.
Вважається, що більшість чоловіків старших за 60 років тією чи іншою мірою відчувають симптоми, пов’язані з ДГПЗ. У США на лікування цих хворих щорічно припадає близько 1,7 млн візитів до лікаря [2, 3, 8].
Причини захворювання на сьогоднішній день до кінця не з’ясовані. Вважається, що гіперплазія передміхурової залози є одним із проявів чоловічого клімаксу. До факторів ризику відносяться тільки вік і рівень андрогенів у крові. З віком в організмі чоловіка порушується фізіологічний баланс між андрогенами і естрогенами, що веде до порушення контролю за ростом і функцією клітин передміхурової залози. Не виявлено достовірного зв’язку між виникненням ДГПЗ і статевою активністю, сексуальною орієнтацією, палінням і вживанням алкоголю, перенесеними запальними і венеричними захворюваннями статевих органів [1, 9].
Хронічний простатит – найбільш поширена хвороба передміхурової залози в осіб працездатного віку, що становить, за даними різних авторів, 40‑75% усіх запальних захворювань нижніх сечових шляхів у чоловіків [5, 6]. Часте необґрунтоване призначення антибіотиків призвело до поширення нечутливих до них госпітальних штамів мікроорганізмів. У великій кількості випадків інфекційний збудник взагалі неможливо визначити, тому зростає роль профілактики загострень, призначення в лікувальних схемах небактеріостатичних засобів [2, 7].
Пацієнти з ХП скаржаться на наявність симптомів нижніх сечових шляхів переважно іритативного характеру – часте сечовипускання, імперативні позиви до сечовипускання, виникнення неприємних відчуттів над лоном, у паху, сечовому каналі. Розлади сечовипускання характерні для 52‑88% хворих на ХП [3, 10].
Вважають, що причинами дизурії при ХП є збільшення передміхурової залози, викликане набряком внаслідок венозного стазу, тиск збільшеної передміхурової залози на шийку сечового міхура, помірне стискання простатичної частини сечового каналу, вплив на α1-адренорецептори передміхурової залози, а також нестабільність детрузора [3, 11].
Оперативне втручання по праву вважається єдиним методом радикального лікування ДГПЗ. Однак головною перешкодою до повсюдного хірургічного лікування ДГПЗ є високий операційний ризик у хворих похилого та старечого віку, в осіб із супутніми захворюваннями (летальність до 1,5%), а також високий відсоток післяопераційних ускладнень, який, за зведеними даними, становить від 10 до 35%. Це, безумовно, позбавляє задоволеності і значно знижує якість життя хворих після операції. Проте до кінця 80-х років минулого століття, за зведеними світовими даними, оперативному лікуванню піддавалися до 75% хворих [6, 10].
Медикаментозна терапія ДГПЗ посідає значне місце в урологічній практиці. На вибір препарату тієї чи іншої групи впливає цілий ряд факторів, а саме: характер клінічних проявів захворювання, об’єм гіперплазованої простати, виразність і особливості розладів сечовипускання та порушень функціонального стану сечового міхура. При виборі лікарського засобу повинні враховуватися його переносимість, можливість виникнення і характер побічних ефектів. Важливість обліку цих факторів зумовлена віком пацієнтів, наявністю інтеркурентної патології і необхідністю багаторічної терапії [4, 14].
Успіхи в пізнанні патогенезу гіперплазії передміхурової залози і досягнення фармакології привели до створення медикаментозних засобів для лікування цього захворювання, що мають патогенетичні механізми дії. Їх можна розділити на три групи:
- Альфа1-адреноблокатори (альфузозин, доксазозин, тамсулозин, теразозин). Препарати цієї групи блокують α1-адренорецептори гіперплазованої простати і в такий спосіб ліквідують динамічний компонент інфравезикальної обструкції. Вплив на α1-адренорецептори детрузора і його судин сприяє кровообігу стінки міхура, підвищує енергетичні запаси клітин і поліпшує скорочувальну здатність мускулатури сечового міхура.
- Інгібітори 5-α-редуктази (фінастерид, дутастерид). Ці лікарські засоби блокують 5-α-редуктазу клітин простати і переривають ланку метаболізму тестостерону – перетворення на дигідротестостерон. Саме цей механізм відповідальний за процеси власне клітинної проліферації.
- Препарати рослинного походження. Такі препарати мають складні патогенетичні механізми впливу при гіперплазії передміхурової залози. Основними з них є інгібування активності 5-α-редуктази, протинабрякова і протизапальна дія, блокування тканинних факторів росту [4, 15].
Велика кількість літературних даних свідчить про ефективність медикаментозної терапії, здатність її не тільки полегшувати страждання хворих, але й у ряді випадків уникнути операції або створити кращі умови для хірургічного лікування. Безумовно, у зв’язку з різними варіантами клінічного перебігу захворювання, переважанням іритативних або обструктивних симптомів необхідно диференційовано підходити до питання лікування ДГПЗ, вибираючи монотерапію α-адреноблокаторами, інгібіторами 5-α-редуктази або комбіновану фітотерапію. Варто оцінювати ефект проведеного лікування за допомогою методів клінічної та апаратної уродинаміки. Можливості фармакологічної корекції акту сечовипускання досить великі. Пошук оптимальних комбінацій препаратів і технології застосування, безумовно, дасть свої результати [13, 15].
На жаль, медикаментозна терапія не дає можливості вилікувати хворого від гіперплазії простати. Однак найчастіше ефективність лікарської терапії дозволяє настільки суттєво підвищити якість життя пацієнта, що він і не думає про операцію. Ефект, досягнутий при консервативній терапії, необхідно підтримувати повторними курсами медикаментозного лікування [1, 8, 12].
Фітотерапія ДГПЗ набула значної популярності у світі, для лікування застосовуються фітопрепарати з плодів американської карликової пальми, кори сливи африканської, екстракту пилку рослин, екстракту квіток опунції (рослина із сімейства кактусових), екстракту коренів кропиви, олії насіння гарбуза. Також використовуються рецепти народної медицини: водний екстракт зі шкірки насіння каштана кінського, настій із трави зніту мілкоцвітного, ліщина звичайна (відвар листя, екстракт шкаралупи горіхів); цибуля ріпчаста (свіжі цибулини, настій цибулин), льнянка звичайна (настій трави), омела біла (настій листя і молодих пагонів), осика звичайна (відвар бруньок і настій кори, листя), спаржа лікарська (відвар кореневищ із корінням, настій трави і плодів), лопух великий (відвар коріння), мед тощо [3, 9].
Препарати рослинного походження мають широку популярність у багатьох країнах світу, насамперед завдяки мінімальній виразності побічних реакцій. Однак до кінця їх місце в медикаментозній терапії хворих на гіперплазію передміхурової залози не визначено. Відповідно до Рекомендацій Об’єднавчого комітету ВООЗ із гіперплазії передміхурової залози необхідні подальші дослідження препаратів рослинного походження, що дозволять вивчити патогенетичний механізм дії, вірогідно оцінити ефективність і визначити їх місце серед численних медикаментозних засобів [12].
Одним із найбільш ефективних фітопрепаратів для лікування ДГПЗ та хронічного простатиту наразі є Неопрост-форте. Чому так? Тому що цей препатат створений у нашій країні з використанням натуральної сировини (EUSA, Франція) у відповідності до міжнародних стандартів ISO/HACCP.
Неопрост-форте рекомендований як додаткове джерело сапонінів, фітостеролів та інших біологічно активних речовин з метою покращення функціонального стану сечостатевої системи у чоловіків; сприяє зменшенню запальних процесів у передміхуровій залозі при простатиті, полегшує сечовиділення, поліпшує загальний стан та покращує якість життя чоловіків із ДГПЗ за рахунок нормалізації об’єму простати, що відбувається при гальмуванні розвитку гіперпроліферативних процесів.
Основним діючим компонентом Неопрост-форте є екстракт африканської сливи. Африканська слива (Pygeum africanum) – це вічнозелена рослина, що досягає до 50 м висоти, зустрічається в Африці повсюдно, росте на висоті 1000 м і вище. Інтерес до цієї рослини в Європі вперше виник у XVIII ст., коли мандрівники почули від аборигенів Південної Африки розповіді про можливості лікування порушень сечовипускання і «хвороб літньої людини» за допомогою екстракту кори цього дерева. З 60-х років минулого століття екстракт кори Pygeum africanum почали вивчати з метою широкого застосування для лікування чоловіків, які страждають на аденому передміхурової залози [5, 7]. Екстракт Pygeum africanum покращує роботу гладкої мускулатури сечового міхура, має протизапальну активність, знижує продукцію лейкотрієнів та інших метаболітів 5-ліпооксигенази, за рахунок пригнічення факторів росту передміхурової залози гальмує проліферацію фібробластів, позитивно впливає на продукцію надниркових андрогенів, а також відновлює активність секреторного епітелію передміхурової залози. Такий комплексний лікувальний вплив має свою обґрунтовану позитивну спрямованість, що вкрай важливо для успішної патогенетичної терапії проявів не тільки гіперплазії простати, але й ХП [4, 6].
У 2000 р. було опубліковано результати метааналізу 18 подвійних сліпих плацебо-контрольованих досліджень (n=1562) препаратів, що містять екстракт Pygeum africanum. Було продемонстровано покращення параметрів сечовипускання у пацієнтів із ДГПЗ, а саме зменшення об’єму залишкової сечі та збільшення об’ємної швидкості сечовипускання [5].
Одним із факторів, що підтверджують позитивну ефективність екстракту Pygeum africanum у лікуванні хворих на ДГПЗ з легкою і помірною симптоматикою і високою комплаєнтністю даної терапії, є велика поширеність його застосування в країнах Європи (найбільш відомий препарат – таденан), де накопичено чимало даних, що підтверджують цінність такого виду фітотерапії ДГПЗ та ХП [14].
Неопрост-форте є унікальним фітотерапевтичним комплексом, оскільки, окрім екстракту Pygeum africanum, містить інші компоненти, які підсилюють та доповнюють дію першого.
Екстракт кореня кропиви має протизапальні, антипроліферативні та імуномодулюючі властивості. У дослідженнях екстракт кореня кропиви в поєднанні з екстрактом кори африканської сливи показали більш високу ефективність, ніж окреме застосування [16, 20, 21].
Екстракт насіння селери має протизапальні та сечогінні властивості, нормалізує нейроендокринну функцію передміхурової залози, запобігає розростанню її тканин, має антиоксидантну дію [19].
Ехінацея стимулює імунну систему, покращує витривалість чоловічого організму [23].
Календула лікарська має бактерицидну, протизапальну дію, підвищує секреторну функцію передміхурової залози [17, 18, 22].
Саме завдяки такому складу Неопрост-форте є особливо цікавим для призначення пацієнтам з ДГПЗ та ХП.
Метою власного відкритого дослідження була оцінка ефективності і переносимості Неопрост-форте при лікуванні хворих на ДГПЗ та ХП.
Матеріали і методи дослідження
Згідно із критеріями відбору у дослідження увійшли пацієнти, які мали:
- легкі і помірні симптоми ДГПЗ та ХП без ускладнень;
- вік ≥50 років;
- діагноз ДГПЗ і симптоми нижніх сечових шляхів із сумарною оцінкою за шкалою International Prostate Symptom Score (IPSS) >13 балів і оцінкою якості життя (QOL) >3 бали;
- максимальну об’ємну швидкість потоку сечі 5‑12 мл/с (об’єм спорожнювання >150 мл);
- об’єм залишкової сечі (ОЗС) не більше 200 мл.
Неопрост-форте призначали перорально після їди по 1 таблетці двічі на день протягом 3 міс.
У результаті добору в дослідження було включено 25 пацієнтів віком від 61 до 82 років (у середньому 66±9 років), із тривалістю захворювання від півроку до 4 років. У всіх хворих проводили збір анамнезу, оцінювали симптоматику із використанням анкети IPSS і показник якості життя, проводили пальцеве ректальне дослідження простати.
На початку і по закінченні дослідження виконували ультразвукове дослідження простати з виміром її об’єму й ОЗС та урофлоуметрію. Оцінку впливу лікування на сексуальну функцію хворих проводили за допомогою анкетного опитування.
Дванадцятитижневий курс лікування препаратом Неопрост-форте повністю завершили 22 хворих (88±6%). Троє пацієнтів не пройшли контрольне дослідження після лікування з сімейних обставин. Випадків вибуття з дослідження через побічні ефекти не спостерігалось. Таким чином, оцінка ефективності препарату виконана у 22 пацієнтів, оцінка переносимості – у 25.
Результати дослідження
У більшості пацієнтів на початку дослідження відмічались симптоми почастішання сечовипускання (нічна полакіурія – у 96±4%, денна – у 72±9%), странгурія – у 88±7% та імперативні позиви – у 68±10%. По завершенню терапії покращання спостерігалось у 84±8% осіб, середня частота нічних сечовипускань знизилась із 3,6 до 1,9 (р<0,05), середня частота денних сечовипускань – із 6,2 до 4,8 (р>0,05), ступінь виразності странгурії та імперативних позивів зменшився відповідно у 72±9% і 84±8% пацієнтів. При дослідженні секрету передміхурової залози значна лейкоцитарна реакція виявлена у 12 (48%) хворих, помірно виражена – у 7 (37,4%), слабка – у 3 (15%).
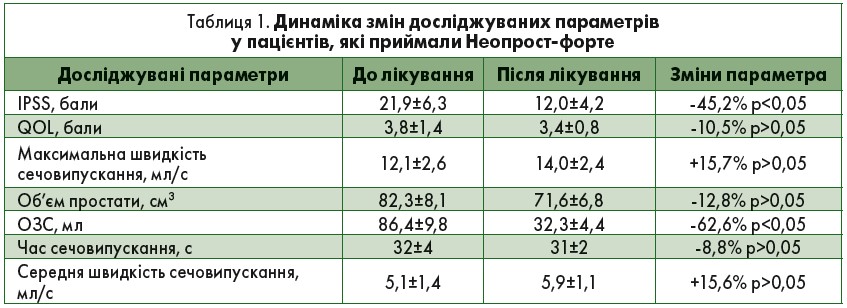
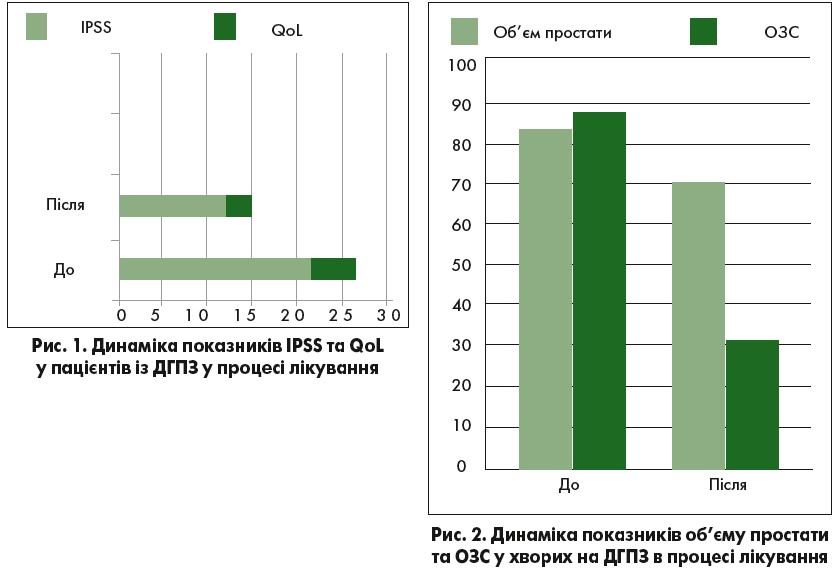
Лікування препаратом Неопрост-форте протягом 3 міс (табл. 1) сприяло зменшенню дизурії, що проявилося в статистично вірогідному зменшенні кількості балів за шкалою IPSS з 21,9 до 12,0 бала, а також зменшенням ОЗС з 86,4 до 32,3 мл (р<0,05). Слід зазначити, що в 7 пацієнтів (30±10%) з вихідним обсягом простати до 100 мл і ОЗС до 200 мл у результаті лікування відбулося найбільше і вірогідне зниження даного показника в середньому до 40±6 мл (р<0,05). Крім цього мало місце зниження показника QOL на 10,5% (р>0,05), зменшення об’єму простати на 12,8% (р>0,05), підвищення максимальної і середньої швидкості сечовипускання (на 15,7 і 15,6% відповідно; р>0,05) (рис. 1, 2).
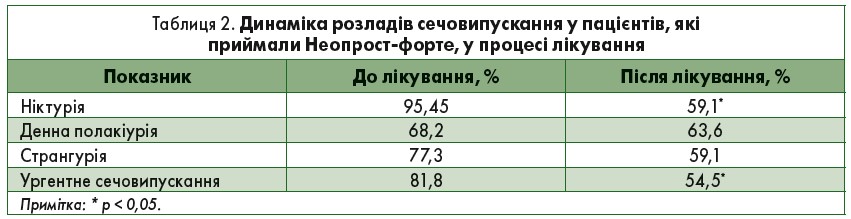
Оцінюючи показники дизурії в процесі лікування, слід зазначити, що ніктурія спостерігалась у 95,45% пацієнтів до лікування і у 59,1% – після, денна полакіурія – відповідно у 68,2 та 63,6%, странгурія – у 77,3 і 59,1%, ургентне сечовипускання – у 81,8% до лікування і у 54,5% – після лікування (табл. 2, рис. 3).
Незважаючи на те що антибактеріальну терапію не призначали, після завершення лікування значна лейкоцитарна реакція в секреті передміхурової залози спостерігалась у восьми хворих (32%), помірна – у п’яти (20%) і слабка – у двох (8%) осіб.
 Статева функція у пацієнтів під час прийому препарату істотно не змінилася; побічних ефектів лікування, що вимагали його припинення, також не виявлено.
Статева функція у пацієнтів під час прийому препарату істотно не змінилася; побічних ефектів лікування, що вимагали його припинення, також не виявлено.
Висновки
Отже, у ході проведеного нами тримісячного дослідження Неопрост-форте продемонстрував свою ефективність у лікуванні ДГПЗ І‑ІІ стадій та ХП як за суб’єктивними показниками (IPSS), так і за об’єктивними (зменшення лейкоцитарної реакції секрету передміхурової залози, об’єму простати та ОЗС).
Неопрост-форте добре переноситься хворими, не викликає побічних ефектів, що вимагають припинення лікування, не порушує статеву функцію хворих на ДГПЗ та ХП.
Найвищу ефективність препарат виявив у пацієнтів з обсягом простати до 100 мл і вихідним обсягом залишкової сечі до 200 мл. Подальше дослідження динаміки об’єктивних показників у цієї категорії хворих, можливо, дозволить скоригувати критерії відбору осіб для успішного лікування препаратом Неопрост-форте.
У рекомендаціях Міжнародного наукового комітету 4-ї Міжнародної наради з ДГПЗ наголошується: щоб той або інший вид лікування був розцінений як прийнятний, він «...повинен переслідувати принаймні одну з нижчеперелічених цілей: рятування пацієнта від симптомів захворювання, зменшення обструкції або запобігання пізнім ускладненням…» [11]. Виходячи з цього положення, аналіз результатів як раніше опублікованих, так і власних досліджень дозволяє вважати застосування Неопрост-форте цілком прийнятним, патогенетично обґрунтованим видом лікування ДГПЗ та ХП.
Література
- Горпинченко И. И., Исаков В. Л. Новые методы и аппараты для лечения хронического простатита и эректильной дисфункции // Здоровье мужчины. – 2004. – № 3 (10). – С. 190‑192.
- Лесовой В. Н., Аркатов А. В., Книгавко А. В. Лечение простатита у пациентов с доброкачественной гиперплазией предстательной железы // Здоровье мужчины. – 2006. – № 2. – С. 96‑98.
- Лопаткин Н. А., Перепанова Т. С. Рациональная фармакотерапия в урологи. – М.; 2006. – 818 с.
- Bales G. T., Christiano A. P., Kirsh E. J., Gerber G. S. Phytotherapeutic agents in the treatment of lower urinary tract symptoms: a demographic analysis of awareness and use at the University of Chicago. Urology. 1999; 54: 86‑89.
- Wilt T. J., MacDonald R., Ishani A. Beta-sitosterol for the treatment of benign prostatic hyperplasia: a systematic review. BJU International. 2000; 83: 976‑983.
- Paubert-Braquet M., Cave A., Hocquemill R. et al. Effect of Pygeum africanum extract on A23187-stimulated production of lipoxygenase metabolite from human polymorphonuclear cells. J Lipid Mediators. 1994; 9: 285‑290.
- Yablonsky F., Nicolas V., Riffaud J. P., Bellamy F. Antiproliferative effect of Pygeum africanum extract on rat prostatic fibroblasts. J Urol. 1997; 157: 2381‑2387.
- Lukacs B. et al. History of 7 093 Patients with Lower Urinary Tract Symptoms Related to Benign Prosattic Hyperplasia Treated with Alfuzosin in General Practice up to 3 Years. Eur. Urol. 2000. Vol. 37. P. 183‑190.
- Berry S. J. et al. The development of human prostatic hyperplasia with age. J. Urol. 2014. Vol. 132. P. 474‑479.
- Chappee C. R. et. al. A three-month double-blind study of doxazosin as treatment for benign prostatic obstruction. Br. J. Urol. 2014. Vol. 74. P. 50‑56.
- McConnell et al. The effects of finasteride on the risk of acute urinary retention and the need for surgical treatment among men with benign prostatic hyperplasia. N. Engl. J. Med. 2008. Vol. 338. P. 557‑563.
- Gormley G. J. et al. The effect of finesteride in men with benign prostatic hyperplasia. N. Engl. J. Med. 2002. Vol. 327. P. 1185‑1191.
- Boyle P. C. Prostate volume predicts outcomes of treatment of benign prostatic hyperplasia with finasteride: meta-analysis of randomized clinical trials. Urology. 2016. Vol. 48. P. 398‑405.
- Lepor H. For the Veterans Affairs Cooperative Studies Benign Prostatic Hyperplasia Study Group. The impact of medical therapy оn bother due to symptoms, quality of life and global outcome, and factors predicting response. J. Urol. 1998. Vol. 160. P. 1358‑1367.
- The 4th International Consultation on BPH. Proceedings/ Ed. A. Cockett [et al.] // S.C.I. – Paris, 2007. – P. 13‑24.
- Alternative Medicine Review Volume 12, Number 3 2007 Urtica dioica; Urtica urens (Nettle).
- The Center for Holistic Pediatric Education and Research Calendula (Calendula officinalis) Kathi J. Kemper, MD, MPH.
- Muley B., Khadabadi S., Banarase N. Phytochemical Constituents and Pharmacological Activities of Calendula officinalis Linn (Asteraceae): A Review. Tropical Journal of Pharmaceutical Research [Internet]. African Journals Online (AJOL); 2009 Nov 24; 8 (5).
- Wesam K., Ali-Akbari S. et al. A review on medicinal plant of Apium graveolens. Advanced Herbal Medicine, 2014; 1 (1): 48‑59.
- Hartmann R. W., Mark M., Soldati F. Inhibition of 5 α-reductase and aromatase by PHL‑00801 (Prostatonin®), a combination of PY102 (Pygeum africanum) and UR102 (Urtica dioica) extracts. Phytomedicine. 1996 Sep; 3 (2): 121‑128.
- Chrubasik J. E., Roufogalis B. D., Wagner H., Chrubasik S. A comprehensive review on the stinging nettle effect and efficacy profiles. Part II: urticae radix.
- Jimenez-Medina E., Garcia-Lora A., Paco L., Algarra I., Collado A., Garrido F. A new extract of the plant Calendula officinalis produces a dual in vitro effect: cytotoxic anti-tumor activity and lymphocyte activation. BMC Cancer. 2006;6:119.
- Assessment report on Echinacea purpurea (L.) Moench, radix, 2016.
Тематичний номер «Урологія. Нефрологія. Андрологія» № 2-3 (16-17) 2019 р.
СТАТТІ ЗА ТЕМОЮ Урологія та андрологія
Кальцій є одним із найважливіших елементів в організмі людини, оскільки підтримує належний стан кісток і зубів, зменшує ризик остеопорозу, а також знижує імовірність розвитку серцево-судинних хвороб і ожиріння (Institute of Medicine, 2011; Zhang F. et al., 2019; Teegarden D., 2003). Значна кількість людей потребує кальцієвих добавок, але водночас боїться каменеутворення. Сечокам’яна хвороба (СКХ) – поширене в наш час захворювання; більшість каменів становлять кальцій-оксалатні (Wei L. et al., 2022)....
Рак передміхурової залози (РПЗ) – злоякісне новоутворення, що розвивається з епітелію передміхурової залози. РПЗ вважається одним із найпоширеніших видів раку у чоловіків та однією з головних причин смерті у чоловіків похилого віку в Україні і світі. Лікарі загальної практики – сімейної медицини, лікарі інших спеціальностей мають бути обізнані щодо основних факторів ризику та початкових клінічних проявів РПЗ з метою їх раннього виявлення та направлення пацієнта до закладу охорони здоров’я (ЗОЗ), що надає спеціалізовану медичну допомогу, а також сприяти виконанню усіх рекомендацій фахівців онкологічного профілю під час протипухлинного лікування та організації належної паліативної допомоги пацієнтам, які виявляють бажання перебувати вдома на термінальних стадіях захворювання. ...
У статті представлено коментарі до дослідження TRAVERSE* , яке оцінювало ризик виникнення довгострокових серцево-судинних подій у чоловіків із гіпогонадизмом, що застосовують тестостерон-замісну терапію....
Переважна більшість хворих урологічного профілю страждають від больового синдрому. Гострий біль, який може виникнути внаслідок перенесеного хірургічного втручання на передміхуровій залозі або сечовому міхурі, при гострих запальних захворюваннях сечовивідних шляхів або при нирковій кольці (НК), вимагає невідкладної аналгезії з використанням ефективного та безпечного препарату, який не викликає серйозних побічних явищ. Хронічний біль, який є основним симптомом хронічного простатиту (ХП) та синдрому хронічного тазового болю (СХТБ) у чоловіків, суттєво впливає на якість життя, сексуальну сферу та психоемоційний стан пацієнтів, що також потребує проведення раціональної знеболювальної терапії. Нестероїдні протизапальні препарати (НПЗП), зокрема диклофенак натрію, довели свою ефективність за рахунок вираженої знеболювальної й протизапальної дії при оперативних втручаннях в урології, у хворих урологічного профілю з хронічною патологією (ХП/СХТБ) або невідкладними станами. ...