Профілактика інсульту при фібриляції передсердь: майстер-клас щодо ведення пацієнта
У межах науково-освітнього форуму «Академія інсульту – 2019», що відбувся 30 жовтня – 1 листопада 2019 року в Києві, працювала секція профілактики інсульту. Пропонуємо до вашої уваги огляд представлених на секції доповідей, що присвячені детальному розгляду питань стратифікації ризику, вибору оптимальної тактики та порівнянню ефективності сучасних препаратів.
Професійний погляд кардіолога: профілактика інсульту при фібриляції передсердь
 Таїсія В’ячеславівна Гетьман, к. мед. н., старший науковий співробітник Інституту кардіології ім. акад. М.Д. Стражеска НАМН України (м. Київ), поділилася власним поглядом на оптимальну тактику профілактики інсульту в пацієнта з порушенням серцевого ритму.
Таїсія В’ячеславівна Гетьман, к. мед. н., старший науковий співробітник Інституту кардіології ім. акад. М.Д. Стражеска НАМН України (м. Київ), поділилася власним поглядом на оптимальну тактику профілактики інсульту в пацієнта з порушенням серцевого ритму.
За даними Фремінгемського дослідження (n=5070), ризик ішемічного інсульту в осіб із фібриляцією передсердь (ФП) зростає у п’ять разів (Wolf, 1991). Проведення скринінгу пацієнтів із ФП відповідно до настанови Європейського товариства кардіологів (ESC, 2016) підпорядковується таким правилам (Kirchhof et al., 2016):
- Позаплановий скринінг на виявлення ФП рекомендований хворим віком від 65 років шляхом визначення пульсу або проведення ЕКГ (I, В).
- У пацієнтів із транзиторною ішемічною атакою (ТІА) або ішемічним інсультом скринінг на ФП проводять шляхом аналізу даних моніторингу ЕКГ тривалістю принаймні 72 год (I, В).
Доповідачка наголосила, що в пацієнтів, у яких були імплантовані пристрої, слід аналізувати запис кардіостимулятора та імплантованого кардіовертера-дефібрилятора для визначення високочастотних передсердних епізодів (AHRE). У хворих із зафіксованими AHRE варто забезпечити проведення ЕКГ-моніторингу для реєстрації ФП до ініціації лікування (I, В). Вибір антикоагулянтної терапії має ґрунтуватися на ризику тромбоемболії незалежно від форми ФП: пароксизмальної, персистувальної або постійної (I, В) (January et al., 2019).
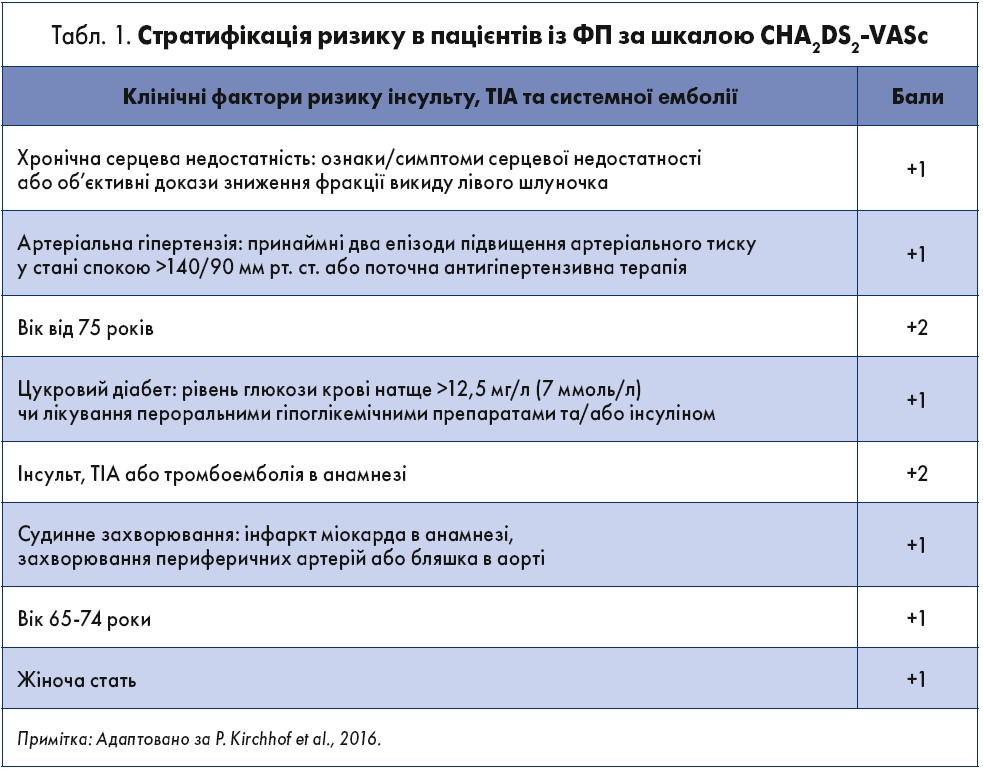
Для прогнозування вірогідності розвитку інсульту в пацієнтів із ФП використовують шкалу CHA2DS2VASc (І, А) (табл. 1). Окрім того, для виявлення модифікованих ризиків застосовують шкали ризику кровотеч (HAS-BLED, HEMORR2HAGES, ATRIA, ORBIT, Bleeding Score [BS]) (ІІа, В).
Як зауважила спікер, відповідно до кількості балів за CHA2DS2VASc, слід прийняти рішення щодо наступної тактики:
- За наявності 0 балів: антитромбоцитарні засоби та антикоагулянти не призначають (ІІІ, В).
- За наявності 1 бала: розглянути призначення оральних антикоагулянтів (ОАК) (ІІа, В) (Kirchhof et al., 2016); на користь ОАК свідчать фактори: вік >65 років, цукровий діабет 2го типу, ФП (не тріпотіння), персистувальна/постійна форма ФП.
Додатковими факторами для модифікації ризику тромбемболії є (Lüscher, 2019): ожиріння (індекс маси тіла ≥30 балів); протеїнурія (>150 мг/24 год або еквівалент); кліренс креатиніну <45 мл/год; вміст мозкового натрійуретичного пропептиду в крові (NTpro BNP) >1400 нг/л (позитивно корелює зі ступенем серцевої недостатності та може виявлятися при лівошлуночковій дисфункції); наявність високочутливого тропоніну Т та І; збільшення об’єму лівого шлуночка (≥73 мл) або його діаметра (≥4,7 см); швидкість вигнання з вушка лівого передсердя <20 см/с; показник за шкалою АВС (вік, біомаркери, клінічний анамнез).
3. За наявності ≥2 балів: призначити ОАК, оцінити протипоказання, скорегувати фактори ризику кровотечі:
- для пацієнтів із чіткими протипоказаннями щодо ОАК розглянути призначення пристрою для оклюзії вушка лівого передсердя;
- призначити прямі пероральні вітамін К-незалежні антикоагулянти (ПОАК) (І, А);
- призначити антагоніст вітаміну К (АВК) – рекомендовано за наявності механічного клапана або виразного мітрального стенозу (І, А).
Т.В. Гетьман зауважила, що при веденні пацієнтів із неклапанною формою ФП доцільно віддавати перевагу призначенню ПОАК (апіксабан, дабігатран, ривароксабан тощо) перед АВК (І, А). Для профілактики інсульту при ФП антитромбоцитарну монотерапію застосовувати не варто (ІІІ, А) (Kirchhof et al., 2016). Серед пацієнтів, які отримують варфарин, міжнародне нормалізоване відношення (МНВ) слід визначати щотижня на початку антикоагулянтної терапії та щомісяця, коли гіпокоагуляція (МНВ=23) стабілізується (І, А).
У клінічній практиці адекватного контролю досягти важко, тому приймання АВК супроводжується підвищеним ризиком інсульту, кровотечею та смертністю (Haas, 2016). Аналіз даних дослідження ARISTOTLE, в якому взяв участь 18 201 пацієнт із ФП, показав, що терапія апіксабаном у дозі 5 мг двічі на день характеризувалася нижчим ризиком інсульту або системної емболії, великих кровотеч та летальності, ніж варфарином (Wallentin et al., 2013).
При виборі конкретного ПОАК слід враховувати, що тривалість періодів напіввиведення (Т1/2) у всіх представників цього класу є зіставною, втім режими дозування значно відрізняються (Heidbuchel et al., 2015): двічі на добу – апіксабан (Т1/2=12 год), дабігатран (Т1/2=12-17 год); 1 раз на добу – едоксабан (Т1/2=10-14 год), ривароксабан (Т1/2=5-9 год у дорослих, 11-13 год у літніх осіб). Виявлено, що апіксабан характеризується більш постійною концентрацією за умови приймання двічі на добу, внаслідок чого застосування апіксабану в такому режимі приводить до меншого співвідношення піку та падіння концентрації з нижчим коливанням дії препарату протягом 24 год. Стійкий вплив ліків у межах діапазону концентрацій може бути ключовим для підтримання оптимального балансу користі та ризику для апіксабану (Frost, 2013).
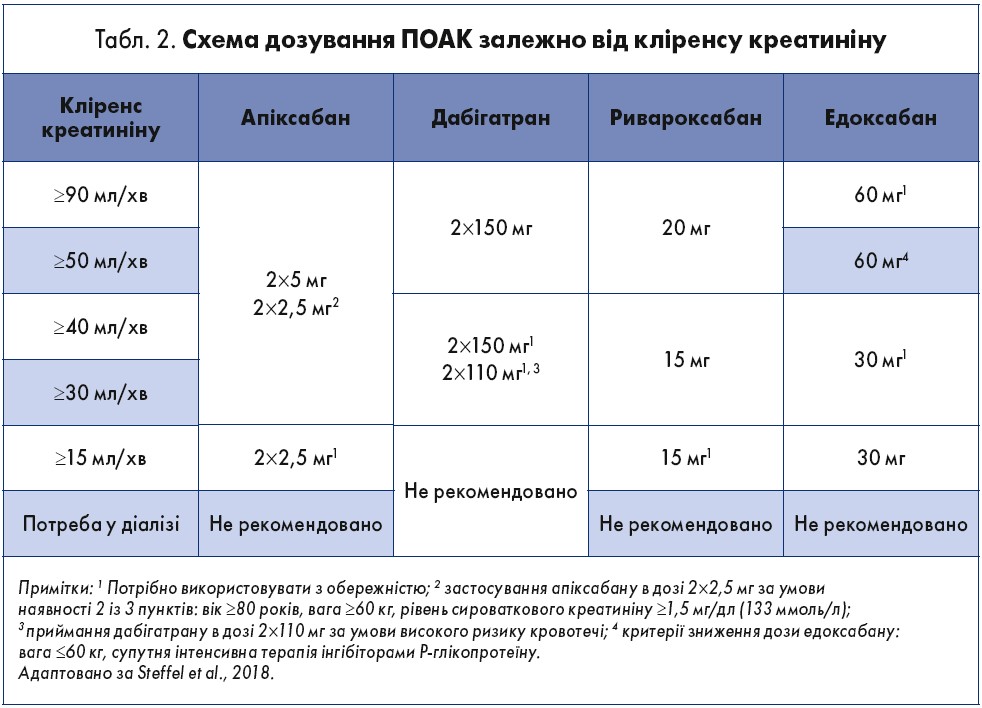
Всі представники ПОАК затверджені для використання Управлінням із санітарного нагляду за якістю харчових продуктів та медикаментів США (FDA) з огляду на функцію нирок, зокрема, оцінку рівня кліренсу креатиніну, розрахованого за формулою Кокрофта – Голта (January et al., 2019). Так, залежно від даного показника, визначається схема дозування ПОАК (табл. 2).
Таїсія В’ячеславівна також наголосила на необхідності ретельного моніторингу функції печінки при застосуванні інгібіторів фактора Ха. ПОАК не рекомендовані пацієнтам із виразною печінковою дисфункцією (January et al., 2019). Всі ПОАК протипоказані особам із хворобою печінки, що супроводжується коагулопатією або значним ризиком кровотечі, а також при порушенні функції печінки, що відповідає категорії С за класифікацією Чайлда – П’ю (табл. 3) (Steffel et al., 2018).
Також Т.В. Гетьман навела аналіз даних дослідження ARISTOTLE з урахуванням вікового параметра пацієнтів із ФП та підвищеним ризиком інсульту (Halvorsen et al., 2014). Як відомо, хворі були рандомізовані для приймання варфарину чи апіксабану по 5 мг двічі на добу зі зменшенням дози до 2,5 мг два рази на день, або плацебо. У старших вікових групах частота інсульту, масивних кровотеч, смерті від усіх причин була вищою (p<0,001 для всіх).
Апіксабан виявився ефективнішим, ніж варфарин для запобігання інсульту та зменшення летальності й асоціювався зі зниженням ризику масивних, усіх кровотеч та внутрішньочерепних крововиливів незалежно від віку (p>0,11 для всіх показників). Не спостерігалося значущого впливу дози апіксабану на основні результати лікування.
Відповідно до субаналізу в межах дослідження AVERROES, виявлене суттєвіше зниження ВР інсульту в пацієнтів ≥75 років (порівнянне з таким у віці <75 років) на тлі використання апіксабану при зіставленні з терапією ацетилсаліциловою кислотою (АСК) (Hunfeld et al., 2016). Додатково виявлено, що застосування антикоагулянтів знижує частоту дементного синдрому (Friberg et al., 2018).
На завершення доповіді спікер виклала основні принципи профілактики повторного інсульту:
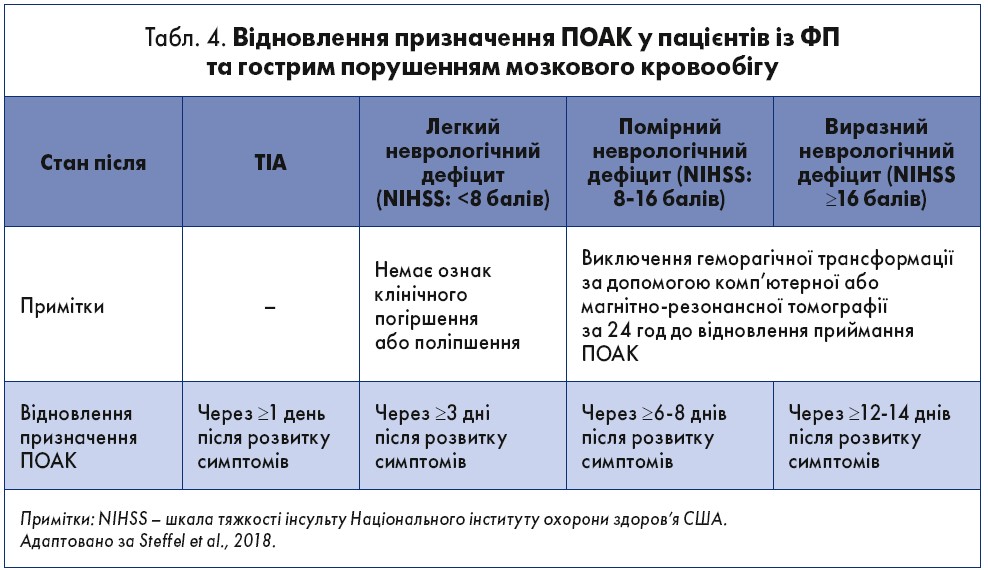
- Для пацієнтів із ФП після інсульту слід розглядати призначення АСК для профілактики повторного епізоду до початку або відновлення приймання ОАК (IIa, B) (табл. 4).
- Системний тромболіз із використанням рекомбінантного тканинного активатора плазміногену не рекомендований, якщо МНВ >1,7 (або у хворих, що приймали дабігатран, якщо активований частковий тромбопластиновий час [АЧТЧ] за межами нормального діапазону) (III, C).
- Слід віддавати перевагу ПОАК перед АВК чи АСК в осіб із ФП після попереднього інсульту (I, B).
- Після ТІА або інсульту комбіновану терапію ОАК і антитромбоцитарними засобами призначати не варто (III, B).
- Після внутрішньочерепної кровотечі застосування ОАК пацієнтами з ФП може бути відновлене через
4-8 тижнів, якщо причина кровотечі / відповідний фактор ризику усунутий або взятий під контроль (ІІb, B) (Kirchhof et al., 2016).
Ефективність та безпека антикоагулянтів при вторинній профілактиці інсульту
 Завідувач інсультного центру універсальної клініки «Оберіг», к. мед. н., лікар-невролог Юрій Володимирович Фломін привернув увагу присутніх до актуальності профілактики інсульту в Україні. Згідно з даними Всесвітньої книги фактів (The World Factbook), Україна посідає 5-те місце у світі за частотою летальних наслідків інсульту, що становила 14,40 на 1 тис. населення 2017 року. У 2016 р. ризик інсульту в осіб віком від 25 років у світі в середньому становив 25% (25,1% у жінок, 24,7% у чоловіків); у Центральній і Східній Європі – 32%, в Латвії – 41,7% (N Engl J Med, 2018).
Завідувач інсультного центру універсальної клініки «Оберіг», к. мед. н., лікар-невролог Юрій Володимирович Фломін привернув увагу присутніх до актуальності профілактики інсульту в Україні. Згідно з даними Всесвітньої книги фактів (The World Factbook), Україна посідає 5-те місце у світі за частотою летальних наслідків інсульту, що становила 14,40 на 1 тис. населення 2017 року. У 2016 р. ризик інсульту в осіб віком від 25 років у світі в середньому становив 25% (25,1% у жінок, 24,7% у чоловіків); у Центральній і Східній Європі – 32%, в Латвії – 41,7% (N Engl J Med, 2018).
Виявлено, що ФП є незалежним фактором ризику рецидиву інсульту протягом широкого вікового діапазону. Так, з 829 пацієнтів, які перенесли перший інсульт, у 163 (20%) відбувся рецидив: у 27% осіб із ФП, які не приймали антикоагулянти; у 18% хворих на ФП на тлі медикаментозної профілактики; у 17% пацієнтів без порушення ритму серцевої діяльності. Коефіцієнт небезпеки для повторного інсульту серед осіб із ФП, які не лікувались антикоагулянтами, становив 2,1 (95% довірчий інтервал (ДІ) 1,4‑2,9; р<0,001), тоді як коефіцієнт небезпеки для повторного тяжкого інсульту – 2,4 (95% ДІ: 1,6‑3,6; р<0,001) (Penado et al., 2003).
Доповідач навів чіткі рекомендації Американської асоціації кардіологів, Американської колегії кардіологів і Товариства серцевого ритму США (AHA/ACC/HRS, 2019) відносно показань до призначення прямих оральних антикоагулянтів (ПОАК):
- призначення ПОАК рекомендоване при показниках за шкалою CHA2DS2-VASc: ≥2 балів у чоловіків, ≥3 балів у жінок;
- призначення ПОАК доречне при показниках за шкалою CHA2DS2-VASc: 1 бал у чоловіків та 2 бали у жінок;
- ПОАК ефективніші за варфарин;
- призначати АСК не рекомендовано;
- апіксабан є доречним при термінальній хронічній хворобі нирок.
Доповідач навів дані метааналізу, в якому проаналізовано вплив чотирьох ПОАК у пацієнтів із ФП. ПОАК мали сприятливий профіль ризику та користі порівняно з варфарином. Результатом терапії цими препаратами було значуще (на 19%) зменшення ризику інсульту, внутрішньочерепного крововиливу, смертності (на 10%), масивних кровотеч, однак при цьому збільшувався такий шлунково-кишкових кровотеч. Підтверджено відносну ефективність та безпеку ПОАК для широкого кола пацієнтів (Ruff et al., 2014).
У дослідженні Y. Xian et al. (2017) за участю 94 474 пацієнтів із ФП, які перенесли гострий ішемічний інсульт, була показана тенденція превалювання неадекватної терапевтичної антикоагуляції, що передувала інсульту: 7,6% застосовували варфарин у профілактичній дозі та 8,8% – ПОАК, 83,6% не отримували антикоагулянтної терапії (з них 13,5% під час інсульту мали субтерапевтичну антикоагуляцію на тлі приймання варфарину [МНВ<2], 39,9% використовували тільки антитромбоцитарну терапію, 30,3% не отримували антитромбоцитарного лікування). Терапевтична антикоагуляція була пов’язана з меншим ризиком помірного й тяжкого інсульту та нижчою внутрішньолікарняною летальністю. Інсульти середнього ступеня тяжкості й тяжкі рідше траплялися в пацієнтів, які застосовували варфарин у профілактичній дозі (15,8%) та ПОАК (17,5%), ніж серед тих, які не отримували антикоагулянтної терапії (27,1%), або отримували лише антитромбоцитарну терапію (24,8%) чи варфарин у субтерапевтичній дозі (25,8%).
Показники внутрішньолікарняної летальності також були нижчими для тих, хто приймав варфарин у терапевтичній дозі (6,4%) та ПОАК (6,3%) порівняно з тими, хто не отримував антикоагулянтної терапії (9,3%) або використовував лише антитромбоцитарне лікування (8,1%) чи варфарин у субтерапевтичній дозі (8,8%).
Ефективність антикоагулянтів (у порядку зростання ризику судинної катастрофи), за результатами досліджень, можна представити у такому вигляді: 150 мг дабігатрану 2 р/добу (Connolly et al., 2009, 2010, 2014) → 5/2,5 мг апіксабану 2 р/добу (Granger et al., 2011) → 60/30 мг/добу едоксабану (Giugliano et al., 2013) → 20/15 мг/добу ривароксабану (Patel et al., 2011) → 110 мг дабігатрану 2 р/добу (Connolly et al., 2009, 2010, 2014) → 30/15 мг/добу едоксабану (Giugliano et al., 2013).
Порівняння ефективності апіксабану та варфарину, за словами Ю.В. Фломіна, дозволяє дійти висновку, що перевага апіксабану в зменшенні ризику інсульту та системної емболії становить 8%, ризику геморагічного інсульту – 55%, летальної кровотечі – 50%, внутрішньочерепного крововиливу – 58% та смерті від будь-якої причини – 11%. Дабігатран та апіксабан є дієвішими, ніж варфарин, а ефективність ривароксабану щодо профілактики інсульту при ФП така ж, як у варфарину (Lowenstern et al., 2018).
Вплив АСК та апіксабану вивчали у субаналізі результатів дослідження AVERROES, в якому взяли участь 5599 пацієнтів, з яких 784 (14%) перенесли транзиторну ішемічну атаку (ТІА) або інсульт та у 92% випадків мали ≥3 балів за шкалою прогнозування й оцінки ризику ішемічного інсульту (CHADS2). Так, при порівнянні з АСК приймання апіксабану було асоційоване зі зменшенням на 71% ризику інсульту чи системної емболії. Відносно ризику великих кровотеч значущих відмінностей не виявлено, тому можна стверджувати, що апіксабан є суттєво ефективнішим порівняно з варфарином і має такий самий профіль безпеки (Diener et al., 2012).
Додатково в субаналізі результатів дослідження ARISTOTLE, в межах якого 3436 (20%) пацієнтів перенесли ТІА або інсульт (92% з цієї підгрупи мали ризик за шкалою CHADS2 ≥3 балів), визначали ефективність вторинної профілактики. При порівнянні з варфарином апіксабан характеризувався меншим ризиком (Easton et al., 2012):
- інсульту або системної емболії (менше на 24%);
- великої кровотечі (менше на 27%);
- внутрішньочерепного крововиливу (менше на 63%);
- смерті (менше на 11%).
За словами Ю.В. Фломіна, незважаючи на лікування прямими ПОАК, повторні інсульти трапляються. Для виявлення причини повторного інсульту на тлі використання ПОАК М. Paciaroni et al. (2019) провели дослідження типу випадок/контроль. Було проаналізовано дані 713 пацієнтів (641 випадок ішемічного інсульту та 72 – ТІА, медіана віку – 80 років) і 700 осіб групи контролю; 64% повторних ішемічних інсультів були до кардіоемболічними.
При багатофакторному аналізі незалежними предикторами повторної події були: низька доза ПОАК (поза зареєстрованими показаннями – off-label); відношення шансів (ВШ) 3,18; збільшення передсердя (ВШ 6,64); гіперліпідемія (ВШ 2,40); вища оцінка за CHA2DS2-VASc (ВШ 1,72 на кожен додатковий бал).
За твердженням В.М. Фломіна, спостереження за пацієнтами після інсульту – важлива умова безпеки та ефективності лікування. Дослідження M.J. Ross et al. (2011) з участю 3500 пацієнтів з інсультом показало, що: цільовий артеріальний тиск підтримується у 56% пацієнтів; цільовий рівень холестерину ліпопротеїдів низької щільності – у 36%, глікозильованого гемоглобіну – у 40%; терапевтичний діапазон МНВ – у 41%; адекватний контроль симптомів депресії – у 39%. Організоване спостереження знижує ризик смерті на 25% протягом першого року після інсульту.
На думку доповідача, необхідними компонентами адекватного ведення пацієнта є (Adeoye et al., 2019):
- спостереження протягом ≥1 року;
- консультації фахівців з інсульту за направленням від сімейного лікаря;
- менеджмент ТІА;
- оцінка результатів (за модифікованою шкалою Ренкіна через 90 днів і т.д.);
- контроль пізніх ускладнень (депресія, біль, спастичність, інсомнія та ін.);
- навчання лікарів інших спеціальностей та медсестер;
- нагляд сімейного лікаря і профільних фахівців (за потреби) за всіма пацієнтами, виписаними зі стаціонара після лікування із приводу інсульту; навчання хворого і членів його родини.
- проведення скринінгу на пізні ускладнення, розробка індивідуальних планів лікування, забезпечення вторинної профілактики, зокрема модифікації способу життя і корекції факторів ризику, – необхідні напрями роботи інсультних центрів з метою стандартизації спостереження за пацієнтами після інсульту.
Окрім того, Ю.В. Фломін навів тактику ведення пацієнта з гострим ішемічним інсультом з потенційно інвалідизувальним дефіцитом, який виник на тлі терапії ПОАК (Steffel et al., 2018):
- Визначення концентрації ПОАК у крові.
- Якщо ПОАК у крові відсутній (лабораторно не визначається), слід розглянути проведення тромболізису та/або тромбектомії.
- Якщо ПОАК у крові виявлений чи його визначення недоступне, але достеменно відомо, що останній прийом антикоагулянту був >48 год тому, і функція нирок нормальна, слід розглянути проведення тромболізису та/або тромбектомії.
- Якщо ПОАК у крові виявлений або його визначення недоступне, але є антидот (реверсант), слід ввести антидот і розглянути проведення тромболізису та/або тромбектомії після припинення дії ПОАК.
- Якщо ПОАК у плазмі виявлений і антидоту (реверсанту) немає, але достеменно відомо, що останній прийом антикоагулянту був >4 год тому, і концентрація ПОАК у плазмі <30 нг/мл (апіксабан, ривароксабан, едоксабан), в окремих випадках можна розглянути можливість проведення тромболізису та/або тромбектомії.
Доповідач підкреслив, що профілактика інсульту в осіб із неклапанною ФП, безумовно, має полягати в застосуванні ПОАК, які сприяють подовженню безцінного часу якісного життя пацієнта.
Підготувала Маргарита Марчук
Стаття друкується за підтримки компанії «Пфайзер»
PP-ELI-UKR-0060
Спецвипуск «Інсульт». Додаток до № 1 (52), 2020 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Стрес і тривожність чинять потужний несприятливий вплив і на самопочуття окремих індивідуумів, і на загальний стан здоров’я всієї популяції світу. Цей несприятливий вплив значно підсилили пандемія COVID‑19 та війна в Україні (Celuch M. et al., 2023)....
16-17 лютого в Києві відбувся науково-практичний майстер-клас «Хронічний стрес сьогодення: обрані запитання про здоров’я жінки в різні вікові періоди». Під час заходу виступили фахівці різних спеціальностей, було обговорено важливі аспекти жіночого здоров’я як психологічного, так і фізичного. Доповіді присвячувалися різноманітним питанням, зокрема репродуктивним проблемам, онкологічним захворюванням, психосоматичним розладам. Під час події виступила засновниця Академії довголіття Dr. Skytalinska, віцепрезидент Асоціації дієтологів України, лікар-дієтолог Оксана Василівна Скиталінська. Доповідь Оксани Василівни була присвячена впливу тривалого стресу на харчування та пов’язані з цим наслідки для здоров’я жінок. Окрім пояснення механізмів негативного впливу стресу, під час доповіді лікарка також надала важливі практичні рекомендації стосовно здорового харчування....
Події останніх 5 років є неабияким викликом для психічного стану кожного українця: спочатку – пандемія коронавірусу та запроваджені через неї карантинні обмеження, а далі – повномасштабне російське вторгнення, що триває уже понад 2 роки. Все це спричиняє погіршення психічного здоров’я населення. Такі надзвичайні ситуації, що характеризуються загрозою з невизначеною тривалістю, створюють масивне стресове навантаження, яке підсилюється відчуттям самотності та відчуженості, підвищують тривожність, а також є підґрунтям розвитку психічних розладів. Відомо, що ці стани порушують розумову діяльність, тобто перешкоджають концентрації та аналізу інформації. ...