Мультидисциплінарний підхід до ведення пацієнта з алергопатологією: фокус на комплаєнс лікування та якість життя
За матеріалами засідання Національної ради експертів
 Наприкінці 2019 року сталася важлива для алергологічної спільноти подія – засідання Національної ради експертів, присвячене питанням ведення пацієнтів з алергічними захворюваннями (АЗ) та поліпшення якості життя хворих. Зокрема, були розглянуті сучасні рекомендації щодо лікування пацієнтів з алергічним ринітом (АР) та хронічною кропив’янкою (ХК), а також роль спеціалістів первинної та вторинної ланки в лікуванні цієї когорти пацієнтів. Особливу увагу учасники засідання приділили заходам із підвищення професійного рівня надання медичної допомоги хворим на алергопатологію.
Наприкінці 2019 року сталася важлива для алергологічної спільноти подія – засідання Національної ради експертів, присвячене питанням ведення пацієнтів з алергічними захворюваннями (АЗ) та поліпшення якості життя хворих. Зокрема, були розглянуті сучасні рекомендації щодо лікування пацієнтів з алергічним ринітом (АР) та хронічною кропив’янкою (ХК), а також роль спеціалістів первинної та вторинної ланки в лікуванні цієї когорти пацієнтів. Особливу увагу учасники засідання приділили заходам із підвищення професійного рівня надання медичної допомоги хворим на алергопатологію.
У засіданні взяли участь провідні вітчизняні та зарубіжні експерти:
І.Дж. Ансотегуї (м. Більбао, Іспанія) – президент Всесвітньої алергологічної організації (WAO) і Південно-Європейської алергологічної спільноти, доктор медичних наук, завідувач Центру алергології та імунології клініки м. Більбао.
С.В. Зайков (м. Київ, Україна) – президент Асоціації алергологів України, доктор медичних наук, професор кафедри фтизіатрії і пульмонології Національної медичної академії післядипломної освіти ім. П.Л. Шупика (м. Київ).
І.В. Гогунська (м. Київ, Україна) – віце-президент Асоціації алергологів України, доктор медичних наук, провідний науковий співробітник ДУ «Інститут отоларингології ім. О.С. Коломійченка НАМН України», заступник керівника Центру алергічних захворювань верхніх дихальних шляхів і вуха ДУ «Інститут отоларингології ім. О.С. Коломійченка НАМН України», заслужений лікар України.
Л.І. Романюк (м. Київ, Україна) – віце-президент Асоціації алергологів України, доктор медичних наук, професор, заслужений лікар України, Київський міський алергоцентр.
Я.О. Дзюблик (м. Київ, Україна) – доктор медичних наук, провідний науковий співробітник ДУ «Національний інститут фтизіатрії і пульмонології ім. Ф.Г. Яновського НАМН України».
Т.В. Святенко (м. Дніпро, Україна) – професор, доктор медичних наук, віце-президент Української Асоціації лікарів дерматовенерологів і косметологів, член Європейської Академії дерматовенерології, професор кафедри шкірних та венеричних хвороб Дніпропетровської медичної академії, засновник Центрів дерматології і косметології професора Святенко (м. Дніпро).
М.Н. Кочуєва (м. Харків, Україна) – доктор медичних наук, професор, завідувач кафедри фтизіатрії, пульмонології та сімейної медицини Харківської медичної академії післядипломної освіти, керівник ГО «Асоціація безперервної медичної освіти та професійного розвитку лікарів України».
Сучасний стан проблеми алерголопатології в Україні та світі
 АЗ є глобальною медичною проблемою. Через їх високу поширеність, а також негативний соціально-економічний вплив, пов’язаний із погіршенням якості життя пацієнтів, АЗ були визначені як епідемія XXI століття. Частота алергічної патології у світі становить приблизно 30-40% у загальній популяції і продовжує зростати. В Україні спостерігається аналогічна ситуація, але статистика суперечлива, і об’єктивні дані на сьогодні відсутні, що зумовлено низкою причин:
АЗ є глобальною медичною проблемою. Через їх високу поширеність, а також негативний соціально-економічний вплив, пов’язаний із погіршенням якості життя пацієнтів, АЗ були визначені як епідемія XXI століття. Частота алергічної патології у світі становить приблизно 30-40% у загальній популяції і продовжує зростати. В Україні спостерігається аналогічна ситуація, але статистика суперечлива, і об’єктивні дані на сьогодні відсутні, що зумовлено низкою причин:
- Глобальна і перманентна реструктуризація системи охорони здоров’я з втратою точок збору статистичних даних.
- Несвоєчасне звернення за медичною допомогою та самолікування.
- Відсутність єдиного реєстру між дитячою і дорослою алергологічною службою.
- Неможливість отримання статистичних даних із приватних медичних центрів.
Тільки за попередній рік у Києві в алергологічному центрі було проліковано 1617 тис пацієнтів із різною алергічною патологією, з них майже 10 тис мали діагноз «алергічний риніт» (АР), причому чверть уперше звернулися за медичною допомогою.
У переважній більшості випадків захворювання дебютує до 20 років, з його піком у працездатному віці. За даними деяких авторів, 25% випадків алергічної патології реєструється у віці 20-40 років. У 20% дітей із атопічним дерматитом у майбутньому розвивається бронхіальна астма (БА). За оцінками Всесвітньої організації охорони здоров’я (ВООЗ), сьогодні у світі АР діагностується в 400 млн осіб, а БА – у 300 млн. І прогнози, на жаль, невтішні – до 2050 року кількість осіб, які страждають на ту чи іншу алергічну патологі, збільшиться до 4 млрд, набуваючи характеру неінфекційної епідемії.
 Шлях, який долає пацієнт з алергією, для діагностики, отримання адекватного лікування та усунення симптомів, часто неймовірно складний і тривалий, і це ще більше погіршує якість його життя. Відомо, що в пацієнтів з АЗ, зокрема з АР, без проведення спеціального тестування з алергенами доволі складно визначити наявність алергії. Однієї історії хвороби може бути недостатньо для точної діагностики етіології АР. Саме тому важливо мати чітке уявлення про основні механізми розвитку АЗ, принципи їх діагностики та лікування.
Шлях, який долає пацієнт з алергією, для діагностики, отримання адекватного лікування та усунення симптомів, часто неймовірно складний і тривалий, і це ще більше погіршує якість його життя. Відомо, що в пацієнтів з АЗ, зокрема з АР, без проведення спеціального тестування з алергенами доволі складно визначити наявність алергії. Однієї історії хвороби може бути недостатньо для точної діагностики етіології АР. Саме тому важливо мати чітке уявлення про основні механізми розвитку АЗ, принципи їх діагностики та лікування.
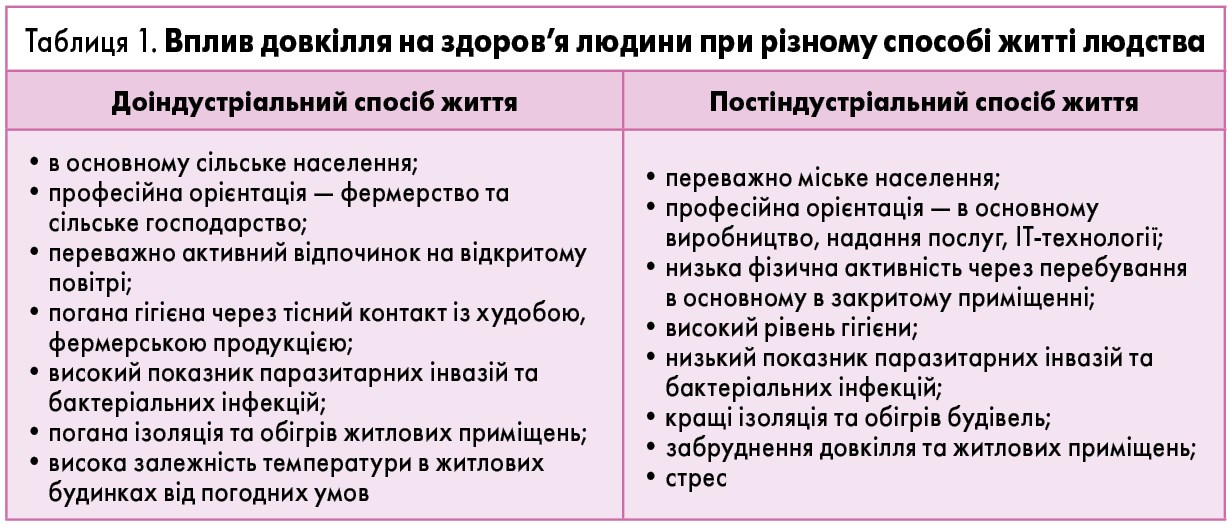
АЗ є генетично детермінованими, і в пацієнтів із гіперчутливістю до алергенів кількість відповідальних генів значно більша, ніж в інших хворих. Однак реалізація алергічної реакції залежить не тільки від спадковості, а й від впливу факторів довкілля. За останні 100 років індустріалізація та урбанізація внесли свої корективи в повсякденне життя людини, що стало причиною зростання алергічної патології. А саме:
- Значуще підвищився рівень гігієни та знизився контакт із бактеріальною або паразитарною інфекцією (табл. 1).
- Сьогодні людина більше часу перебуває не на свіжому повітрі, а в приміщенні зі стабільним температурним режимом. І всупереч поширеній думці, усередині будівель кількість алергенів може в багато разів перевищувати таку на вулиці.
- Суттєво підвищився рівень забруднення повітря, що, з одного боку, є прямою причиною розвитку алергії, а з іншого – опосередковано підвищує ризик розвитку БА через порушення нормального формування бронхолегеневої системи. У низці публікацій показано зростання поширеності респіраторних симптомів у дітей, які живуть у будинках уздовж доріг.
- У сучасної людини наявний високий рівень стресу. А гістамін є одним із важливих нейромедіаторів, який бере безпосередню участь у цьому процесі.
- Унаслідок парникового ефекту збільшується тривалість періоду цвітіння рослин.
Коморбідність та якість життя пацієнтів із алергопатологією
Відомо, що 80% пацієнтів з АЗ в Україні мають множинну сенсибілізацію, зокрема щонайменше до трьох алергенів. Це було продемонстровано в дослідженні із застосуванням ALEX-тесту в 3 тис пацієнтів. До того ж важливо враховувати, що пацієнти з АЗ частіше страждають на різні респіраторні інфекції. При цьому спостерігається взаємне потенціювання – підвищується як алергічна, так і запальна відповідь, включається ціла низка складних імунних реакцій, які поки є предметом наукових досліджень.
Незважаючи на те що АР або кропив’янка не сприймаються як тяжкі захворювання, якість життя пацієнтів значно погіршується. У 56% із них спостерігається зниження працездатності, 48% скаржаться на порушення сну, понад 50% зазначають вплив захворювання на повсякденну діяльність. Крім того, у декого з них можливий розвиток депресії на тлі алергічної патології. Основна невирішена проблема терапії цієї категорії хворих – гіподіагностика та невірно обрана тактика лікування.
 Нерідко пацієнтам з АЗ виставляється діагноз тієї або іншої респіраторної інфекції. Необґрунтовано призначаються антигістамінні препарати 1-го покоління (АГП‑1), деконгестанти тривалої дії та глюкокортикоїди (ГК) в якості першої лінії терапії. Застосування АГП‑1 у пацієнтів з алергопатологією є спільною проблемою для всіх країн, і вона посилюється через широку рекламу в засобах масової інформації, що неприпустимо. З огляду на те що пацієнти звертаються до фахівців різних спеціальностей, дуже важливого значення набуває підвищення кваліфікації лікарів в області алергології, і насамперед це стосується лікарів загальної практики – сімейної медицини. У 2019 р. в Україні вже понад 2 тис фахівців пройшли навчання в рамках освітньої програми, і така практика має продовжитися і набути більш широкого поширення.
Нерідко пацієнтам з АЗ виставляється діагноз тієї або іншої респіраторної інфекції. Необґрунтовано призначаються антигістамінні препарати 1-го покоління (АГП‑1), деконгестанти тривалої дії та глюкокортикоїди (ГК) в якості першої лінії терапії. Застосування АГП‑1 у пацієнтів з алергопатологією є спільною проблемою для всіх країн, і вона посилюється через широку рекламу в засобах масової інформації, що неприпустимо. З огляду на те що пацієнти звертаються до фахівців різних спеціальностей, дуже важливого значення набуває підвищення кваліфікації лікарів в області алергології, і насамперед це стосується лікарів загальної практики – сімейної медицини. У 2019 р. в Україні вже понад 2 тис фахівців пройшли навчання в рамках освітньої програми, і така практика має продовжитися і набути більш широкого поширення.
Ведення пацієнтів з АР та ХК
Як уже було зазначено, АР негативно впливає на якість життя пацієнтів. Наслідки таких симптомів, як порушення сну, стомлюваність протягом дня, застосування АГП‑1, можуть призвести до зниження працездатності тих, хто працює або вчиться. До того ж це захворювання є фактором розвитку БА. Незважаючи на пильну увагу лікарів різних спеціальностей до проблеми АР і успіхи медицини в діагностиці та лікуванні пацієнтів з указаною патологією, є низка важливих аспектів і питань, вирішення яких необхідно для підвищення ефективності ведення хворих на АР.
Негативний вплив на якість життя пацієнтів має кропив’янка. Дослідження перебігу ХК виявили серйозні порушення у хворих сну, їх соціальну ізоляцію, нестабільну емоційну сферу, проблеми на роботі, у сім’ї, пов’язані як із самим захворюванням, так і з проведеним лікуванням. Якість життя – це ступінь відчуття пацієнтом комфортності, як особистої, так і в рамках суспільства.
Згідно з оновленими Рекомендаціями ARIA (2017) перша лінія терапії АР і ХК – це тривалий курс прийому АГП 2-го покоління (АГП‑2). Треба зменшити застосування АГП‑1, а також розробити навчальні курси для фармацевтів і лікарів суміжних спеціальностей, спрямовані на правильний вибір у рамках комплексного обстеження та лікування.
Ефективність АГП‑2 продемонстрована не лише в лікуванні ХК і АР, а й у складі комплексної терапії БА – продукція слизу і вираженість симптомів на тлі прийому АГП‑2 достовірно знижується.
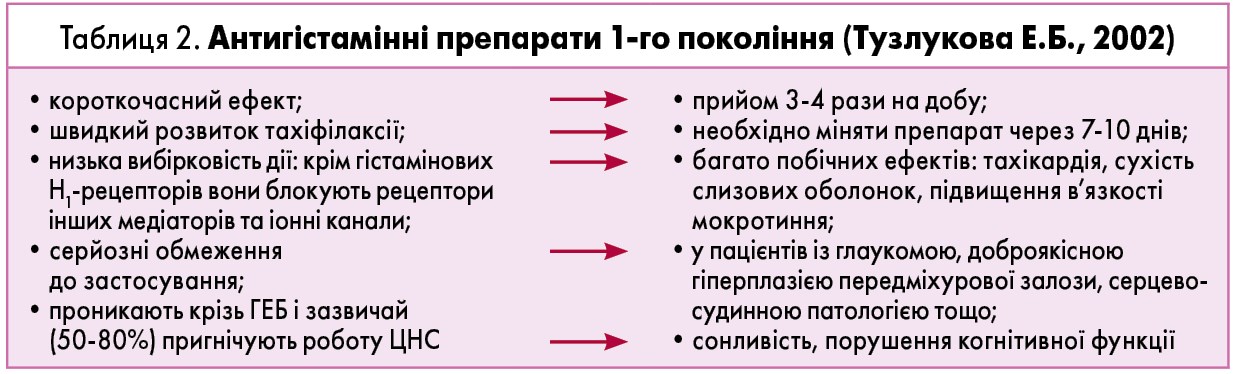
У цілому механізм дії АГП реалізується шляхом конкурентного інгібування Н1-рецепторів, тим самим блокуючи дію гістаміну. Але є значущі відмінності між препаратами 1-го та 2-го покоління. АГП‑1, крім Н1-рецепторів, також блокують холіно- і адренорецептори, реалізуючи цілий перелік побічних ефектів із боку серцево-судинної, сечовидільної і травної систем. Крім цього, вони є жиророзчинними амінами і легко проникають крізь гематоенцефалічний бар’єр (ГЕБ), провокуючи виражений снодійний ефект. Це пояснюється тим, що гістамін регулює циркадні ритми сну й неспання. Але прийом АГП‑1 не рекомендується навіть на ніч, з огляду на порушення якості сну і розвиток у подальшому денної сонливості (табл. 2).
АГП‑2, на відміну від АГП‑1, вибірково й тривало блокують тільки Н1-рецептори – через високу афінність, що запобігає появі побічних ефектів із боку серцево-судинної, сечовидільної і травної систем та забезпечує пролонгований клінічний ефект. При цьому завдяки своїй структурі АГП‑2 практично не проникають крізь ГЕБ і не викликають небажаних явищ із боку центральної нервової системи (ЦНС).
Слід звернути увагу на наявність концепції мінімального постійного запалення у хворих на АЗ навіть за відсутності симптомів, а АГП‑2, крім антигістамінної, мають протизапальну дію, знижуючи рівень прозапальних цитокінів, що пояснює більш високу результативність пролонгованих курсів лікування, показану в результатах численних досліджень.
Синтез цієї групи препаратів став значущим проривом, тому що крім очевидної ефективності вони продемонстрували хорошу безпеку і комплаєнс, забезпечивши високу якість життя пацієнтів.
Принцип, який добре себе зарекомендував, а саме принцип ступеневого підходу ARIA до лікування пацієнтів з АР, полягає в збільшенні обсягу терапії / переході на щабель угору (step-up) за відсутності контролю симптомів АР і зниженні обсягу терапії / переході на щабель униз (step-down) у разі досягнення й підтримки контролю симптомів. Для цього сьогодні застосовують топічні та пероральні АГП‑2, кромони, антагоністи лейкотрієнових рецепторів, інтраназальні ГК коротким курсом і їх комбінацію з АГП. Комбінація декількох АГП виявилася невиправданою. При незадовільному контролі симптомів потрібно обрати один препарат, який добре переноситься, але в більш високій дозі.
Надзвичайно важливо підходити до лікування кожного пацієнта індивідуально. Головними завданнями лікування пацієнтів з АЗ є: контроль симптомів; профілактика ускладнень; відсутність обмежень у повсякденному житті, фізичній активності і впливу симптомів алергії на навчання та працездатність; профілактика БА і відсутність побічних ефектів терапії. Призначене лікування має усунути симптоми в пацієнтів з АЗ та підвищити якість їх життя, а це включає не тільки прийом препаратів або алерген-специфічну імунотерапію (АСІТ). Дуже важливий момент – елімінація алергенів у приміщенні, відмова від вживання потенційно небезпечних продуктів, від виїздів на природу, пікніків і тривалих прогулянок у період цвітіння рослин.
Важливу роль у поліпшенні стану та підвищенні якості життя хворого відведено спеціалістам первинної ланки – сімейним лікарям, основне завдання яких своєчасно діагностувати алергію і призначити адекватне лікування та направити пацієнта до лікарів-алергологів для проведення специфічної алергодіагностики та АСІТ. Рекомендації лікаря, з одного боку, мають відповідати міжнародним стандартам ведення пацієнтів з АЗ, а з другого – полегшити повсякденне життя хворих на алергію. Відповідно до міжнародних рекомендацій АГП‑2 призначають на всіх етапах терапії АЗ, незалежно від ступеня їх тяжкості.
Незважаючи на всі переваги АГП‑2, між окремими препаратами цієї групи є відмінності щодо тривалості дії, наявності побічних ефектів, окупації рецепторів ЦНС або взаємодії із системою цитохрому Р‑450. Ефективнішими та безпечнішими вважаються активні метаболіти АГП‑2, які характеризуються мінімальною кількістю побічних ефектів, тривалою дією, зручним прийомом 1 раз на добу та відсутністю звикання. Одним із представників цієї групи є фексофенадин у складі препарату Аллегра® (ТОВ «Санофі – Авентіс Україна»).
Фексофенадин позбавлений кардіотоксичної дії навіть при 10-кратному збільшенні дози, не метаболізується в печінці, не впливає на нирковий кліренс, тому зарекомендував себе в лікуванні АЗ як ефективний препарат із високим профілем безпеки, передусім у пацієнтів з обтяженим або невідомим соматичним статусом.
Фексофенадин має такі характеристики:
- Селективна блокада H1-рецепторів.
- Ефективний проти широкого спектру симптомів АР і ХК, що позитивно впливає на якість життя хворих.
- Швидкий початок дії.
- Відрізняється довготривалою (24 год) дією.
- Не виявлено седативного ефекту й впливу на когнітивні та психомоторні функції.
Одне з великих плацебо-контрольованих досліджень за участю 1700 пацієнтів з АР показало високу ефективність фексофенадину в купіруванні основних симптомів навіть у дозах, нижчих за терапевтичні (<120 мг). При цьому частота побічних ефектів була порівнянна з такою в групі плацебо. Фексофенадин не викликав сонливості, не порушував когнітивну функцію і не впливав на швидкість реакції навіть при 3-кратному збільшенні терапевтичної дози, що дає можливість призначати його пацієнтам, які керують транспортними засобами. Також в одному з досліджень була показана безпека фексофенадину в разі одночасного з його прийманням вживання алкоголю в малих дозах.
Фексофенадин має всі переваги сучасного АГП: ефективність, безпеку, пролонговану дію, хороший комплаєнс.
Після доповідей експертів, які було вислухано з великим інтересом, відбулася дискусія з проблеми ведення пацієнтів з алергопатологією. У ході діалогу було визначено роль сімейного лікаря та лікаря-алерголога на різних етапах діагностики та лікування АЗ, окреслені проблеми, з якими стикаються пацієнти на цих етапах, а також шляхи підвищення якості життя хворих.
За результатами обговорення експерти вирішили заявити про таке:
- Чітке визначення зон відповідальності між лікарем первинної ланки і спеціалізованої допомоги, а саме: пацієнти з алергічними захворюваннями обов’язково мають бути проконсультовані лікарем-алергологом.
- Проведення за участю сімейних лікарів освітніх та науково-просвітницьких проектів, присвячених проблемі діагностики й лікування алергічних захворювань, важливості більш глибокого обстеження для виключення або підтвердження супутньої бронхіальної астми, а також визначення критеріїв для направлення до лікарів-алергологів для проведення специфічної алергодіагностики та алерген-специфічної терапії. Покращення взаємодії лікарів, фармацевтів та провізорів.
- Всі дії лікаря мають бути максимально спрямовані на усунення симптомів та поліпшення якості життя пацієнта: своєчасна і правильна діагностика, у тому числі алергодіагностика, лікування згідно з міжнародними стандартами, яке відповідає основним вимогам пацієнта і має високу ефективність, швидкість терапевтичної дії і тривалість, що забезпечувало б зручну кратність прийому препарату, його безпеку, можливість збільшувати дозу в разі необхідності, відсутність седативного ефекту.
- Необхідно роз'яснити пацієнту важливість потенційного шкідливого впливу факторів довкілля та порадити, як мінімізувати цей вплив. Рекомендується звертати увагу пацієнта на додаткові немедикаментозні засоби корекції для підвищення ефективності терапії – відмову від куріння, елімінацію причинно-значущих алергенів у приміщенні, виключення з раціону потенційно небезпечних продуктів, уникнення тривалих прогулянок у період цвітіння рослин.
- В якості симптоматичної терапії рекомендується використовувати антигістамінні засоби 2-го покоління, в яких відсутні антихолінергічна або антиадренергічна активність і седативний ефект. Оригінальний препарат фексофенадину призначений для усунення симптомів алергічного риніту та кропив’янки і відповідає всім вимогам міжнародних протоколів лікування алергічних захворювань (EAACI, GA2LEN, EDF, WAO і ARIA).
Підготувала Ірина Чумак
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 1 (50), 2020 р.
СТАТТІ ЗА ТЕМОЮ Алергія та імунологія
Організм людини – це складна жива система, функціонування якої визначається безліччю змінних і задіює величезну кількість механізмів. Зовнішні і внутрішні чинники здатні порушувати регуляцію її діяльності. Однак є механізми, які допомагають ефективно усувати «поломки» в організмі і нормалізувати його стан. Така здатність має назву біорегуляції. Основою біорегуляційної медицини є комплексні біорегуляційні препарати, серед яких одним із найвідоміших є Ехінацея Композитум С. ...
Проблема гострих запальних захворювань верхніх дихальних шляхів (ВДШ), гострого риносинуситу (ГРС) зокрема, є однією з найактуальніших у сучасній клінічній медицині. Останніми роками спостерігають зростання частоти захворювань носа і приносових пазух, що проявляється збільшенням як абсолютних (захворюваності та поширеності), так і відносних (частка в структурі оториноларингологічної патології) показників. В Україні поширеність гострих ринітів, риносинуситів та ринофарингітів сягає 489,9 випадку на 10 тис. населення, а захворюваність – 5-15 випадків на 1 тис. населення залежно від сезону. Такі хворі становлять 60-65% амбулаторних пацієнтів лікарів-отоларингологів. Уніфікований клінічний протокол первинної та спеціалізованої медичної допомоги (УКПМД) призначений забезпечити організацію надання медичної допомоги пацієнтам із ГРС на всіх етапах медичної допомоги для своєчасного виявлення, профілактики та лікування ГРС. ...
Хронічна кропив’янка (ХК) – це патологія, яка характеризується рецидивними нестійкими висипаннями з/без ангіоневротичного набряку, які виникають мало не щодня впродовж більш як 6 тиж [1]. Розрізняють два варіанти ХК – хронічна індукована кропив’янка (ХІК), або фізична кропив’янка, зумовлена певними фізичними подразниками, такими як тиск, тепло або холод, і більш поширена хронічна спонтанна кропив’янка (ХСК), яка розвивається у 80-90% випадків і характеризується відсутністю відомих екзогенних чинників і причин [2]. На це захворювання страждає від 0,5 до 1% населення світу, переважно особи жіночої статі [3]. Повторні симптоми часто призводять до порушень сну та чинять виражений негативний вплив на якість життя (QoL) [4]. ...
Алергічний риніт (АР) є поширеним запальним захворюванням верхніх дихальних шляхів (ВДШ), особливо серед педіатричних пацієнтів. Ця патологія може знижувати якість життя, погіршувати сон та щоденну продуктивність. Метою наведеного огляду є надання оновленої інформації щодо епідеміології АР та його діагностики, з урахуванням зв’язку з бронхіальною астмою (БА). ...