Огляд результатів довготривалого глобального неінтервенційного дослідження ACROSTUDY (2004-2017)
за матеріалами C.J. Strasburger at al. Increasing frequency of combination medical therapy in the treatment of acromegaly with the GH receptor antagonist pegvisomant. European Journal of Endocrinology, 2018
Хоча операція на гіпофізі залишається терапією першої лінії для лікування акромегалії, приблизно 50% пацієнтів, для яких хірургічне втручання не є ефективним, необхідна медикаментозна терапія.
Варіанти медикаментозної терапії залишкової хвороби або пацієнтів, яким не показана операція, включають аналоги соматостатину (AСС), агоністи дофаміну (AД) та антагоніст рецепторів гормону росту (ГР) пегвісомант. Було продемонстровано, що монотерапія пегвісомантом нормалізує рівень інсуліноподібного фактора росту 1 (IФР-I) у 63-97% пацієнтів. Ефективність монотерапії АСС різниться, повідомлялося, що 17-55% хворих на акромегалію мали нормальні рівні ІФР-I на тлі цієї терапії. Пацієнтів, в яких відсутня задовільна відповідь на терапію АСС, можна переводити на монотерапію пегвісомантом. Однак іноді лікарі можуть приймати рішення щодо лікування пацієнтів, які не досягли адекватного контролю на терапії АСС, радше комбінацією АСС та пегвісоманту, ніж заміною AСС на пегвісомант, щоби поєднати сприятливий вплив обох препаратів.
У розпочатому в 2004 р. довготривалому глобальному неінтервенційному дослідженні ACROSTUDY, що збирало дані з клінічної практики в пацієнтів з акромегалією, які отримували пегвісомант, було визначено, що значна кількість пацієнтів отримувала комбіновану терапію. У ході аналізу було розглянуто дані тих пацієнтів, залучених до ACROSTUDY, які отримували пегвісомант разом із принаймні одним іншим препаратом для лікування акромегалії, щоб дізнатися більше про комбіноване медикаментозне лікування в реальній практиці.
Матеріали та методи дослідження
Усі залучені до ACROSTUDY до 17 листопада 2014 року пацієнти були ретроспективно класифіковані на 3 основні категорії на основі їх «вихідної» медикаментозної терапії акромегалії, яку визначали як дату початку отримання пегвісоманту. 76% пацієнтів розпочали терапію пегвісомантом до залучення до ACROSTUDY. Три основні режими терапії включали:
- терапію АСС пролонгованої дії в комбінації з пегвісомантом, або «Комбо АСС»;
- АД у комбінації з пегвісомантом, або «Комбо АД»;
- монотерапію пегвісомантом, яку назвали «Пег моно».
Пацієнти, які отримували як АСС, так і АД додатково до пегвісоманту, були включені в групу «Комбо AСС». Пацієнтів могли переводити на інші режими лікування в будь-який час за призначенням лікаря. Щоб вирішити цю складність, в аналізі визначено «періоди експозиції» трьох різних режимів лікування. Ті пацієнти, які змінили експозицію під час спостереження, згодом були класифіковані за типом терапії на дату щорічних візитів, кожен з яких представляв собою точку перехресного аналізу. Щорічний візит визначався як клінічний візит, найближчий до кожної 12-місячної часової точки після дати включення з інтервалом +/- 6 міс від цієї дати. Оскільки ін’єкції АСС пролонгованої дії не завжди вводяться через рівні 4-тижневі інтервали, пацієнтів вважали належними до категорії «Комбо АСС» доти, доки остання ін’єкція AСС була в межах 6 тиж, що передували даті візиту. Пацієнти в категорії «Комбо AД» мали були отримати дозу AД протягом 30 днів до дати класифікації. Для включення до категорії «Пег моно» AСС або AД не дозволялося протягом 42 або 30 днів відповідно. Графіки застосування пегвісоманту рідше, ніж щодня, трансформували в еквівалентні добові дози перед оцінкою. Дані про препарати та ефект лікування, включаючи дозу пегвісоманту і відсоток пацієнтів із рівнями ІФР-I у межах норми, представлені як щорічні перехресні значення на основі всіх наявних даних пацієнтів, які залишаються в тій самій категорії терапії з початку застосування пегвісоманту до переведення на іншу терапію або, якщо терапію не змінювали, до останнього зареєстрованого візиту.
Дослідниками було зареєстровано такі причини застосування комбінованої терапії АСС або АД із пегвісомантом у 416 пацієнтів: ІФР-I не контролюється, головний біль, гіперпролактинемія, пухлина біля хіазми зорового нерву, коекспресія пролактину, вартість чи інше. Варіанти відповіді для дослідника включали «так» або «ні»; дозволялася більш як одна відповідь.
Рівні ІФР-I у сироватці крові та біохімічні показники функції печінки визначали в місцевих лабораторіях. Магнітно-резонансну томографію (МРТ) гіпофіза необхідно було надсилати для центральної оцінки, якщо місцевий рентгенолог повідомляв про значні зміни в об’ємі гіпофіза незалежно від клінічного значення зміни.
Безпеку додатково аналізували шляхом оцінки всіх побічних явищ (ПЯ), про які повідомлялося після залучення до ACROSTUDY. ПЯ відносили до періоду експозиції режиму терапії, протягом якого вони розвинулися («Комбо АСС», «Комбо АД», «Пег моно»). Усі повідомлення дослідників про ПЯ були закодовані менеджером даних згідно з Медичним словником регуляторної діяльності (MedDRA 14.1).
Популяція дослідження
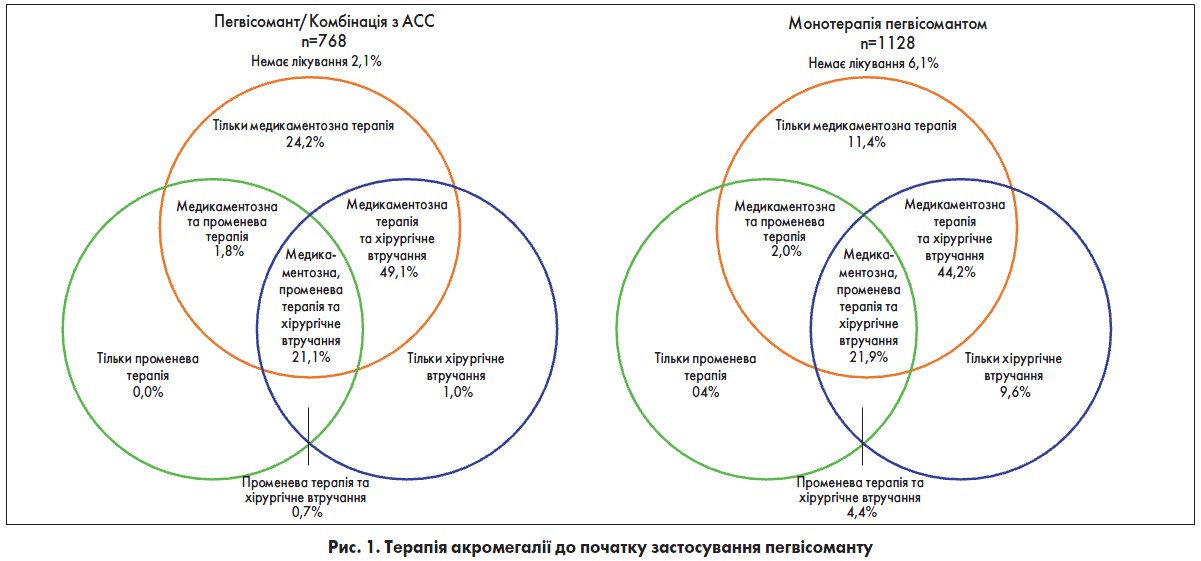
Станом на дату завершення збору даних, тобто на 17 листопада 2014 року, до ACROSTUDY було залучено всього 2043 пацієнти. Більшість (77%) перенесли операцію на гіпофізі, третині з них також проводили променеву терапію. Розподіл за статтю, середній вік, вага та індекс маси тіла (ІМТ) на момент включення в дослідження були зіставними між трьома категоріями. Рисунок 1 представляє різні методи лікування до початку прийому пегвісоманту в категоріях «Комбо АСС» та «Пег моно».
Результати дослідження
Характеристика пацієнтів
На основі ретроспективної класифікації медикаментозної терапії на момент початку застосування пегвісоманту 768 (38%) пацієнтів отримували «Комбо AСС», 123 (6%) – «Комбо AД», 1128 (55%) – «Пег моно» та 24 (1%) – інші препарати. У категорії «Пег моно» 20,6% не повідомляли про жодну медикаментозну терапію акромегалії до початку застосування пегвісоманту, а в категорії «Комбо AСС» – 3,8%. Час із моменту діагностування акромегалії до початку терапії пегвісомантом був коротшим у категорії «Комбо AСС», ніж у категоріях «Пег моно» та «Комбо AД». Однак більшість із цих пацієнтів перенесли хірургічне втручання та/або пройшли через променеву терапію. Час експозиції препаратів становив 2179 років у категорії «Комбо AСС», 412 – «Комбо АД» та 3578 – «Пег моно».
Серед 571 пацієнта із 7-річним спостереженням 55% залишилися в початковій категорії лікування, тоді як решта хоча б раз змінювала терапію, що могло статися в будь-який момент часу. Відсоток пацієнтів, які залишалися в початковій категорії лікування через 7 років після початку терапії пегвісомантом, складав: «Комбо AСС» – 44%, «Комбо АД» – 38%, «Пег моно» – 64%. У цілому цукровий діабет (ЦД) як супутнє захворювання було виявлено у 31% (діапазон: 30-35%) пацієнтів на початку терапії пегвісомантом, тоді як 54% (діапазон: 52-60%) повідомляли про гіпертонію.
Причина переходу на комбіновану терапію
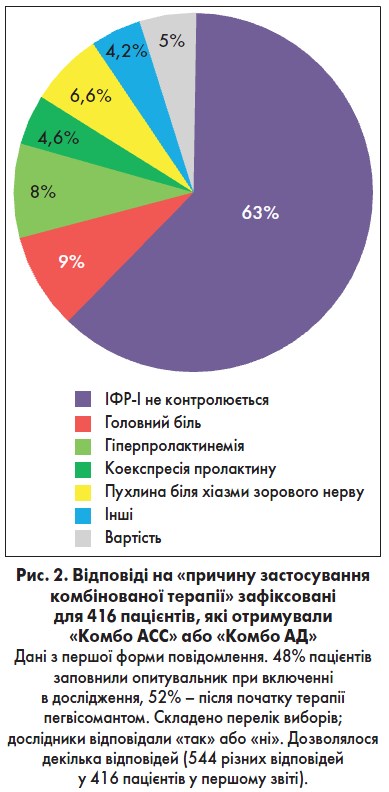 Після 7 років спостереження, за даними періоду експозиції, 45% пацієнтів хоча б один раз змінювали категорію лікування. Дані щодо причин(-и) комбінування пегвісоманту з іншим препаратом були доступні для 416 пацієнтів (рис. 2).
Після 7 років спостереження, за даними періоду експозиції, 45% пацієнтів хоча б один раз змінювали категорію лікування. Дані щодо причин(-и) комбінування пегвісоманту з іншим препаратом були доступні для 416 пацієнтів (рис. 2).
Режими терапії на момент початку застосування пегвісоманту за календарним роком та країною
Загальна схема лікування в ACROSTUDY змінювалася в ході дослідження з більшим відсотком пацієнтів на комбінованій терапії. У 2003 р. 20% пацієнтів отримували «Комбо AСС» або «Комбо АД» на початку залучення до ACROSTUDY порівняно з 54% у 2012 році. Також значні відмінності спостерігалися в практиці призначення між країнами. Пегвісомант у комбінації з AСС пролонгованої дії зазвичай застосовували в Нідерландах та Італії (69 і 52% пацієнтів відповідно), тоді як «Пег моно» частіше використовували у США, Іспанії та Німеччині (72, 70 і 66% пацієнтів відповідно).
Ефективність
Загалом у всіх групах середня доза пегвісоманту з часом незначуще збільшувалася, але не для всіх пацієнтів дозу достатньо титрували. Наприклад, на 4-му році, коли загальна кількість пацієнтів, які залишалися в початковій категорії лікування, становила 492 особи, вона включала 62% з нормальним ІФР-I у категорії «Комбо AСС», 63% – у «Комбо AД» та 65% – у «Пег моно». В усіх режимах лікування на момент включення пегвісомант застосовували у формі щоденних ін’єкцій 83% пацієнтів. У групі «Пег моно» щоденні ін’єкції застосовували 94% хворих, у той час як пегвісомант застосовували щоденно 66% пацієнтів із групи «Комбо AСС» і 91% – із групи «Комбо AД».
Безпека
Побічні явища
Для аналізу безпеки оцінці щодо ПЯ підлягали всього 1865 пацієнтів. Протягом періоду експозиції після початку ACROSTUDY у 946 (51%) пацієнтів було зареєстровано 3424 ПЯ, з яких 617 (18%) були віднесені до серйозних, 401 (12%) дослідники асоціювали з прийманням препарату. У 87 (4,7%) пацієнтів його було відмінено (тимчасово, остаточно або відстрочена доза) через серйозні ПЯ, незалежно від того, чи вважалися вони дослідниками пов’язаними з препаратом. Протягом указаного періоду було зафіксовано 48 смертей, і жодну дослідники не вважали як зумовлену препаратом. Найчастіше (>1,5% пацієнтів) повідомлялося про такі ПЯ (незалежно від того, чи вважалися вони дослідниками пов’язаними з препаратом): підвищення ІФР-I у 10,1% пацієнтів, підвищення печінкових трансаміназ (4,8%), головний біль (4,2%), дефіцит вітаміну D (3,6%), артралгія (3,6%), остеоартрит (2,7%), реакція в місці ін’єкції (3,0%), астенія (2,1%), депресія (1,9%), поліпи товстої кишки (1,8%), жовчнокам’яна хвороба (1,8%) та рецидив пухлини гіпофіза (1,6%).
Оцінка пухлини гіпофіза
Місцеву оцінку МРТ розміру пухлини гіпофіза реєстрували принаймні 1 раз в 1816 осіб у цілому, тоді як в 1647 було зареєстровано одне або декілька зображень упродовж щонайменше 30 днів після початку терапії пегвісомантом. За наявності дослідження МРТ про зменшення розмірів пухлини повідомлялося місцевими рентгенологами в 323 (19,6%) пацієнтів, про збільшення – у 119 (7,2%), а 54 (3,3%) демонстрували як збільшення, так і зменшення. Хоча всі випадки, коли локальна оцінка МРТ показала зміну (інтерпретовану як зменшення або збільшення), треба було подати для центральної інтерпретації МРТ, це було зроблено лише у 228 випадках. Додаткова центральна оцінка виявила зменшення розміру пухлини гіпофіза в 75 пацієнтів, збільшення – у 42, збільшення/зменшення – у 10, відсутність змін – у 71, щодо 30 пацієнтів не вистачало даних для визначення. Місцеві інтерпретації МРТ, подані як збільшення розміру пухлини (n=50), підтверджено в 20 випадках як збільшення, ще в 20 випадках їх було перекласифіковано як відсутність змін, у 3 – як збільшення і зменшення з часом. Серед тих пацієнтів, в яких місцеві дослідження показали зменшення розміру пухлини (n=80), центральна інтерпретація виявила зменшення в 48 осіб, у 24 перекласифікувала як відсутність змін, у 7 – виявила збільшення пухлини. Через зміни режимів лікування в різні інтервали між візитами виявилося неможливо окремо оцінити результати МРТ із часом відносно груп лікування.
Реакції в місці ін’єкції
Про проблеми в місці ін’єкції повідомляв 51 (3%) пацієнт. Найпоширеніші реакції в місці ін’єкції включали ліпогіпертрофію (n=18), реакцію в місці ін’єкції (n=12) і ліподистрофію (n=7). Кількість зареєстрованих реакцій у місці ін’єкції була низькою у всіх групах лікування.
Обговорення
Цей аналіз оцінював безпеку та ефективність довготривалої терапії з трьома різними методами лікування в пацієнтів з акромегалією в ході дослідження ACROSTUDY. Оцінювали дані пацієнтів, яким призначали комбінацію пегвісоманту та аналогу соматостатину, а також пацієнтів, які отримували монотерапію пегвісомантом або пегвісомант у комбінації з АД, протягом тих самих років. У цьому звіті використовуються нові дати закінчення збору даних, що забезпечує більшу когорту та включення двох додаткових років включення та спостереження порівняно з останньою публікацією ACROSTUDY, яка була зосереджена виключно на монотерапії пегвісомантом.
У цьому звіті частка пацієнтів на будь-якій комбінованій терапії, яких включали до ACROSTUDY, за майже 10 років значно зросла: із 20% у 2003 до 54% у 2012 році.
Понад десятиліття тому були опубліковані результати першого клінічного дослідження комбінації пегвісоманту та AСС, яке проводили в одному центрі в Нідерландах; пізніше з’явилися публікації про більш тривалі дослідження, в яких було показано нормалізацію рівнів ІФР-I у приблизно 90% пацієнтів. Інші публікації результатів комбінованої терапії включають обмежену кількість пацієнтів із нормалізацією ІФР-I між 58 і 97% залежно від визначення способу лікування та ефективності. Неггерс та співавт. повідомляли, що рівень ІФР-I був нормальним у 97% зі 112 пацієнтів, які отримували лікування АСС та ін’єкції пегвісоманту 1 раз або 2 рази на тиждень у дозі 80 мг на тиждень із медіаною 4,9 року (міжквартильний діапазон: 60-120 мг).
Пегвісомант найчастіше призначають у формі щоденних підшкірних ін’єкцій. Понад 90% пацієнтів у групах «Пег моно» та «Комбо АД» отримували щоденні ін’єкції, тоді як у групі «Комбо AСС» пегвісомант щодня отримували 66% хворих. Хайем та співавт. повідомили про невелике дослідження, в якому деяких пацієнтів було успішно переведено з щоденного приймання пегвісоманту на застосування 2 рази або 1 раз на тиждень. Інші дослідження показали застосування AСС у комбінації з пегвісомантом рідше, ніж щоденно, що могло сприяти цій практиці в реальних умовах.
У попередніх публікаціях підвищення рівнів печінкових ферментів спостерігалися частіше в пацієнтів, які отримували комбіновану терапію, порівняно з монотерапією пегвісомантом. Для цього аналізу важко визначити, чи пов’язана комбінована терапія з більш високою частотою підвищення рівня печінкових ферментів, оскільки 45% пацієнтів змінювали групи лікування хоча б один раз. Однак загальна частота повідомлень про підвищення рівня печінкових ферментів нижча, ніж у попередніх публікаціях. Це можна пояснити декількома причинами. Можливо, підвищені біохімічні показники функції печінки спостерігалися в декого з пацієнтів після початку терапії пегвісомантом, але до залучення їх до ACROSTUDY; ще однією причиною може бути впевненість дослідників у тому, що пацієнти, яких було включено в ACROSTUDY, добре переносять препарат. Крім того, оскільки показники функції печінки реєстрували лише щорічно в багатьох центрах, тимчасові підвищення, можливо, пройшли повз такої реєстрації.
Хоча відомо, що лікування соматотрофних аденом АСС зменшує розмір пухлин, цей аналіз не дає можливості оцінити будь-яку різницю між комбінацією пегвісоманту з AСС або AД та монотерапією пегвісомантом у зв’язку зі змінами режимів лікування. Через 7 років 45% пацієнтів змінювали режим лікування принаймні один раз, тому «групи» не були постійними в часі. Також буде помилкою вважати, ніби пацієнти зі складно контрольованою хворобою більш схильні до переходу з одного режиму на інший. Для оцінки розміру пухлини гіпофіза у 80% пацієнтів повідомлялося про принаймні дві оцінки МРТ. Надаючи можливість дослідникам надсилати МРТ, що на місцевому рівні показали зміни розміру гіпофіза, було підтверджено, що збільшення пухлин під час терапії пегвісомантом, як і в попередніх звітах, спостерігається не часто.
У невеликому дослідженні Йоргенсен та співавт. оцінили вплив супутньої терапії пегвісомантом та АСС на секрецію ГР, рівень ІФР-I та толерантність до глюкози. Вони повідомили, що пегвісомант покращив толерантність до глюкози в пацієнтів із відсутністю відповіді на лікування АСС. В ACROSTUDY понад 30% пацієнтів на момент включення повідомили про ЦД як супутнє захворювання.
До того ж слід зважати на звичайні обмеження обсерваційних досліджень; хоча вони й цінні, оскільки відображають «реальне» клінічне лікування, дані про візити пацієнтів не збираються в попередньо визначених регулярних часових точках, як це відбувається в проспективному дослідженні. У результаті часом відсутні дані у визначених часових точках, недостатньо реєструються ПЯ, порівняно з клінічними дослідженнями. Обмеження щодо ефективності полягає в тому, що дози пегвісоманту, які застосовували в ACROSTUDY, часто були низькими; якщо б застосовували більш високі дози, частота досягнення нормальних рівнів ІФР-I могла би бути вищою.
Важливо також зазначити, що категорії режимів лікування не були незалежними; дані одного пацієнта могли бути внесені в більш як одну категорію, якщо з часом лікування змінювали з монотерапії на комбіновану терапію.
У цілому це великий набір даних, що надає опис клінічної терапії пацієнтів, які отримують пегвісомант у комбінації з іншими препаратами, у 15 країнах.
Стаття друкується у скороченні.
Список літератури знаходиться в редакції.
C.J. Strasburger at al. Increasing frequency of combination medical therapy in the treatment of acromegaly
with the GH receptor antagonist pegvisomant. European Journal of Endocrinology. 2018. V 178: I 4. р.321-329;
doi.org/10.1530/EJE‑17-0996.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
21 березня в рамках II Міжнародної школи «Сучасний лікар: від теорії до практики» професор кафедри ендокринології Львівського національного медичного університету ім. Данила Галицького, лікар-ендокринолог вищої категорії, доктор медичних наук Вікторія Олександрівна Сергієнко представила доповідь, присвячену хронічним ускладненням цукрового діабету (ЦД). Зокрема, було акцентовано увагу на причинах розвитку діабетичної полінейропатії (ДП), розглянуто клінічні варіанти цього ускладнення, діагностичні підходи та основні принципи лікування. Пропонуємо огляд цієї доповіді у форматі «запитання – відповідь»....
Останніми десятиліттями в усьому світі спостерігалося значне зростання поширеності цукрового діабету (ЦД), що зумовило серйозні наслідки стосовно якості життя населення, а також спричинило певний тягар для системи охорони здоров’я та економічні витрати [1]. За даними Діабетичного атласу Міжнародної діабетичної федерації (International Diabetes Federation Diabetes Atlas), у 2021 р. ≈537 млн людей мали ЦД і, за прогнозами, до 2045 р. цей показник досягне 783 млн [2]. Значна захворюваність і підвищена смертність асоційовані з пов’язаними із ЦД макросудинними (інфаркт міокарда, інсульт) і мікросудинними (сліпота, ниркова недостатність, ампутації) ускладненнями [3]....
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....