Актуальні питання лікування спондилоартритів
 Спондилоартрити (СпА) – це група хронічних запальних ревматичних захворювань, при яких переважно уражається осьовий скелет, відбувається ерозування та надалі кістковий анкілоз у хребті та/або крижово-клубових суглобах. Майже в чверті випадків СпА з часом прогресують, що асоційовано з чоловічою статтю, наявністю органічного пошкодження хребта/суглобів на момент початку лікування, ступенем активності захворювання.
Спондилоартрити (СпА) – це група хронічних запальних ревматичних захворювань, при яких переважно уражається осьовий скелет, відбувається ерозування та надалі кістковий анкілоз у хребті та/або крижово-клубових суглобах. Майже в чверті випадків СпА з часом прогресують, що асоційовано з чоловічою статтю, наявністю органічного пошкодження хребта/суглобів на момент початку лікування, ступенем активності захворювання.
Головними завданнями терапії СпА є максимальне збереження функціональної активності хребта та/або суглобів, запобігання структурним незворотним змінам, покращення якості життя пацієнтів і збереження їхньої соціальної функції шляхом контролю основних проявів захворювання. Лікування до досягнення мети (treat to target) – сучасна концепція ведення ревматологічних хворих, яка передбачає насамперед моніторинг стану пацієнта з використанням інтегральних показників кожні 1-3 міс і за потреби – відповідну корекцію терапії з досягненням ремісії чи мінімальної активності захворювання. Для визначення останньої експерти ASAS-EULAR рекомендують шкали ASDAS (оцінка активності анкілозивного спондиліту), BASDAI (оцінка активності анкілозивного спондиліту при СпA), DAPSA (оцінка активності псоріатичного артриту – ПсА) чи MDA (мінімальна активність захворювання у хворих на ПсA).
На сьогодні цілком доведеним є вплив інгібіторів фактора некрозу пухлини (ФНП) на показники активності СпА. Анти-ФНП-препарати застосовуються при лікуванні СпА з переважними аксіальними проявами в пацієнтів, які не мають достатнього ефекту від застосування нестероїдних протизапальних препаратів (НПЗП) і в яких переважають периферичні прояви захворювання за відсутності достатнього ефекту від сульфосалазину (Van der Heijde D. et al., 2017). Отже, арсенал фармакологічних засобів, які могли б ефективно вплинути на перебіг і прогресування СпА, досить незначний, і більшість хворих потребує призначення анти-ФНП-препаратів.
Одним з інгібіторів ФНП, доступних на ринку України та дозволених до використання, є голімумаб – повністю людський моноклональний анти-ФНП-препарат. Голімумаб схвалено регуляторними органами Європейського Союзу (ЕМА) та США (FDA) для лікування запальних ревматичних захворювань (СпА, ПсА, ревматоїдного артриту – РА) та запальних захворювань кишечнику (виразкового коліту, хвороби Крона). Підставою для цього стали результати низки масштабних досліджень щодо ефективності та безпеки голімумабу для лікування СпА (GO-RAISE), дорентгенологічної форми СпА (GO-AHEAD), РА (GO-BEFORE, GO-AFTER, GO-FORTH, GO-FORWARD) і ПсА (GO-REVEAL, GO-VIBRANT).
У дослідження GO-RAISE було включено 356 пацієнтів зі СпА, в яких попередньо відзначали недостатній ефект від НПЗП і базисних засобів. Пацієнтів рандомізовано на три групи: голімумаб 50, 100 мг або плацебо 1 раз на 4 тиж. У разі недосягнення ASAS 20 на 16-му тижні пацієнти з групи плацебо переводилися до групи голімумабу. За результатами дослідження, на 14-й тиждень ASAS 20 у групі пацієнтів, які отримували голімумаб 50 мг, досягнуто в 59,4%, голімумаб 100 мг – у 60%. Покращення за BASMI ≥1,0 од. на 14-му тижні мали 44,2% хворих, які отримували голімумаб у дозі 50 мг, а на 24-му – 47,2%. На 104-му тижні лікування щонайменше 20% покращення за шкалою ASAS мали 60,1% пацієнтів групи голімумабу 50 мг, 71,4% – групи голімумабу 100 мг, 38,5% пацієнтів групи плацебо; досягнення ASAS 40 зафіксовано в 55,8; 54,3 та 38,5% осіб відповідно. Середнього показника BASDAI та BASFI <3 на 104-й тиждень досягнуто в усіх групах.
Випробування GO-AHEAD проводилося за участі 198 пацієнтів із дорентгенологічним аксіальним спондилітом. Лікування голімумабом 50 мг підшкірно (п/ш) упродовж 16 тиж, порівняно з плацебо, сприяло достовірному зменшенню інтенсивності запалення в сакроілеальних з’єднаннях за результатами МРТ: -5,3 проти -1,0 відповідно (p=0,001). Загалом покращення за МРТ-шкалою ураження сакроілеальних з’єднань було більш значним у пацієнтів, які на початок лікування мали активний сакроілеїт за результатами МРТ та/або підвищення рівня С-реактивного білка (СРБ). Автори припускають, що саме ці прогностичні фактори відповіді на лікування можуть бути використані в клінічній практиці для персоналізації терапевтичного підходу. Крім того, на 16-му тижні лікування покращення ASAS 20 зареєстровано в 71,1% хворих, які приймали голімумаб, а також відзначено достовірне зниження показників BASFI, BASMI, MASES (Маастрихтський індекс підрахунку ентезитів) порівняно з плацебо.
У реальній клінічній практиці в Німеччині проведено неінвазивне дослідження GO-NICE. До проспективного аналізу ефективності та безпеки голімумабу в дозі 50 мг 1 р/міс включено 1458 пацієнтів: 474 – з РА, 501 – із ПсА, 483 – із СпА. Середній показник BASDAI знизився в пацієнтів зі СпА з 5,0 до 3,4 через 3 міс лікування, далі продовжував знижуватися й до 24 міс утримувався на рівні 2,4. Частота відповіді за критерієм ефективності ПсА (PsARC) становила 67,9% через 24 міс. Лікування добре переносилося, профіль безпеки був зіставний із таким у попередніх рандомізованих клінічних випробуваннях.
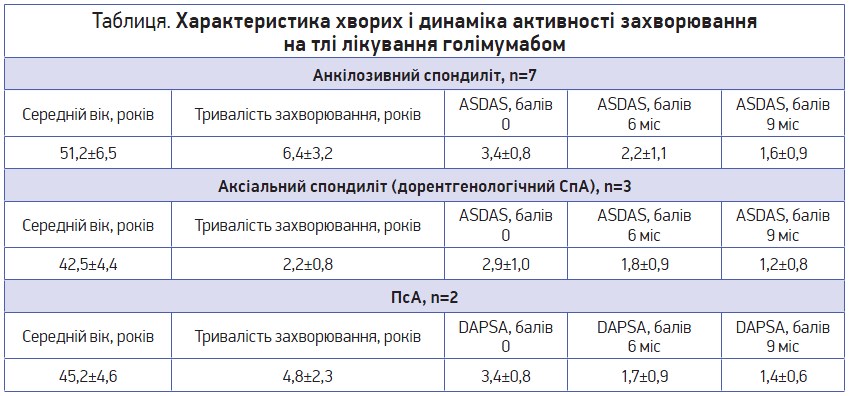
Власне дослідження проведено на базі першого ревматологічного відділення Олександрівської клінічної лікарні м. Києва, де під спостереженням перебувають 12 пацієнтів (1 жінка й 11 чоловіків), які отримують лікування голімумабом у дозі 50 мг п/ш 1 раз на 4 тиж. Характеристику хворих і динаміку активності захворювання за основними показниками наведено в таблиці.
На тлі лікування стан хворих значно покращився: зменшилися тривалість ранкової скутості, больові відчуття й обмеження рухів у хребті, знизилися гострофазові показники активності захворювання (СРБ, ШОЕ). У 2 пацієнтів, які на початку лікування приймали глюкокортикоїди, вже через 1 міс їх поступово відмінили. Покращення відзначали вже після першого застосування голімумабу, що виявлялося в зменшенні тривалості ранкової скутості та зниженні індексів BASFI, BASDAI, BASMI. Вираженіший ефект спостерігали в пацієнтів із дорентгенологічною формою аксіального спондиліту. Поліпшилися функціональна спроможність та якість життя хворих. Серед небажаних явищ фіксували транзиторне підвищення АСТ і АЛТ, яке не потребувало відміни препарату чи додаткового лікування, – в 1 пацієнта, а також інфекцію верхніх дихальних шляхів у легкій формі – у 2.
Варто зауважити, що функціональна активність хворих невід’ємно пов’язана з рентгенологічним прогресуванням захворювання. У разі спондиліту воно виявляється насамперед ерозуванням і появою нових синдесмофітів, які обмежують обсяг рухів у хребті та погіршують функціональні можливості пацієнта. Для оцінки рентгенологічного прогресування захворювання рекомендовано використовувати шкалу mSASSS (Stoke Ankylosing Spondylitis Spine Score). Згідно з методикою на бічних рентгенограмах оцінюють передні кути кожного з тіл хребців у грудному й поперековому відділах хребта на наявність ерозій та/або склерозу та/або квадратизації (1 бал), синдесмофітів (2 бали) та синдесмофітів, які з’єднують 2 хребці (3 бали). Загальна сума балів становить від 0 до 72.
У ході тривалих спостережень доведено зв’язок між активністю захворювання та виникненням нових синдесмофітів. Взаємозв’язок запалення й рентгенологічного прогресування СпА оцінювався впродовж 12 років у когорті пацієнтів OASIS. Підвищення активності СпА на 1 од. за ASDAS призводило до збільшення рентгенпрогресування на 0,72 од. кожні 2 роки. У пацієнтів з ASDAS ≥3,5 (висока активність захворювання) оцінка за шкалою mSASSS за 2 роки збільшилася на 2,3 од. Через 12 років у пацієнтів із високою активністю СпА показник mSASSS збільшувався на 19 од., а в разі неактивного захворювання – на 5 од. (Ramiro S. et al., 2014).
У дослідженні GO-RAISE у хворих без синдесмофітів на початку лікування, котрі протягом 4 років приймали голімумаб (у дозі як 50, так і 100 мг), зафіксовано достовірну відсутність рентгенологічного прогресування за шкалою mSASSS. Отже, за відсутності синдесмофітів запобігти їх розвитку можливо, застосовуючи в лікуванні анти-ФНП-препарати, що забезпечують достовірне зниження запального процесу.
У рандомізованих клінічних дослідженнях із тривалим періодом спостереження показано уповільнення рентгенологічного прогресування на тлі терапії блокаторами ФНП. Утім, синдесмофіти, котрі вже були в пацієнтів на момент призначення препаратів, не зникли (Harron N. et al., 2013; Baraliakos X. et al., 2014; Molnar C. et al., 2018). Згідно з даними літератури, інгібітори ФНП найефективніші, коли прийом розпочато досить рано (при дорентгенологічному СпА) й лікування триває досить довго (12-24 міс). Найбільш значущими факторами ризику рентгенологічного прогресування при СпА визнано куріння та високу активність запалення.
Позаскелетні прояви СпА
Частота позаскелетних проявів (ПСП) при СпА, за даними літератури, коливається в межах від 10 до 50%. Їх інтенсивність не завжди чітко асоційована з активністю захворювання. Найчастішими ПСП при СпА є ураження очей (увеїт), шкіри (псоріаз), запальні захворювання кишечнику (виразковий коліт і хвороба Крона), що значно погіршують якість життя пацієнтів, недостатньо відповідають на традиційне лікування НПЗП та синтетичними хворобомодифікувальними протиревматичними препаратами (сульфасалазином, метотрексатом тощо).
Метою дослідження GO-EASY було оцінити частоту увеїту при СпА за рік до початку лікування голімумабом і впродовж 12 міс його застосування. У випробуванні взяли участь 93 пацієнти зі СпА, серед яких 7 мали епізоди увеїту за рік до початку лікування, 5 – увеїт на момент включення в дослідження. Через 3 міс відповідь на лікування за ASAS 20 мали 36,5% хворих. Після завершення лікування (через 12 міс) достовірне покращення реєстрували за основним показником активності СпА (зниження BASMI: з 0,6 до 0,4 бала, BASDAI: з 5,4 до 3,3 бала; ASDAS: із 3,1 до 1,6 бала; BASFI: з 4,5 до 3,2 бала). Упродовж лікування голімумабом тільки 2 хворих мали 2 нові епізоди увеїту. Важливо, що в пацієнтів, які мали увеїт за рік до початку терапії чи на момент включення в дослідження, не реєстрували жодного нового епізоду. Автори дійшли висновку, що лікування голімумабом знижує ризик виникнення увеїту, в тому числі повторного (рецидивного), при СпА.
Ефективність голімумабу при ПсА доведена в клінічних дослідженнях GO-REVEAL і GO-VIBRANT. Перше являло собою багатоцентрове плацебо-контрольоване дослідження ІІІ фази, що проводилося з 2005 по 2012 р. У дослідження було включено 405 пацієнтів з активним ПсА, котрих рандомізували на три групи лікування: голімумаб 50, 100 мг або плацебо, що вводилися кожні 4 тиж до 252-го тижня лікування. Після останньої ін’єкції спостереження тривало ще 16 тиж. Ураження поверхні тіла псоріазом за показником PASI на 256-му тижні в групах голімумабу 50 і 100 мг зменшилося з 9,8±8,6 до 2,7±4,5 та з 11,1±9,5 до 2,2±3,9; досягнення PASI 75 зареєстровано в 61,5 та 72,2% пацієнтів відповідно. Достовірну позитивну динаміку також фіксували за індексом ураження нігтів, кількістю ентезитів (MASES) і дактилітів, інтегральними показниками активності DAS28-CRP, PsACR. Покращення фізичної активності за шкалами SF36 і HAQ-DI відзначали в 54,1% осіб групи голімумабу 50 мг і 58,2% – голімумабу 100 мг.
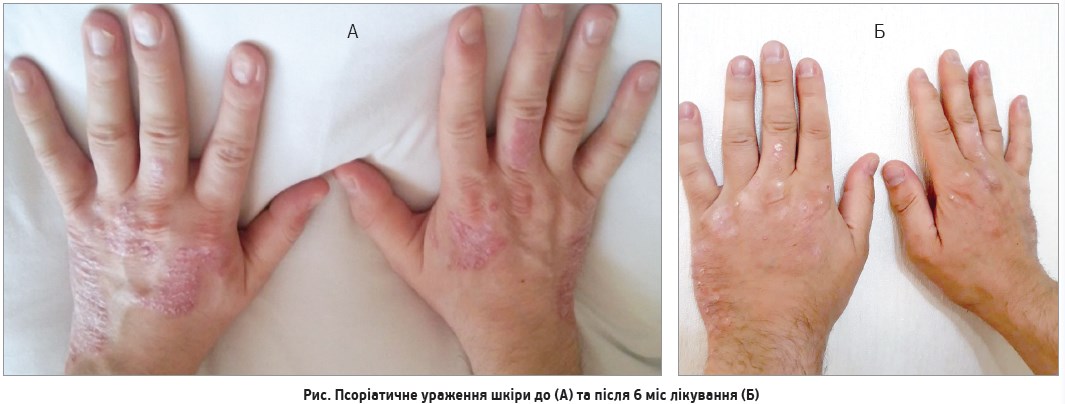
Власний досвід підтверджує, що лікування голімумабом сприяє зменшенню псоріатичного ураження шкіри через 6 міс (рис.). Клінічний діагноз хворого: ПсА, спондилоартритичний варіант, активність 3 ступеня з ураженням шийного та поперекового відділів хребта, правобічний сакроілеїт з ураженням колінних і правого променево-зап’ясткового суглобів, а також суглобів стоп і кистей, дактиліти, рентген-стадія ІІ, ФНС ІІ. Псоріаз шкіри поширений, генералізована форма, стаціонарна стадія. Динаміку основних інтегральних показників щодо активності ПсА відображено в таблиці. Через 6 міс лікування в пацієнта повністю відмінено глюкокортикоїди, через 9 міс досягнуто стійкої клініко-лабораторної ремісії.
Вплив інгібіторів ФНП на стан кісткової тканини при СпА
Призначення анти-ФНП-препаратів позитивно впливає на стан кісткової тканини пацієнтів зі СпА. Високий ступінь активності захворювання та різке обмеження функціональних можливостей пацієнтів асоційовано з порушенням стану кісткової тканини та розвитком системного остеопорозу (ОП). Зниження мінеральної щільності кісткової тканини (МЩКТ) при СпА відбувається переважно в аксіальному скелеті та шийці стегнової кістки. Частота ОП при СпА коливається від 11 до 35%, остеопенії – досягає 89%. Вертебральні переломи як ускладнення ОП хребта трапляються в 11-25% випадків, їх наявність посилює больовий синдром і ще більше обмежує рухи в хребті (Kilic E. et al., 2015; Ramírez J. et al., 2018).
Цікавою є оцінка стану кісткової тканини у хворих на СпА на тлі лікування імунобіологічними засобами. Позитивний вплив блокаторів ФНП був продемонстрований у багатьох дослідженнях (Haroon N.N. et al., 2014; Beek K.J. et al., 2019).
Клінічний випадок: пацієнт
П., 36 років, тривалість захворювання – 2,5 роки. Перед початком лікування обстежений згідно з протоколом призначення біологічних агентів, проведена рентгенівська абсорбціометрія. Встановлено клінічний діагноз: аксіальний спондиліт, хронічний перебіг, активність 3 ступеня з переважним ураженням грудного та поперекового відділів хребта, двобічний сакроілеїт, ентезити, рентген-стадія І, ФНС ІІ, HLA-B27-позитивність. ОП хребта без патологічних переломів.
Зважаючи на високу активність захворювання, центральну форму, відсутність ефекту від тривалого прийому НПЗП, молодий вік і згоду хворого на запропоноване лікування, було вирішено призначити біологічну терапію – інгібітор ФНП голімумаб. Упродовж 12 міс пацієнт отримував лікування голімумабом у дозі 50 мг п/ш 1 раз на 4 тиж. Стан хворого значно покращився: через 1 міс пацієнт не потребував прийому НПЗП, значно зменшилися ранкова скутість, біль та обмеження рухів у хребті. Під час проведення денситометрії через 12 міс відзначили збільшення МЩКТ хребта. Показник МЩКТ поперекового відділу L1-L4 до початку лікування становив 1,001 г/см2, через 12 міс – 1,080 г/см2, критерій Z – -2,5 та -1,8 SD відповідно. Приріст кісткової тканини за рік становив 7,9%. При оцінці МЩКТ хребців у латеральній проекції виявили збільшення показника на 9,5%.
Отже, зменшення активності запалення сприяло підвищенню МЩКТ, зокрема тіл хребців. Призначення хворому біологічної терапії, а саме інгібітора ФНП, на нашу думку, було патогенетично обґрунтованим з огляду на аксіальну форму СпА, сприятливий вплив цих препаратів на перебіг і рентгенологічне прогресування захворювання, їх доведену позитивну дію на структурно-функціональний стан кісткової тканини.
Висновки
Сучасні протоколи з ведення ревматологічних хворих вимагають від лікаря динамічної оцінки стану пацієнта з метою своєчасної корекції терапії за потреби. У реальній клінічній практиці оцінювати ефективність лікування при аксіальній формі СпА досить складно, особливо при короткостроковому спостереженні. Найдоцільніше це робити, використовуючи опитувальники, шкали оцінки запалення й інтегральні показники активності захворювання. Лікування до досягнення мети (treat to target) при СпА можливе при поєднаному застосуванні адекватної протизапальної терапії, фізичної реабілітації та, за можливості, призначенні анти-ФНП-препаратів.
Голімумаб – лікарський засіб, дозволений для застосування при СпА, з доведеним впливом на показники запалення, рентгенологічне прогресування захворювання та функціональну активність хворих. Найдоцільнішим є призначення анти-ФНП-препаратів при ранній, дорентгенологічній формі аксіального спондиліту, оскільки запобігти виникненню синдесмофітів можливо при ефективному зменшенні запалення.
Доведено ефективність голімумабу в лікуванні ПСП, які досить часто можуть переважати в клінічній картині СпА та значно погіршувати якість життя пацієнтів. Окрім того, застосування інгібіторів ФНП позитивно впливає не лише на перебіг захворювання, а й на стан кісткової тканини.
Профіль безпеки голімумабу при тривалому спостереженні (протягом 2 і 5 років) також досліджений і загалом відповідає такому інших ФНП-препаратів. У тривалих дослідженнях доведено стійке збереження досягнутих результатів лікування.
Список літератури знаходиться в редакції.
СР-143869
Медична газета «Здоров’я України 21 сторіччя» № 4 (473), лютий 2020 р.
СТАТТІ ЗА ТЕМОЮ Ревматологія
Сечова кислота (СК) – кінцевий продукт метаболізму пуринів, який здебільшого синтезується в печінці та виводиться нирками і кишечником [1, 2]. Гіперурикемія – підвищений рівень СК у сироватці крові – є метаболічною основою подагри, одного з найпоширеніших запальних артритів. У середні віки подагра вважалася хворобою надмірності аристократії, нині її поширеність зростає у всьому світі через зміни в харчуванні, переважання в дієті оброблених продуктів, фруктози та збільшення поширеності ожиріння [3]....
Глюкокортикоїди (ГК), які використовуються з початку 1950-х рр., стали невід’ємною частиною лікування ревматоїдного артриту (РА) [1]. Ключовою перевагою ГК є швидке настання ефекту, особливо порівняно з класичними синтетичними хворобомодифікувальними антиревматичними препаратами (ХМАРП) на кшталт метотрексату. Відповідно, ГК мають привабливий профіль для лікування спалахів хвороби або для застосування в ролі засобів для бридж-терапії на ранніх стадіях РА в очікуванні ефекту класичних синтетичних ХМАРП. Ця стратегія широко використовується після публікації результатів дослідження COBRA в 1997 р. [2]. ...
Гостре розтягнення зв’язок гомілковостопного суглоба (ГРЗГС) є поширеним, інвалідизувальним, клінічно значущим захворюванням, щодо якого по медичну допомогу щороку звертається >1 млн пацієнтів [1]; асоціюється зі значним соціально-економічним тягарем [2]. Майже 16-40% випадків ГРЗГС – спортивна травма, а час одужання є дуже важливим для спортсменів, професіоналів та осіб, котрі готуються до великих змагань. Найпоширенішими (85%) є латеральні (бічні) розтягнення зв’язок гомілковостопного суглоба; особливо часто ушкоджується передня таранно-гомілкова зв’язка – зазвичай унаслідок високошвидкісної інверсії та внутрішньої ротаційної травми [3]; ≈40% розтягнень гомілковостопного суглоба мають ризик хронізації. Характерними ознаками ГРЗГС є біль під час навантаження, нестабільність гомілковостопного суглоба та проблеми з рухливістю [4-6]....
Наприкінці жовтня минулого року Всеукраїнська асоціація ревматологів України провела науково-практичну конференцію, до якої було залучено фахівців різних галузей медицини, як-от ревматологія, загальна практика (сімейна медицина), терапія, кардіологія, медицина невідкладних станів, неврологія, функціональна й ультразвукова діагностика. Захід відбувся у змішаному форматі (онлайн / офлайн). До участі в конференції було запрошено не лише вітчизняних спікерів із різних регіонів України, а і закордонних, зокрема з Канади, США та Великої Британії. ...