Дифференциальная диагностика кардиомиопатии такоцубо и острого инфаркта миокарда
T.H. Nguyen, J.D. Horowitz
В основе кардиомиопатии такоцубо (КМПТ) , которую также называют стрессорной КМП, апикальным баллонным синдромом, «синдромом разбитого сердца», лежит острое, индуцированное катехоламинами воспаление миокарда, возникающее после тяжелого эмоционального стресса, главным образом у женщин. При этом заболевании почти обязательно формируется острая сегментарная (обычно периапикальная) систолическая дисфункция левого желудочка (ЛЖ), провоцируемая острым выраженным стрессом.
К настоящему времени проведено когортное исследование, которое включало 136 пациентов. Из них 96% были женщинами, возраст 90% больных превышал 50 лет. В типичных случаях КМПТ имитировала острый инфаркт миокарда (ОИМ): сопровождалась интенсивной острой болью в грудной клетке, одышкой и «инфарктными» признаками на электрокардиограмме (ЭКГ), в частности элевацией сегмента ST в дебюте заболевания. Эхокардиографическое исследование функции ЛЖ, как правило, выявляло периапикальную зону акинеза либо гипокинеза. В ряде работ удалось показать, что движение стенки ЛЖ нормализуется в течение ближайших недель, а симптоматика разрешается через несколько суток. Тем не менее у таких больных могут возникать тяжелые осложнения (разрыв свободной стенки ЛЖ, отек легких, сердечная недостаточность, аритмии сердца, динамическая обструкция выносящего тракта ЛЖ, артериальная гипотензия) и даже смерть (Y. Akashi et al., 2008; S. Sharkey et al., 2010; M. Sato et al., 2006; I. Wittstein et al., 2005).
Исключение ишемии миокарда и верификация выраженного воспаления сердечной мышцы
Доказано, что КМПТ является клиническим следствием миокардиального воспаления, индуцированного «пульс»-воздействием катехоламинов на чувствительную мышцу сердца. Данные, полученные в экспериментальных исследованиях на крысах, свидетельствуют, что основные эффекты катехоламинов опосредованы стимуляцией β2-адренорецепторов (H. Paur et al., 2012). По предварительным данным, также имеет значение функциональная связь этих рецепторов с образованием оксида азота (T. Nguyen et al., 2013). Кроме того, нельзя исключить потенциального влияния на миокард энергетического дисбаланса, ассоциированного с активацией провоспалительных процессов и нитрозативным стрессом (J. Horowitz et al., 2011).
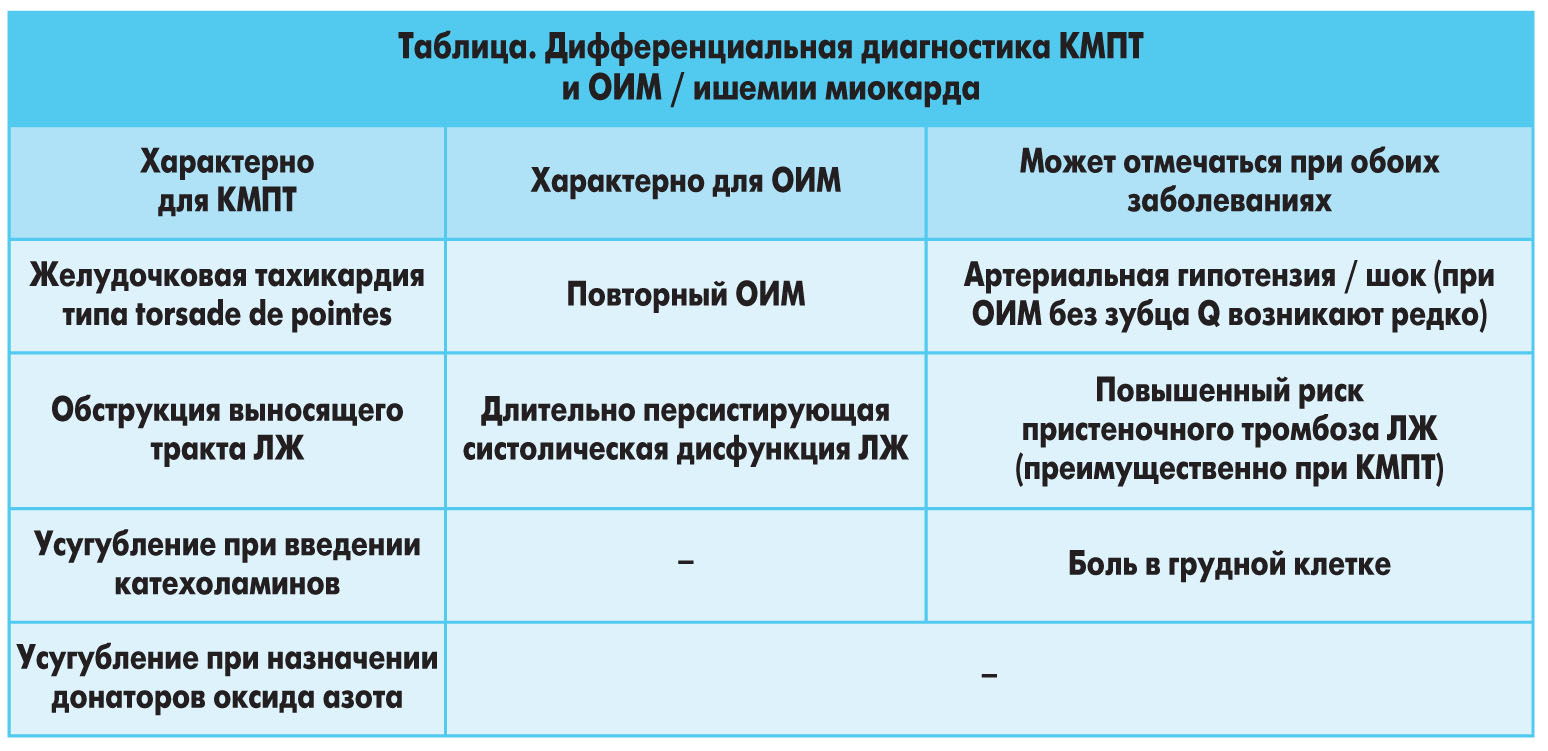
В ранних сообщениях констатировалась относительная редкость КМПТ, но четко ее патогенез не описывался. В такой ситуации возникла острая необходимость поиска диагностических критериев, исключающих ишемию миокарда (K. Bybee et al., 2004). Сейчас стало ясным, что теоретически КМПТ может сопутствовать и ишемическая болезнь сердца (ИБС). Следовательно, диагноз этой КМП должен быть основан на распознавании выраженного воспаления сердечной мышцы. В то же время клиническая дифференциация с ОИМ достаточно трудна. В таблице приведены принципы дифференциальной диагностики КМПТ и ОИМ / ишемии миокарда.
Диагностические критерии клиники Мейо
Специалисты клиники Мейо устанавливают диагноз КМПТ при одновременном наличии следующих 4 критериев (A. Prasad et al., 2008):
1) регионарные нарушения движений стенки ЛЖ (преходящие гипокинез, акинез или дискинез средних либо верхушечных отделов);
2) отсутствие обструктивных форм ИБС и острого разрыва бляшки, по данным ангиографии;
3) «новые» элевация сегмента ST и/или инверсия зубца Т либо умеренное повышение сывороточного уровня сердечного тропонина;
4) отсутствие феохромоцитомы и миокардита.
Обновленные критерии (2008) не содержат:
1. Обоснования того, почему нужно исключать больных с феохромоцитомой (высвобождение надпочечниками гормонов, вызывающих постоянное либо эпизодическое повышение артериального давления) либо миокардитом в анамнезе (J. Madias, 2014). Кроме того, критерии не учитывают возможности случайного выявления ИБС.
2. Упоминаний о систематической ошибке отбора при катетеризации у пациентов с острой болью в грудной клетке, которую расценивали как проявление острого коронарного синдрома (ОКС). В дебюте заболевания у этих больных отмечалась элевация сегмента ST, из-за чего им по неотложным показаниям катетеризировали сердце. Однако позже было установлено, что подъем сегмента ST отмечался лишь в 40% случаев (C. Dib et al., 2009; M. Madhavan et al., 2011).
3. Указаний на спазм одной или нескольких коронарных артерий как возможную причину заболевания – расположение зон гипокинеза редко соответствует ходу какой-то одной коронарной артерии.
Очень пожилым, ослабленным пациентам, у которых боль в грудной клетке сохраняется долго, а элевация сегмента ST отсутствует, катетеризацию сердца могут не выполнять, что служит потенциальным источником гиподиагностики.
Все это следует учитывать при разработке корректных диагностических критериев.
Общие замечания
Согласно результатам работ, в которых катетеризацию сердца не выполняли, КМПТ отличается от острой ишемии миокарда / ОИМ двумя особенностями:
1. Ограниченным высвобождением кардиоспецифических маркеров. Низкие уровни тропонина и креатинкиназы отмечаются у большинства больных, у которых кардиоваскулярная магнитно-резонансная томография (МРТ) не выявляет признаков перенесенного ранее ОИМ.
2. Феноменом миокардиального «станнинга». Отсутствие ОИМ в сочетании с быстрой положительной динамикой регионарной сократимости ЛЖ указывают на возможность обратимого химического повреждения сердечной мышцы, аналогичного миокардиальному «станнингу». Действительно, по данным многочисленных работ, выполненных в последние годы, после острого приступа формируются локальные участки интрамурального воспаления (биопсия (H. Nef et al., 2007) и отека (кардиоваскулярная МРТ (C. Neil et al., 2012).
Дифференциальная диагностика КМПТ и ОИМ без зубца Q
Клинические особенности
1. Внезапный эмоциональный либо физический стресс. КМПТ часто провоцируется внезапным эмоциональным или физическим стрессом, который обусловлен индивидуально либо общественно значимыми обстоятельствами. Вероятность развития КМП под действием указанных стрессоров пока не установлена. В части случаев не удается выявить влияния того или иного стрессора. Однако в недавнем анамнезе большинства больных (90% из них женщины) прослеживается воздействие по меньшей мере одного стресс-фактора (I. Wittstein, 2008).
2. Связь с острым ишемическим инсультом. Известно, что КМПТ осложняется ишемическим или геморрагическим инсультом (T. Abd et al., 2014), но возможен и эмболический инфаркт мозга (Y. Kato et al., 2009).
3. Симптоматика ОКС. Субъективные признаки у таких пациентов обычно напоминают жалобы, свойственные ОКС: различной выраженности боль в грудной клетке в покое (у 50-60% пациентов) и/или одышка.
4. Артериальная гипотензия и шок – частые осложнения раннего периода. Механизмы, ответственные за расстройства гемодинамики, вероятно, представляют собой нарушения сократимости ЛЖ, неадекватно высокий прирост частоты сердечного ритма, а иногда и вазодилатацию, опосредованную эффектами мозгового натрийуретического пептида – BNP (C. Chong et al., 2013).
Лабораторная диагностика
Используется ряд лабораторных тестов, результаты которых, однако, не способны четко разграничить КМПТ и ОИМ.
1. Определение уровня катехоламинов. Их уровень не отличается от такового при ОКС. Хотя I. Wittstein и соавт. (2005) обнаружили, что у поступающих в стационар больных КМПТ концентрация катехоламинов достоверно выше, чем при ОИМ, в других работах эти данные не подтвердились (M. Madhavan et al., 2009). Несоответствие результатов, возможно, объясняется тем, что забор крови осуществляли в разное время от начала заболевания.
2. Повышение кардиоспецифических биомаркеров. У большинства пациентов уровень кардиоспецифических биомаркеров (тропонина, креатинфосфокиназы, ее МВ фракции) слегка повышен (T. Pilgrim, Т. Wyss, 2008). В нескольких исследованиях было выявлено значительное увеличение концентрации BNP и N-концевого предшественника BNP – NT-proBNP (T. Nguyen et al., 2011).
ЭКГ-признаки
ЭКГ-изменения индивидуально варьируют, однако могут быть такими же, как и при ОИМ: элевация сегмента ST, инверсия зубца Т, патологический зубец Q (M. Gianni et al., 2006). Следовательно, ЭКГ позволяет выявить гетерогенные изменения сегмента ST и зубца Т.
По данным систематического обзора, проведенного Т. Pilgrim и Т. Wyss (2008), подъем сегмента ST регистрируют, особенно в грудных отведениях, у 70% больных. Однако, согласно выводам C. Dib и соавт. (2009), обследовавших 105 пациентов, элевация сегмента ST встречается лишь в 34,2% случаев. Весьма распространенной находкой является инверсия зубца Т. Кроме того, часто фиксируется удлинение интервала QT (F. Mahfoud et al., 2009), что может приводить к возникновению желудочковой тахикардии типа «пируэт» (S. Denney et al., 2005; C. Madias et al., 2011).
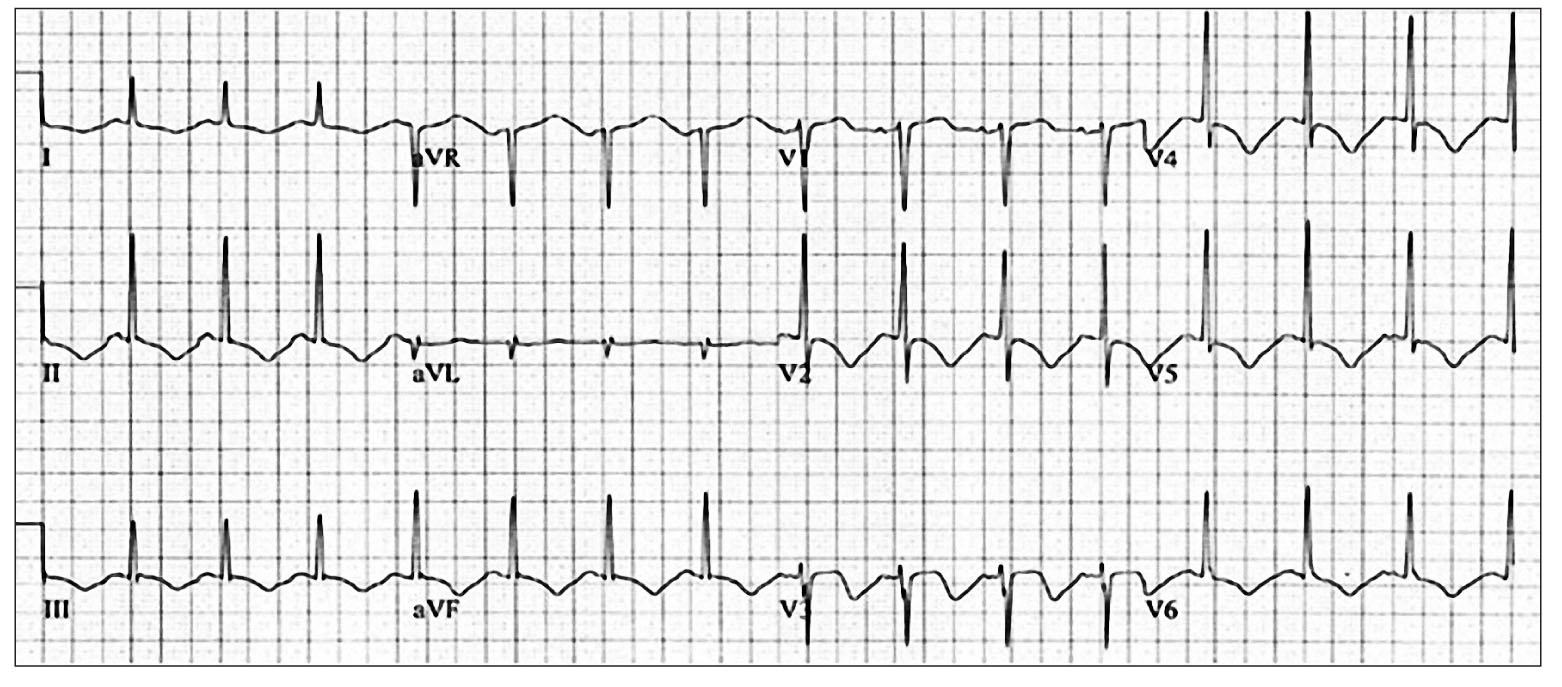
Неоднократно предпринимались попытки разработать дифференциально-диагностические ЭКГ-критерии КМПТ и переднего ОИМ с подъемом сегмента ST, развившегося вследствие окклюзии левой передней нисходящей артерии. Оказалось, что элевация сегмента ST и нарастающая инверсия зубца Т не позволяют дифференцировать эти заболевания (S. Sharkey et al., 2008). Для КМПТ характерна «анатомическая гетерогенность» изменений сегмента ST и зубца Т, что свидетельствует о вовлечении в процесс нескольких бассейнов коронарного кровообращения (рис.).
Эхокардиография
Эхокардиография часто визуализирует апикальный и/или среднежелудочковый акинез/гипокинез в сочетании с базальным гиперкинезом. Это изменяет ЛЖ, придавая его верхушке форму баллона. Примерно у трети больных, помимо прочего, отмечается гипокинез апикальных отделов правого желудочка (K. Singh et al., 2014). Нарушение сократительной функции ЛЖ снижает его фракцию выброса. Довольно часто, хотя и не всегда, формируется умеренная либо тяжелая систолическая/диастолическая дисфункция ЛЖ. В острую фазу миокард акинетических зон истончается. Тем не менее эти зоны отличаются от гиперэхогенных участков фиброза при трансмуральном инфаркте миокарда. Важнее, однако, то, что у больных регистрируют не столько общие, сколько сегментарные нарушения движений стенки ЛЖ. Данные нарушения не соответствуют какому-то определенному сосудистому бассейну и могут быть использованы для дифференциальной диагностики с ОИМ (R. Citro et al., 2011). N. Mansencal и соавт. (2009) для количественной оценки регионарной сократимости ЛЖ использовали спекл-трекинг эхокардиографию. Было установлено существование значительных отличий в напряжении, его частоте и пиковой систолической скорости в острую и хроническую фазы. Кроме того, в острую фазу систолическая дисфункция была циркулярной, а скорости движения базальных, среднежелудочковых и апикальных сегментов оказались одинаковыми. Это отличало КМПТ от обструкции нисходящей ветви левой коронарной артерии.
Катетеризация сердца / коронарная ангиография
Диагноз КМПТ, как правило, устанавливают с помощью инвазивной коронароангиографии. При поступлении в стационар болезнь распознают редко. У большинства пациентов гемодинамически значимый стеноз коронарных артерий отсутствует. Левосторонняя вентрикулография является ценным методом диагностики, позволяющим определить форму ЛЖ. В типичных случаях он напоминает сосуд с закругленным дном и узким горлышком – его использовали в Японии для ловли осьминогов. Примерно у 30% больных гипокинез охватывает средние отделы ЛЖ. Изредка встречается базальный, или «инвертированный», вариант (R. Hurst et al., 2006).
Следует отметить такие гемодинамические особенности острой стадии, как системная артериальная гипотензия или шок (C. Chong et al., 2013) и небольшое повышение давления заклинивания в легочных артериях (отек легких при этом развивается редко) (T. Nguyen et al., 2011). В отдельных случаях можно задокументировать внутрижелудочковый градиент давления и/или тяжелую митральную недостаточность. Так как (согласно подходу клиники Мейо) этим больным необходимо выполнять катетеризацию сердца, не исключено, что диагностике может помешать систематическая ошибка отбора. С учетом этого к данному методу целесообразно прибегать лишь у пациентов с тяжелым течением заболевания.
Кардиоваскулярная МРТ
Кардиоваскулярная МРТ – высокочувствительный метод, позволяющий оценить функцию сердца и локальные нарушения сократимости ЛЖ. Результаты Т2-взвешенной МРТ свидетельствуют о том, что у большинства больных имеется околоверхушечный отек (A. Rolf et al., 2009). Правда, более тщательное исследование выявляет тотальный отек ЛЖ (C. Neil et al., 2012). При КМПТ МРТ с контрастным усилением, как правило, не обнаруживает феномена отсроченного усиления, однако иногда он все же формируется (из-за увеличения количества внеклеточного матрикса) (A. Rolf et al., 2009). Значительное повышение плазменного уровня BNP/NT-proBNP и положительный тропониновый тест у женщин, которые испытали эмоциональную либо физическую травматизацию и у которых на ЭКГ отмечаются мультизональные изменения в отсутствие подъема сегмента ST, может указывать на КМПТ. Диагноз подтверждают эхокардиографической или коронароангиографической оценкой регионарной сократимости ЛЖ и последующей констатацией отека миокарда (без его некроза), по данным кардиоваскулярной МРТ с поздним гадолиниевым усилением и Т2-взвешенной визуализацией.
Лечение
Общепринятая терапевтическая тактика при КМПТ отсутствует. Обычно применяют такие подходы:
1) мониторирование сердечных аритмий в течение ≥2 сут;
2) введение антикоагулянтов (гепарина) для снижения риска пристеночного тромбоза;
3) исключение катехоламинов;
4) исключение органических нитратов, поскольку КМПТ присущ нитрозативный стресс (G. Licari et al., 2013);
5) назначение ингибиторов ангиотензинпревращающего фермента, которые, согласно выводам метаанализа K. Singh и соавт. (2014), при длительном приеме уменьшают риск повторных эпизодов.
В то же время остаются открытыми вопросы адекватного лечения шоковых состояний и быстрого восстановления функции ЛЖ.
Выводы
КМПТ – заболевание, требующее проведения дифференциальной диагностики с ОИМ вне зависимости от того, происходит подъем сегмента ST или нет. Важность дифференциального диагноза объясняется различиями в лечебных подходах. Так, при элевации сегмента ST необходима немедленная катетеризация сердца. На практике параллельно этому производят клиническую оценку, устанавливают повышенные уровни BNP /NT-proBNP, регистрируют ЭКГ, выполняют эхокардиографию, а далее с помощью кардиоваскулярной МРТ демонстрируют обширный отек миокарда.
E-Journal of Cardiology Practice. – 2014. – Vol. 13.
Перевод с англ. Глеба Данина
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....