Эффективное или безопасное лечение остеоартроза: разрешая дилемму выбора
Боль, неизбежная и естественная спутница человечества, досаждает и мучает многих больных. Пациенты с остеоартрозом (ОА) ощущают ее практически ежедневно: в той или иной мере, утром или вечером, при ходьбе или подъеме по лестнице. Боль создает множество проблем, затрудняет передвижение и ухудшает качество жизни, приводит к преждевременной потере трудоспособности и инвалидности, увеличивая вероятность развития и прогрессирования сопутствующей патологии.
Пациенты пожилого возраста с ОА, испытывающие хроническую боль, обращаются за медицинской помощью, надеясь облегчить свои страдания. Однако камнем преткновения в их лечении может стать наличие коморбидных заболеваний: сопутствующая патология желудочно-кишечного тракта или сердечно-сосудистой системы значительно ограничивает возможности фармакотерапии. Попытка разорвать эти прочные болевые узы ставит врача перед дилеммой: назначить симптоматическое средство быстрого действия (например, нестероидный противовоспалительный препарат – НПВП) и пренебречь высоким гастроинтестинальным и кардиоваскулярным риском либо использовать модифицирующие средства замедленного действия (SYSADOA), лишенные подобных побочных эффектов. Какой выбор сделать в этой непростой ситуации? Постараемся ответить на этот вопрос, воспользовавшись современными данными доказательной медицины.
Наиболее эффективные хондропротекторы
Авторы систематического обзора 13 рандомизированных контролированных исследований – РКИ (Gallagher В. et al., 2015) считают, что лучшим консервативным способом защиты хряща и замедления прогрессирования ОА у пациентов группы высокого риска является применение глюкозамина (ГА) и хондроитинсульфата (ХС). В этой работе исследователи поставили перед собой интересную и непростую задачу: установить, какой препарат группы SYSADOА (ГА, хондроитин, полиненасыщенные жирные кислоты, неомыляемые соединения авокадо и сои, диацереин, гиалуроновая кислота) или другие лекарственные средства (НПВП, S-аденозилметионин, метилсульфонилметан, витамины С, D, Е, обогащенная тромбоцитами плазма) обладают наиболее выраженными хондропротекторными свойствами. Среди перечисленных лекарственных средств наиболее эффективными оказались ГА и ХС: первый благоприятно влиял на состояние всех структурных компонентов коленного сустава (данные 2 из 3 РКИ), а второй замедлял дегенерацию суставного хряща по сравнению с плацебо (данные 3 из 4 РКИ). Несмотря на то что внутрисуставное введение гиалуроновой кислоты замедляло скорость потери хряща по сравнению с плацебо, доказательная база эффективности ее назначения была относительно невелика (данные 1 из 3 РКИ). Применение НПВП, витаминов Е и D не оказывало значимого влияния на состояние хрящевой ткани (данные 6 РКИ).
В единстве – сила, а в силе единства – победа
Важными являются результаты основополагающего РКИ в области клинической эффективности и безопасности хондропротекторов, известного под названием GAIT (Clegg D. O. et al., 2006). Данное испытание выполнялось в 16 исследовательских центрах США, в нем приняли участие 1583 пациента с рентгенологически подтвержденным диагнозом ОА коленных суставов 2-3 степени по классификации Kellgren и Lawrence. В соответствии с дизайном РКИ пациентов рандомизировали для монотерапии ГА (1500 мг/сут), ХС (1200 мг/сут), целекоксибом (200 мг), комбинированной терапии ГА и хондроитином или плацебо в течение 24 нед. При необходимости для купирования болевых ощущений пациентам дополнительно назначали парацетамол в дозе до 4 г/сут. Эффективность назначенной терапии анализировалась в зависимости от исходной степени тяжести боли: результативность лечения больных с незначительно выраженным болевым синдромом (n=1229) сопоставлялась с таковой у пациентов с умеренными/сильными болевыми ощущениями (n=354). Первичной конечной точкой исследования являлось 20% снижение интенсивности болевого синдрома через 24 нед по сравнению с исходными показателями.
Несмотря на то что монотерапия ГА и хондроитином не превышала результативность плацебо относительно частоты достижения первичной конечной точки (64; 65,4 и 60,1% соответственно; р=0,30 и р=0,17), комбинация этих двух препаратов способствовала достоверному 20% уменьшению выраженности болевого синдрома по сравнению с плацебо через 24 нед лечения (66,6 vs 60,1% соответственно; р=0,09). Эффективность целекоксиба на 10% превосходила результативность плацебо (р=0,008). Исследователи отметили еще один интересный факт: назначение комбинации ГА и хондроитина пациентам с умеренным/выраженным болевым синдромом оказывало более выраженный аналгетический эффект (79,2%), чем применение плацебо (54,3%; р=0,002). У больных, испытывавших болевые ощущения легкой степени тяжести, комбинированная терапия двумя хондропротекторами оказалась не более эффективной, чем прием плацебо. Данный факт исследователи объяснили низкой чувствительностью методики, использовавшейся для оценки клинических данных. Все пациенты хорошо переносили терапию исследуемыми препаратами. Нежелательные побочные реакции были незначительными, частота их появления не превышала аналогичный показатель в группе плацебо и они в равной степени возникали во всех исследуемых группах. Таким образом, в работе впервые были получены данные, подтверждавшие эффективность комбинированной терапии ГА и хондроитином.
В 2010 г. А. D. Sawitzke и соавт. представили результаты 2-летнего наблюдения за пациентами, принимавшими участие в исследовании GAIT. Результаты этого испытания оказались несколько пессимистичными: 24-месячное применение комбинации ГА и ХС было признано нецелесообразным. Оказалось, что ни длительная монотерапия ГА (отношение шансов – ОШ – 1,16; 95% доверительный интервал – ДИ – 0,65-2,04), ХС (ОШ 0,69; 95% ДИ 0,40-1,21), целекоксибом (ОШ 1,21; 95% ДИ 0,71-2,07), ни комбинированное лечение двумя хондропротекторами (ОШ 0,83; 95% ДИ 0,51-1,34) не сопряжены с достоверным 20% снижением индекса WOMAC по сравнению с плацебо. Аналогичная ситуация наблюдалась в отношении функциональных критериев эффективности терапии OMERACT/OARSI: 24-месячное применение ГА (ОШ 1,16; 95% ДИ 0,74-1,83), хондроитина (ОШ 0,89; 95% ДИ 0,53-1,50), а также комбинации этих препаратов (ОШ 0,85; 95% ДИ 0,55-1,31) не позволило статистически значимо снизить интенсивность болевых ощущений на 20%.
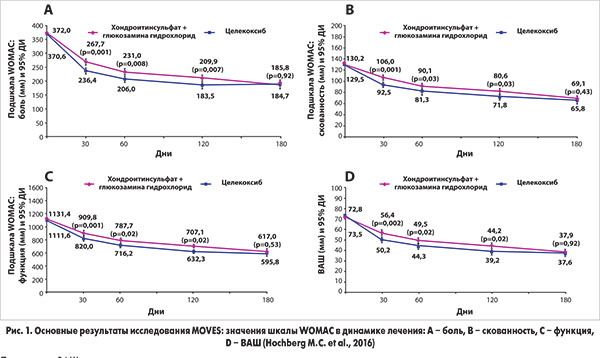
Абсолютно другие данные были получены в международном исследовании MOVES (Multicentre Osteoarthritis interVEntion trial with SYSADOA), в котором сопоставлялась эффективность 6-месячного применения комбинации ХС и ГА с результативностью использования целекоксиба (Hochberg М. С. et al., 2016). В соответствии с дизайном данного РКИ пациентов с ОА коленных суставов 2-3 степени по классификации Kellgren и Lawrence с умеренным или значительно выраженным болевым синдромом (индекс WOMAC ≥301 мм; n=606) рандомизировали для ежедневного приема 1200 мг ХС и 1500 мг ГА гидрохлорида или 200 мг целекоксиба на протяжении 6 мес. Первичной конечной точкой являлась 6-месячная динамика средних значений индекса WOMAC по сравнению с исходными данными. В качестве вторичных конечных точек были выбраны такие показатели, как степень скованности коленного сустава, значения визуальной аналоговой шкалы интенсивности боли, наличие отека/выпота в коленном суставе, необходимость приема препаратов «спасения», эффективность терапии по критериям OMERACT-OARSI, качество жизни по шкале EuroQoL‑5D.
Эффективность длительной комбинированной терапии хондроитином и ГА оказалась сопоставимой с результативностью применения целекоксиба (рис. 1). Использование указанного хондропротектора обеспечило 50,1% снижение интенсивности болевого синдрома (скорректированные средние значения индекса WOMAC: -185,7 мм; 95% ДИ от -200 до -171,1 мм), а назначение селективного ингибитора циклооксигеназы‑2 ЦОГ‑2 способствовало уменьшению боли на 50,2% (индекс WOMAC: -186,8 мм; 95% ДИ от -201,7 до -171,9 мм).
После 6-месячного курса лечения критерии оценки эффективности лечения OMERACT-OARSI были достигнуты у 79,7% пациентов, получавших комбинацию хондроитина и ГА, и у 79,2% больных, принимавших целекоксиб. Прием как модифицирующих средств замедленного действия, так и целекоксиба способствовал уменьшению отечности коленного сустава на >50%. В отношении других вторичных конечных точек не было зафиксировано достоверных межгрупповых различий. Основываясь на результатах проведенного исследования, М. С. Hochberg и соавт. предположили, что комбинация хондроитина и ГА может использоваться в качестве альтернативы НПВП при лечении пациентов с ОА коленных суставов.
Мнение экспертов Кокрановского сотрудничества
Эксперты Кокрановского сотрудничества изучили вопрос целесообразности длительной терапии SYSADOA и опубликовали систематический обзор, посвященный эффективности применения хондроитина в лечении ОА. J. A. Singh и соавт. (2015) провели огромную работу: они проанализировали результаты 43 РКИ, в которых приняли участие 9110 больных ОА коленных, тазобедренных суставов и кистей рук, из них 4962 пациента получали хондроитин, а 4148 участников принимали плацебо или другой активный препарат сравнения (НПВП, аналгетики, опиоиды, ГА). Продолжительность исследований варьировала от 1 мес до 3 лет.
В этом систематическом обзоре эксперты Кокрановского сотрудничества представили данные об эффективности комбинированной терапии хондроитином и ГА. Доказано, что сочетание хондроитина и ГА эффективнее купирует болевой синдром по сравнению с плацебо или другим активным препаратом сравнения (АРР 10%; 95% ДИ 5-14). В то же время установлено, что комбинация указанных хондропротекторов не оказывает значимого влияния на уровень физического функционирования в отличие от плацебо или другого активного препарата сравнения (АРР 1%; 95% ДИ 6-3). Сочетанная терапия хондроитином и ГА улучшает значения индекса Лекена (АРР 8%; 95% ДИ 4-12;). Эксперты Кокрановского сотрудничества также подчеркнули высокий профиль безопасности комбинации хондроитина и ГА: применение этого комбинированного препарата не сопровождалось увеличением количества нежелательных побочных эффектов, возрастанием числа случаев преждевременного прекращения терапии по причине появления побочных реакций, а также повышением частоты серьезных нежелательных явлений по сравнению с плацебо или другим препаратом сравнения. Таким образом, эксперты Кокрановского сотрудничества представили убедительные доказательства эффективности длительной (>6 мес) комбинированной терапии хондроитином и ГА в купировании болевого синдрома у больных ОА.
Рекомендации ESCEO
В 2014 г. Европейское общество по клиническим и экономическим аспектам остеопороза и остеоартроза (European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis – ESCEO) опубликовало руководство по лечению ОА коленных суставов (Bruyere O. et al., 2014). В этом руководстве указывается, что лечение ОА направлено на уменьшение выраженности патологических симптомов, замедление прогрессирования заболевания, а также на увеличение двигательной активности и улучшение качества жизни, снижение потребности в приеме аналгетических препаратов и проведении операций по протезированию суставов. Следует отметить, что ESCEO – это некоммерческая организация и представленный ею алгоритм лечения ОА коленных суставов был разработан независимо от участия каких-либо финансирующих организаций, следовательно, ни одна из финансово заинтересованных компаний не принимала участия в подготовке рассматриваемого документа.
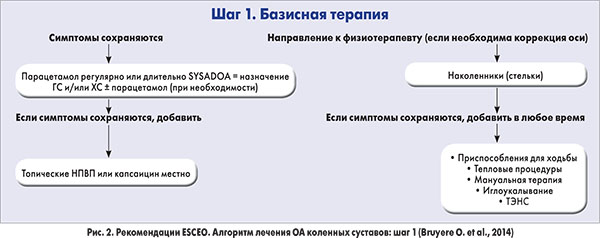
Помимо общих принципов ведения больных ОА (использования информационно-обучающих программ, снижения веса при наличии избыточной массы тела, выполнения аэробных физических упражнений) разработанный алгоритм предусматривает 4 последовательных шага. 1-й шаг – это назначение базисного лечения, 2-й шаг – расширенная фармакотерапия для больных с сохраняющимся болевым синдромом (за счет назначения НПВП), 3-й шаг – кратковременное применение слабых опиоидов или дулоксетина, 4-й шаг – хирургическое лечение.
Что касается инициального фармакологического лечения ОА, специалисты ESCEO предусматривают возможность применения парацетамола, но при этом подчеркивают, что назначение парацетамола может спровоцировать развитие различных серьезных нежелательных реакций. Поэтому эксперты указанного общества считают, что терапией первой линии в лечении ОА коленных суставов является назначение медленно действующих симптоматических лекарственных средств – SYSADOA (рис. 2).
В руководстве подчеркивается, что среди всех SYSADOA наибольшей доказательной базой обладают глюкозамина сульфат и ХС, тогда как другим представителям этой группы (диацереину, неомыляемым соединениям авокадо и сои, коллагену, экстрактам лекарственных трав) еще предстоит доказать свои эффективность и безопасность.
В руководстве ESCEO отмечаются безопасность и хорошая переносимость комбинированного лечения ГА и хондроитином по сравнению с плацебо, симптоммодифицирующее действие SYSADOA при длительном применении, а также способность этих препаратов замедлять прогрессирование заболевания.
В качестве терапии первой линии рабочая группа ESCEO также предусматривает возможность назначения топических НПВП при условии, если использование SYSADOA и парацетамола не позволяет достичь необходимого эффекта. В руководстве подчеркивается, что локальное применение НПВП (ВЭ 0,44; 95% ДИ 0,27-0,62) так же эффективно, как и пероральный прием этих препаратов, но реже сопровождается развитием нарушений со стороны желудочно-кишечного тракта.
Как свидетельствуют представленные данные доказательной медицины, современное лечение ОА может быть не только эффективным, но и безопасным при условии назначения таких представителей группы SYSADOA, как ГА и хондроитин. Применение этих модифицирующих средств замедленного действия позволяет не только купировать болевой синдром, но и приостановить прогрессирование заболевания, расширить двигательную активность, а также улучшить качество жизни пациентов. Комплексный подход и длительный прием комбинаций SYSADOA – это основа эффективного лечения симптомного ОА.
Список литературы находится в редакции.
| Медична газета «Здоров’я України 21 сторіччя» №5 (378), березень 2016 р |
СТАТТІ ЗА ТЕМОЮ Ревматологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....
Зв’язок між рівнем сироваткової сечової кислоти (ССК) і ризиком серцево-судинних захворювань (ССЗ) упродовж багатьох років є предметом вивчення дослідників. Установлено, що рівень ССК – незалежний предиктор смерті від усіх причин і серцево-судинної смерті, зокрема від гострого коронарного синдрому, інсульту та серцевої недостатності (СН). Також опубліковано багато робіт про зв’язок між ССК і функцією нирок. Попри значну кількість публікацій, деякі моменти, а саме: яким є оптимальний поріг ССК для визначення ризику ССЗ, чи необхідна корекція значень ССК для функції нирок, чи є ССК ключовим патологічним елементом метаболічної дисрегуляції, потребують прояснення....