Доступно про актуальне: особливості діагностики інсультів-хамелеонів, інфузійної терапії та лікування вторинного менінгіту
10‑11 жовтня 2019 р. на базі клінічної лікарні «Феофанія» Державного управління справами було проведено науково-практичну конференцію з міжнародною участю «Feofaniya. Neurointensive». Представляємо до вашої уваги огляд доповідей учасників заходу, присвячених особливостям діагностики інсультів із неоднозначною клінічною картиною, рекомендаціям щодо оптимальної інфузійної терапії при порушеннях кислотно-основного та електролітного балансу, застосуванню невідкладної терапії при рухових розладах, а також вибору адекватного антибактеріального лікування за вторинного менінгіту.
«Інсульти-хамелеони»: як не пропустити інсульт при атиповій клінічній картині
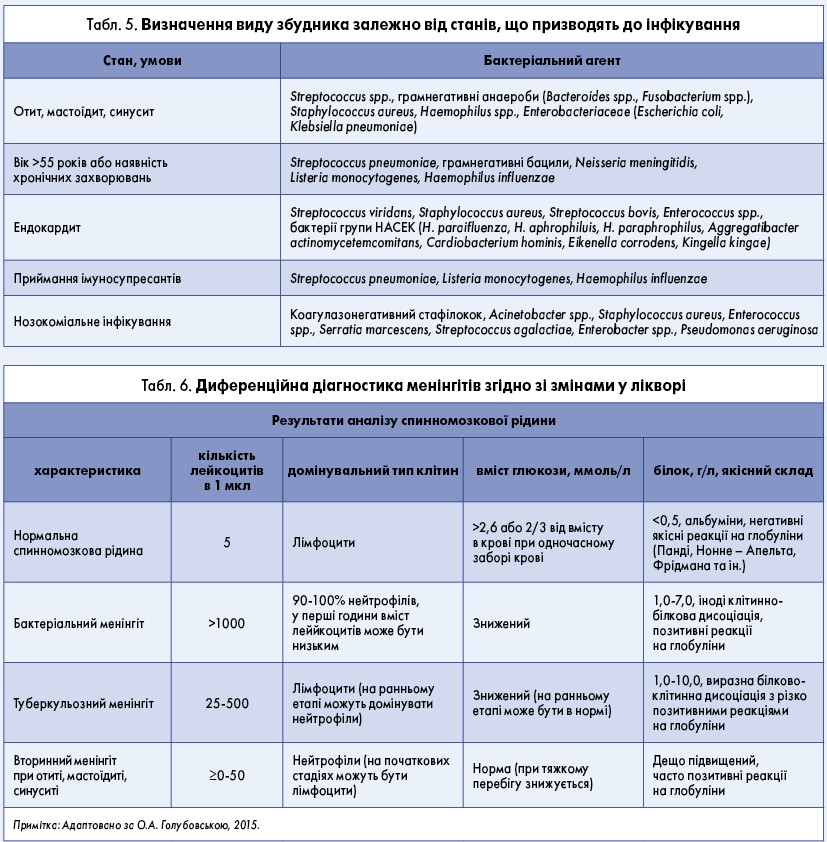
 Завідувачка кафедри клінічної неврології, психіатрії та наркології Харківського національного університету імені В.Н. Каразіна, головний науковий співробітник Інституту неврології, психіатрії та наркології НАМН України (м. Харків), д. мед. н., професор Тамара Сергіївна Міщенко привернула увагу учасників конференції до проблеми інсультів, що не були діагностовані вчасно. Так, за даними Newman-Toker et al. (2009), частота невиявлених інсультів становить 1,2‑12,7%, що відповідає 15‑165 тис. інсультів і транзиторних ішемічних атак щорічно. Наявність «нетрадиційних» симптомів збільшує ймовірність помилкового діагнозу в 43 рази. У пацієнтів з «інсультами-хамелеонами» (табл. 1) спостерігаються менш сприятливі результати та вищий ризик смерті протягом 12 місяців після інсульту, оскільки їм не проводять тромболізис, своєчасно не призначають базисну терапію та із затримкою застосовують вторинну профілактику (Richoz et al., 2015).
Завідувачка кафедри клінічної неврології, психіатрії та наркології Харківського національного університету імені В.Н. Каразіна, головний науковий співробітник Інституту неврології, психіатрії та наркології НАМН України (м. Харків), д. мед. н., професор Тамара Сергіївна Міщенко привернула увагу учасників конференції до проблеми інсультів, що не були діагностовані вчасно. Так, за даними Newman-Toker et al. (2009), частота невиявлених інсультів становить 1,2‑12,7%, що відповідає 15‑165 тис. інсультів і транзиторних ішемічних атак щорічно. Наявність «нетрадиційних» симптомів збільшує ймовірність помилкового діагнозу в 43 рази. У пацієнтів з «інсультами-хамелеонами» (табл. 1) спостерігаються менш сприятливі результати та вищий ризик смерті протягом 12 місяців після інсульту, оскільки їм не проводять тромболізис, своєчасно не призначають базисну терапію та із затримкою застосовують вторинну профілактику (Richoz et al., 2015).
Доповідачка зазначила, що гострий вестибулярний синдром (вертиго, нудота, блювання, непереносимість рухів головою, ністагм, атаксія) частіше виникає у межах периферичної вестибутопатії; для його диференціювання рекомендовано застосувати трикомпонентний протокол HiNTs (head impulse, nystagmus and skew): імпульс-тест, оцінку ністагму, тест косої девіації. Чутливість даного методу вища, ніж у комп’ютерної та магнітно-резонансної томографії в режимі DWI (100% проти 16 та 88% відповідно).
 Професор представила детальний опис протоколу HiNTs:
Професор представила детальний опис протоколу HiNTs:
1. Нead impulse – тест різкого руху (імпульсу) голови. Попросіть пацієнта розслабити голову і утримати погляд на носі / очах лікаря / камері. Акуратно нахиліть голову пацієнта в один бік (до 20°), після чого швидко перемістіть її назад до серединного положення.
Пояснення. У пацієнта може виникнути незначна корекційна саккада. Тест на імпульс голови є позитивним (підтверджує периферичне запаморочення), якщо виявлене значне відставання корекційних саккад (фіксації погляду). Порівняйте результат з контралатерального боку – слід відзначити різницю у швидкості корекції погляду. Результат тесту різкого руху голови відповідає периферичному запамороченню, якщо він позитивний лише в одному напрямку. Якщо ж в обох спостерігається відставання корекційних саккад, це може свідчити про центральний генез запаморочення. Тест можна також виконати у вертикальній площині. Відставання корекційних саккад у ній завжди свідчить про центральну етіологію вертиго.
2. Nystagmus (ністагм). Зверніть увагу на ністагм, якщо він наявний при погляді прямо або вбік.
Пояснення. Якщо ністагм виникає при погляді в одну сторону, а швидкий компонент наявний у тому ж напрямку при погляді в контралатеральний бік (наприклад, у пацієнта є правобічний ністагм при погляді вправо та вліво – це односпрямований правобічний ністагм), він є свідченням на користь периферичного запаморочення. Найпоширеніший ністагм складається з односпрямованого горизонтального ністагму з торсійним компонентом (патологія в задньому напівколовому каналі). Двоспрямований ністагм – швидкий компонент справа при погляді праворуч та зліва при погляді ліворуч – є свідченням на користь центрального ґенезу, як і вертикальний або виключно торсійний ністагм.
3. Skew (відхилення / коса девіація). Пацієнт має поглянути на ніс, по черзі прикрийте кожне його око.
Пояснення. Позитивним результатом є відхилення одного ока під час закриття з наступним поверненням до погляду на ніс після розкриття.
Інтерпретація результатів HiNTs: якщо отримані позитивний тест на імпульс голови, односпрямований і горизонтальний ністагм, негативний тест косої девіації, то, згідно з дослідженнями, HiNTs є на 100% чутливим і на 96% специфічним для периферичної причини запаморочення (Newman-Toker et al., 2009).
Підсумовуючи доповідь, Т.С. Міщенко зазначила, що підтвердження існування атипових інсультів створює потребу в підвищенні кваліфікації лікарів та їхньої обізнаності щодо існування «інсультів-хамелеонів». Застосування допоміжних методів діагностики є наступним кроком після клінічного огляду в алгоритмі обстеження пацієнта з незвичними проявами.
Інтенсивна інфузійна терапія у неврології: консенсус ESICM
 Головний науковий співробітник наукового відділу малоінвазивної хірургії ДНУ «Науково-практичний центр профілактичної та клінічної медицини» Державного управління справами, д. мед. н., професор, член-кореспондент НАМН України Володимир Ілліч Черній продовжив тему важливості застосування оптимальної інфузійної терапії в умовах неврологічного стаціонара. При висвітленні теми лектор спирався на оновлені настанови Європейського товариства інтенсивної терапії (ESICM) від 2018 р. «Інтенсивна інфузійна терапія в неврології: консенсус ESICM та рекомендації клінічної практики» (Oddo et al, 2018):
Головний науковий співробітник наукового відділу малоінвазивної хірургії ДНУ «Науково-практичний центр профілактичної та клінічної медицини» Державного управління справами, д. мед. н., професор, член-кореспондент НАМН України Володимир Ілліч Черній продовжив тему важливості застосування оптимальної інфузійної терапії в умовах неврологічного стаціонара. При висвітленні теми лектор спирався на оновлені настанови Європейського товариства інтенсивної терапії (ESICM) від 2018 р. «Інтенсивна інфузійна терапія в неврології: консенсус ESICM та рекомендації клінічної практики» (Oddo et al, 2018):
- Доцільно віддавати перевагу кристалоїдам (сильна рекомендація).
- Не рекомендоване використання колоїдів, глюкозовмісних та інших гіпотонічних розчинів, а також низько- (4%) або висококонцентрованих (20‑25%) розчинів альбуміну як підтримувальних та реанімаційних інфузійних засобів при гострій церебральній патології (субарахноїдальний крововилив, черепно-мозкова травма, інсульт).
- В осіб із низьким артеріальним тиском (АТ) для реанімації як інфузійні розчини першої лінії мають бути використані кристалоїди; пацієнтам даної групи не слід призначати колоїди та гіпертонічні сольові розчини (слабка рекомендація).
- Для оптимізації рідинної ресусцитації у пацієнтів NIC (neurointensive care – нейроінтенсивного догляду) як основні кінцеві точки доцільно використовувати параметри АТ та балансу рідини (сильна рекомендація), як вторинні точки – показники діурезу, серцевого викиду, рівень лактату, сатурацію венозної крові киснем (слабка рекомендація). Не варто застосовувати центральний венозний тиск як кінцеву точку для проведення рідинної ресусцитації у пацієнтів NIC (сильна рекомендація).
- Не слід використовувати рестриктивну інфузійну терапію (загальний негативний баланс рідини) у пацієнтів NIC (слабка рекомендація).
- Рекомендовано проводити моніторинг вмісту електролітів (Na+, Cl–) та зміни осмолярності як кінцевої точки безпеки для інфузійної терапії хворих NIC (слабка рекомендація).
Спікер привернув увагу до основного постулату нейрофізіології: для функціонування нейрона необхідно, щоб рівень метаболізму відповідав можливості його забезпечення, тобто нормальному перфузійно-метаболічному співвідношенню (Gromov el al., 2016). На жаль, при критичних станах нервової системи це співвідношення суттєво порушується, що призводить до вторинного необоротного пошкодження. Саме тому слід досконало розуміти принципи адекватного забезпечення перфузійно-метаболічного співвідношення:
- У нормі осмолярність плазми, мозкової інтерстиціальної рідини та ліквору є однаковою (Stokum et al., 2016).
- Локальне пошкодження гематоенцефалічного бар’єра спричиняє порушення контролю гомеостазу H2O, електролітів та інших розчинених речовин; рух рідини більшою мірою залежатиме від перепаду тиску між інтра- та екстравазальним (інтерстиціальним) сектором, ніж від осмотичного напруження (Ertmer et al., 2014).
- Оскільки більшість пацієнтів із гострим порушенням мозкового кровообігу перебувають у стані дегідратації на момент прибуття до стаціонара (причини дегідратації осіб з інсультом представлені у табл. 2), оптимальним вважається введення рідини внутрішньовенно; у таких випадках слід враховувати показник гематокриту.
- Осмолярність – сумарна осмотична концентрація розчинених кінетично активних частинок в 1 л розчинника (нормальне значення для крові = 280‑295 мосм/л).
- Колоїдно-осмотичний тиск становить лише 1/150 осмолярності (близько 2 мосм/л або 25 мм рт. ст.) та залежить від кількості білкових крупномолекулярних складових.
- Об’єм води в організмі становить приблизно 60%: 20% позаклітинної (5% – судинний, 15% – інтерстиціальний сектор) та 40% внутрішньоклітинної рідини.
- При інсульті зазвичай розвивається ізотонічна або гіпертонічна дегідратація (розчинник із клітини переміщується в інтерстицій та судинне русло).
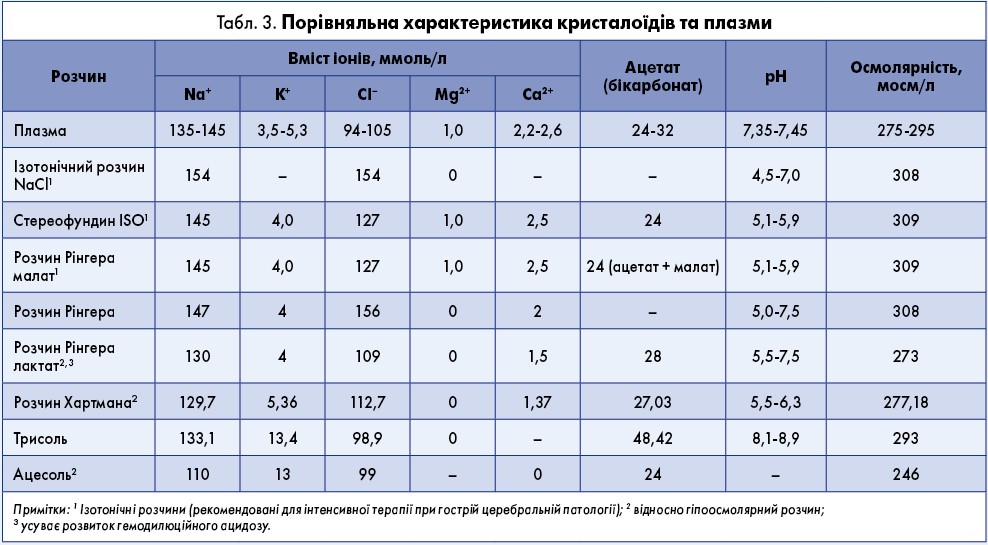
- Введення гіпотонічних розчинів (розчин Рінгера лактат) та тих, що містять вільну воду (наприклад, ізотонічний розчин 5% глюкози), сприяє поповненню внутрішньоклітинного простору (тим самим зростає ризик розвитку внутрішньоклітинного набряку, набряку мозку в новонароджених), ізотонічних – поповненню інтерстиціального простору та судинного русла, гіпертонічних розчинів та колоїдів – поповненню переважно судинного руслу. Порівняльна характеристика кристалоїдів наведена в таблиці 3.

За словами В.І. Чернія, сучасні вітчизняні рекомендації виступають за використання ізотонічних розчинів при інтенсивній терапії гострої церебральної патології (див. табл. 2).
Варто зауважити, що відмова від розчинів, що містять іони резервної лужності, через можливі побічні реакції викликає зменшення буферної ємності крові та призводить до розвитку гемодилюційного ацидозу, наслідком чого є підвищення ризику смерті. Так, малат і ацетат метаболізуються у м’язах, останній не є токсичним у високих дозах (до 4,7 ммоль/кг/год), лактат підвищує глікемію, не утилізується при печінковій недостатності, знижує діагностичну цінність, цитрат має високу токсичність (летальна доза 50% – 1,75 ммоль/кг), глюконат суттєво впливає на збільшення використання кисню.
У даному контексті професор поділився висновками дослідження ефективності та безпеки застосування натрію бікарбонату для корекції виразного метаболічного ацидозу (Jacer et al., 2018). Альтернативним та безпечнішим варіантом є інфузія розчину Рінгера лактату, що корегує гемодилюційний ацидоз.
 Було детально розглянуте застосування ізотонічного розчину Рінгера малату. Даний препарат, за словами доповідача, є ідеальним електролітним розчином відносно плазми крові:
Було детально розглянуте застосування ізотонічного розчину Рінгера малату. Даний препарат, за словами доповідача, є ідеальним електролітним розчином відносно плазми крові:
- ізоволемічний (60‑70 мл/кг);
- ізогідротичний (рН=7,38‑7,42);
- ізоонкотичний (25‑30 мм рт. ст.);
- містить ацетат та малат, що за 60‑90 хв метаболізуються до еквівалентної кількості гідрокарбонату (при цьому використовується вдвічі менше кисню, ніж у разі застосування розчину Рінгера лактату);
- чинить дезінтоксикаційний, антиоксидантний ефект (малат є субстратом орнітинового циклу сечовини – бере участь у зв’язуванні аміаку в м’язовій тканині та збільшує біодоступність сукцинату);
- не спричиняє ризику ятрогенних ускладнень;
- може застосовуватися при дисфункції печінки.
Водночас негативний вплив 0,9% NaCl пов’язують із високою концентрацією іонів Cl–. Це призводить до транзиторного гіпрехлоремічного ацидозу, зниження діурезу, підвищення об’єму інтерстиціальної рідини, що було підтверджено у дослідженні Orbegozo (2014), та, як наслідок, зростання ризику смерті через дисфункцію нирок. Таким чином, застосування збалансованих розчинів кристалоїдів є оптимальнішим, ніж фізіологічного розчину NaCl.
На додаток, лектор навів дані, оприлюднені на конференції, що відбулася у Каліфорнії (США) 2010 р., за якими лікування інсульту передбачає використання виключно фізіологічного розчину протягом 24 год; при гіпотонії, спричиненій гіповолемією або неврологічним порушенням, рекомендоване введення плазмоекспандерів.
В.І. Черній класифікував розчини за фізико-хімічними властивостями:
1. Мають колоїдно-осмотичний тиск:
- альбумін (5 та 10%);
- декстрани (реополіглюкін);
- гідроксиетилкрохмаль (стабізол, гекодез 6%, рефортан);
- модифікований желатин (волютенз 5‑10 мл/кг – волемічний ефект, аналогічний розчину альбуміну, зберігається протягом 3‑4 год).
2. Мають осмотичний тиск:
- сорбіт (реосорбілакт, сорбілакт);
- полііонні, ізоіонні, ізоосмолярні розчини (Рінгера лактат, розчини Хартмана, NaCl).
3. Притаманна комбінація властивостей (збільшення осмолярності та онкотичного тиску плазми): збалансований колоїдно-гіперосмолярний розчин (гекотон).
Прицільний аналіз вмісту електролітів у крові хворих є обов’язковою умовою наступного вибору варіанта інфузійної терапії. Слід враховувати, що у пацієнтів із гострою неврологічною патологією часто має місце виразне порушення електролітного балансу у вигляді гіпер- або гіпонатріємії. Остання є результатом ураження діенцефальних структур із розвитком синдрому неадекватної корекції антидіуретичного гормону або синдрому церебральної втрати солі.
Вкрай небезпечною є швидка корекція гіпонатріємії. У такому клінічному випадку розвивається центральний понтинний мієліноліз – особлива форма демієлінізаційного процесу в ділянці моста. Саме тому гіпонатріємія є протипоказанням для внутрішньовенного введення гіпертонічних розчинів NaCl (Стаховська та співавт., 2000).
Висновками доповіді професора В.І. Чернія стали такі постулати:
- Інтенсивна інфузійна терапія має бути спрямована на досягнення еуволемії з використанням ізотонічних кристалоїдів.
- Не рекомендовано застосовувати колоїди, глюкозовмісні, гіпотонічні розчини та розчин альбуміну як підтримувальну терапію в умовах NIC.
- Корекція волемії, водно-електролітного та кислотно-лужного гомеостазу, метаболізму в мозку є основною метою інфузійної терапії.
Гіперосмолярний синдром у пацієнтів неврологічного та нейрохірургічного профілю
 Лікар-анестезіолог клінічної лікарні «Феофанія» ДУС (м. Київ) Юрій Володимирович Гнатів ознайомив авдиторію з основами осмолярності – концентрацією кінетично активних частинок в 1 л розчину (води). У нормі осмолярність плазми, міжклітинної та внутрішньоклітинної рідини є однаковою і становить 285‑310 мосм/л. Зміна осмолярності в одному з секторів призводить до перерозподілу води, яка переходитиме у сектор із вищою осмолярністю; відповідно, виникне його гіпергідратація та зневоднення сектора з меншою осмолярністю.
Лікар-анестезіолог клінічної лікарні «Феофанія» ДУС (м. Київ) Юрій Володимирович Гнатів ознайомив авдиторію з основами осмолярності – концентрацією кінетично активних частинок в 1 л розчину (води). У нормі осмолярність плазми, міжклітинної та внутрішньоклітинної рідини є однаковою і становить 285‑310 мосм/л. Зміна осмолярності в одному з секторів призводить до перерозподілу води, яка переходитиме у сектор із вищою осмолярністю; відповідно, виникне його гіпергідратація та зневоднення сектора з меншою осмолярністю.
За словами спікера, осмолярність має вимірюватися осмометром, однак у реальних умовах клініцисти не забезпечені цим апаратом, тому використовують для розрахунку формулу:
Осмолярність (мосм/л) = 1,86 × вміст Na (ммоль/л) + вміст глюкози (ммоль/л) + вміст сечовини (ммоль/л) + 10
Надалі доповідач розглянув причини зміни кількості кожного з компонентів, що впливають на осмолярність:
1. Азотемія (підвищення рівня сечовини у крові) може бути наслідком:
- патології нирок (ниркова недостатність);
- нераціональної витрати білка (переважання катаболізму, недоїдання);
- хронічної інфекційної патології;
- гострої серцевої недостатності;
- ятрогенії (у високих дозах аргінін як попередник сечовини може призводити до азотемії).
2. Гіперглікемія (перевищення нормального вмісту глюкози – 3,3‑5,5 ммоль/л у капілярній крові, 4,0‑6,1 ммоль/л у венозній) спостерігається при:
- декомпенсації цукрового діабету;
- стресі (гостре порушення мозкового кровообігу, інфаркт міокарда);
- медикаментозному впливі кортикостероїдів, діуретиків, антидепресантів, ніацину);
- аліментарному навантаженні.
3. Гіпернатріємія (перевищення нормального вмісту натрію у плазмі – 136‑142 ммоль/л) є результатом:
- надмірного надходження іонів Na+ ззовні;
- втрати вільної води, поліурії, діареї;
- ураження гіпоталамуса з пошкодженням центру спраги й осморецепторів;
- порушення продукції антидіуретичного гормону (есенціальна гіпернатріємія);
- гіперпродукції мінералокортикоїдів (синдром Конна);
- судом;
- перевантаження організму іонами Na+ (зловживання гіпертонічним розчином NaCl);
- терапії осмодіуретиками (рівень Na+ >155 ммоль/л є протипоказанням для їхнього використання).
Лектор зауважив, що рівень Na+ впливає на стан свідомості пацієнта. Так, підвищення вмісту іонів Na+ до 170 ммоль/л спричиняє сопорозний стан, до 180 ммоль/л – кому, до 200 ммоль/л – смерть. Лікувальна тактика включає: припинення введення Na+ в організм, активацію ентерального поповнення вільною водою (пиття, введення рідини через шлунковий/кишковий зонд / товстий кишечник – до 5 л, під контролем діурезу та центрального венозного тиску), а також внутрішньовенне, внутрішньокісткове, підшкірне введення ізотонічного або гіпотонічного розчину NaCl.
Дефіцит води при дегідратації розраховується за такими формулами:
- у пацієнта без кровотечі та з показником гематокриту >0,44:
Дефіцит води = 0,2 × маса тіла × (1 – гематокрит пацієнта) / 0,44;
- у хворого після кровотечі або з анемією та рівнем Na+ >142 ммоль/л:
Дефіцит води = 0,2 × маса тіла × (1 – вміст Na+ пацієнта) / 142.
Ю.В. Гнатів наголосив, що особливу увагу слід привернути до рекомендації стосовно того, що швидкість корекції хронічної гіпернатріємії не повинна перевищувати 8 ммоль/добу. Корекцію гострої гіпернатріємії не можна проводити швидше ніж на 1 ммоль/год. Швидка корекція значно підвищує ризик розвитку набряку головного мозку.
Підсумовуючи промову, доповідач зауважив, що вчасна адекватна корекція гіпернатріємії, гіперглікемії, азотемії є невід’ємною частиною лікування пацієнтів неврологічного та нейрохірургічного профілю.
Невідкладна терапія при рухових розладах
 Професор кафедри неврології № 1 Національної медичної академії післядипломної освіти імені П.Л. Шупика (м. Київ), д. мед. н. Тетяна Миколаївна Слободін акцентувала увагу на актуальній патології серотонінового синдрому – ятрогенному потенційно летальному стані, що викликається гіперстимуляцією 5-гідрокситриптамінових (5-HT) рецепторів. До медикаментозних засобів, що можуть викликати серотоніновий синдром, відносять:
Професор кафедри неврології № 1 Національної медичної академії післядипломної освіти імені П.Л. Шупика (м. Київ), д. мед. н. Тетяна Миколаївна Слободін акцентувала увагу на актуальній патології серотонінового синдрому – ятрогенному потенційно летальному стані, що викликається гіперстимуляцією 5-гідрокситриптамінових (5-HT) рецепторів. До медикаментозних засобів, що можуть викликати серотоніновий синдром, відносять:
- інгібітори моноаміноксидази;
- селективні інгібітори зворотного захоплення серотоніну;
- трициклічні антидепресанти;
- L-триптофан;
- буспірону гідрохлорид;
- опіати (крім морфіну);
- літій;
- триптани;
- «екстазі» (MDMA – 3,4-метилендіокси-N-метамфетамін);
- амфетамін;
- кокаїн.
Проявами серотонінової інтоксикації є швидко прогресувальні міоклонуси, гіперрефлексія, епінапади, гіпертермія, гіперпірексія (до 42 °C), артеріальна гіпертензія, тахікардія, діарея, мідріаз, поведінкові розлади (ейфорія, летаргія, кома). Невідкладна терапія полягає у відміні препаратів, що викликали серотоніновий синдром, призначенні бензодіазепінів, оланзапіну. У тяжких випадках слід застосовувати ципрогептадину гідрохлорид (навантажувальна доза – 12 мг, надалі по 4‑6 мг кожні 6 год (до 32 мг/добу) – антигістамінний засіб, що є антагоністом серотоніну.
У клінічній практиці надзвичайно важливо диференціювати серотоніновий синдром від злоякісного нейролептичного – ятрогеного синдрому, що виникає на тлі приймання блокаторів дофамінових рецепторів (як-то нейролептики, метоклопрамід, прохлорперазин, прометазин).
У даному контексті професор Т.М. Слободін надала порівняльну характеристику цих патологічних станів, що наведена у таблиці 4.
.jpg) Провокувальними факторами для розвитку злоякісного нейролептичного синдрому є:
Провокувальними факторами для розвитку злоякісного нейролептичного синдрому є:
- підвищення дози нейролептика;
- зневоднення;
- наявність інтеркурентних захворювань із гіпертермією;
- електролітні порушення (гіпонатріємія, гіпокаліємія);
- аліментарна недостатність;
- гіпоглікемія, гіпопротеїнемія, дефіцит заліза;
- ендокринні розлади (патологія щитоподібної залози);
- нейродегенеративні захворювання (декомпенсація хвороби Паркінсона);
- чоловіча стать, молодий вік.
Останньою нозологією з подібною клінічною картиною, яка була представлена спікером, був синдром паркінсонізму-гіперпірексії (акінетичний криз). Він подібний до злоякісного нейролептичного синдрому, що виникає у пацієнтів із хворобою Паркінсона на тлі зменшення/скасування дофамінергічної терапії, зниження її ефективності.
Насамкінець лекторка зауважила, що лікувальні стратегії у разі злоякісного нейролептичного синдрому та акінетичного кризу є подібними:
- Скасування причинного фактора (медикаменти).
- Зниження температурної реакції, профілактика інфекційних ускладнень (пневмонія, пролежні).
- При тяжкому перебігу – 20 мг дексаметазону або 250 мг метипреднізолону.
- Із метою зниження м’язової ригідності – бензодіазепіни, міорелаксанти (дантролен).
- Леводопа (100 мг із поступовим підвищенням дози на 100 мг кожні три доби).
- Амантадин (200‑400 мг/добу).
Вторинний гнійний менінгіт у пацієнтів відділень інтенсивної терапії
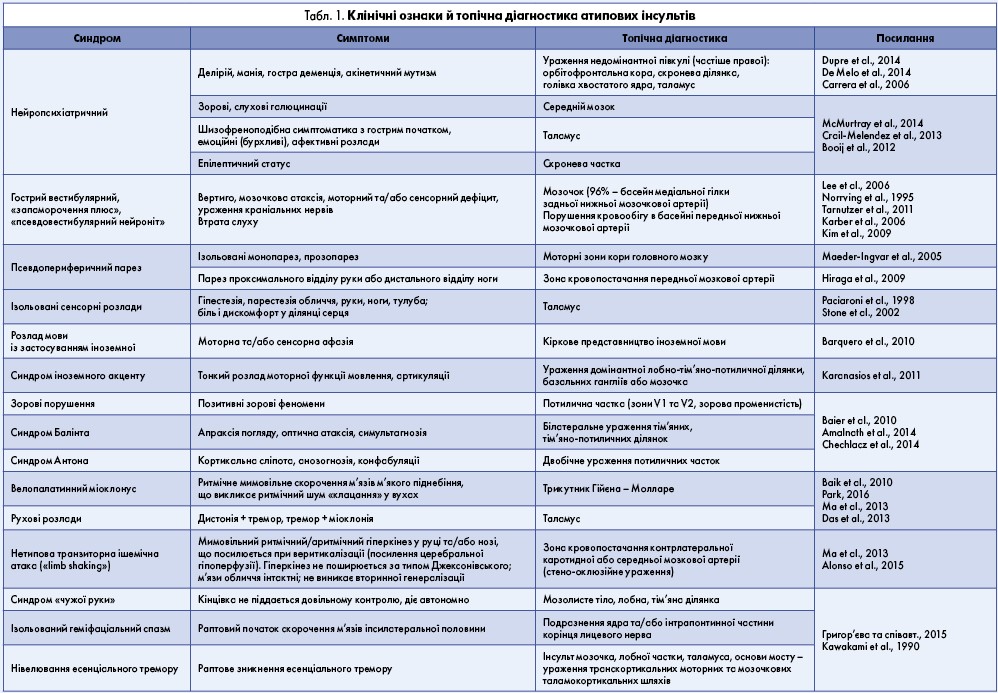
 Професор кафедри анестезіології та інтенсивної терапії Національної медичної академії післядипломної освіти імені П.Л. Шупика (м. Київ), д. мед. н. Олександр Анатолійович Галушко, користуючись власним досвідом, представив актуальну інформацію щодо тактики діагностики й лікування пацієнтів із вторинним гнійним менінгітом. Доповідач нагадав слухачам, що менінгіт – клінічний синдром, що характеризується запаленням мозкових оболонок. Класична тріада менінгіту включає лихоманку, головний біль, ригідність потиличних м’язів (Degraeve et al., 2016).
Професор кафедри анестезіології та інтенсивної терапії Національної медичної академії післядипломної освіти імені П.Л. Шупика (м. Київ), д. мед. н. Олександр Анатолійович Галушко, користуючись власним досвідом, представив актуальну інформацію щодо тактики діагностики й лікування пацієнтів із вторинним гнійним менінгітом. Доповідач нагадав слухачам, що менінгіт – клінічний синдром, що характеризується запаленням мозкових оболонок. Класична тріада менінгіту включає лихоманку, головний біль, ригідність потиличних м’язів (Degraeve et al., 2016).
Класифікація менінгітів (Brouwer et al., 2016):
1. За характером змін у лікворі: гнійні та серозні.
2. За етіологією: бактеріальні, рикетсійні, спірохетозні, бореліозні, вірусні, грибкові; спричинені найпростішими, гельмінтами; змішаної етіології:
- найчастішими збудниками гнійного менінгіту є (в порядку зменшення частоти): менінгокок, пневмокок (Streptococcus pneumoniae), гемофільна паличка, стафілококи, інші стрептококи, найпростіші (табл. 5);
- найчастішими збудниками серозного менінгіту є (в порядку зменшення частоти): ентеровіруси, вірус епідемічного паротиту, борелії, мікобактерії, вірус імунодефіциту людини, віруси герпес-групи.
3. За механізмом виникнення гнійні менінгіти поділяють на:
- первинні (розвиваються при гострому інфекційному процесі);
- вторинні (ускладнення місцевого або загального інфекційного процесу):
- посттравматичні (при відкритій черепно-мозковій травмі);
- ятрогенні (спричинені порушенням правил асептики при анестезіологічних та нейрохірургічних маніпуляціях);
- такі, що розвинулися внаслідок захворювань ЦНС (субарахноїдальний крововилив при розриві артеріальної аневризми, спонтанний внутрішньомозковий крововилив);
- такі, що розвинулися внаслідок наявності метастатичних гнійних вогнищ при госпітальній бактеріємії.
За словами доповідача, останніми роками підвищується частота вторинних гнійних менінгітів, спричинених Acinetobacter spp., яким притаманні такі характеристики: стійкі в навколишньому середовищі, зберігаються на відкритих поверхнях, передаються контактним шляхом через пацієнтів та руки медичного персоналу, мають високу резистентність до антибіотиків (Klein et al., 2016).
До факторів, що сприяють розвитку вторинних гнійних менінгітів професор О.А. Галушко відніс (Kubrakov et al, 2019):
- перебування в палаті відділення інтенсивної терапії;
- тривалу штучну вентиляцію легень;
- часті ін’єкції, тривалу катетеризацію магістральних судин;
- наркоманію;
- лікворею;
- гнійні синусити, отити, мастоїдити;
- остеомієліт, флегмону обличчя;
- ендокардит;
- повторний гемодіаліз;
- злоякісні новоутворення в анамнезі;
- цереброваскулярні захворювання;
- цукровий діабет;
- хронічне захворювання нирок, печінки, легень;
- сепсиси.
Актуальними методами діагностики є оцінка клінічних даних (інтоксикаційний, менінгеальний, загальномозковий синдром, пригнічення свідомості, збільшення внутрішньочерепного тиску), дослідження ліквору (загальноклінічний, бактеріологічний аналіз) (Miro et al., 2016). Також проводять визначення рівня лактату в лікворі (1,1‑2,4 ммоль/л) та крові (0,5‑2,2 ммоль/л) – чутливість та специфічність >90%, прокальцитоніну в крові, особливо у перші 24 год (у лікворі зміни неспецифічні). Проте слід враховувати, що вміст прокальцитоніну підвищується при шоках, політравмі, респіраторному дистрес-синдромі. Одночасне зростання рівня прокальцитоніну (>0,075 нг/мл) і лактату (>3,45 ммоль/л) у лікворі є специфічним на 96%.
Окрім того, доповідач детально представив диференційну діагностику менінгітів згідно зі змінами у лікворі (табл. 6).
Специфічна діагностика менінгітів включає такі процедури (Godet et al., 2016):
- Бактеріологічний метод (змив із носоглотки, мокротиння, кров, ліквор).
- Фарбування за Грамом із наступною бактеріоскопією.
- Полімеразно-ланцюгова реакція (чутливість та специфічність – 98‑99%).
- Серологічна діагностика, основана на виявленні антитіл до менінгококу (реакція непрямої гемаглютинації); має допоміжне значення та використовується для визначення серотипу збудника.
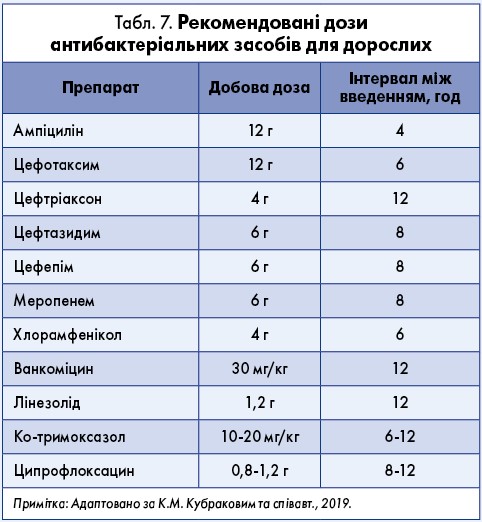
Наступним кроком є раціональна антибіотикотерапія (дозування представлене в табл. 7). За словами спікер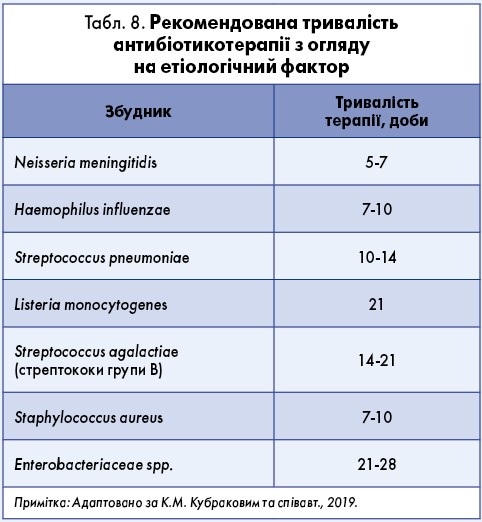 а, при вторинних бактеріальних менінгітах призначають β-лактамні антибіотики (пеніциліни, цефалоспорини, карбапенеми) та фторхінолони з урахуванням проникності через гематоенцефалічний бар’єр. Найпоширеніша схема включає: цефалосприн ІІІ покоління (цефтріаксон або цефотаксим) та/або ванкоміцин (IDSA, SFNS, 2016). Для лікування вторинного бактеріального менінгіту, викликаного Staphylococcus aureus або грамнегативними бактеріями, застосовують комбінацію цефепіму/меропенему з ванкоміцином. Ця схема також ефективна для ерадикації метицилін-резистентного золотистого стафілококу. При виявленні резистентності до ванкоміцину препаратом резерву є лінезолід у дозі 600 мг двічі на добу.
а, при вторинних бактеріальних менінгітах призначають β-лактамні антибіотики (пеніциліни, цефалоспорини, карбапенеми) та фторхінолони з урахуванням проникності через гематоенцефалічний бар’єр. Найпоширеніша схема включає: цефалосприн ІІІ покоління (цефтріаксон або цефотаксим) та/або ванкоміцин (IDSA, SFNS, 2016). Для лікування вторинного бактеріального менінгіту, викликаного Staphylococcus aureus або грамнегативними бактеріями, застосовують комбінацію цефепіму/меропенему з ванкоміцином. Ця схема також ефективна для ерадикації метицилін-резистентного золотистого стафілококу. При виявленні резистентності до ванкоміцину препаратом резерву є лінезолід у дозі 600 мг двічі на добу.
Тривалість антибіотикотерапії визначається етіологією процесу (табл. 8) та динамікою санації ліквору (стерильність ліквору – негативне бактеріологічне дослідження, цитоз <100 кл/мкл, лімфоцити >90%, нормалізація рівня білка та глюкози) (Hasbun, 2017). За браку даних про ідентифікацію етіологічного чинника тривалість антибіотикотерапії становить 14‑21 день з урахуванням динаміки зміни клінічної картини та лабораторних показників (Van de Beek et al., 2016).
Підсумовуючи доповідь, професор О.А. Галушко зауважив, що додатково до етіологічної терапії слід впроваджувати введення збалансованих розчинів кристалоїдів (рівень доказовості С) (ESICM, 2018; NICE, 2018). Глюкокортикоїди (дексаметазон у дозі 4‑8 мг протягом 3‑4 днів) сприяє зниженню запалення в субарахноїдальному просторі та вазогенного набряку в пацієнтів із вторинним гнійним менінгітом й ознаками набряку головного мозку. Раннє введення дексаметазону корелює зі зниженням неврологічного дефіциту (виняток становлять особи з імунодефіцитом) (Wu et al., 2016).
Підготувала Маргарита Марчук
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 1 (52) 2020 р
СТАТТІ ЗА ТЕМОЮ Неврологія
Проблема когнітивних розладів є однією з найважливіших у сучасній клінічній медицині. Це зумовлено не тільки збільшенням частки людей старшого віку серед населення, а й посиленням ролі стресу та інших патогенетичних чинників. У березні відбувся семінар «Академія сімейного лікаря. Біль в грудній клітині. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста», у якому прийняли участь провідні вітчизняні науковці і фахівці різних галузей. У рамках заходу професор кафедри військової терапії Української військово-медичної академії Міністерства оборони України, кандидат медичних наук Мар’яна Миколаївна Селюк представила доповідь «Війна та когнітивні порушення. Причина чи наслідок? Як вирішити проблему?». Подаємо огляд цієї доповіді у форматі «запитання – відповідь»....
Хоча нестероїдні протизапальні препарати (НПЗП) мають численні серйозні побічні ефекти, вони належать до найчастіше застосовуваних препаратів у всьому світі (McGettigan P., Henry D., 2013). Через часте застосування побічні дії НПЗП становлять значну загрозу для громадського здоров’я. Так, уже декілька декад тому було описано підвищення артеріального тиску та ризик загострень серцевої недостатності на тлі прийому цих препаратів (Staessen J. et al., 1983; Cannon P.J., 1986)....
У лютому відбувся медичний форум Ukraine Neuro Global 2024, організований ГО «Українська асоціація медичної освіти» (м. Київ). Під час заходу обговорювалися найактуальніші проблеми сучасної неврології. У рамках форуму відбувся сателітний симпозіум «Актуальні питання фармакотерапії в неврології». Слово мала в.о. завідувача кафедри неврології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор Марина Анатоліївна Тріщинська з доповіддю «Краніоцервікалгії: особливості діагностики та лікування»....
Запаморочення є поширеним та іноді стійким симптомом після струсу мозку чи легкої черепно-мозкової травми (лЧМТ). Терміном «запаморочення» часто описують декілька симптомів, як-от головокружіння (вертиго; ілюзія руху), порушення рівноваги (нестійкість, нестабільність) і, власне, запаморочення (пресинкопальний стан). Запаморочення після струсу мозку є клінічним викликом, оскільки існує багато причин цього розладу, а його ведення залежить від етіології [1-3]. Однією з таких причин є пошкодження периферичної вестибулярної системи (внутрішнього вуха). У разі травм, отриманих під час війни, лЧМТ часто пов’язана з вибуховою дією, яка може пошкоджувати внутрішнє вухо. Лікарям важливо розуміти вестибулярні наслідки вибухової лЧМТ, оскільки ЧМТ є дуже характерною для сучасних війн [4]....