Роль активного метаболіту норкветіапіну в механізмі антидепресивної дії кветіапіну при лікуванні розладів настрою
Активні метаболіти певних антипсихотичних препаратів проявляють фармакодинамічні та фармакокінетичні властивості, які можуть бути схожими або відрізнятися від таких у вихідних сполуках. Проте чи можуть активні метаболіти антипсихотиків брати участь у механізмі їхньої антидепресивної дії? У статті F. López-Muñoz та C. Álamo, опублікованій у журналі Frontiers in Psychiatry (2013; 4 (102): 1‑8), огляд якої представлено до вашої уваги, проаналізовано фармакологічні аспекти застосування антипсихотиків кветіапіну та норкветіапіну залежно від фармакокінетики й фармакодинаміки (афінність до дофамінергічних, норадренегічних та/або серотонінергічних рецепторів тощо), а також відмінності їхніх нейропротекторних властивостей.
Активні метаболіти вважаються клінічно значущими, коли їхній рівень достатньо високий для здійснення фармакологічної дії. Принаймні, вони настільки ж активні, як вихідний лікарський засіб, або виявляються в більших концентраціях у певних тканинах, приміром у мозку (Wille et al., 2005; Tekes et al., 2011). Активні метаболіти можуть повністю або частково відповідати за терапевтичний ефект препарату. Деякі проявляють фармакологічну активність, не пов’язану з основною дією вихідної сполуки, а іноді змінюють чи дезактивують її (Fura, 2006). Поширена думка, що дія багатьох психоактивних засобів є результатом впливу не тільки вихідної речовини, але також її активних метаболітів. До того ж деякі препарати самі не є фармакологічно активними та при введенні в організм внаслідок біотрансформації набувають активності; їх називають проліками.
У психофармакології серед активних метаболітів, що поліпшують фармакодинамічні, фармакокінетичні або токсикологічні властивості вихідного лікарського засобу, виділяють дезипрамін (дезметиліміпрамін), похідні антидепресанту іміпрамін, мезоридазин та паліперидон, похідні антипсихотиків тіоридазин і рисперидон, а також метаболіт діазепаму оксазепам (Wille et al., 2005; Fura, 2006). Деякі активні метаболіти антипсихотиків впливають на їхню антидепресивну дію, як-от мета-хлорфенілпіперазин, 9-гідроксирисперидон і норкветіапін. Останній вибірково інгібує зворотне захоплення норадреналіну, є частковим агоністом рецептора 5-HT1A та діє як антагоніст пресинаптичних рецепторів α2, 5-HT2C і 5-HT7.
Активні метаболіти антидепресантів
Антидепресанти – широка й різноманітна група препаратів, що включає багато активних метаболітів. Деякі з них стали виробляти як окремі лікарські засоби. У таблиці представлені основні активні метаболіти та відповідні антидепресанти.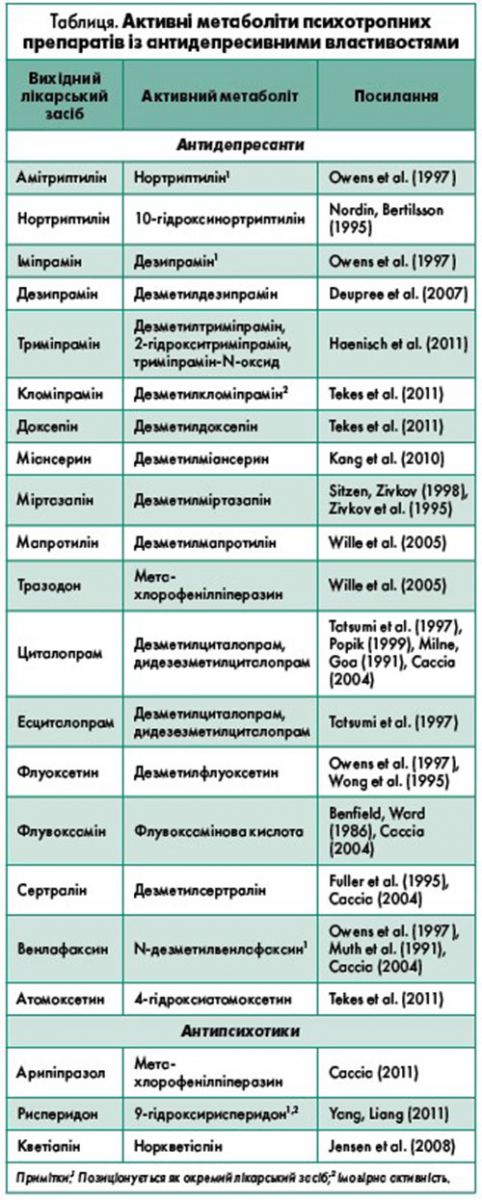
Амітриптилін – інгібітор транспортера моноамінів – норадреналіну (норадреналіновий білок-транспортер [NET]) та серотоніну (серотоніновий білок-транспортер [SERT]). Нортриптилін є його активним метаболітом та потужнішим інгібітором зворотного захоплення NET, ніж SERT. Дезипрамін – активний метаболіт іміпраміну, інгібітор зворотного захоплення більшою мірою NET, меншою – SERT. З-поміж доступних трициклічних антидепресантів (ТЦА) дезипрамін та нортриптилін є найпотужнішими інгібіторами зворотного захоплення NET (Owens et al., 1997). Інші ТЦА також мають активні метаболіти, але їхній профіль щодо вихідних сполук потребує ретельнішого вивчення (Kang et al., 2010).
Серед селективних інгібіторів зворотного захоплення серотоніну (СІЗЗС) унаслідок деметилювання циталопраму, флуоксетину та сертраліну утворюються дезметилциталопрам, норфлуоксетин та норсертралін відповідно, які також інгібують SERT (Fuller et al., 1995). Концентрація норциталопраму в плазмі крові у стаціонарному стані наближається до майже 40% від такої циталопраму, також цей метаболіт інгібує SERT у 3‑8 разів слабше, ніж вихідна сполука (Tatsumi et al., 1997; Popik, 1999). Унаслідок біотрансформації флувоксаміну утворюється декілька активних метаболітів. Відомо, що карбоксильна кислота інгібує SERT слабко порівняно з вихідною речовиною (Caccia, 1998; Milne, Goa, 1991). Флуоксетин метаболізується шляхом N-деметилювання в основний активний метаболіт норфлуоксетин, порівнянний із вихідним лікарським засобом за фармакологічними властивостями (Owens et al., 1997; Wong et al., 1995). Проте норфлуоксетин легше проникає через гематоенцефалічний бар’єр та має більший період напіввиведення, ніж флуоксетин (Hiran et al., 2005; Qu et al., 2009). Сертралін утворює деметильований метаболіт дезметилсертралін, який є слабшим інгібітором зворотного захоплення SERT, ніж основна сполука in vivo (Caccia, 1998; Fuller et al., 1995).
Венлафаксин – інгібітор зворотного захоплення SERT і NET із подвійним механізмом дії. В організмі людини метаболізм препарату відбувається в основному шляхом O-деметилювання. Інші незначні метаболічні напрями включають N-деметилювання, внаслідок якого утворюється N-дезметилвенлафаксин. О-дезметилвенлафаксин проявляє схожу фармакологічну активність з його вихідною сполукою як in vitro, так і in vivo (Caccia, 1998; Owens et al., 1997).
Атомоксетин є селективним інгібітором зворотного захоплення NET, який застосовують при лікуванні розладу з дефіцитом уваги та гіперактивністю. Він утворює низку окисних метаболітів, з-поміж яких можна виділити 4-гідроксиатомоксетин, що блокує NET подібним до вихідної речовини чином (Sauer et al., 2003).
Активні метаболіти атипових антипсихотиків з антидепресивною дією
Антипсихотики давно зарекомендували себе як ефективні засоби для терапії депресії. У 1954 р. P. Kielhoz припустив, що хлорпромазин ефективний для лікування депресивних та маніакальних епізодів. Потім K. Nahunek et al. (1973) повідомили про ефективність першого атипового антипсихотика клозапіну за ендогенної депресії. Сьогодні атипові антипсихотичні препарати визнані ефективними при лікуванні біполярної депресії, проте при уніполярній вони переважно показані для комбінованої терапії або як допоміжний засіб у разі резистентності до призначеного лікування (Cruz et al., 2010; Vieta et al., 2011; Nelson, Papakostas, 2009). Яким же чином активні метаболіти антипсихотиків задіяні в механізмах їхньої антидепресивної активності?
Серед атипових антипсихотиків оланзапін у поєднанні з флуоксетином вперше продемонстрували більшу ефективність, ніж кожен препарат окремо (Chen et al., 2011; Shelton et al., 2001). З-поміж метаболітів оланзапіну в людини застосовується кон’югований 10-N-глюкуронід. Наявні дані свідчать про те, що всі метаболіти оланзапіну менш активні, ніж він сам, тому, ймовірно, не впливають на його фармакологічний профіль (Calligaro et al., 1997).
Рисперидон виявився ефективним як засіб допоміжної терапії, особливо у поєднанні з СІЗЗС, у пацієнтів із ВДР (Chen et al., 2011). Він метаболізується головним чином за допомогою CYP2D6, утворюючи 9-гідроксирисперидон або паліперидон, шляхом гідроксилювання. З огляду на те, що при його пероральному прийманні у багатьох пацієнтів рівень 9-гідроксирисперидону в плазмі у 5‑10 разів перевищує такий рисперидону, цей метаболіт, імовірно, робить важливий внесок в антидепресивну дію антипсихотика (De León et al., 2010; Álamo et al., 2013). Паліперидон із пролонгованим вивільненням у формі перорального препарату або ін’єкцій був ефективним при лікуванні симптомів шизофренії, що супроводжувала депресію (Yang, 2011; Canuso et al., 2010). Тож він проявляє активність як метаболіт рисперидону та має антидепресивну дію. Проте його ефективність у лікуванні ВДР ще не вивчали.
Атиповий антипсихотик кветіапін інтенсивно метаболізується в печінці. Його основним метаболітом є N-дезалкілкветіапін, також відомий як норкветіапін, фармакологічна активність якого відрізняється від дії основної сполуки, зумовлюючи його важливу роль як антидепресанту.
Норкветіапін – активний метаболіт кветіапіну з антидепресивною активністю
Ефективність кветіапіну в лікуванні психотичних захворювань – як шизофренії, так і манії, а також розладів настрою та тривожних розладів дозволяє розглядати його як багатофункціональний психоактивний засіб. Широкий спектр ефективності препарату, ймовірно, зумовлений його здатністю модифікувати системи дофамінергічної, норадренергічної та серотонінергічної нейротрансмісії. Кветіапін являє собою похідне дибензотіазепіну; він доступний у двох різних фармацевтичних формах: негайного (IR) та пролонгованого вивільнення (XR) (Riedel et al., 2008). Обидві інтенсивно метаболізуються печінкою до різних метаболітів, при цьому лише 1% елімінується без змін із сечею (Peuskens, 2011).
Норкветіапін виробляється під дією ізоферменту CYP3A4 цитохрому Р450. Жоден генетичний поліморфізм не впливає на CYP3A4, тому зміни метаболізму кветіапіну залежно від раси чи генетичних особливостей малоймовірні. Фармакокінетика кветіапіну дещо відрізняється в осіб похилого віку та пацієнтів, що приймають супутні препарати; на концентрацію норкветіапіну ці фактори впливають менше (Bakken et al., 2001). CYP2D6 також робить внесок у метаболізм кветіапіну, хоча й меншою мірою, внаслідок чого утворюється невелика кількість 7-гідроксикветіапіну, активність якого детально ще не вивчено (Fisher et al., 2012; Bakken et al., 2012).
За даними M.C. Mauri et al. (2007), концентрація кветіапіну в плазмі крові не є настільки високою, щоб пояснити його дію на рецептори або клінічні ефекти. Це дозволяє припустити, що активні метаболіти препарату беруть участь у його фармакодинаміці. Однак рівень у сироватці крові препаратів, що діють на ЦНС, є поганим предиктором центральної активності, оскільки є інші численні фактори впливу, як-то проникнення через гематоенцефалічний бар’єр, накопичення у ЦНС та кінетика асоціації/дисоціації з рецептором.
Фармакодинамічний профіль норкветіапіну порівняно із кветіапіном
Норкветіапін та кветіапін взаємодіють із дофамінергічною, норадренергічною та серотонінергічною системами, але відрізняються за здатністю змінювати їхнє функціонування. Як і інші атипові антипсихотики, кветіапін спроможний блокувати 5-НТ2А-рецептори з більшою афінністю, ніж D2, що може пояснити його антипсихотичні властивості та меншу схильність викликати екстрапірамідні симптоми й гіперпролактинемію (Peuskens, 2011). Крім того, кветіапін проявляє спорідненість до різних серотонінергічних та норадренергічних рецепторів, що може сприяти його антидепресивній та анксіолітичній дії (Seeman, Tallerico, 1999). Його активний метаболіт норкветіапін також важливий, оскільки, крім інгібування зворотного захоплення NET, він проявляє спорідненість до кількох рецепторів SERT (Winter et al., 2008; Prieto et al., 2010).
Загальна картина рецепторних профілів кветіапіну та норкветіапіну представлена на рисунку.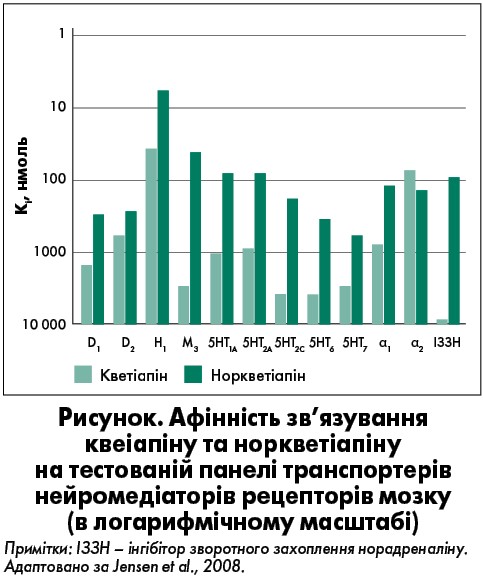
Функціонування дофамінергічних рецепторів. Зайнятість D2-рецепторів у лімбічній системі є основним механізмом для досягнення антипсихотичних ефектів. Кветіапін і норкветіапін демонструють помірну спорідненість до зв’язування з рецепторами дофаміну D1 та D2. Крім того, кветіапін швидко дисоціює від D2-рецепторів, тому для досягнення антипсихотичного ефекту його потрібно вводити у високих дозах. Він лише зрідка спричиняє екстрапірамідні ефекти через низьку здатність посилювати експресію відповідних рецепторів, що пояснює низьку частоту пов’язаної з ним пізньої дискінезії (Peuskens, 2011; Seeman et al., 1999).
На рівні нігростріального і тубероінфундибулярного дофамінових шляхів SERT діє як гальмівний модулятор шляхом стимуляції 5-HT2A-рецепторів. Кветіапін і норкветіапін є антагоністами 5-HT2A-рецепторів, що сприяє вивільненню дофаміну цими шляхами (Jensen et al., 2008). Позитронно-емісійні томографічні дослідження виявили вищий антагонізм до 5-HT2A-, ніж D2-рецепторів на рівні зазначених трактів; це пояснює, чому кветіапін не асоційований із розвитком гіперпролактинемії (Gefvert et al., 2001). Зважаючи на те, що норкветіапін здатний краще блокувати 5-HT2A-, ніж D2-рецептори, його переносимість подібна до такої кветіапіну або навіть краща. Окрім того, завдяки різним механізмам вивільнення дофаміну на мезокортикальному шляху, при застосуванні кветіапіну та норкветіапіну спостерігається поліпшення функціонування префронтальних регіонів та гіпокампу. На додачу до позбавлення від негативних, зокрема когнітивних, симптомів при шизофренії, це сприяє антидепресивній дії (Montgomery, 2008). Переносник NET відповідає за зворотне захоплення дофаміну в префронтальній корі, а норкветіапін (але не кветіапін) інгібує цей транспортер, унаслідок чого підвищується рівень дофаміну в лобній корі та посилюється антидепресивний ефект (Möller, 2005).
Функціонування серотонінергічних рецепторів. Крім того, що кветіапін та норкветіапін здатні блокувати різні рецептори SERT (це полегшує передачу дофаміну), вони також сприяють трансмісії SERT. Тобто кветіапін і більшою мірою норкветіапін полегшують серотонінергічну передачу, діючи як часткові агоністи 5-HT1A-рецепторів, що асоційовані з антидепресивним та анксіолітичним ефектами в людини. Норкветіапін має високу спорідненість до 5-HT1A-рецепторів, схожу на таку звичайних агоністів 5-HT1A буспірону та гепірону, та у 10 разів вищу, ніж у кветіапіну (Becker et al., 2006). Отже, норкветіапін сприяє активації постсинаптичних 5-HT1A-рецепторів у гіпокампі, порушення в якому спостерігаються на тлі депресії. Це може зумовлювати регенерацію нейронів у цій ділянці шляхом збільшення вивільнення факторів росту нервів, як-от нейротрофічного фактора мозку (BDNF) (McIntyre et al., 2009; Fumagalli et al., 2004). Також завдяки стимуляції 5-HT1A-рецепторів зростає вивільнення ацетилхоліну в префронтальній корі, що сприяє синаптичній пластичності, пов’язаній із навчанням та пам’яттю (Ichikawa et al., 2002).
Норкветіапін також має більшу афінність до 5-HT7-рецептора, ніж кветіапін, а відповідно, ефективний при депресії та розладах циркадного ритму, пов’язаних зі сном (Guscott et al., 2005). Хоча даних про вплив антагоністів 5-HT7 у людини немає, можливо, антагонізм до 5-HT7-рецепторів, притаманний норкветіапіну, сприяє антидепресивній дії кветіапіну. Як зазначалося вище, кветіапін і більшою мірою норкветіапін мають антагоністичні властивості щодо рецепторів 5-HT2A. Застосування антагоністів 5-HT2A було запропоноване для лікування безсоння. Можливо, норкветіапін, що є потужним антагоністом Н1-рецептора, сприяє значному седативному ефекту при лікуванні кветіапіном (Jensen et al., 2008).
Функціонування норадренергічної системи. Норкветіапін діє як потужний інгібітор NET-транспортера. Його афінність до цього переносника подібна до такої деяких антидепресантів, як-от нортриптилін, амітриптилін та дулоксетин. Кветіапін, навпаки, не може зв’язуватися з NET-транспортером. Також норкветіапін збільшує норадренергічне функціонування, блокуючи пресинаптичні α2-рецептори значно сильніше, ніж кветіапін. Шляхом інгібування переносника NET норкветіапін підвищує рівень дофаміну в префронтальній корі, оскільки останній також використовує цей транспортер для зворотного захоплення (Möller, 2005). За даними, отриманими in vivo, норкветіапін у дозі до 0,1 мг/кг демонстрував антидепресивну активність в експериментах на тваринах (Jensen et al., 2008).
Інші механізми, що впливають на антидепресивний ефект кветіапіну. Механізми без включення моноамінів вивчені менш ретельно. Так, стрес і депресія, як відомо, посилюють нейродегенерацію, а антидепресанти можуть зменшити чи усунути цей ефект. В експериментальних дослідженнях показано, що кветіапін запобігає зниженню вмісту BDNF та хронічній клітинній дегенерації в гіпокампі, пов’язаній зі стресом. Автори вважають, що заявдяки цьому можна зменшити деякі симптоми та когнітивний дефіцит при депресії (Xu et al., 2006). Крім того, J. Ichikawa et al. (2001) виявили, що кветіапін модулює активність рецепторів глутамату для гіпотетичного відновлення їхнього нормального функціонування. Це зменшує нейротоксичність, викликану надлишком нейромедіатора глутамату. R.C. Shelton та G.I. Papakostas (2008) стверджують, що антидепресивний ефект кветіапіну може бути зумовлений контролем запальних цитокінів і цитопротекторних молекул та антиоксидантною дією. Ці механізми пов’язані з початком депресивної симптоматики, хоча необхідні експериментальні та клінічні дослідження для підтвердження даної гіпотези. Роль норкветіапіну щодо таких процесів поки що не вивчали.
Небажані явища, асоційовані з норкветіапіном та кветіапіном. При лікуванні депресії виникають певні несприятливі ефекти, пов’язані з їхніми рецепторними профілями. Здатність кветіапіну та норкетіапіну зв’язуватися з гістаміновими H1-рецепторами призводить до розвитку седації, снодійного ефекту, підвищення апетиту та збільшення маси тіла. Блокування α1-адренергічних рецепторів у деяких пацієнтів пов’язане з ортостатичною гіпертензією. Це меншою мірою стосується кветіапіну XR, якому притаманні лише кілька плазматичних «піків». Норкветіапін демонструє афінність до мускаринових рецепторів, виступаючи антагоністом, особливо щодо M1, M3 та M5. Цей ефект у 20‑80 разів сильніший, ніж у кветіапіну, тому вважається, що такі небажані явища, як сухість у роті, затримка сечі, мідріаз, підвищення внутрішньоочного тиску та гіпотермія асоційовані з його активним метаболітом. Деякі дослідники стверджують, що антагонізм до М3-рецепторів, принаймні частково, відповідальний за виникнення гіперглікемії та цукрового діабету, спричинених антипсихотичним лікуванням (Johnson et al., 2005). Вони вважають, що більшість побічних ефектів після передозування кветіапіном зумовлені насамперед дією норкветіапіну (Jensen et al., 2008; Balit et al., 2003).
Висновки
Підсумовуючи викладене, автори зазначають, що кветіапін проявляє антидепресивні властивості завдяки норадренергічному, серотонінергічному та дофамінергічному механізмам. Препарат демонструє клінічно значущу ефективність при лікуванні уніполярної депресії у монотерапії (офіційно затверджений лише в Австралії та Канаді) і додатковий засіб для пацієнтів, які погано або зовсім не відповідають на антидепресанти. Крім того, кветіапін – єдиний препарат, який продемонстрував ефективність за наявності уніполярної та біполярної депресії без ризику розвитку манії (Shelton, Papakostas, 2008; Bauer et al., 2009). Антидепресивна активність кветіапіну, принаймні частково, опосередкована дією активного метаболіту норкветіапіну, який вибірково інгібує зворотне захоплення NET, є частковим агоністом 5-HT1A-рецепторів і діє як антагоніст пресинаптичних рецепторів α2, 5-HT2C та 5-HT7. Норкветіапін являє собою яскравий приклад активного метаболіту, завдяки якому кветіапін, що насамперед застосовують як антипсихотичний засіб, демонструє антидепресивну ефективність.
Підготувала Олена Коробка
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 1 (52) 2020 р
СТАТТІ ЗА ТЕМОЮ Психіатрія
У березні відбулася науково-практична конференція «Мультидисциплінарний підхід до проблемних питань неврології та психіатрії: нові стратегії лікування. Стрес-асоційовані розлади – виклики сьогодення». Захід був присвячений питанням вирішення проблем психічного та неврологічного характеру як однієї з загроз сучасного суспільства. ...
У сучасному світі люди щодня мають справу з величезною кількістю стресових ситуацій. Стрес – неспецифічна реакція організму у відповідь на стресовий фактор / небезпеку [1]. Сьогодення – вкрай стресовий час; ми постійно відчуваємо ті чи інші стресові ситуації, але в частки людей стресова подія трансформується і прогресує у тривожні розлади; іноді достатньо щонайменшого стресового епізоду, щоб зумовити розвиток тривожних розладів. Деякі люди, які перманентно перебувають у поточній стресовій ситуації, котрі зазнають один стрес за іншим, зберігають достатньо адекватне емоційне реагування, тобто адекватна емоційна реакція не перетворюється на тривожні розлади. ...
Наші діти зростають та живуть у складний час. Під час воєнного стану окупантами завдано значної шкоди як інфраструктурі України, так і життю й здоров’ю багатьох людей, особливо дітей, адже це найнезахищеніша категорія нашої спільноти. Найвищими цінностями зараз залишаються відчуття захищеності та безпеки як дітей, так і родини; однак на сучасному етапі наявність стійких стресів, постійної потреби переміщатися із класів або домівки до сховища на тлі відчуття страху обстрілів, почуття особистої тривоги, внутрішнього занепокоєння є невід’ємними супутниками загального стану наших дітей....
Депресія – це тяжка й поширена хвороба, яка уражає понад 300 млн осіб у всьому світі та вважається однією з найвагоміших проблем громадського здоров’я у ХХІ столітті (WHO, 2017). Інвалідизувальна природа депресії призводить до низки професійних, економічних, соціальних та особистих несприятливих наслідків (Thompson C., 2010). Протягом останніх років кількість випадків депресії значно зросла, перевантажуючи систему охорони здоров’я (Cipriani A. et al., 2018)....




