Пембролізумаб у лікуванні недрібноклітинного раку легені
Рак легені посідає одне з перших місць у структурі онкологічної захворюваності та смертності не лише в Україні, а й у світі. Протягом останніх десятиліть активно проводились дослідження, присвячені таргетній терапії та імунотерапії при недрібноклітинному раку легені (НДРЛ), за результатами яких вдалось істотно покращити результати лікування хворих із цією онкологічною патологією.
Зазвичай імунна система розпізнає пухлинні клітини та знищує їх, проте ухилення від імунної відповіді не дозволяє організму надати ефективну протипухлинну відповідь. Експресія молекул, які є інгібіторами імунної відповіді, відіграє ключову роль в імунному ухиленні при НДРЛ.
Ліганд програмованої клітинної смерті 1 (programmed cell death‑1 ligand 1 – PD-L1) та рецептор програмованої клітинної смерті (PD‑1) широко досліджувались при НДРЛ. Відомо, що зв’язування PD‑1 та PD-L1 пригнічує протипухлинну цитотоксичну відповідь Т-лімфоцитів, це дає змогу пухлинній клітині залишитись поза увагою імунної системи. Блокада PD‑1 та/або PD-L1, навпаки, дозволяє зробити пухлину «видимою» для власних імунних клітин і досягти вираженого протипухлинного ефекту.
Пембролізумаб (Кітруда®, MK3475) – гуманізоване IgG4 моноклональне антитіло з високою афінністю селективно до PD‑1, що дозволяє йому блокувати шлях PD‑1/PD-L1. За результатами серії клінічних досліджень KEYNOTE, пембролізумаб показав виражену протипухлинну активність у пацієнтів з НДРЛ та прийнятний профіль токсичності (як у режимі монотерапії, так і в комбінації з хіміотерапією).
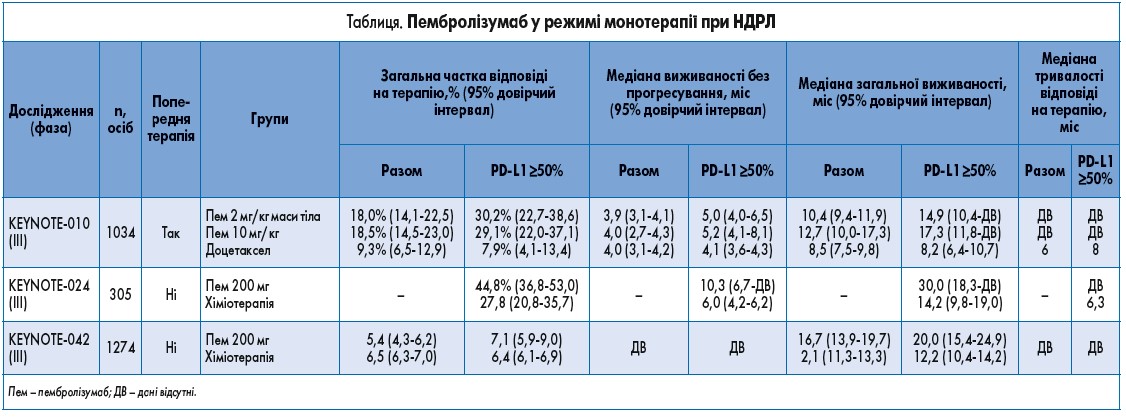
Монотерапія. Вивчення пембролізумабу як монотерапії при НДРЛ проводилось в рамках трьох досліджень III фази: KEYNOTE‑010, KEYNOTE‑024 та KEYNOTE‑042 (табл.). Дослідження III фази KEYNOTE‑010 дозволило затвердити пембролізумаб (2 мг/кг) як терапевтичну опцію для пацієнтів з поширеним НДРЛ, які вже отримували протипухлинне лікування. Загальна виживаність (ЗВ) була достовірно вищою при терапії пембролізумабом у дозі 2 мг/кг, ніж доцетакселом (відношення ризиків – ВР – 0,71; 95% довірчий інтервал – ДІ – 0,58‑0,88; p=0,0008), та при збільшенні дозування пембролізумабу до 10 мг/кг порівняно з доцетакселом (ВР 0,61; 95% ДІ 0,49-0,75; p <0,0001).
Зважаючи на істотну відмінність ефективності лікування пембролізумабом серед пацієнтів з експресією PD-L1 ≥50%, було проведено дослідження саме за участю цієї категорії хворих на НДРЛ – KEYNOTE‑024. Відмінність від попередніх досліджень полягала у призначенні пембролізумабу у монотерапії у першій лінії, яку порівнювали зі стандартним режимом хіміотерапії. Медіана виживаності без прогресування (ВБП) була достовірно вищою у групі пембролізумабу порівняно з групою хіміотерапії (ВР 0,50; 95% ДІ 0,37‑0,68; p <0,001). Перевага поширювалась у тому числі і на ЗВ як при первинному аналізі даних (ВР 0,60; 95% ДІ 0,41‑0,89; p=0,005), так і при його перегляді після більш тривалого спостереження (ВР 0,63; 95% ДІ 0,47‑0,86; p=0,002). Отриманий позитивний результат слугував підґрунтям для затвердження пембролізумабу (200 мг) як першої лінії терапії хворих на поширений НДРЛ при експресії PD‑L1 ≥50%. Результати дослідження KEYNOTE‑024 було підтверджено у дослідженні KEYNOTE‑042.
Хіміотерапія у комбінації з пембролізумабом. За відсутності специфічних мутацій, що можуть бути використані для призначення таргетної терапії, платиновмісні режими хіміотерапії є стандартом першої лінії лікування при НДРЛ. Зважаючи на те що пембролізумаб має прийнятний профіль токсичності, не вищий за токсичність стандартних режимів системної протипухлинної терапії, їх комбінація у першій лінії лікування може бути цілком обґрунтованою. Хіміотерапія чинить не лише прямий цитотоксичний вплив на пухлинні клітини, а й на імунну регуляцію шляхом дії на Т-клітини та індукує експресію PD-L1. Це дає підстави припускати наявність синергічної протипухлинної дії хіміотерапії у комбінації з пембролізумабом.
KEYNOTE‑189 – дослідження III фази, яке включало пацієнтів з неплоскоклітинним метастатичним НДРЛ. Хворі, які додатково до хіміотерапії отримували пембролізумаб, мали достовірно кращі показники ВБП (ВР 0,52; 95% ДІ 0,43-0,64; p <0,001) та 12-місячної виживаності (ВР 0,49; 95% ДІ 0,38-0,64; p <0,001). Позитивний вплив пембролізумабу на ЗВ був продемонстрований незалежно від рівня експресії PD-L1 (хоча певні переваги у хворих з експресією PD‑L1 ≥50% були зареєстровані). Це означає, що будь-які пацієнти з неплоскоклітинним НДРЛ можуть отримувати в першій лінії системну протипухлинну терапію в комбінації з пембролізумабом.
Терапевтичний ефект пембролізумабу у поєднанні з хіміотерапією у першій лінії у пацієнтів з плоскоклітинним метастатичним НДРЛ вивчали у дослідженні III фази KEYNOTE‑407. Як і у KEYNOTE‑189, подовження ВБП (ВР 0,56; 95% ДІ 0,45‑0,70; p <0,001) та ЗВ (ВР 0,64; 95% ДІ 0,49-0,85; p <0,001) відмічалось незалежно від рівня експресії PD‑L1.
Зважаючи на отримані результати, пембролізумаб у комбінації зі стандартними режимами хіміотерапії є схемою першої лінії лікування, якій має надаватись перевага у пацієнтів з метастатичним НДРЛ при рівні експресії PD-L1 <50%. Для хворих із рівнем експресії PD-L1 ≥50% поєднання хіміотерапії з пембролізумабом або монотерапія пембролізумабом є більш ефективними, ніж лише хіміотерапія. Наразі відсутні результати досліджень, у яких безпосередньо порівнювали б ці два варіанти лікування, тому вибір між ними має бути персоналізованим, здійснюватися з урахуванням потенційних ризиків і переваг для кожного конкретного пацієнта.
Метастатичне ураження головного мозку є характерним проявом поширеного НДРЛ, який розвивається у 25-40% хворих. Цей прояв НДРЛ зазвичай є протипоказанням для включення до більшості клінічних досліджень (у тому числі KEYNOTE). У одноцентровому дослідженні II фази вивчали роль пембролізумабу у лікуванні хворих з меланомою або НДРЛ, які мали вторинне ураження головного мозку. Включені пацієнти мали експресію PD-L1, не мали неврологічної симптоматики або не потребували терапії кортикостероїдами. З 18 хворих у групі НДРЛ у 4 було досягнуто повної ремісії, у 2 – часткової тривалої ремісії. Отримані дані є недостатніми для поширення такого терапевтичного підходу у клінічній практиці, тому роль пембролізумабу при НДРЛ з метастатичним ураженням головного мозку потребує подальших досліджень.
Пацієнти похилого віку. K. Nosaki та співавт. (2019) висвітлюють це питання на основі узагальненого аналізу результатів досліджень KEYNOTE‑010, KEYNOTE‑024 та KEYNOTE‑042. Загалом результат був аналогічним отриманим даним у більш молодих пацієнтів. Пембролізумаб не тільки покращує ЗВ хворих віком старше 75 років з поширеним НДРЛ порівняно з хіміотерапією, а також є більш безпечним. Вищу ефективність пембролізумабу у пацієнтів похилого віку отримано у разі експресії PD-L1 ≥50%.
Побічні явища. У більшості випадків побічні явища (ПЯ), пов’язані з застосуванням пембролізумабу, були нетяжкими. До них належали підвищена втомлюваність, зниження апетиту, висип, діарея, нудота. ПЯ 3-4 ступеня тяжкості спостерігали у 9,5‑26,6% хворих, які отримували пембролізумаб у монотерапії. Аналогічний показник при застосуванні хіміотерапії становив 35,0‑53,3%. Для пембролізумабу характерні специфічні ПЯ, які пов’язані з впливом на PD‑1/PD‑L1 та імунотерапією. Найбільш частими з них є гіпо- та гіпертиреоїдизм, пневмоніт, коліт, панкреатит, шкірні та інфузійні реакції. Імуноасоційовані ПЯ 3-4 ступеня тяжкості трапляються у менш ніж 2% хворих, летальні випадки – менше ніж у 1% (переважно внаслідок пневмоніту).
Пневмоніт – фокальне або дифузне запалення легеневої паренхіми без інфекційної складової. Приблизно у третини хворих немає жодних симптомів на момент діагностики пневмоніту (від 9 днів до 19 міс від початку лікування пембролізумабом), пацієнти можуть скаржитися на кашель та задишку.
Висновки. Застосування пембролізумабу дозволяє істотно покращити результати лікування пацієнтів з поширеним НДРЛ. Це особливо важливо для хворих, які не мають мутацій, що можуть піддаватись таргетній терапії. Предметом подальших досліджень залишаються питання доцільності застосування пембролізумабу з метою консолідації після хіміопроменевого лікування пацієнтів з ІІІ стадією НДРЛ, а також неоад’ювантного та ад’ювантного лікування при І-ІІІ стадії у пацієнтів, які є кандидатами на хірургічне втручання. Загалом пембролізумаб має прийнятний профіль токсичності, наявність специфічних ПЯ (у тому числі пневмоніту) слід враховувати при проведенні імунотерапії. Похилий вік не є протипоказанням до проведення імунотерапії. При виборі оптимальної схеми протипухлинного лікування слід враховувати низку особливостей (у тому числі супутню патологію, характеристики онкологічного процесу та вік).
Підготувала Олена Поступаленко
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 3 (64) 2020 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...