Тривога та дефіцит магнію: як зберегти емоційне здоров’я й імунітет під час пандемії
Тривожні розлади сьогодні є найпоширенішим нейропсихічним порушенням у країнах західного світу [1]. Із появою нової коронавірусної хвороби проблема тривожних розладів іще більше загострилася: пандемія COVID‑19 швидко та глибоко змінила кожен аспект повсякденного життя – від того, як люди працюють, відпочивають, спілкуються та здійснюють покупки в магазинах, до планів на майбутнє [2, 3]. Одним із внутрішніх факторів, які спричиняють розвиток тривожних розладів, є дефіцит магнію [4-6]. Важливо, що і тривога, і недостатні рівні магнію порушують здатність організму боротися з вірусною інфекцією.
Дефіцит магнію
Для розвитку тривожного розладу необхідний збіг певних внутрішніх і зовнішніх факторів, одним з яких, попри очевидну проблему переїдання в сучасному індустріалізованому та глобалізованому світі, є погане харчування [7]. Існують докази зв’язку між зміною рівнів мікронутрієнтів, включно з електролітами, та симптомами різноманітних психіатричних захворювань [8-10].
Магній (Mg) – це нутрієнт, життєво необхідний для здоров’я всього організму людини. З огляду на його участь у понад 300 біохімічних реакцій цілком можливо, що магній залучений у більшу кількість метаболічних процесів, аніж будь-який інший мінерал [11]. Дієта сучасної людини відійшла від зелених листових овочів до більш оброблених, бідних на мікронутрієнти продуктів, через що дефіцит магнію є поширеним явищем у багатьох регіонах світу. Приміром, нещодавнє дослідження в США показало, що недостатні рівні Mg спостерігаються в 68% американців [12].
Дефіцит Mg є потужним стресором, який підвищує чутливість організму до психологічного стресу та тривоги з подальшою активацією гіпоталамо-гіпофізарно-надниркової осі та симпатичної нервової системи [13]. Рівні магнію в центральній нервовій системі (ЦНС) є стабільнішими та знижуються повільніше, ніж в інших тканинах, але навіть невелике зниження Mg призводить до порушення нормального функціонування нейронів [14]. Недостатність магнію може проявлятися такими симптомами, як тривога, депресія, ажитація (рухове й емоційне збудження, що супроводжується відчуттям тривоги та страху), запаморочення, зниження уваги та безсоння [15-18].
З іншого боку, магній відіграє важливу роль у роботі імунної системи [19-22]. В експериментальних дослідженнях було встановлено, що дефіцит Mg супроводжується підвищенням рівнів субстанції Р та запальних цитокінів, передусім IL‑6 і TNF, зниженням активності поліморфноядерних клітин та апоптозом В-лімфоцитів [23-26].
Мутація гена магнієвого транспортера-1 (MAGT1) призводить до первинного імунодефіциту, відомого як XMEN-синдром (зчеплений з Х-хромосомою імунодефіцит із дефектом Mg2+, інфекцією вірусу Епштейна-Барр і неоплазіями) [27]. MAGT1 селективно транспортує іони Mg2+ всередину клітин, отож мутації MAGT1 супроводжуються зниженням внутрішньоклітинних рівнів магнію. У нещодавньому дослідженні за участю пацієнтів із XMEN-синдромом було встановлено, що внутрішньоклітинний вільний Mg2+ контролює експресію активувального рецептора NKG2D і тому є необхідним для реалізації цитотоксичної активності Т-лімфоцитів і натуральних кілерів. Призначення препаратів магнію пацієнтам із XMEN-синдромом супроводжувалося підвищенням внутрішньоклітинних рівнів вільного Mg2+, підвищенням експресії NKG2D і зниженням частки уражених вірусом клітин [28]. Отже, це дослідження показало, що адекватні рівні магнію необхідні для реалізації противірусного імунітету.
Тривога й імунітет
Виникнення тривоги – це універсальна психічна реакція людини на загрозу комфорту, благополуччю, здоров’ю та ін. Із цього погляду тривога може бути корисною – вона здатна мобілізувати людину на подолання дискомфорту, запобігання самій можливості будь-якої загрози, тобто виконує адаптаційну функцію. Надмірна за силою та/або тривалістю тривога набуває самостійного клінічного значення у вигляді різних порушень здоров’я [29]. У контексті пандемії нової коронавірусної хвороби суттєво зростає негативний вплив хронічної тривоги на стан імунітету.
Ще на початку нашої ери, приблизно у 200 році, Клавдій Гален спостерігав, що меланхолічні жінки (котрі мають підвищений рівень тривоги та стресу та, як наслідок, порушену імунну функцію) частіше хворіють на рак, аніж жінки з позитивнішим настроєм і меншим рівнем стресу [30]. У 1920-х роках було встановлено, що тривалий стрес і тривога підвищують ризик туберкульозу внаслідок пригнічення імунної системи, а в тих, хто вже захворів на туберкульоз, знижують активність фагоцитів [31]. У 1960-1980-х роках інші дослідники продемонстрували, що надмірна тривога підвищує ймовірність багатьох інфекційних і неінфекційних захворювань [32-34]. Дослідження останніх десятиліть підтвердили, що медіатори тривоги та стресу можуть проникати крізь гематоенцефалічний бар’єр і проявляти свої ефекти на імунну функцію [35-38].
На сьогодні двобічний зв’язок між ЦНС й імунною системою є добре відомим, існує навіть галузь медицини – психонейроімунологія, котра вивчає процеси функціональної взаємодії нервової системи організму людини та її психіки з різними відділами імунної системи [39]. Ці складні взаємодії опосередковуються ендокринною системою та включають продукцію гормонів стресу гіпоталамо-гіпофізарно-наднирковою та симпато-адренало-медулярною системами [40, 41].
В експериментальних і клінічних дослідженнях було продемонстровано, що тривалий стрес і тривога порушують здатність імунної системи реагувати на різні інфекційні агенти, наслідком чого може бути тяжча хвороба чи вищий ризик смерті від інфекції [41-45].
Цікаві результати надав нещодавній метааналіз понад 300 досліджень, у яких вивчався взаємозв’язок між психологічним стресом та імунною системою людини [46]. Було встановлено, що гострі стресори (тривалістю декілька хвилин) супроводжуються адаптивною активацією деяких параметрів вродженого імунітету та послабленням певних функцій специфічного імунітету. Короткі природні стресори (приміром, екзамени) пригнічують клітинний імунітет за збереження гуморального імунітету. І зрештою, хронічні стресори призводять до супресії обох ланок імунітету, при цьому що довшими є стрес і тривога, то більше компонентів імунної системи порушуються.
Дослідження, проведені після початку пандемії нової коронавірусної інфекції, підтверджують негативний вплив тривоги на імунну систему [47]. Встановлено, що хронічне надмірне занепокоєння через COVID‑19 діє як тригер так званої стерильної імунної відповіді, котра підвищує системне запалення до шкідливого рівня. У результаті пошкоджуються клітини власного організму з утворенням молекулярних патернів DAMP (damage associated molecular pattern). Інші молекулярні патерни, PAMP (pathogen associated molecular pattern), є характерними для патогенних мікроорганізмів. PAMP і DAMP часто розпізнаються одними й тими самими патерн-розпізнавальними рецепторами (наприклад, TLR‑4), що призводить до подібних молекулярних і функціональних наслідків. Отже, при інфікуванні SARS-CoV‑2 людини, котра перебуває під впливом хронічного стресу, імунна система вже реагує на DAMP, що, з одного боку, послаблює специфічну імунну відповідь на коронавірусні PAMP, а з іншого – спричиняє надмірну системну запальну реакцію, так званий цитокіновий шторм. Останній вважається провідною причиною тяжкого перебігу COVID‑19 та асоційованої летальності [48].
Лікування тривожних розладів
Для лікування тривожних розладів часто використовують анксіолітики (так звані малі транквілізатори; зазвичай бензодіазепіни) й антидепресанти (селективні інгібітори зворотного захоплення серотоніну – СІЗЗС, трициклічні, мультимодальні антидепресанти тощо) [49]. Ці препарати мають широкий спектр побічних ефектів; багато з них можуть зумовити залежність і повернення симптомів у разі відміни [50, 51]. До того ж занепокоєння викликають результати останніх досліджень, які свідчать про підвищений ризик тяжких ускладнень і навіть смерті при застосуванні зазначених засобів.
Систематичний огляд і метааналіз 25 досліджень (понад 2 млн пацієнтів) показав, що застосування анксіолітиків асоціюється з підвищенням ризику смерті від будь-яких причин на 43-60% [50]. В іншому метааналізі, що охопив 16 досліджень і 375 тис. пацієнтів, було встановлено, що антидепресанти підвищують ризик передчасної смерті на 33% та на 14% збільшують ризик інсульту чи інфаркту міокарда [51]. При цьому не було різниці між трициклічними антидепресантами та сучаснішими СІЗЗС. На думку дослідників, це може пояснюватися впливом згаданих препаратів на нейротрансмітери поза ЦНС. Наприклад, серотонін бере участь у таких критично важливих процесах, як ріст, травлення й імунна відповідь, тому порушення рівнів серотоніну може мати широкі негативні ефекти на здоров’я [52].
Безпечною альтернативою традиційним анксіолітикам та антидепресантам є пероральні препарати магнію. У неврології та психіатрії магній використовують для корекції метаболічних порушень і як заспокійливий засіб, зокрема для лікування тривоги [53-57].
Механізми, за допомогою яких магній полегшує тривожні розлади й запобігає панічним атакам, включають зниження активності з’єднаних із рецепторами NMDA (N-метил-D-аспартату) кальцієвих каналів, зменшення пресинаптичного вивільнення адреналіну й норадреналіну в ЦНС, підвищення концентрації гамма-аміномасляної кислоти (ГАМК) у певних ділянках головного мозку, модуляцію вивільнення глутамату на пресинаптичному рівні [58-60].
Клінічний досвід застосування перорального магнію (в монотерапії чи в комбінації з іншими компонентами) в лікуванні тривожних розладів узагальнений у систематичному огляді, що включив 18 досліджень [61]. У пацієнтів із легкою чи помірною тривогою препарати магнію, призначені на період від 4 до 12 тиж, значно зменшували параметри тривоги порівняно з плацебо й забезпечували таку саму ефективність, як і «тяжкі» лікарські засоби з доведеною анксіолітичною дією – лоразепам і буспірон. Препарати магнію також були ефективними в пацієнтів із тривогою різного ступеня, асоційованою з передменструальним синдромом й артеріальною гіпертензією. Автори зазначають, що в дослідженнях препаратів магнію з додатковими компонентами (наприклад, вітаміном В6, екстрактами глоду чи каліфорнійського маку) не вивчалися ефекти окремих компонентів, тому неможливо розрізнити відносний вклад кожного компонента або підтвердити, чи є позитивні ефекти адитивними або синергічними [61].
Відмінності препаратів магнію
 Через визнання важливої ролі магнію в підтриманні доброго загального стану здоров’я, профілактиці й лікуванні цілої низки захворювань препарати та дієтичні добавки з магнієм сьогодні дуже популярні. Приміром, опитування в Нідерландах показало, що такі засоби застосовують 7% населення країни й до 25% осіб, які займаються спортом [62].
Через визнання важливої ролі магнію в підтриманні доброго загального стану здоров’я, профілактиці й лікуванні цілої низки захворювань препарати та дієтичні добавки з магнієм сьогодні дуже популярні. Приміром, опитування в Нідерландах показало, що такі засоби застосовують 7% населення країни й до 25% осіб, які займаються спортом [62].
Препарати магнію, присутні на сучасному фармринку, містять одне з двох джерел елементарного Mg: неорганічні або органічні солі магнію. Неорганічні солі (наприклад, магнію оксид) містять велику кількість елементарного Mg, але мають дуже обмежену біодоступність. У разі застосування таких препаратів у кров всмоктується незначна частина Mg, при цьому надлишок магнію, що залишається в кишечнику, може порушувати абсорбцію інших нутрієнтів, зокрема кальцію, та спричиняти диспепсію. З іншого боку, органічні солі магнію (приміром, магнію оротат) містять відносно меншу кількість елементарного Mg, але мають вищу розчинність, кращу біодоступність і забезпечують вищі сироваткові рівні магнію порівняно з неорганічними солями.
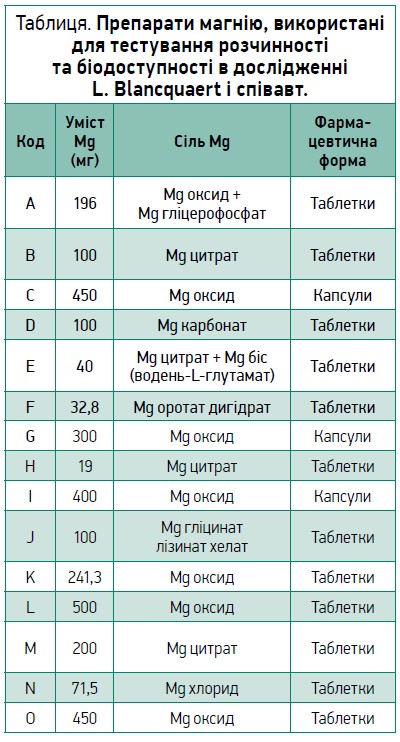
Погана розчинність і біодоступність можуть призводити до субоптимальної ефективності та/або підвищення частоти небажаних явищ. З огляду на це цікавими є результати нещодавнього дослідження, проведеного вченими з Гентського університету (Бельгія) [63]. Дослідники протестували 15 комерційно доступних препаратів магнію (табл.). Спочатку вони використали модель, яка симулює різні умови шлунково-кишкового тракту, щоб порівняти розчинність та абсорбцію. Результати показали значні відмінності між препаратами магнію. Найвищий ступінь абсорбції продемонстрував препарат F (Магнерот® виробництва Woerwag Pharma, Німеччина), що містить органічний оротат магнію, – його біодоступність досягала 85-90% (рис.). Щодо препаратів неорганічного магнію, їхня біодоступність не перевищувала 30%, а в найгіршому випадку становила лише 4%. Отже, сіль магнію відіграє велику роль у тому, наскільки добре цей мінерал всмоктується з кишечнику в кровоток.
Потім дослідники протестували два препарати магнію в здорових добровольців – чоловіків і жінок, щоб перевірити, чи є результати, отримані за допомогою симуляційної моделі, дійсними для організму людини. Виявилося, що препарат неорганічної солі, котрий показав погану біодоступність на моделі, так само значно менше підвищував сироваткову концентрацію Mg, ніж препарат із високою біодоступністю. При цьому навіть дуже висока концентрація магнію в першому випадку не змогла компенсувати наслідки низької біодоступності неорганічної солі Mg. Отже, не можна говорити про класовий ефект магнійумісних препаратів, оскільки лише сполуки з високою біодоступністю дають змогу ефективно компенсувати дефіцит Mg при застосуванні нижчих доз. Нижча доза магнію означає кращу переносимість, оскільки надлишок Mg у кишечнику може призводити до побічних ефектів. За рекомендаціями німецького Федерального інституту оцінки ризиків (BfR), максимальна добова кількість магнію становить 250 мг, розділені на два прийоми. Відповідну дозу, котра добре переноситься, містить Магнерот® [64]. У цьому лікарському засобі, що відпускається без рецепта, Mg поєднаний з органічною речовиною – оротовою кислотою, котра, як і магній, відіграє важливу роль в енергетичному обміні.
Ключові висновки
- Тривога – дуже поширене нейропсихічне порушення; додатковим фактором збільшення випадків тривожних розладів стала пандемія нової коронавірусної хвороби.
- Хронічна тривога, зокрема пов’язана з надмірним занепокоєнням через COVID‑19, порушує нормальну роботу імунної системи, що може призводити до підвищення ризику інфікування та тяжчого перебігу інфекційних захворювань.
- Одним із факторів, який зменшує стійкість організму до стресу, спричиняє розвиток і хронізацію тривоги, є дефіцит магнію, присутній у кожного другого дорослого.
- Магній також відіграє важливу роль у роботі імунної системи; адекватні внутрішньоклітинні рівні Mg2+ необхідні для реалізації противірусної імунної відповіді.
- Традиційні лікарські засоби для лікування тривоги, як-от анксіолітики й антидепресанти, мають широкий спектр побічних ефектів, можуть підвищувати ризик судинних подій і смерті, порушувати імунну відповідь.
- Пероральна терапія препаратами магнію є безпечною, ефективно зменшує симптоми тривоги та пов’язаних порушень, підтримує нормальне функціонування імунної системи.
- Обираючи препарат магнію для лікування тривожних розладів, перевагу слід віддавати органічним солям з огляду на їхню високу біодоступність, яка дає змогу досягти адекватних сироваткових рівнів Mg без надлишкових концентрацій Mg у кишечнику.
- Для лікування тривоги пероральні препарати магнію рекомендовано призначати тривалістю не менш як 4 тиж у добовій дозі до 250 мг елементарного Mg (наприклад, магнію оротат – по 2 таблетки 500 мг 3 рази на добу, що відповідає 196,8 мг елементарного Mg).
Список літератури див. на сайті health-ua.com.
Підготував Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 16 (485), 2020 р.
СТАТТІ ЗА ТЕМОЮ Неврологія
Стрес і тривожність чинять потужний несприятливий вплив і на самопочуття окремих індивідуумів, і на загальний стан здоров’я всієї популяції світу. Цей несприятливий вплив значно підсилили пандемія COVID‑19 та війна в Україні (Celuch M. et al., 2023)....
16-17 лютого в Києві відбувся науково-практичний майстер-клас «Хронічний стрес сьогодення: обрані запитання про здоров’я жінки в різні вікові періоди». Під час заходу виступили фахівці різних спеціальностей, було обговорено важливі аспекти жіночого здоров’я як психологічного, так і фізичного. Доповіді присвячувалися різноманітним питанням, зокрема репродуктивним проблемам, онкологічним захворюванням, психосоматичним розладам. Під час події виступила засновниця Академії довголіття Dr. Skytalinska, віцепрезидент Асоціації дієтологів України, лікар-дієтолог Оксана Василівна Скиталінська. Доповідь Оксани Василівни була присвячена впливу тривалого стресу на харчування та пов’язані з цим наслідки для здоров’я жінок. Окрім пояснення механізмів негативного впливу стресу, під час доповіді лікарка також надала важливі практичні рекомендації стосовно здорового харчування....
Події останніх 5 років є неабияким викликом для психічного стану кожного українця: спочатку – пандемія коронавірусу та запроваджені через неї карантинні обмеження, а далі – повномасштабне російське вторгнення, що триває уже понад 2 роки. Все це спричиняє погіршення психічного здоров’я населення. Такі надзвичайні ситуації, що характеризуються загрозою з невизначеною тривалістю, створюють масивне стресове навантаження, яке підсилюється відчуттям самотності та відчуженості, підвищують тривожність, а також є підґрунтям розвитку психічних розладів. Відомо, що ці стани порушують розумову діяльність, тобто перешкоджають концентрації та аналізу інформації. ...
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....





