Вплив цитопротектора Антраль® на оксидантно-антиоксидантний гомеостаз у хворих на хронічний панкреатит
 Проблема лікування та реабілітації хворих на хронічний панкреатит (ХП) є надзвичайно актуальною в сучасній гастроентерології, оскільки кількість хворих на ХП продовжує зростати [1-4]. Вплив кількох етіологічних чинників (зловживання алкоголем, хронічна запальна патологія гепатобіліарної системи, постхолецистектомічний синдром, автоімунні, хронічні вірусні гепатити В, С, токсичні, медикаментозні впливи, гіперліпідемія, ішемія підшлункової залози (ПЗ) тощо) в комбінації з несприятливими ефектами факторів ризику ХП (зловживання екстрактивними, жирними, смаженими стравами, солодкими газованими напоями, продуктами з умістом шкідливих консервантів; нераціональне харчування з виключенням білків тваринного походження, молока; куріння тютюну тощо) спричиняє часті загострення ХП, його прогресивний перебіг із формуванням зовнішньосекреторної недостатності (ЗСН) ПЗ, мальдигестії, мальабсорбції, порушення всіх видів обміну, зниження нутритивного забезпечення організму та трофологічної недостатності [1-7].
Проблема лікування та реабілітації хворих на хронічний панкреатит (ХП) є надзвичайно актуальною в сучасній гастроентерології, оскільки кількість хворих на ХП продовжує зростати [1-4]. Вплив кількох етіологічних чинників (зловживання алкоголем, хронічна запальна патологія гепатобіліарної системи, постхолецистектомічний синдром, автоімунні, хронічні вірусні гепатити В, С, токсичні, медикаментозні впливи, гіперліпідемія, ішемія підшлункової залози (ПЗ) тощо) в комбінації з несприятливими ефектами факторів ризику ХП (зловживання екстрактивними, жирними, смаженими стравами, солодкими газованими напоями, продуктами з умістом шкідливих консервантів; нераціональне харчування з виключенням білків тваринного походження, молока; куріння тютюну тощо) спричиняє часті загострення ХП, його прогресивний перебіг із формуванням зовнішньосекреторної недостатності (ЗСН) ПЗ, мальдигестії, мальабсорбції, порушення всіх видів обміну, зниження нутритивного забезпечення організму та трофологічної недостатності [1-7].
Аналіз результатів досліджень різних ланок патогенезу ХП, проведених вітчизняними та закордонними вченими, вказує на істотну роль порушення оксидантно-антиоксидантного гомеостазу (ОАГ) з активацією оксидативного (ОС) і нітрозитивного стресу (НС) на тлі дефіциту природних антиоксидантів й агентів детоксикації [1, 2, 5-9], які є універсальним механізмом ушкодження клітинних мембран, прискорення апоптозу панкреатоцитів, їх цитолізу, гальмування процесів репарації й активації фіброзування ПЗ [1-4]. Саме тому логічним для корекції ОАГ, на нашу думку, було би внесення до протоколу лікування хворих на ХП препаратів антиоксидантної дії. Одним із препаратів вітчизняного виробництва, що чинить потужний антиоксидантний ефект, є Антраль® – універсальний цитопротектор із мембраностабілізувальною, антиоксидантною, протизапальною й імуномодулювальною дією, котрий широко апробований у клініці гастроентерології та гепатології [1, 10-12]. Антраль® є комплексною сполукою алюмінію з мефенаміновою кислотою (похідна антранілової кислоти), що забезпечує вищезазначені властивості препарату [1]. Водночас Антраль® не має жовчогінної дії, що дає змогу призначати його пацієнтам із загостренням ХП. Робочою гіпотезою нашого дослідження є досягнення балансу чинників природної системи антиоксидантного захисту (АОЗ) під впливом препарату Антраль® і зниження інтенсивності ОС і НС, що, ймовірно, зумовить швидше настання клінічної ремісії ХП.
Мета цього дослідження – встановити ефективність впливу препарату Антраль® у лікуванні ХП у фазі загострення на підставі комплексної оцінки клінічного перебігу ХП та ОАГ.
Матеріал і методи
Обстежено 52 пацієнти з ХП змішаної етіології у фазі загострення середньої тяжкості. Для визначення ефективності лікування за випадковою ознакою сформовано 2 репрезентативні групи учасників. Середній вік хворих дорівнював 41,3±4,5 року. Групу порівняння становили 30 практично здорових осіб відповідного віку та статі. Перша група (група 1 – контрольна, 24 особи) отримувала адаптовану дієту № 5П, розчин для інфузій, який впливає на електролітний баланс, 400 мл внутрішньовенно № 5, рабепразол (20 мг 2 р/добу), платифіліну гідротартрат 0,2% 1 мл підшкірно № 10, поліферментний (20 тис. ОД 2 р/добу) препарат упродовж 10 днів у стаціонарі. На амбулаторному етапі пацієнти отримували антисекреторний засіб (рабепразол), спазмолітичний (мебеверину гідрохлорид) і поліферментний препарати впродовж 20 днів. Основна група (група 2, n=28), окрім вищезазначеної терапії, отримувала Антраль® (ПАТ «Фармак», м. Київ) по 1 таблетці (200 мг) 3 р/добу впродовж 30 днів.
Діагноз ХП встановлювали на підставі скарг, анамнестичних даних, результатів клінічних, лабораторних та інструментальних досліджень згідно з наказом МОЗ України № 271 від 13.06.2005, який був оновлений наказом МОЗ України № 638 від 10.09.2014. Для класифікації та рубрикації випадків ХП використовувалася Міжнародна статистична класифікація хвороб і причин смерті 10-го перегляду (К 86.1. Хронічний панкреатит). Дизайн дослідження передбачав клінічні, лабораторні, біохімічні дослідження крові (активність α-амілази в крові), імуноферментні методи (ІФА) (аналіз калу на вміст еластази‑1), біохімічний аналіз дуоденального вмісту (активність ферментів ПЗ), копрограму, ультрасонографію (УСГ) ПЗ. Аналіз клінічних та УСГ-проявів ХП, біохімічних (α-амілаза крові), лабораторних показників функціонального стану ПЗ проводили за загальноприйнятими методиками, що досліджували в динаміці через 30 днів лікування. Комплексне УСГ-дослідження здійснювали на ультразвуковому сканері AU‑4 Idea (Biomedica, Італія) конвексним датчиком із частотою 3,5 МГц, уміст С-реактивного протеїну (СРП) у сироватці крові – латексним методом за допомогою набору «НВЛ Гранум» (Україна). У хворих вивчали показники фекальної панкреатичної еластази‑1 методом ІФА на імуноферментному аналізаторі Labsystems Multiskan MS (Нідерланди).
Концентрацію в крові молекулярних продуктів пероксидного окиснення ліпідів (ПОЛ) ізольованих подвійних зв’язків (ІПЗ) у сполуках, дію нових кон’югатів вивчали за І.А. Волчегорським і співавт., малонового альдегіду у плазмі крові й еритроцитах (МА ер) – за Ю.А. Владимировим, А.І. Арчаковим. Інтенсивність окиснювальної модифікації білків (ОМБ) визначали за вмістом у сироватці крові альдегід- і кетондинітрофенілгідразонів основного (АКДНФГ ОХ) і нейтрального характеру за методом О.Є. Дубініної, І.Ф. Мещишина (1998). Уміст у крові метаболітів NO (нітритів/нітратів) вивчали за методикою L.C. Green і співавт. Уміст у крові глутатіону відновленого (ГВ) визначали титраційним методом за О.В. Травіною в модифікації І.Ф. Мещишина, І.В. Петрової. Активність ферменту системи АОЗ каталази вивчали за методом М.А. Королюк і співавт.
Перед перевіркою статистичних гіпотез проведено аналіз нормальності розподілу величин у рандомізованих вибірках через визначення коефіцієнтів асиметрії та ексцесу за допомогою критерію Хана-Шапіро-Уїлкі. Вірогідність змін варіацій у динаміці лікування в разі нормального розподілу у вибірках визначали за парним критерієм Стьюдента, в інших випадках – за непараметричним парним Т-критерієм Вілкоксона. Для виявлення ефективності застосування Антралю використовували методику розрахунку показника відношення шансів (ВШ) і визначення його 95% довірчого інтервалу (ДІ). Математичну обробку отриманих даних проводили на комп’ютері на базі процесора AMD Athlon 64 за допомогою програми Primer of Biostatistics. Version 4.03.
Результати й обговорення
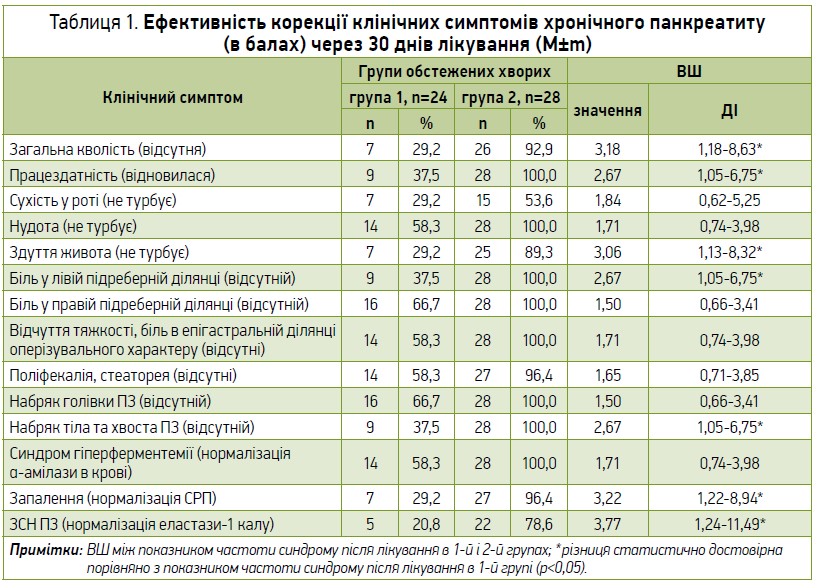
Аналіз впливу терапії, запропонованої хворим на ХП (група 2), на перебіг захворювання порівняно з 1-ю групою показує (табл. 1), що через місяць від початку терапії прояви астеновегетативного синдрому (загальна кволість, нездужання, зниження фізичної працездатності) були усунуті в більшості хворих – 26 осіб (92,9%) 2-ї групи, тоді як у 1-й групі ці симптоми зберігалися в 17 хворих (70,8%) (ВШ 3,18; 95% ДІ 1,18-8,63). У всіх пацієнтів 2-ї групи (100,0%) після лікування зникли біль і відчуття тяжкості в епігастральній ділянці (проти 14 (58,3%) у 1-й групі) (ВШ 1,71; 95% ДІ 0,74-3,98), біль у лівій підреберній ділянці (100,0% проти 37,5%) (ВШ 2,67; 95% ДІ 1,05-6,75), біль у правій підреберній ділянці (100,0% проти 66,7%) (ВШ 1,50; 95% ДІ 0,66-3,41), а також практично не турбувала нудота (у 28 хворих (100,0%) проти 14 (58,3%) відповідно в 1-й групі) (ВШ 1,71; 95% ДІ 0,74-3,98).
Прояви диспепсичного синдрому (сухість у роті, здуття живота) суб’єктивно зменшилися в більшої кількості хворих 2-ї групи, що відрізнялося від показника в 1-й групі в 1,8 раза (ВШ 1,84; 95% ДІ 0,62-5,25) і 3,1 раза (ВШ 3,06; 95% ДІ 1,13-8,32) відповідно (р<0,05). Позитивним проявом ефективності лікування було відновлення фізичної працездатності в 100,0% пацієнтів 2-ї групи проти 37,5% хворих 1-ї групи (ВШ 2,67; 95% ДІ 1,05-6,75), що можна пояснити протизапальними та дезінтоксикаційними ефектами Антралю.
УСГ-показники розмірів ПЗ також змінилися нерівнозначно: у хворих 2-ї групи в 100,0% пацієнтів усунуто набряк ПЗ у ділянці як голівки, так і тіла та хвоста ПЗ, тоді як у хворих 1-ї групи зберігалися набряк і збільшення голівки ПЗ у 8 осіб (33,3%) (ВШ 1,50; 95% ДІ 0,66-3,41), а в 15 осіб (62,5%) залишався набряк тіла та хвоста ПЗ (ВШ 2,67; 95% ДІ 1,05-6,75; р<0,05). За інтенсивністю зменшення запального набряку хвоста ПЗ у групах порівняння результат лікування в пацієнтів 2-ї групи перевищував показник в осіб 1-ї групи у 2,7 раза (р<0,05). Отже, Антраль® має потужні протизапальні, протинабрякові, модифікувальні властивості щодо структури ПЗ відносно зменшення її запальної інфільтрації, що потенціює вплив традиційної терапії ХП.
Активність α-амілази в крові на тлі встановленої до лікування гіперферментемії у фазі загострення ХП після 30 днів лікування істотно знизилася в обох групах спостереження, однак у 2-й групі синдром відхилення ферментів у кров був усунутий у 100,0% осіб, тоді як у 1-й групі – лише в 58,3% (ВШ 1,71; 95% ДІ 0,74-3,98). Показник активності запального синдрому у хворих на ХП (уміст у крові СРП) вказує на його усунення після лікування в 96,4% пацієнтів 2-ї групи проти 29,2% хворих 1-ї групи (ВШ 3,22; 95% ДІ 1,22-8,94; р<0,05). Цей факт свідчить про достовірний протизапальний ефект терапії, підсиленої додаванням Антралю впродовж місяця.
Аналіз умісту фекальної еластази‑1 у хворих на ХП на 30-й день лікування вказує на достовірне зростання показника лише в 2-й групі з відновленням секреторної здатності ПЗ у 78,6% проти 20,8% хворих 1-ї групи (ВШ 3,77; 95% ДІ 1,24-11,49), що можна пояснити потужними протизапальними та регенераторними властивостями Антралю [1, 4, 5, 7].
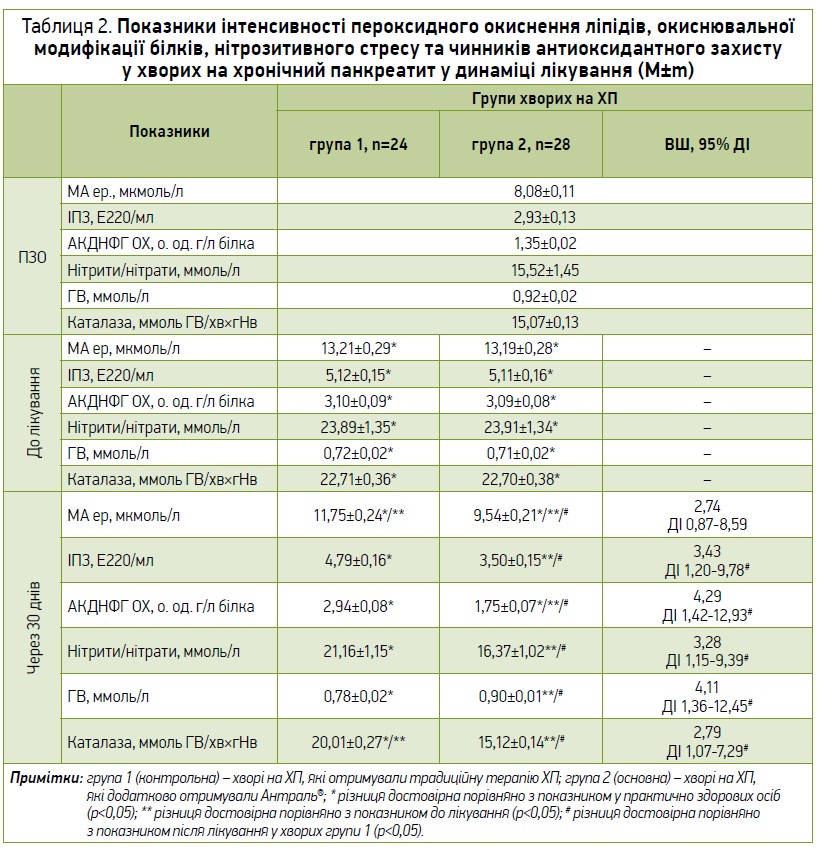
До лікування у хворих із загостренням ХП встановлено істотне зростання інтенсивності ОС за зростанням умісту в крові проміжних і кінцевих продуктів ПОЛ: МА ер – у 1,6 раза, ІПЗ – у 1,7 раза порівняно з показником у ПЗО (р<0,05). Зважаючи на той факт, що до терапії хворих 1-ї групи не були включені препарати антиоксидантної дії, динамічні показники інтенсивності ПОЛ та ОМБ достовірно відрізнялися від вихідних переважно в 2-й групі спостереження (табл. 2). Так, уміст МА ер після лікування в 1-й групі знизився на 10,9% (р<0,05), у 2-й групі – на 27,7% (р<0,05) із наявністю достовірної різниці з 1-ю групою (р<0,05), проте нормативних показників не досяг. Обчислення за теорією ВШ імовірності досягнення нормативних показників хворими 2-ї групи внаслідок лікування Антралем вказує на вищу ймовірність (ВШ 2,74; 95% ДІ 0,87-8,59). Для підвищення шансу нормалізації вмісту МА ер у хворих на ХП за допомогою Антралю потрібно продовжити курс лікування.
Концентрація ІПЗ після лікування в 1-й групі мала лише тенденцію до зниження (р>0,05), а в 2-й групі знизилася в 1,5 раза (р<0,05) з наявністю достовірної різниці з 1-ю групою (р<0,05) та з досягненням нормативних показників. Шанс досягнення нормативних показників умісту ІПЗ хворими 2-ї групи впродовж місяця лікування Антралем істотно перевищує такий у пацієнтів 1-ї групи (ВШ 3,43; 95% ДІ 1,20-9,78; р<0,05).
До лікування у хворих на ХП у фазі загострення встановлено достовірне підвищення інтенсивності ОМБ за зростанням показника вмісту в крові АКДНФГ ОХ у 2,3 раза (р<0,05). Водночас найвища ефективність впливу терапії, що містить Антраль®, встановлена щодо корекції процесів ОМБ у хворих на ХП, де зниження вмісту в крові АКДНФГ ОХ після лікування становило 1,8 раза (р<0,05) порівняно з показником до лікування з нормалізацією показників (р>0,05). У 1-й групі зниження вмісту в крові карбонільних похідних у динаміці лікування було недостовірним і нормативних значень не досягало. Шанс досягнення нормативних показників вмісту АКДНФГ ОХ хворими 2-ї групи впродовж місяця істотно перевищував такий у хворих 1-ї групи (ВШ 4,29; 95% ДІ 1,42-12,93; р<0,05), що вказує на доцільність призначення Антралю в терапії загострення ХП.
Уміст у крові токсичних метаболітів NO (нітритів/нітратів), надлишок яких був встановлений до лікування у хворих на ХП, після лікування в 1-й групі мав лише тенденцію до зниження (р>0,05), а в 2-й групі знизився в 1,5 раза (р<0,05) з наявністю достовірної різниці з 1-ю групою (р<0,05) та з досягненням нормативних показників у 2-й групі. Шанс досягнення нормативних показників умісту нітритів/нітратів хворими 2-ї групи впродовж місяця лікування Антралем, а отже, й подолання ушкоджувального впливу НС істотно перевищує такий у хворих 1-ї групи (ВШ 3,28; 95% ДІ 1,15-9,39; р<0,05).
Аналіз показників АОЗ до лікування у хворих на ХП вказує на істотний дефіцит умісту в крові ГВ – важливого чинника АОЗ і природної системи детоксикації. Антиоксидантні властивості Антралю зумовили його здатність заміщувати дефіцит і підсилювати ефекти ГВ цих осіб. Дійсно, динамічні показники вмісту ГВ змінювалися достовірно у хворих 2-ї групи – на момент завершення лікування вміст ГВ зріс достовірно в 1,3 раза (р<0,05) та було досягнуто фактичної нормалізації показника. У хворих 1-ї групи вміст ГВ у крові змінювався недостовірно (р>0,05). Шанс досягнення нормативних показників умісту ГВ хворими 2-ї групи впродовж місяця лікування Антралем, а отже, й подолання ушкоджувального впливу ОС і НС істотно перевищує такий у хворих 1-ї групи (ВШ 4,11; 95% ДІ 1,36-12,45; р<0,05).
Водночас активність каталази, котра до лікування у хворих на ХП була компенсаторно підвищеною в 1,5 раза (р<0,05), після лікування в обох групах порівняння достовірно знизилася: в 1-й групі – на 11,5%, а в 2-й групі – на 29,0% із нормалізацією показника в 2-й групі порівняння (р>0,05). Обчислення шансу досягнення нормативних показників активності каталази хворими 2-ї групи впродовж місяця лікування Антралем істотно перевищує відповідний показник у хворих 1-ї групи (ВШ 2,79; 95% ДІ 1,07-7,29; р<0,05).
Отже, запропонована комплексна терапія з додаванням Антралю виявила вищий ступінь ефективності в досягненні антиоксидантного ефекту, що дало змогу знизити інтенсивність процесів ПОЛ та ОМБ, НС, які є ключовою ланкою патогенезу загострення ХП.
Висновки
- У хворих на ХП до лікування встановлено значну інтенсивність ОС зі зростанням умісту в крові проміжних і кінцевих продуктів ПОЛ (у 1,6-1,7 раза; р<0,05), ОМБ (у 2,3 раза; р<0,05), індукції НС (у 1,5 раза; р<0,05), які виникли на тлі істотного дефіциту в крові ГВ (зменшення в 1,3 раза; р<0,05) і супроводжувалися компенсаторним напруженням активності каталази (зростання в 1,5 раза; р<0,05).
- Призначення Антралю на тлі комплексної терапії загострення ХП упродовж 30 днів зумовило істотну корекцію ОАГ у хворих на ХП із достовірним зниженням умісту в крові МА (в 1,3 раза; р<0,05), ІПЗ (у 1,5 раза; р<0,05), АКДНФГ ОХ (в 1,8 раза; р<0,05), нітритів/нітратів (у 1,5 раза; р<0,05) завдяки достовірному зростанню й нормалізації вмісту в еритроцитах ГВ (у 1,3 раза; р<0,05), нормалізації активності каталази, що супроводжувалося достовірним усуненням клінічних проявів загострення ХП: астеновегетативного синдрому (ВШ 3,18; 95% ДІ 1,18-8,63), болю в лівій підреберній ділянці (ВШ 2,67; 95% ДІ 1,05-6,75), здуття живота (ВШ 3,06; 95% ДІ 1,13-8,32; р<0,05), запального набряку ПЗ (ВШ 2,67; 95% ДІ 1,05-6,75), синдрому гіперферментемії, запального синдрому (ВШ 3,22; 95% ДІ 1,22-8,94) та підвищенням екзокринної функції ПЗ (ВШ 3,77; 95% ДІ 1,24-11,49; р<0,05).
Перспективою подальших досліджень у цьому напрямі є дослідження впливу препарату Антраль® на стан чинників протеїназо-інгібіторної системи, інтенсивність колагенолізу й ендогенної інтоксикації в динаміці лікування хворих на ХП у фазі загострення.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 16 (485), 2020 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...