Вплив комбінації розувастатину та езетимібу на атеросклеротичну бляшку у пацієнтів з ішемічною хворобою серця
Атеросклероз – складний хронічний процес, в основі якого лежать надмірна запальна відповідь та накопичення ліпідів. На сьогодні існують три основні підходи до ведення осіб з атеросклеротичною ішемічною хворобою серця (ІХС): медикаментозне лікування, черезшкірне коронарне втручання (ЧКВ) та аортокоронарне шунтування (АКШ). X. Wang et al. провели дослідження з метою вивчення ефективності поєднання езетимібу зі статинами, зокрема розувастатином, у пацієнтів з атеросклеротичною ІХС. Автори проаналізували вплив потужної ліпідознижувальної терапії на ураження коронарних артерій та фактори й можливі механізми запалення. Отримані результати опубліковані в журналі Heart, Lung and Circulation (2016; 25: 459‑465).
Приблизно 80% летальних випадків через серцево-судинні захворювання (ССЗ) пов’язані з атеросклеротичною ІХС (Libby et al., 2011). Фармакотерапія є ключовою стратегією для всіх осіб з ІХС, зокрема пацієнтів з пограничними ураженнями коронарного русла, вираженим стенозом коронарної артерії, які не можуть чи не бажають проходити ЧКВ та/або АКШ. Статини здатні ефективно стабілізувати або зменшити бляшку шляхом зниження рівня ліпідів у крові, покращити прогноз, скоротити захворюваність і смертність серед хворих (Schwartz et al., 2001). Однак деякі пацієнти погано відповідають на ці препарати навіть у максимальних дозах. У таких випадках необхідно комбінувати статини з іншими гіполіпідемічними засобами.
У дослідженні X. Wang et al. пацієнтам із пограничними ураженнями коронарного русла та/або тяжкою атеросклеротичною ІХС у поєднанні з гіперліпідемією, які не могли чи не хотіли проходити ЧКВ або АКШ, призначали комбінацію розувастатину та езетимібу чи лише розувастатин. Внутрішньосудинне ультразвукове дослідження (ВУЗД) і віртуальну гістологію використовували для визначення розміру коронарної бляшки та змін її клітинного складу до й після лікування.
Матеріали й методи дослідження
Вибірка пацієнтів
У дослідження було включено 106 пацієнтів (168 уражень) відділення кардіології з 2011 по 2014 рр. Критеріями включення були: виявлення шляхом проведення коронароангіографії (КА) одного чи більше атеросклеротичних уражень коронарної артерії (пограничних та/або тяжких), загальний ХС ≥5,2 ммоль/л та/або ХС ліпопротеїнів низької щільності (ЛПНЩ) ≥3,6 ммоль/л. Пограничний стеноз становив 40‑70%, тяжкий – понад 75%, виявлені за допомогою кількісної КА. Критерії виключення: протипоказання до втручання чи призначення статинів (наприклад, активний гепатит), високий рівень трансаміназ (більш ніж двократне перевищення норми).
Пацієнти були рандомним чином розподілені на дві групи лікування:
- перша група отримувала розувастатин 10 мг та езетиміб 10 мг (n=55);
- друга група отримувала розувастатин 10 мг (n=51).
Суттєвих відмінностей у базових характеристиках між двома досліджуваними групами не виявлено (р>0,05). Основними кінцевими точками випробування були новий або повторний інфаркт міокарда (ІМ), нестабільна стенокардія, кардіальна смерть, інсульт.
Обстеження та процедури
Рівень ліпідів у крові, високочутливий С-реактивний білок (вчСРБ), інтерлейкін‑6 (ІЛ‑6) та матриксну металопротеїназу 9 (MMP‑9) вимірювали до лікування, через 1, 6 і 12 місяців після нього. КА та ВУЗД проводили повторно через 12 місяців після терапії. Пацієнти підписали інформовану згоду на добровільну участь у дослідженні, інтервенційне обстеження та лікування (включно із ВУЗД).
Рівень загального ХС, тригліцеридів (ТГ), ХС ліпопротеїнів високої щільності (ЛПВЩ) та ЛПНЩ у сироватці крові вимірювали стандартними ферментативними методами, вчСРБ – імунотурбідиметричним. ІЛ‑6 та ММР‑9 визначали за допомогою імуноферментного аналізу ELISA. КА проводили через доступ до променевої артерії, за неможливості – правої стегнової. Було проаналізовано ступінь ураження коронарної артерії, додатково – судини діаметром понад 2,5 мм. Після КА шляхом виконання ВУЗД вимірювали такі показники, як площа зовнішньої еластичної мембрани (EEM), мінімальна площа просвіту (MLA), площа поперечного перерізу бляшки (EEM‑MLA) та навантаження бляшкою – ступінь стенозу (MLA/EEM × 100%).
Статистичний аналіз
Всі дані аналізували за допомогою програмного забезпечення SPSS 13.0 (Чикаго, Іллінойс, США). Результати вимірювань були виражені як середнє значення ± стандартне відхилення. Середні показники у двох групах порівнювали з використанням t-тесту для незалежних вибірок. Середні значення у групі до та після лікування були зіставлені за допомогою парного t-тесту. Значення р<0,05 вважали статистично значущим.
Результати дослідження
Первинна кінцева точка
Первинні кінцеві точки знижувалися ефективніше при застосуванні комбінації препаратів розувастатин + езетиміб порівняно з монотерапією розувастатином. У групі розувастатину був один пацієнт з новим випадком ІМ та п’ятеро з симптомами нестабільної стенокардії. При лікуванні розувастатином і езетимібом не було нових або повторних ІМ, у двох хворих виявлено симптоми нестабільної стенокардії (р<0,05).
Рівень ліпідів у крові та запальних цитокінів
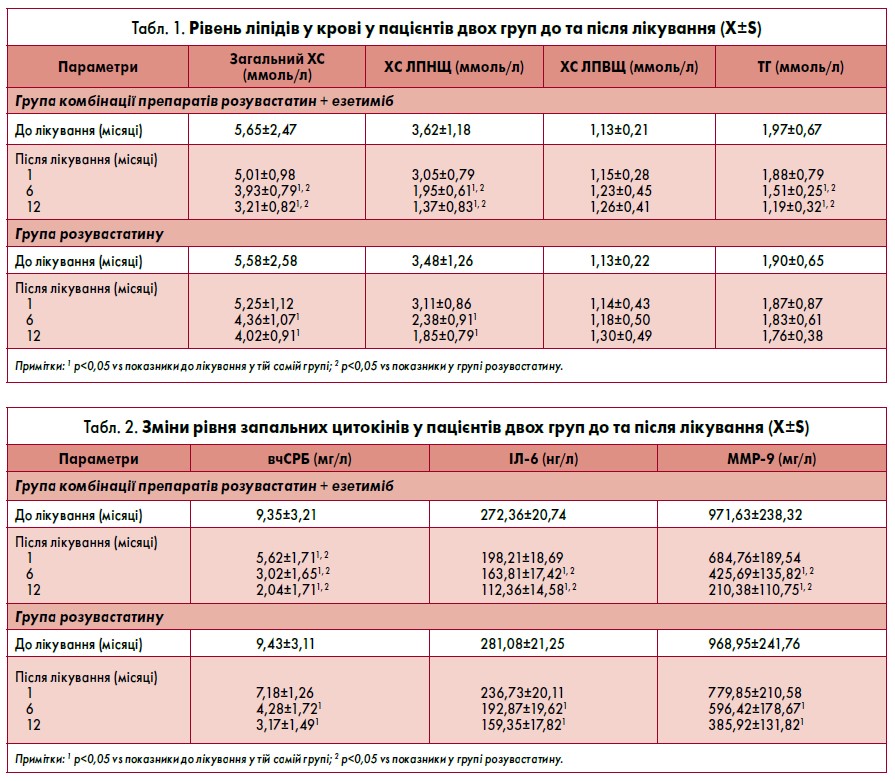
Венозну кров натщесерце було взято у пацієнтів обох груп вранці до лікування та через 1, 6 і 12 місяців після нього для встановлення рівня ліпідів у крові та запальних цитокінів. Вміст загального ХС, ХС ЛПНП, вчСРБ, ІЛ‑6 та MMP‑9 зменшився після терапії в обох групах порівняно з параметрами до лікування. Крім того, вищезазначені показники були нижчими у групі розувастатину та езетимібу, ніж серед пацієнтів, що приймали лише розувастатин (р<0,05) (табл. 1, 2).
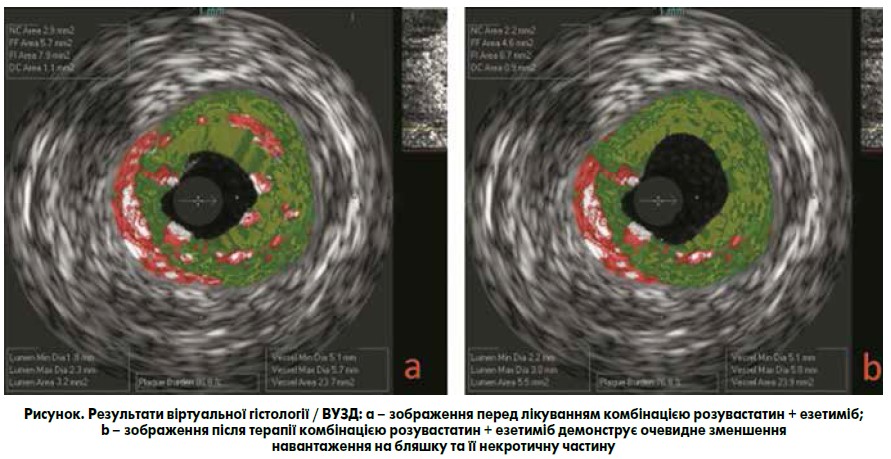
Зображення ВУЗД та віртуальної гістології
Як показано на рисунку, ЕЕМ, MLA, навантаження бляшки, EEM‑MLA та відсотковий вміст некротичної частини бляшки були зіставними у групах комбінації препаратів розувастатин + езетиміб та розувастатину перед лікуванням без суттєвої статистичної різниці (р>0,05). Через 12 місяців навантаження бляшки, EEM‑MLA та відсотковий вміст некротичної частини бляшки ефективніше зменшилися у групі лікування розувастатином і езетимібом, ніж лише розувастатином (р<0,05).
Обговорення
Езетиміб – це представник нового класу ліпідознижувальних речовин, які селективно пригнічують інтестинальну абсорбцію ХС та відповідних рослинних стеролів. Молекулярною мішенню езетимібу є переносник стеролів Niemann-Pick Cl-Like 1 (NPC1L1). Така дія езетимібу приводить до активізації печінкових рецепторів ХС ЛПНЩ та збільшує кліренс циркулюючого ХС ЛПНЩ. Езетиміб головним чином блокує всмоктування екзогенного ХС, діє на щіткову кайму клітин кишечника та гальмує всмоктування ХС і рослинних стеролів. Це може зменшувати надходження ХС до печінки, стимулювати синтез печінкових рецепторів ЛПНЩ та прискорювати метаболізм ЛПНЩ.
За даними багатьох досліджень, езетиміб здатний знижувати абсорбцію ХС у кишечнику на 54‑67% (Sudhop et al., 2002; van Heek et al., 2001; Califf et al., 2009). Інші випробування підтвердили, що у пацієнтів при лікуванні статинами, в яких рівень ХС ЛПНЩ не досягав нормального рівня або цільового значення, комбінація статину з езетимібом зменшувала ХС ЛПНЩ і ТГ, збільшувала ХС ЛПВЩ та апопротеїн AI (Patrick et al., 2002).
Оскільки езетиміб та статини мають різні ліпідознижувальні механізми дії, X. Wang et al. (2016) об’єднали їх для досягнення найпотужніших ефектів лікування. Було показано, що розувастатин + езетиміб ефективно знижують загальний ХС, ХС ЛПНЩ, ТГ та посилюють ліпідознижувальні ефекти.
У раніше проведених клінічних випробуваннях вплив розувастатину та езетимібу на площу коронарної бляшки не розглядався.
Однак X. Wang et al. (2016) виявили, що розувастатин + езетиміб здатні додатково зменшувати площі та стабілізувати структуру бляшок завдяки зниженню рівня ліпідів і потужному пригніченню запалення.
Окрім того, у клінічному дослідженні IMPROVE-IT оцінювали лікування езетимібом та статинами у пацієнтів, що перенесли гострий коронарний синдром. Автори відзначили суттєве зниження ХС ЛПНЩ на фоні лікування кобінацією статину та езетимібу, що привело до значного зменшення ризику розвитку кардіальних подій порівняно з монотерапією статином. До того ж жодних побічних чи токсичних явищ не спостерігалось (Cannon et al., 2015).
На додачу, в низці досліджень було продемонстровано, що СРБ є незалежним фактором ризику розвитку атеросклеротичної ІХС. ІЛ‑6 також нерозривно пов’язаний із цим та бере участь у запальному процесі при нестабільній бляшці. Підвищена концентрація ІЛ‑6 показує, що бляшки схильні до розриву. ММР можуть руйнувати позаклітинний матрикс в умовах нейтрального рН. Вони значною мірою впливають на товщину фіброзної оболонки та вміст колагену. Надмірна секреція MMP‑9 спричиняє розрив атеросклеротичної бляшки шляхом деградації колагену в фіброзній оболонці (Li et al., 2008).
У раніше проведених дослідженнях було підтверджено, що езетиміб у поєднанні зі статинами здатен значно знижувати рівень вчСРБ (Devaraj et al., 2006; Sager et al., 2005). У дослідженні ENHANCE також показано, що езетиміб + статини можуть краще впливати на зниження рівня ХС ЛПНЩ та СРБ (на цей показник – вдвічі) (Kastelein et al., 2005). Коли концентрація ХС ЛПНЩ зменшується до певного рівня, езетиміб знижує маркери запалення, посилюючи інгібувальну дію статинів на СРБ у печінці (Gomma et al., 2004).
Слід зазначити, що останнім часом ВУЗД та віртуальна гістологія / ВУЗД широко використовуються для оцінки навантаження коронарної атеросклеротичної бляшки та її стабільності. У багатьох попередніх дослідженнях, в яких вивчали вплив статинів на бляшки, було підтверджено, що вони можуть інгібувати їх шляхом зниження рівня ХС ЛПНЩ.
У випробуванні X. Wang et al. (2016) ВУЗД та віртуальна гістологія / ВУЗД застосовувалися для оцінки впливу потужних гіполіпідемічних засобів розувастатину та езетимібу на бляшки. Отримані результати дослідження показали, що комбінація розувастатину та езетимібу здатна ефективно знижувати рівень ліпідів у крові й інгібувати експресію запальних цитокінів, значно зменшувати навантаження бляшки та стабілізувати її.
Варто зауважити, що це дослідження включало осіб із тяжкою ІХС. Інтенсивна фармакотерапія є ключовою стратегією у цій групі хворих. Серед доступних на сьогодні методів гіполіпідемічна терапія може забезпечити дуже велику користь. Розувастатин + езетиміб здатні зменшувати площу бляшки та стабілізувати її структуру. У дослідженні X. Wang et al. (2016) комбінація розувастатину та езетимібу ефективно знижувала ризик розвитку гострого коронарного синдрому.
Висновки
Таким чином, поєднання езетимібу зі статинами, зокрема розувастатином, здатне дієво знижувати рівень ліпідів у крові. Це пов’язано з потужним інгібувальним ефектом розувастатину та езетимібу на запальні цитокіни, що зменшує навантаження бляшки і поліпшує її стабільність. Така лікувальна тактика є особливо корисною для пацієнтів з атеросклеротичною ІХС.
Довідка «ЗУ»
Відповідно до рекомендацій Європейського товариства кардіологів (ESC) та Європейського товариства з атеросклерозу (EAS), що вийшли 2019 р., фармакологічне зниження ХС ЛПНЩ на 1-му кроці передбачає призначення високоактивних статинів до найвищої толерантної дози для зниження ризику ССЗ (І, А). Якщо цільового рівня ХС ЛПНЩ не досягнуто, до статину слід додати езетиміб (І, В) – 2-й крок.
На українському фармринку представлені препарати Розуліп® (1 таблетка містить 10 або 20 мг розувастатину) та Розуліп® Плюс (1 капсула містить 10 мг розувастатину та 10 мг езетимібу або 20 мг розувастатину та 10 мг езетимібу) компанії «ЕГІС» (Угорщина).
Серед переваг згаданих препаратів слід відзначити широкий спектр дозування, актуальність комбінації та вдале співвідношення ціна/якість, що суттєво підвищує прихильність пацієнтів до лікування.
Підготувала Олена Коробка
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (71) 2020 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Кору та листя верби тисячоліттями використовували як знеболювальний та жарознижувальний засіб. У ХІХ ст. із цих рослинних продуктів кристалізовано активну речовину – саліцин, згодом синтезували саліцилову кислоту, а в 1899 році її ацетильовану форму – ацетилсаліцилову кислоту (АСК) запатентовано як удосконалений лікарський засіб під назвою «аспірин» [1]. Лише в другій половині ХХ ст. детально вивчено молекулярні мішені АСК; зокрема, отримав належну оцінку та пояснення її антитромботичний ефект....
Артеріальна гіпертензія (АГ) є провідною причиною смерті та інвалідизації у всьому світі. Відповідно до серії досліджень Global Burden of Disease, ≈13% смертей так чи інакше пов’язані з АГ (Forouzanfar M.H. et al., 2017; Lewington S. et al., 2002; World Health Organization, 2009)....
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9). Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи. ...