Еволюція та сучасні підходи до ведення пацієнтів із хронічною серцевою недостатністю та коморбідними станами
 Лікування серцевої недостатності (СН) та досягнення її тривалої компенсації є вельми складним процесом. Адже нерідко виникає резистентність до діуретичної терапії як основного інструменту для зменшення виразності симптомів даної патології. В межах Х науково-практичної конференції Всеукраїнської асоціації фахівців із серцевої недостатності (27‑28 травня 2020 року) про сучасні стандарти лікування діуретиками в таких пацієнтів із коморбідними станами розповів завідувач кафедри нефрології та нирковозамісної терапії Національної медичної академії післядипломної освіти імені П.Л. Шупика (м. Київ), д. мед. н., професор Дмитро Дмитрович Іванов.
Лікування серцевої недостатності (СН) та досягнення її тривалої компенсації є вельми складним процесом. Адже нерідко виникає резистентність до діуретичної терапії як основного інструменту для зменшення виразності симптомів даної патології. В межах Х науково-практичної конференції Всеукраїнської асоціації фахівців із серцевої недостатності (27‑28 травня 2020 року) про сучасні стандарти лікування діуретиками в таких пацієнтів із коморбідними станами розповів завідувач кафедри нефрології та нирковозамісної терапії Національної медичної академії післядипломної освіти імені П.Л. Шупика (м. Київ), д. мед. н., професор Дмитро Дмитрович Іванов.
Як зазначив спікер, СН є одним із найпоширеніших ускладнень в осіб із хронічною нирковою недостатністю (ХНН). Патофізіологічні порушення в роботі серця та нирок у вигляді гострої або хронічної дисфункції в одному органі, які зумовлюють таку ж дисфункцію в іншому, об’єднуються під терміном «кардіоренальний синдром» (КРС).
На сьогодні відома класифікація КРС, в якій виділяють п’ять його типів:
- тип І (гострий КРС) – різке зниження серцевої функції, що зумовлює гостру ниркову недостатність (ГНН); причини: гостра СН, оперативні втручання на серці, гострий коронарний синдром, контраст-індукована нефропатія після коронароангіографії, кардіогенний шок;
- тип ІІ (хронічний КРС) – хронічна серцева дисфункція, яка спричиняє ХНН; причини: ішемічна хвороба серця, артеріальна гіпертензія, вроджені патології серця, хронічна СН (ХСН);
- тип ІІІ (гострий ренокардіальний синдром) – різке зниження ниркової функції, що призводить до розвитку гострої серцевої дисфункції; причини: гострий набряк легень при ГНН, аритмії, контраст-індукована нефропатія, що викликає розвиток серцевої дисфункції;
- тип IV (хронічний ренокардіальний синдром) – ХНН, яка зумовлює хронічну серцеву дисфункцію; причини: гіпертрофія міокарда лівого шлуночка при ХНН, кардіоваскулярна дисфункція при ХНН, автосомно-домінантний полікістоз нирок;
- тип V (вторинний кардіоренальний синдром) – інші коморбідні стани, що призводять до розвитку ниркової та серцевої дисфункції; причини: сепсис, цукровий діабет, системний червоний вовчак, саркоїдоз, амілоїдоз.
Також у нефрологічній практиці існує декілька термінів для характеристики хвороби нирок. Так, хронічна хвороба нирок (ХХН) передбачає наявність змін в аналізах сечі/крові або ж зниження швидкості клубочкової фільтрації (ШКФ) <60 мл/хв/м2 понад три місяці. Своєю чергою діабетична нефропатія характеризується наявністю ХХН та цукрового діабету. Крім того, окремо виділяють гіпертензивну (ХХН, спричинена артеріальною гіпертензією) та ішемічну (ХХН унаслідок атеросклерозу) хворобу нирок.
Поєднання ХХН із серцево-судинними захворюваннями асоційоване з підвищенням кардіоваскулярної смертності за рахунок виникнення різноманітних ускладнень, як-то СН та ниркова недостатність. Ці події, що доповнюють одна одну, зумовлюють збільшення об’єму рідини в організмі та виникнення застійних явищ. Вони часто розвиваються протягом тривалого часу до появи ознак декомпенсації. Нерідко основною причиною застійних явищ в організмі є абсолютне або відносне зниження функції нирок.
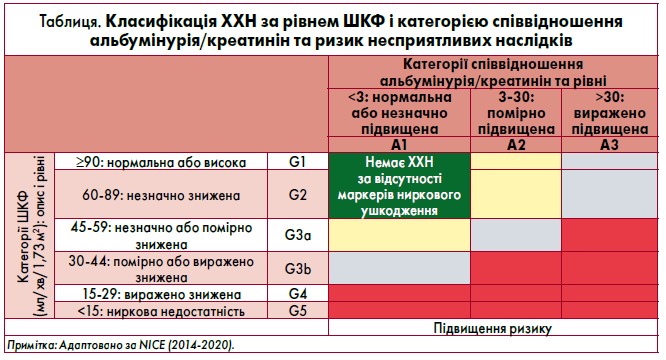
Із 2012 р. нефрологи використовують прогностичний метод для визначення перебігу хвороби нирок, що передбачає оцінку таких двох основних критеріїв, як ШКФ та альбумінурія (таблиця). Сучасним способом для розрахунку ШКФ є формула GFR-EPI, розроблена Товариством з епідеміології хронічної хвороби нирок (Levey et al., 2009). Для обчислення ШКФ також можна застосовувати мобільний додаток yourGFR (Glomerular Filtration Rate). Прогноз пацієнтів переважно погіршується за умови зростання альбумінурії на тлі зниження ШКФ.
У 2019 р. були запропоновані рекомендації Асоціації серцевої недостатності Європейського товариства кардіологів (ESC), які на сьогодні є основними у веденні хворих на ХСН із гіпергідратацією, базисним лікуванням якої є саме діуретична терапія. У даному випадку застосовують високі дози петльових діуретиків, які пригнічують реабсорбцію Na+/K+/Cl– у висхідній петлі Генле (фуросемід, торасемід). При цьому доцільне поступове збільшення дозування препаратів (від 2‑3 діб до тижня) залежно від стану пацієнта.
Як зауважив Дмитро Дмитрович, алгоритм призначення петльового діуретика є наступним: початкова доза має бути еквівалентною 20‑40 мг фуросеміду внутрішньовенно. Первинну оцінку ефективності діуретичної терапії проводять через 2 та 6 годин. Якщо кількість сечі збільшується і становить у середньому 100‑150 мл/год, тобто 600‑900 мл протягом шістьох годин після введення петльового діуретика, така реакція на лікування є задовільною. Якщо при цьому кількість сечі не перебільшує 600 мл, необхідно підвищити дозу препарату вдвічі. Такий зручний алгоритм розроблений для оцінки ефективності терапії петльовим діуретиком протягом першої доби спостереження за пацієнтом.
Із другого дня госпіталізації цільовий добовий діурез в осіб із СН повинен становити більш ніж 3‑4 л. При цьому дозу петльового діуретика за потреби може бути збільшено до досягнення цільового терапевтичного ефекту. З цією метою можливе застосування комбінації петльових діуретиків з тіазидними (ксипамід, індапамід тощо) або калійзберігальними (амілорид) діуретиками, а також інгібіторами натрійзалежного котранспортера глюкози 2-го типу.
Слід зазначити, що не варто поєднувати фуросемід і торасемід, оскільки вони конкуруватимуть між собою через однаковий механізм дії. Дуже важливо оцінити початкову функцію нирок перед призначенням петльових діуретиків. Зазвичай фуросемід як препарат із виразним діуретичним ефектом застосовують у хворих із ШКФ <30 мл/хв/м2. В інших випадках переважно використовують монотерапію торасемідом або його комбінацію із ксипамідом.
Кардинальною відмінністю торасеміду від інших діуретиків є його здатність знижувати активність ренін-ангіотензин-альдостеронової системи. Це забезпечує реалізацію таких ефектів, як блокада вазоспазму та пригнічення продукції альдостерону, що сприяє уповільненню процесу фіброзу в міокарді та стінках судин (Lopez еt al., 2004).
На думку професора, важливо пам’ятати, що торасемід має три терапевтичні інтервали дії залежно від призначеної дози:
- доза 5‑10 мг зумовлює вазодилатацію, а сечогінний ефект практично відсутній;
- доза 20‑40‑60 мг сприяє потужному діуретичному ефекту;
- доза 100‑200 мг застосовується при виразних набряках для забезпечення форсованого діурезу.
Під час приймання торасеміду по 100 чи 200 мг необхідно робити перерву на один день, оскільки може розвиватися резистентність до діуретичної терапії. Проте лікування можна не переривати, якщо добовий діурез пацієнта не зменшується і постійно становить понад 2 л.
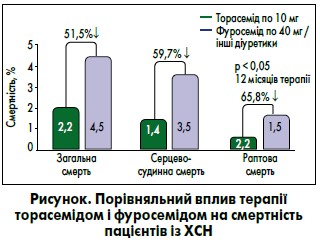 В окремих клінічних випробуваннях торасемід показав певні переваги порівняно з фуросемідом. Зокрема, у дослідженні TORIC вивчали вплив терапії торасемідом і фуросемідом на частоту повторних госпіталізацій та рівень смертності хворих (n=1377) на ХСН II/III функціонального класу (ФК) за класифікацією Нью-Йоркської асоціації серця (NYНА) (рисунок). Отримані результати показали виразніший позитивний вплив торасеміду на всі кінцеві точки (загальну, раптову та серцево-судинну смерть), ніж при лікуванні фуросемідом (Cosin et al., 2002).
В окремих клінічних випробуваннях торасемід показав певні переваги порівняно з фуросемідом. Зокрема, у дослідженні TORIC вивчали вплив терапії торасемідом і фуросемідом на частоту повторних госпіталізацій та рівень смертності хворих (n=1377) на ХСН II/III функціонального класу (ФК) за класифікацією Нью-Йоркської асоціації серця (NYНА) (рисунок). Отримані результати показали виразніший позитивний вплив торасеміду на всі кінцеві точки (загальну, раптову та серцево-судинну смерть), ніж при лікуванні фуросемідом (Cosin et al., 2002).
На українському фармринку доступний таблетований препарат Торасемід Сандоз® із широким спектром дозувань (10, 20, 50, 100 і 200 мг). Це забезпечує можливість вибору оптимальної дози лікарського засобу для досягнення ефективності діуретичної терапії та підвищує комплаєнс пацієнта.
Дмитро Дмитрович підкреслив, що крім діуретичної терапії пацієнти із ХСН та ХХН мають отримувати препарати, що впливають на тонус судинної стінки та знижують артеріальний тиск (АТ). Насамперед це інгібітори ангіотензинперетворювального ферменту (іАПФ), сартани та β-блокатори, які не лише підтвердили свою клінічну ефективність, але й довели позитивний вплив на прогноз в осіб із СН та ХХН.
У сучасній нефрологічній практиці ведення пацієнтів із АГ та ХХН залежить від ШКФ. Якщо даний показник становить більш ніж 120 мл/хв/м2 (стан гіперфільтрації у спортсменів та пацієнтів із І стадією ХХН), відсутня мікроальбумінурія та не відмічено підйомів АТ, застосовувати гіпотензивні препарати немає потреби. Разом із тим призначення іАПФ або сартану в невеликих дозах на ніч в осіб із І стадією діабетичної нефропатії сприяє зменшенню її прогресування майже вдвічі.
Якщо ШКФ становить 120‑60 мл/хв/м2, призначають сартани або іАПФ у дозах, за яких очікується досягнення систолічного АТ (САТ) <130 мм рт. ст. За наявності протеїнурії 0,5‑1 г/л можлива комбінація іАПФ та сартанів. При ШКФ 59‑30 мл/хв/м2 показано монотерапію іАПФ або сартанами.
Яким є цільовий АТ у пацієнтів із ХХН та АГ? Спікер зауважив, що в нефрологічній практиці рекомендований рівень офісного САТ при ХХН становить менш ніж 120 мм рт. ст. (KDIGO, 2020). Слід зазначити, що поняття цільового діастолічного АТ у нефрології немає, але бажаним є показник <80 мм рт. ст. За рекомендаціями Європейського товариства з артеріальної гіпертензії (ESH) та ESC (2018), цільовий САТ у пацієнтів з АГ та ХХН віком 18‑65 років є 130‑140 мм рт. ст.
Варто підкреслити, що, відповідно до вказаних настанов, обов’язковим компонентом антигіпертензивної терапії на кожному етапі лікування АГ є діуретики. При цьому препарати вибору – тіазидні або тіазидоподібні діуретики. Проте слід пам’ятати, що індапамід протипоказаний при ШКФ <60 мл/хв/м2. У разі супутньої ХХН при АГ доцільним є застосування саме петльових діуретиків.
Отже, оптимальний вибір лікувальної стратегії, зокрема, діуретичної в осіб із серцево-судинними захворюваннями та ХХН забезпечує поліпшення якості життя таких пацієнтів, а також сприяє зменшенню смертності через загальні причини та різні кардіоваскулярні ускладнення.
Підготувала Людмила Оніщук
Інформація для спеціалістів сфери охорони здоров’я
3-01-ТОР-РЕЦ-0920
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (71) 2020 р.
СТАТТІ ЗА ТЕМОЮ Терапія та сімейна медицина
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Серед препаратів, які мають велику доказову базу щодо лікування пацієнтів із захворюваннями дихальних шляхів з алергічним компонентом, особливий інтерес становлять антагоністи лейкотрієнових рецепторів (АЛТР). Ці препарати мають хорошу переносимість у дорослих та дітей, а також, на відміну від інгаляційних кортикостероїдів (ІКС), характеризуються високим комплаєнсом, тому посідають чільне місце в лікуванні пацієнтів із респіраторною патологією. У лютому відбувся міждисциплінарний конгрес із міжнародною участю «Життя без алергії International» за участю провідних вітчизняних міжнародних експертів. Слово мав президент Асоціації алергологів України, професор кафедри фтизіатрії та пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук Сергій Вікторович Зайков із доповіддю «Місце АЛТР у лікуванні пацієнтів із респіраторною патологією». ...
Розбір клінічного випадку...