Аналіз ефективності вітамін K-незалежних пероральних антикоагулянтів та антагоністів вітаміну K для лікування пацієнтів із неклапанною фібриляцією передсердь
Неклапанна фібриляція передсердь (НФП) – найпоширеніший тип ФП у розвинених країнах, в основі якої лежать такі основні етіологічні фактори, як артеріальна гіпертензія, атеросклеротична хвороба серця, застійна серцева недостатність, цукровий діабет тощо. Хоча ФП інколи перебігає безсимптомно, часто пацієнти мають прояви, які погіршують якість їхнього життя, як-то дискомфорт, серцебиття, задишка, синкопе, запаморочення, зниження толерантності до фізичних навантажень та хронічна втомлюваність. Застосування антикоагулянтної терапії у хворих на ФП спрямоване на запобігання розвитку ішемічного інсульту (ІІ). C.I. Coleman et al. виконали систематичний огляд досліджень, проведених у реальних клінічних умовах, з метою оцінки ефективності вітамін К-незалежних пероральних антикоагулянтів (НОАК) ривароксабану, дабігатрану та апіксабану порівняно з антагоністами вітаміну К (АВК) у пацієнтів із НФП. Отримані результати опубліковані у виданні Journal of Market Access & Health Policy (2019; 7 (1): 1‑7).
НФП – захворювання, що не супроводжується ревматичною недостатністю мітрального клапана, його протезуванням або пластикою. ФП може призводити до серйозних серцево-судинних наслідків, а саме збільшення вірогідності розвитку інсульту в 2‑7 разів та смерті вдвічі. Поширеність ФП становить 0,4‑1% у всьому світі, серед осіб після 80 років – 10% (Bajpai et al., 2007; Bunch, Gersh, 2011).
АВК – перші антикоагулянти, які призначалися пацієнтам із ФП і тривалий час лишалися основою терапії. АВК знижують ризик появи інсульту на дві третини та смертності – на чверть, однак потребують регулярного моніторингу коагуляції, коригування дозування за необхідності та пов’язані з частою взаємодією з іншими препаратами і продуктами харчування (Kirchhof et al., 2016). НОАК не потребують регулярного контролю коагуляції, а їхню клінічну користь в осіб із НФП підтверджено результатами рандомізованих контрольованих досліджень (РКД) ROCKET-AF, RE-LY, ARISTOTLE та ENGAGE AF-TIMI 48 (Patel et al., 2011; Connolly et al., 2009; Granger et al., 2011; Giugliano et al., 2013).
Ці лікарські засоби продемонстрували зіставну або кращу ефективність порівняно з АВК, що супроводжувалася зниженням частоти розвитку геморагічних інсультів (ГІ) та внутрішньочерепних крововиливів (ВЧК). Згідно з сучасними рекомендаціями Європейського товариства кардіологів (ESC), доцільно віддавати перевагу НОАК перед АВК у пацієнтів із НФП, в яких наявний хоча б один фактор ризику інсульту (Kirchhof et al., 2016).
На додаток до результатів РКД щодо ефективності НОАК, нові дані підтверджують можливість їхнього використання у рутинній клінічній практиці.
Як відомо, АВК добре зарекомендували себе в РКД. Однак через потребу регулярного моніторингу коагуляції та часту взаємодію з іншими ліками і продуктами харчування, АВК вважаються менш ефективними в реальних клінічних умовах. C.I. Coleman et al. провели метааналіз доступних даних для оцінки ефективності НОАК ривароксабану, дабігатрану та апіксабану порівняно з АВК у пацієнтів із НФП.
Матеріали й методи дослідження
Пошук необхідних матеріалів був здійснений у базах даних Medline, Embase та Кокранівській бібліотеці у грудні 2016 р. Випробування, що увійшли до метааналізу, включали популяцію пацієнтів віком ≥18 років із НФП, які отримували НОАК. До уваги були взяті початок антикоагулянтної терапії та її тривалість. Досліджуваними препаратами були інгібітори фактора Xa апіксабан і ривароксабан та прямий інгібітор тромбіну дабігатран. Результати щодо ризику подій, які характеризують ефективність лікарських засобів: ішемічний інсульт, загальна смертність, інфаркт міокарда (ІМ), венозна тромбоемболія (ВТЕ), ІІ + системна емболія (СЕ) та ІІ/СЕ + смерть через будь-які причини. Результати, пов’язані з безпекою препаратів: геморагічний інсульт, ВЧК, великі, шлунково-кишкові та будь-які кровотечі. Показники, що представляли додатковий інтерес для дослідників, являли собою прихильність/неприхильність до терапії, визначену як перерва у лікуванні щонайменше на 60 днів.
Був проведений порівняльний аналіз препаратів із використанням методу розрахунку зворотних дисперсій для об’єднання показників відносного ризику (ВР) і 95% довірчих інтервалів (ДІ) при коригуванні базових характеристик у кожному дослідженні:
- ривароксабану та АВК;
- дабігатрану та АВК;
- апіксабану та АВК.
При проведенні аналізу не враховували дані при застосуванні різних доз препаратів. Гетерогенність даних у випробуваннях оцінювали за рекомендаціями Кокранівського посібника для систематичних оглядів (Higgins, Green, 2011). Також до уваги були взяті моделі фіксованих та випадкових ефектів. З огляду на гетерогенність у дизайні досліджень, враховувалися результати моделі випадкових ефектів.
Результати дослідження
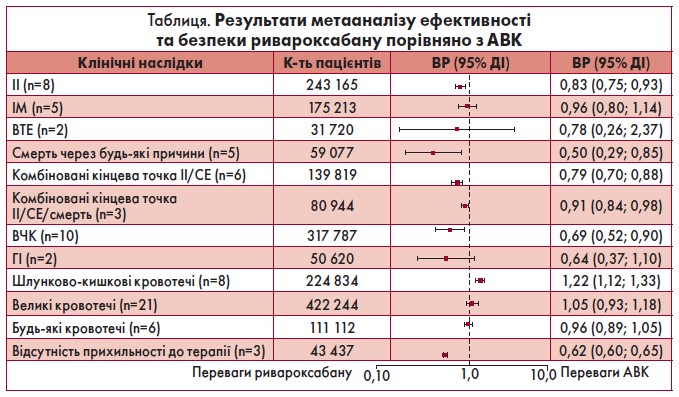
Після детальної оцінки із 562 виявлених у процесі пошуку публікацій 95 були включені у метааналіз (Briere et al., 2018). Із них у 49 із АВК порівнювали ривароксабан, у 79 – дабігатран та у 18 – апіксабан (у деяких дослідженнях вивчали більш ніж один НОАК). Результати зіставного метааналізу ривароксабану та АВК представлені в таблиці.
Згідно з аналізом восьми досліджень, застосування ривароксабану було пов’язане зі значно нижчим ризиком розвитку ІІ, але суттєвої різниці щодо ІМ та ВТЕ не виявлено. За підсумками п’ятьох випробувань, лікування ривароксабаном корелювало з суттєво меншою вірогідністю смерті через будь-які причини, ніж АВК. Також ривароксабан асоціювався зі значно нижчим ризиком комбінованих кінцевих точок порівняно з АВК, як-то ІІ/СЕ та ІІ/СЕ/смерть. Окрім того, використання ривароксабану супроводжувалося достовірно нижчою ймовірністю появи ВЧК, ніж АВК. Суттєві відмінності між двома методами лікування стосовно великих та будь-яких кровотеч не спостерігалися. На додачу, ризик відсутності прихильності до терапії був меншим при застосуванні ривароксабану порівняно з АВК.
При порівнянні дабігатрану та АВК НОАК асоціювався з нижчим ризиком розвитку ІІ, ВТЕ, ВЧК, ГІ та летальності через будь-які причини. Суттєвої різниці між двома методами лікування стосовно вірогідності ІМ, комбінованих кінцевих точок ІІ/СЕ та ІІ/СЕ/смерті не виявлено. Останній також був пов’язаний з меншою імовірністю виникнення великих і будь-яких кровотеч. Суттєвих відмінностей між двома методами терапії щодо відсутності комплаєнсу не виявлено.
Метааналіз порівняння апіксабану та АВК показав відсутність значущих розбіжностей між препаратами щодо розвитку ІІ, смерті через будь-які причини та комбінованої кінцевої точки ІІ/СЕ. Апіксабан асоціювався з суттєво нижчим ризиком комбінованої кінцевої точки ІІ/СЕ/смерті, ВЧК, ГІ, великих та шлунково-кишкових кровотеч. Щодо ймовірності виникнення будь-яких кровотеч і відсутності прихильності до лікування, значної різниці між апіксабаном та АВК не було.
Обговорення
З огляду на великий обсяг проаналізованих доказів, дослідникам вдалося отримати більш чітку картину щодо ефективності НОАК порівняно з АВК у рутинній клінічній практиці. Проведений метааналіз продемонстрував, що пацієнти, які отримували ривароксабан, мали нижчий ризик розвитку ІІ або смерті через будь-які причини, ніж при терапії АВК. У випробуванні ARISTOTLE апіксабан був кращим за варфарин з точки зору первинної кінцевої точки – профілактики інсульту або СЕ (Granger et al., 2011). Однак метааналіз двох досліджень, проведених у реальних клінічних умовах, суттєвої різниці не виявив. Аналогічно, загальна смертність, яка була нижчою у групі апіксабану порівняно з АВК, значно не відрізнялася за даними метааналізу двох подібних випробувань.
Загальновизнано, що дослідження у реальних клінічних умовах надають інформацію про ефективність терапії у більш різноманітних популяціях, ніж тих, що включені у РКД (Silverman, 2009). Крім того, результати випробувань зазвичай базуються на аналізі наміру лікуватися, тоді як докази, отримані у рутинній клінічній практиці, – переважно на оцінюванні терапії. Основними перевагами проведеного аналізу був моніторинг великої кількості досліджень та, зокрема, чималого обсягу результатів (Proietti et al., 2018). Однак варто враховувати певні методологічні фактори, які могли вплинути на отримані дані.
Популяції включених у дослідження учасників були дещо неоднорідними, і деякі характеристики пацієнтів та захворювань могли вплинути на безпеку й ефективність аналізованих НОАК. Тому, враховуючи потенційне викривлення вихідних характеристик, у більшості випробувань було виконане корегування даних для забезпечення надійності результатів метааналізу.
Також у деяких дослідженнях не повідомлялося про застосовану дозу НОАК, що є істотним обмеженням, оскільки, за винятком дабігатрану, для різних груп пацієнтів показане призначення різних доз. На додачу, на визначення клінічних наслідків могло вплинути об’єднання результатів при великих кровотечах, наприклад шлунково-кишкових і ВЧК (Ruff et al., 2014). Відомості про випадки смерті, будь-які кровотечі та ГІ не завжди фіксувалися, що робило оцінку даних складною. Також не було надано інформацію про ступінь тяжкості (велика та незначна) шлунково-кишкових кровотеч. Крім того, якщо у дослідженнях були доступні результати в різні періоди спостереження, в аналізі було використано найдовший.
Висновки
У процесі метааналізу було виявлено багато досліджень, присвячених порівнянню ефективності НОАК та АВК у реальних клінічних умовах. Отримані результати показали, що НОАК є кращою альтернативою АВК у рутинній клінічній практиці. Лікування ривароксабаном та дабігатраном, але не апіксабаном, сприяло значному зниженню ризику розвитку ІІ порівняно з АВК. Ривароксабан також асоціювався з меншою вірогідністю зниження комплаєнсу, ніж АВК. Окрім того, всі НОАК були пов’язані з нижчою частотою виникнення ВЧК порівняно з АВК. Було показано, що НОАК є принаймні такими ж ефективними та безпечними, як АВК для запобігання інсульту при НФП.
Таким чином, сучасні дослідження щодо використання НОАК у реальних клінічних умовах підтверджують результати РКД стосовно їхньої ефективності у відповідній популяції хворих. Доступність таких доказів зростатиме найближчим часом, збільшуючи знання лікарів про застосування НОАК у рутинній клінічній практиці та оптимізацію терапії окремих груп пацієнтів.
Підготувала Олена Коробка
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (71) 2020 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....