Пути оптимизации применения назальных деконгестантов: повышение эффективности и улучшение переносимости
 Назальные деконгестанты (или антиконгестанты) – препараты, обладающие выраженным сосудосуживающим и противоотечным эффектами; применяются в медицинской практике более 5000 лет.
Назальные деконгестанты (или антиконгестанты) – препараты, обладающие выраженным сосудосуживающим и противоотечным эффектами; применяются в медицинской практике более 5000 лет.
Первыми известными вазоконстрикторами принято считать эфедрин и кокаин. Эфедрин, который назначался для снижения отека слизистых при бронхиальной астме в традиционной китайской медицине со времен империи Хань (206 г. до н. э. – 220 г. н. э.), сегодня характеризуется как психоактивный ядовитый алкалоид эфедры хвощевой (Ephedra equisetina); более известен как вещество, непосредственно использующееся при изготовлении наркотиков (Конвенция ООН о борьбе против незаконного оборота наркотических средств), чем как лекарственный препарат [1]. Кокаин для анестезии слизистых дыхательных путей начали применять в странах Европы с 1575 г., куда он был завезен из Южной Америки; в настоящее время это алкалоид тропанового ряда, метиловый сложный эфир бензоилэкгонина – наркотическое вещество, получаемое из растений рода Erythroxylum. В медицине практически не используется, хотя существуют единичные работы экспериментально-научного направления, посвященные его использованию в хирургии глаза и офтальмологии [2].
Первым синтезированным назальным деконгестантом был нафазолин, полученный в конце 30-х гг. прошлого столетия в Германии. Нафазолин – α-адреномиметик короткого действия, имеющий выраженные побочные эффекты, такие как раздражение слизистой оболочки носа, реактивная гиперемия; при длительном применении – набухание слизистой оболочки, что приводит к стойкой заложенности носа, сухости в горле. Системные побочные реакции при его применении – тошнота, головная боль, повышение артериального давления (АД), тахикардия. При длительном приеме нафазолин может индуцировать развитие медикаментозного ринита, а также стойкую физиологическую и психологическую зависимость (т. н. нафазолиновая зависимость) [3].
На современном фармацевтическом рынке назальных деконгестантов представлено более 200 лекарственных препаратов, которые относятся к группе «R01A. Противоотечные и другие препараты для местного применения при заболеваниях полости носа» согласно АТС-классификации (Anatomical Therapeutic Chemical) [4]. Объемы продаж назальных симпатомиметиков превышают 600 млн упаковок в год и продолжают увеличиваться; при этом лекарственные препараты имеют разную степень доказательности, разные фармацевтические подходы к их созданию (вспомогательные вещества, технологический процесс, лекарственная форма) и разные показатели переносимости терапии (частота возникновения побочных эффектов, риск развития привыкания, противопоказания) [5].
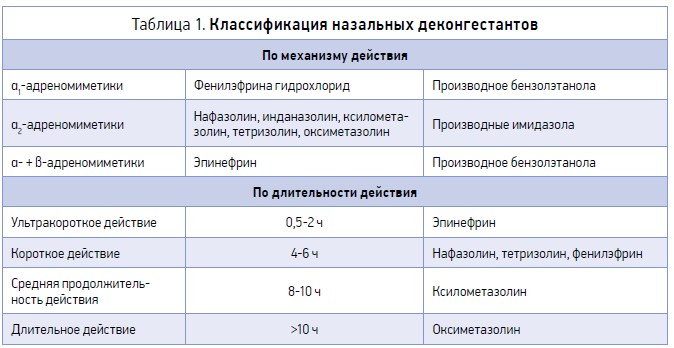
Ранжирование назальных деконгестантов проводят в основном по механизму и длительности действия (табл. 1).
Фармакологическая направленность действия препаратов данной группы ориентирована на улучшение носового дыхания, уменьшение отечности слизистых оболочек носа; их применение эффективно при аллергическом, вазомоторном и инфекционном ринитах, при этом активные фармацевтические ингредиенты (АФИ) будут иметь разную биодоступность и особые указания (табл. 2) [6].
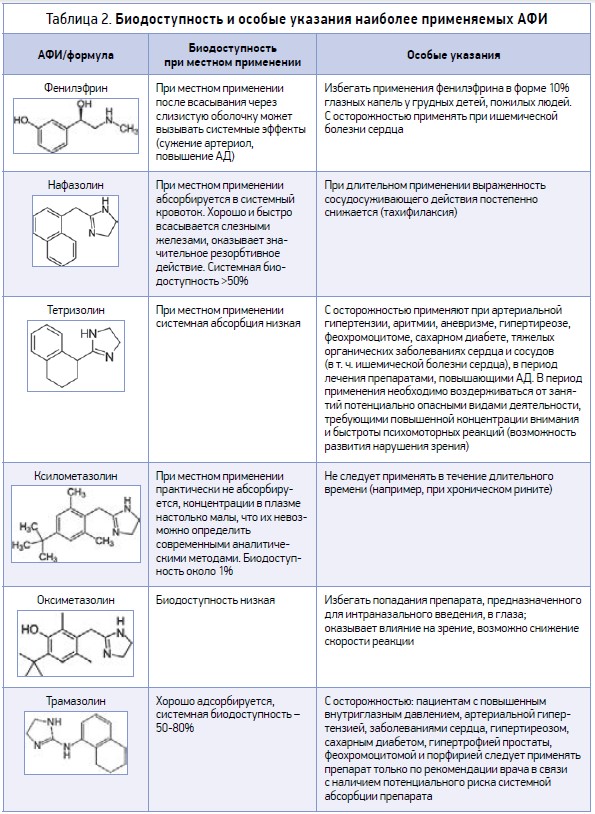 Максимальной биодоступностью (следовательно, повышенным риском развития негативных побочных реакций) характеризуются нафазолин и трамазолин (абсорбция – более 50%), средний показатель характерен для фенилэфрина, низкий – для тетризолина и оксиметазолина, минимальный показатель адсорбции в фармакологических и клинических исследованиях установлен для ксилометазолина (менее 1%).
Максимальной биодоступностью (следовательно, повышенным риском развития негативных побочных реакций) характеризуются нафазолин и трамазолин (абсорбция – более 50%), средний показатель характерен для фенилэфрина, низкий – для тетризолина и оксиметазолина, минимальный показатель адсорбции в фармакологических и клинических исследованиях установлен для ксилометазолина (менее 1%).
Анализ параметра «структура – биодоступность» показал, что по химической структуре АФИ ксилометазолина отличается от АФИ оксиметазолина только отсутствием гидроксильной группы и метильного радикала в ядре молекулы оксиметазолина, но именно эти отличия максимально понижают показатель адсорбции ксилометазолина, снижают до минимума риски развития системных побочных реакций и делают эту молекулу более «клинически привлекательной». Таким образом, целенаправленный химический синтез позволил создать оптимальную молекулу назального деконгестанта.
Следует отметить, что препараты данной подгруппы – «R01A. B. Симпатомиметики в комбинации с другими средствами (за исключением кортикостероидов) (фенилэфрин, нафазолин, ксилометазолин, тетризолин, оксиметазолин, туаминогептан, трамазолин и др.)» – являются безрецептурными; пациенты приобретают их без консультации со специалистами системы здравоохранения (врачи, фармацевты), такая терапия не всегда попадает под категорию «ответственное самолечение». В связи с этим частота возникновения негативных реакций от применения топических симпатомиметиков – особенно актуальный вопрос современной педиатрии, терапии и отоларингологии.
Все побочные эффекты препаратов данной группы (связанные с показателем абсорбции, а также биодоступности) можно разделить на системные и местные.
Системные побочные эффекты связаны с воздействием на адренергическую систему АФИ деконгестантов со средней и высокой биодоступностью, достигших системного кровотока.
Системный адренергический эффект деконгестантов отмечается как при передозировке, так и при правильном режиме применения, а также дозирования препарата; проявляется тахикардией, повышением АД, гипервозбудимостью. При применении у детей (в связи с высокой проницаемостью гематоэнцефалического барьера) происходит стимуляция адренорецепторов сосудодвигательного центра головного мозга, уменьшается поток симпатических импульсов. Клинически это проявляется заторможенностью, вялостью, сонливостью, спутанностью сознания, брадикардией, снижением АД; при продолжении действия препарата симптомы усиливаются с нарушением сознания вплоть до комы [7].
Особенно часто действие на центральную нервную систему отмечается у нафазолина. Применение препаратов данной группы нередко вызывает у пациентов ухудшение общего состояния, головную боль, сердцебиение и т. д. Иногда ситуационное применение деконгестантов с высоким или средним показателем абсорбции может сопровождаться головной болью, вызванной сегментарным спазмом сосудов головного мозга, и даже приводить к ишемическим и геморрагическим инсультам головного мозга [3].
К местным негативным реакциям деконгестантов относят медикаментозный ринит и цилиотоксическое действие.
Медикаментозный ринит (или синдром рикошета) развивается при длительном (свыше 10 дней) использовании топических адреномиметиков и характеризуется выраженным отеком в полости носа, назальной гиперреактивностью и затем – изменениями гистологического строения (ремоделированием) слизистой оболочки носа. Механизм развития данного эффекта обусловлен тем, что α-адреномиметики при длительном и частом применении угнетают эндогенную продукцию норадреналина, синтезируемого в адренорецепторах, а также вызывают снижение чувствительности гладкой мускулатуры сосудов полости носа к эндогенному норадреналину. В результате снижения тонуса α-адренорецепторов формируется развитие медикаментозного ринита. Соблюдение режима дозирования и длительности применения лекарственного препарата позволяет минимизировать развитие данного побочного эффекта.
Цилиотоксичность, по определению, данному в работе Д. А. Тулупова и соавт. (2018) [8], – токсическое действие, возникшее вследствие попадания на слизистую полости носа сосудосуживающего лекарственного препарата и характеризующееся появлением ощущения жжения, сухости, раздражения слизистой полости носа.
Одним из фрагментов цилиотоксического действия назальных деконгестантов является снижение двигательной активности мерцательного эпителия слизистой полости носа (замедление частоты биения ресничек) [9]. В исследовании, проведенном in vitro на культуре клеток мерцательного эпителия человека T. Hofmann и соавт. [10], установлено, что выраженное снижение частоты биения ресничек наблюдается при воздействии нафазолина и оксиметазолина, в то время как ксилометазолин практически не вызывает такого эффекта. Цилиотоксичность после 7-дневного использования 1% раствора эфедрина проявляется в значительной деструкции ультраструктуры мерцательного эпителия полости носа вплоть до слущивания клеток с базальной мембраны [11].
Помимо изучения отдельных АФИ были проведены исследования готовых лекарственных форм назальных деконгестантов; установлено, что их цилиотоксичность значительно выше, причиной чему служит то, что данная группа препаратов в качестве консерванта-антисептика содержит бензалкония хлорид [12].
Бензалкония хлорид – четвертичное аммониевое соединение, молекулы которого обладают высоким аффинитетом к белковым и липидным компонентам клеточных мембран, изменяют их физические свойства, оказывают влияние на обменные процессы, происходящие в клетках. Бензалкония хлорид проявляет выраженную бактерицидную активность в отношении стафилококков, стрептококков, грамотрицательных бактерий (кишечной и синегнойной палочек, протея, клебсиеллы и др.), анаэробных бактерий, грибов и плесеней; действует на штаммы бактерий, устойчивых к антибиотикам и другим химиотерапевтическим лекарственным средствам; подавляет плазмокоагулазу и гиалуронидазу стафилококков.
Токсическое действие бензалкония хлорида как консерванта-антисептика реализуется не только в отношении микроорганизмов, но и распространяется на структуры слизистой оболочки полости носа пациента, что приводит к развитию патологических изменений.
В настоящее время существуют два мнения о тонких биомеханизмах токсического действия бензалкония хлорида на клетки слизистой, приводящих к развитию патологических изменений, – развитие токсичности путем апоптоза или некроза. Предполагают наличие бензалкония хлорид-индуцированной программированной гибели клеток, которая реализуется посредством изменения содержания ионов кальция в клетке, Fas-зависимой активации каспаз, митохондриальной дисфункции, гиперпродукции активных форм кислорода, АТФ-зависимой активации Р2Х7 (purinergic receptor P2X, ligand-gated ion channel 7) рецепторов (или известных более как Р2Z-рецепторы клеточного лизиса) и др. Воздействие бензалкония хлорида в концентрации 0,1-0,05% на эпителиальные клетки приводит к их лизису, в концентрации 0,01% он способен индуцировать апоптоз клеток эпителия [13].
Снижение цилиотоксического эффекта бензалкония хлорида возможно путем введения в состав лекарственной формы назального деконгестанта специфических увлажняющих компонентов, обладающих цилиопротективным действием. Так, в состав разных лекарственных форм оригинального препарата ксилометазолина (Отривин капли назальные 0,05 и 0,1%; Отривин спрей назальный дозированный 0,1%; Отривин спрей назальный дозированный 0,1% с ментолом и эвкалиптом, компания «ГлаксоСмитКляйн Хелскер») введены увлажняющие компоненты – гипромеллоза и сорбит, которые снижают цилиотоксическое действие бензалкония хлорида.
Гипромеллоза (hypromellosum) – эффективный увлажняющий компонент, который защищает эпителий, оказывает смазывающее и смягчающее действия, а также восстанавливает, стабилизирует клетки эпителия.
Сорбит (sorbitum) – органическое соединение (шестиатомный спирт); имеет определенные преимущества в фармакологическом, микробиологическом и технологическом аспектах перед другими углеводами. Сорбит (помимо оказания увлажняющего действия) – оптимальная дисперсионная среда при технологическом производстве лекарственной формы.
Анализируя вышеизложенное, можно сделать вывод, что оптимальным назальным деконгестантом (по таким критериям, как эффективность и безопасность) является ксилометазолин.
Оригинальный ксилометазолин (под торговым названием Отривин) содержит усовершенствованный состав вспомогательных веществ во всех представленных на фармацевтическом рынке лекарственных формах.
Следует отметить, что при регистрации воспроизведенных (генерических) форм ксилометазолина стандартный тест на растворимость, обязательный для пероральных лекарств (таблетка, капсулы, драже и др.), не проводится ввиду особенности лекарственной формы. Проведение биоэквивалентности также невозможно ввиду того, что АФИ ксилометазолина не попадает в системный кровоток. В связи с этим можно предположить, что 100% экстраполяция доказательной базы Отривина на генерические аналоги невозможна.
Более 300 исследований, доступных на сегодняшний день на международном медицинском ресурсе PubMed [14], посвящены фармацевтическому, доклиническому и клиническому исследованию оригинального ксилометазолина (Отривин); первые 7 исследований были проведены в 1978 г. За прошедшие десятилетия с высоким уровнем доказательности подтверждена эффективность основного компонента препарата Отривин – ксилометазолина.
По многочисленным данным, подтвержденным проведением дополнительной компьютерной и магнитно-резонансной томографии, применение Отривина уже через несколько минут вызывает значительное уменьшение размеров нижних и средних носовых раковин у пациентов с ринитами разной этиологии, уменьшение отека в области решетчатой воронки и остеомеатального комплекса. Установлены противовоспалительный и антиоксидантный эффекты разных лекарственных форм Отривина, реализующиеся через блок синтеза фермента NO-синтетазы [15].
В исследовании R. Eccles [16] у пациентов с инфекционным ринитом не только подтверждены высокая эффективность и хорошая переносимость Отривин спрея 0,1%, но и отмечена высокая продолжительность фармакологического эффекта препарата (до 12 ч).
В исследовании V. Joganathan, B. Beigi (2018) [17] Отривин спрей 0,05% применяли у детей в возрасте 1-6 лет с целью подготовки к операции на слезных протоках. Было обнаружено, что интраназальное применение Отривина для предакриматической хирургии у детей младшего школьного возраста является эффективным и безопасным методом терапии. Авторы отмечают полное отсутствие как местных, так и возможных системных негативных реакций.
Для взрослых пациентов предварительное использование Отривин спрея 0,1% значительно оптимизирует проведение назотрахеальной интубации [18].
Особенно хотелось бы отметить исследование С. В. Морозовой, Л. А. Топоркова (2019) [19], в котором представлен метаанализ клинической доказательности различных лекарственных форм Отривина. Авторы исследования делают вывод, что препараты Отривин Увлажняющая формула, Отривин Ментол, Отривин Комплекс являются эффективными и хорошо переносимыми средствами для устранения отека в полости носа и уменьшения выделений из носа, а также профилактики возникновения осложнений риносинусита. Применение данных назальных деконгестантов значительно улучшает обонятельную функцию пациентов.
Выводы
АФИ ксилометазолин обладает неоспоримыми преимуществами перед другими АФИ группы назальных деконгестантов, так как (благодаря уникальной структуре молекулы) практически не адсорбируется через слизистую носа, следовательно, не оказывает системных побочных реакций при применении; имеет оптимальную продолжительность действия (более 8 ч); практическое отсутствие особых указаний подтверждает высокую безопасность АФИ, его хорошую совместимость с другими лекарственными препаратами.
Оригинальный ксилометазолин, зарегистрированный под торговым названием Отривин, имеет уникальный состав вспомогательных веществ в лекарственных формах. В отличие от других назальных деконгестантов, цилиотоксическое действие которых усиливает наличие консерванта-антисептика бензалкония хлорида, Отривин содержит специальные увлажняющие компоненты, нивелирующие токсическое действие бензалкония хлорида.
Эффективность и безопасность Отривина (оригинального ксилометазолина) подтверждены масштабной доказательной базой, что делает его применение клинически обоснованным для разных групп пациентов.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 19 (488), 2020 р.
СТАТТІ ЗА ТЕМОЮ Пульмонологія та оториноларингологія
Реімбурсація – це повне або часткове відшкодування аптечним закладам вартості лікарських засобів або медичних виробів, що були відпущені пацієнту на підставі рецепта, за рахунок коштів програми державних гарантій медичного обслуговування населення. Серед громадськості програма реімбурсації відома як програма «Доступні ліки». Вона робить для українців лікування хронічних захворювань доступнішим....
Хронічна кропив’янка (ХК) – це патологія, яка характеризується рецидивними нестійкими висипаннями з/без ангіоневротичного набряку, які виникають мало не щодня впродовж більш як 6 тиж [1]. Розрізняють два варіанти ХК – хронічна індукована кропив’янка (ХІК), або фізична кропив’янка, зумовлена певними фізичними подразниками, такими як тиск, тепло або холод, і більш поширена хронічна спонтанна кропив’янка (ХСК), яка розвивається у 80-90% випадків і характеризується відсутністю відомих екзогенних чинників і причин [2]. На це захворювання страждає від 0,5 до 1% населення світу, переважно особи жіночої статі [3]. Повторні симптоми часто призводять до порушень сну та чинять виражений негативний вплив на якість життя (QoL) [4]. ...
Риносинусит (РС) незмінно потрапляє до десятки найпоширеніших діагнозів в амбулаторній лікарській практиці та посідає 5-те місце серед захворювань, щодо яких призначається антибактеріальна терапія [1]. Симптоми гострих РС маніфестують тоді, коли уражаються слизові оболонки приносових пазух і порожнини носа. Оскільки слизова оболонка носа та приносових пазух – єдине ціле, гострий запальний процес уражатиме ці слизові оболонки, а ізольоване запалення слизової оболонки порожнини носа чи будь-якої з приносових пазух може визначатися при хронічних захворюваннях [2]. Це обґрунтовує доцільність використання терміна «РС». ...
Застуда та інші інфекції дихальних шляхів – актуальна проблема охорони здоров’я через високий рівень захворюваності, що перевищує такий інших інфекційних патологій. З метою підвищення кваліфікації лікарів загальної практики та обміну досвідом з актуальних питань лікування інфекційних захворювань у лютому була проведена науково-практична конференція «Академія сімейного лікаря. Для кого небезпечні сезонні інфекції? Загроза сезонних інфекцій. Погляд пульмонолога, інфекціоніста, алерголога, ендокринолога, кардіолога, педіатра» за участю провідних вітчизняних спеціалістів-практиків....