Метааналіз даних щодо впливу статинів на перебіг COVID‑19
Із моменту початку нової пандемії коронавірусної хвороби 2019 р. було багато дискусій щодо перепрофілювання наявних препаратів для лікування COVID‑19, одними з яких є статини. C.S. Kow та S.S. Hasan (2020) провели метааналіз з метою узагальнення доступних на сьогодні даних щодо впливу статинів на клінічний перебіг COVID‑19. Отримані результати опубліковані у виданні The American Journal of Cardiology (2020; 134: 153‑155).
Існують дві протилежні точки зору стосовно впливу статинів на клінічний перебіг COVID‑19. Так, при коронавірусній хворобі може спостерігатися порушення регуляції білка гена мієлоїдного диференціювання первинної відповіді (MYD) 88-го шляху, що призводить до тотального запалення (Yuan, 2015; Yuan et al., 2014). Цей патогенетичний механізм асоціювався з поганим прогнозом при інших коронавірусних інфекціях. Статини є відомими інгібіторами MYD88 і можуть стабілізувати рівень MYD88 при зовнішніх стресах, що дозволяє припустити їхню роль у захисті пацієнтів із COVID‑19 від розвитку пригнічувальних запальних реакцій (Totura et al., 2015). Крім того, відомо, що статини експериментально підвищують експресію ангіотензинперетворювального ферменту 2-го типу (АПФ-2) і тому здатні виконувати захисну функцію щодо пошкодження легень, викликаного коронавірусом (Li et al., 2013).
З іншого боку, статини викликають дефіцит вмісту ендогенного холестерину в клітинах, що призводить до посилення регуляції рецепторів ліпопротеїнів низької щільності. Своєю чергою це зумовлює постійне включення екзогенного холестерину в клітинну мембрану і подальше утворення множинних ліпідних плотів, що може підвищувати доступність для коронавірусів (Shresta et al., 2020). E.B. Thorp та T.M. Gallagher (2004) стверджують, що статини здатні спричиняти розвиток тяжчого перебігу COVID‑19 через активацію інфламасомного шляху при гострому респіраторному дистрес-синдромі, що зумовлює підвищення рівня прозапального інтерлейкіну‑18 і подальшого цитокінового шторму (Goldstein et al., 2020; Rogers et al., 2019).
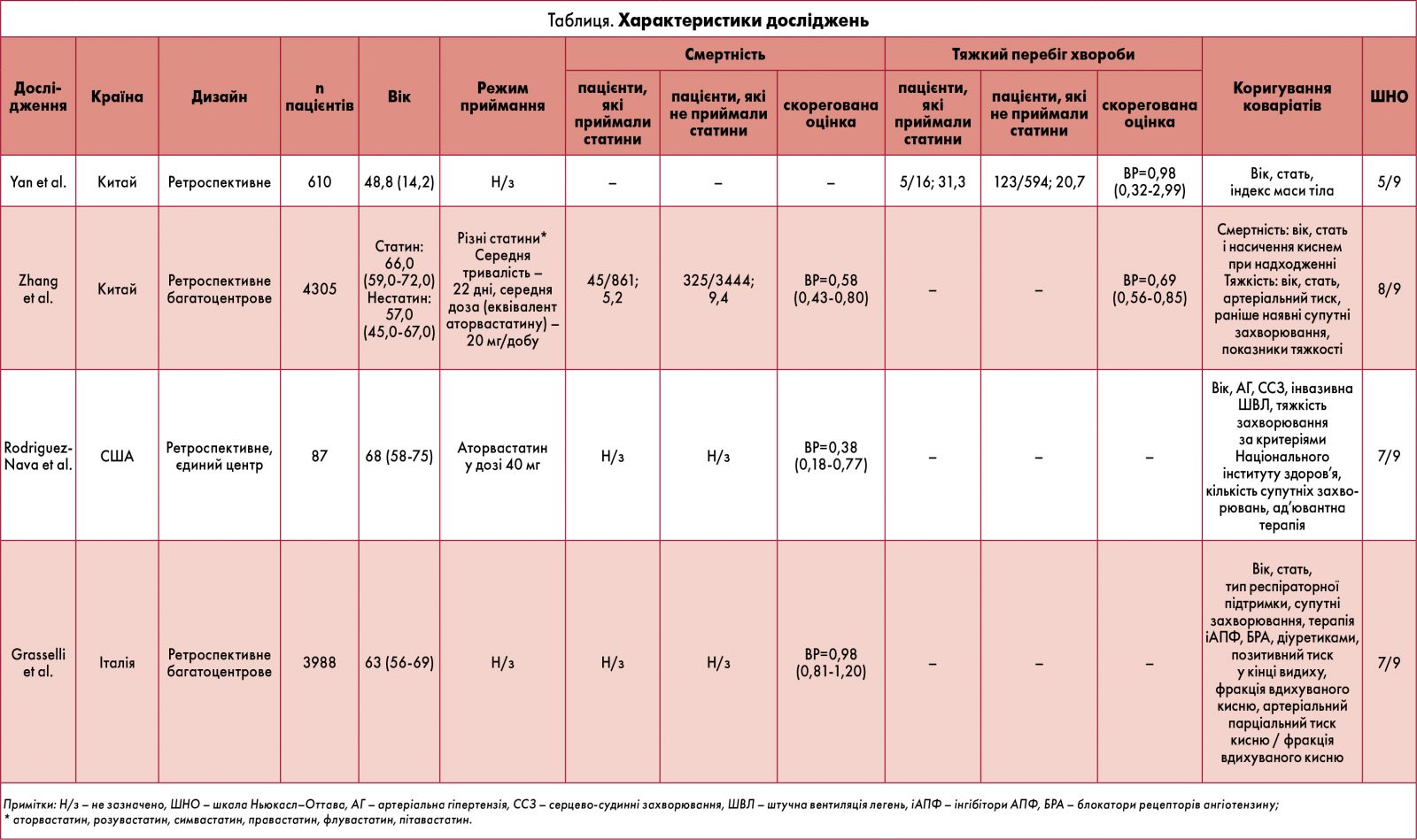
Щоб узагальнити наявні дані про вплив статинів на клінічні результати COVID-19, C.S. Kow та S.S. Hasan (2020) провели метааналіз досліджень. Були враховані дані пацієнтів із підтвердженим COVID‑19 для порівняння ризику тяжких захворювань та/або смертності серед осіб, що отримували статини, порівняно з тими, хто їх не приймав. Внаслідок пошуку даних було виявлено 274 потенційні роботи. Після дедуплікації та застосування критеріїв прийнятності до метааналізу включили чотири дослідження із загальною кількістю 8990 хворих на COVID‑19. Характеристики дослідження наведені в таблиці.
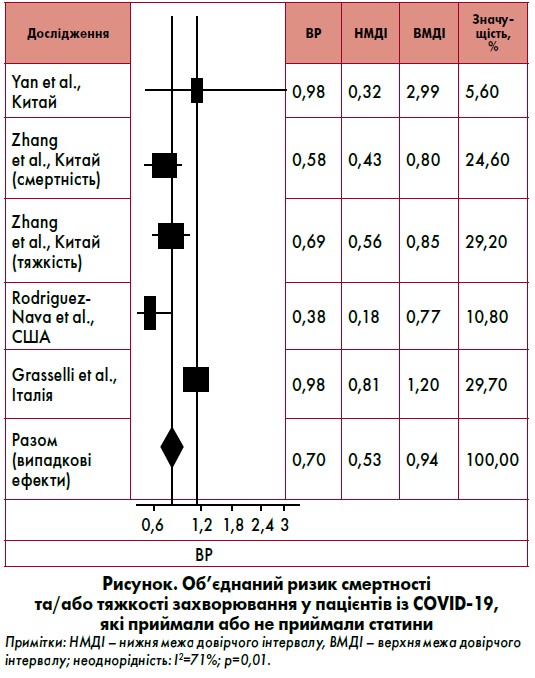 Об’єднаний аналіз виявив достовірно нижчий ризик тяжкого захворювання або смерті в осіб із COVID‑19 при застосуванні статинів (об’єднаний відносний ризик [ВР] 0,70; 95% ДІ 0,53‑0,94) порівняно з тими, хто не отримував даних препаратів (рисунок). Поточні результати свідчать про зменшення кількості тяжких чи летальних наслідків на 30% і дискредитують припущення про шкоду використання статинів у пацієнтів із COVID‑19.
Об’єднаний аналіз виявив достовірно нижчий ризик тяжкого захворювання або смерті в осіб із COVID‑19 при застосуванні статинів (об’єднаний відносний ризик [ВР] 0,70; 95% ДІ 0,53‑0,94) порівняно з тими, хто не отримував даних препаратів (рисунок). Поточні результати свідчать про зменшення кількості тяжких чи летальних наслідків на 30% і дискредитують припущення про шкоду використання статинів у пацієнтів із COVID‑19.
Відкритою лишається низка питань щодо режиму застосування статинів для лікування COVID‑19, хоча, за наявними даними, статинотерапія середньої та високої інтенсивності може бути ефективною. Необхідне проведення додаткових проспективних досліджень, щоб підтвердити отримані науковцями висновки.
Експертна думка
Статини як ефективна допомога у виживанні хворих на COVID‑19
Олена Акіндинівна Коваль, д. мед. н., професорка кафедри внутрішньої медицини 3 Дніпропетровської медичної академії МОЗ України зауважила, що на сьогодні були відсутні чіткі клінічні докази із приводу того, що статини є безперечно корисними для хворих на COVID‑19. Тому проведений високоякісний метааналіз наявних даних, що охопплює доволі велику когорту пацієнтів, є вкрай актуальним.
.jpg) Але ще раніше, починаючи з квітня 2020 р., аналізуючи дані з лікарень та лабораторій, вже формувалося певне розуміння впливу статинів на перебіг COVID-19. Це давало можливість дійти низки висновків, що наразі підтвердилися результатами зазначеного метааналізу. Тож на сьогодні існують щонайменше чотири групи причин, що вказують на важливість статинотерапії.
Але ще раніше, починаючи з квітня 2020 р., аналізуючи дані з лікарень та лабораторій, вже формувалося певне розуміння впливу статинів на перебіг COVID-19. Це давало можливість дійти низки висновків, що наразі підтвердилися результатами зазначеного метааналізу. Тож на сьогодні існують щонайменше чотири групи причин, що вказують на важливість статинотерапії.
По-перше, наявне супутнє серцево-судинне захворювання (ССЗ) або цукровий діабет (ЦД) є важливими факторами ризику ускладненого перебігу чи несприятливих наслідків COVID‑19. Так, було проведене дослідження за участю 138 тяжкохворих, госпіталізованих у відділення інтенсивної терапії з COVID‑19, серед яких 25% мали ССЗ порівняно з 10,8% (p=0,04) у звичайних відділеннях, та, відповідно, ЦД мали 22,2 і 5,9% (p=0,009). В іншому випробуванні з-поміж 191 померлого ЦД був виявлений у 31% порівняно з 14% серед тих, хто вижив (p=0,0051). Аналогічно щодо ішемічної хвороби серця (ІХС): 24 та 1% (p<0,0001) відповідно. Ці дані також підтверджено у великій когорті з 1099 хворих. ЦД мали 16,2% осіб у тяжкому стані та 5,7% – нетяжких пацієнтів, ІХС – 5,8 і 1,8% відповідно.
По-друге, більшість несприятливих серцево-судинних подій у пацієнтів із ССЗ або ЦД та COVID‑19 можуть бути попереджені статинами. Тому такі хворі обов’язково мають отримувати статинотерапію для запобігання розвитку серцево-судинних подій, а також зниження ризику тяжкого перебігу чи смерті від ускладнень COVID‑19.
По-третє, починаючи з 2000 р., доступні результати доволі глибоких попередніх досліджень щодо можливостей статинів впливати на імунну відповідь загалом та покращувати перебіг і наслідки респіраторних вірусних інфекцій, включно із SARS-CoV.
По-четверте, наявні епідеміологічні дані стосовно зниження частоти розвитку вірусних пневмоній на тлі застосування статинів.
Так, у масштабному когортному дослідженні (n=76 232) було доведене зниження ризику смерті від хронічних обструктивних захворювань легень і грипу в пацієнтів, які отримували лікування статинами, порівняно з тими, хто їх не приймав. Аналіз даних іншого випробування у 3043 госпіталізованих хворих із сезонним грипом (2007‑2008 рр.) показав невеликий, але статистично достовірний захисний ефект статинів у зменшенні летальних випадків через грип. У 1520 пацієнтів, які поступили до стаціонара із приводу пандемічного грипу H1N1 (2009 р.), також спостерігався невеликий, але клінічно значущий протективний вплив статинів.
У 2014 р. під час спалаху вірусної лихоманки Ебола у вогнищі епідемії в Сьєрра-Леоне в Африці була спроба лікування статинами. Зокрема, 100 пацієнтів отримували розувастатин у комбінації з БРА, після чого лікарі відмічали значне поліпшення їхнього стану. Незважаючи на те, що контрольованого дослідження не проводили, дані були опубліковані як клінічні спостереження.
На даний час на тлі пандемії COVID‑19 все більшу увагу стала привертати імунологічна протидія впливу вірусу SARS-CoV2 за допомогою різноманітних, а не лише специфічних імунотропних препаратів, як-то тоцилізумаб, довенні імуноглобуліни тощо. Чи є підстави вважати такими і статини, адже їхні протизапальні ефекти (зниження СРБ) загальновідомі? Так, підстави є. Ще 2000 р. група імунологів S.S. Kwak et al. із Базельского інституту імунології (Швейцарія) виявила, що статини впливають на експресію молекул головного комплексу гістосумісності ІІ типу і прямо залучені в активацію Т-лімфоцитів, а також інтенсивність їхньої відповіді на гама-інтерферон. До того ж вони є своєрідними супресорами-модуляторами клітинної імунної відповіді, але за умов її активації вірусами або антигенами трансплантата. За цим самим механізмом відбувається активація ендотеліальних клітин та макрофагів. Таким чином, зазначені властивості статинів можна використовувати для зменшення гіперактивації імунної відповіді на SARS-CoV‑2 та подолання подальших автоімунних розладів (наприклад, синдрому Кавасакі, про що вже доповідали британські лікарі).
Цьогоріч у жовтні S. Copsel et al. (2020) опублікували дані щодо ефекту статинів на регуляторну субпопуляцію Т-лімфоцитів (T-reg), активність яких важлива для запобігання розвитку автоімунних захворювань та сприяє протизапальному потенціалу тканинного середовища. Не останню роль відіграє вплив статинів на класичний шлях активації гуморальної відповіді через NF-kB і, певною мірою, – на цитокіновий шторм із пригніченням експресії гена MYD88, що значно посилюється при впливі коронаровірусу SARS-CoV‑2. При цьому виробляється велика кількість інтерферону 1-го типу з розвитком подальшого нерегульованого системного запалення. Особливо значущим є факт, що вплив статинів на всі перелічені механізми відбувається за умов їхньої активації, без пригнічення у разі відсутності подразників, тобто є імуномодулюючим.
Слід зважати також на додаткові механізми, а саме безпосередній вплив на АПФ 2-го типу та зменшення виділення агресивних прозапальних лейкотрієнів 4-ї серії за рахунок зниження рівня холестерину в мембранах не лише печінкових, але й імунних клітин та фагоцитуючих лейкоцитів.
Ще один важливий механізм впливу, максимально виражений у розувастатину, – це протидія формуванню тромболейкоцитарних агрегатів і роз’єднання тим самим процесів запалення та тромбоутворення, що є дійсно критичним для перебігу COVID‑19. Механізми антитромботичного впливу розуватстатину стали відомі не так давно. Але клінічні підтвердження були отримані значно раніше – у випробуванні JUPITER (2004) та найбільшому метааналізі Kunutsor et al. (2017), до якого увійшло 13 когортних (n=3 148 259!) і 21 плацебо-контрольоване дослідження (n=118 464), зі зниженням венозного тромбоемболізму до 25%, з максимальним впливом розувастатину – до 43%.
Також слід зазначити, що, відповідно до найбільших американських баз даних стосовно хворих на COVID‑19 з ураженням печінки та гіперферментемією, не виключене призначення статинів у гострому періоді, якщо рівні трансаміназ не перевищують норму втричі. З цих міркувань найбезпечнішим є призначення розувастатину, оскільки він має мінімальний метаболізм у печінці та ризик взаємодії з іншими ліками.
Дуже важливими є факт високої безпечності сучасних потужних статинів та наявність їхніх якісних генериків, таких, наприклад, як Роксера®. Це дозволяє більш ефективно та раціонально використовувати обмежені ресурси охорони здоров’я в період пандемії.
Наразі спеціальні клінічні випробування впливу статинотерапії на захист від вірусної пневмонії не проводили. Проте багато експертів стверджують, що наявних даних вже достатньо, щоб присвоїти лікуванню статинами рекомендацію категорії С.
Таким чином, обов’язково слід продовжувати застосування статинотерапії, якщо хворий вже її отримує. Крім того, необхідно призначати статини пацієнтам, що їх потребують, якомога раніше. Важливо використовувати хоча б середні, а краще високі дози препаратів у гострому періоді, що становить 40‑80 мг для аторвастатину та 20‑40 мг для розувастатину. Якщо існує ризик взаємодії з іншими ліками, наприклад при антибіотикотерапії, доцільно використовувати розувастатин.
Список літератури знаходиться в редакції
Підготувала Наталія Нечипорук
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 5 (72) 2020 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....