Хронічне відторгнення ниркового алотрансплантата: діагностика, профілактика, лікування
За матеріалами конференції
 Серед причин втрати алотрансплантата нирки основне місце посідає хронічне відторгнення трансплантата (30-80% за даними різних авторів). Тому пошук дієвих форм профілактики та лікування цього ускладнення є одним з найбільш актуальних завдань сучасної трансплантологічної науки. Саме на цьому питанні в рамках науково-практичної онлайн-конференції «Нефрологія, діаліз, трансплантація нирки: up to date», яка відбулася 17-18 вересня 2020 р., зупинився у своїй доповіді та представив результати власних досліджень ефективності та безпечності різних методів профілактики і лікування цієї патології професор ДУ «Національний інститут хірургії і трансплантології ім. О О. Шалімова НАМН України», доктор медичних наук Рубен Овакимович Зограб’ян.
Серед причин втрати алотрансплантата нирки основне місце посідає хронічне відторгнення трансплантата (30-80% за даними різних авторів). Тому пошук дієвих форм профілактики та лікування цього ускладнення є одним з найбільш актуальних завдань сучасної трансплантологічної науки. Саме на цьому питанні в рамках науково-практичної онлайн-конференції «Нефрологія, діаліз, трансплантація нирки: up to date», яка відбулася 17-18 вересня 2020 р., зупинився у своїй доповіді та представив результати власних досліджень ефективності та безпечності різних методів профілактики і лікування цієї патології професор ДУ «Національний інститут хірургії і трансплантології ім. О О. Шалімова НАМН України», доктор медичних наук Рубен Овакимович Зограб’ян.
Ключові слова: трансплантація нирки, хронічне відторгнення ниркового алотрансплантата, плазмаферез, ритуксимаб
Удосконалення імуносупресивної терапії, діагностики вірусних інфекцій, подальша розробка імунологічного та морфологічного моніторингу дали можливість значно покращити результати операції трансплантації нирки. Так, виживання ниркового алотрансплантата (НАТ) протягом першого року після оперативного втручання на сьогоднішній день перевищує 90%. У той же час його віддалені результати залишаються на незадовільному рівні. Річна втрата НАТ становить ≥ 3-5% і до 10-го року підвищується до 50 %.
Найбільш поширеними причинами втрат НАТ у віддаленому післятрансплантаційному періоді є:
- хронічна дисфункція НАТ, тобто прогресуюче порушення функції пересадженої нирки;
- серцево-судинна патологія;
- інфекційні ускладнення;
- інші причини.
Причин хронічної дисфункції НАТ є досить багато, серед яких і нефротоксичність інгібіторів кальциневрину, і повернення та поява de novo гломерулонефриту, і поліомавірусна нефропатія, і рецидивуюча сечова інфекція, і неспецифічні зміни, проте основне місце (30-80%) посідає хронічне відторгнення трансплантованої нирки.
Хронічна реакція відторгнення характеризується повільним перебігом персистуючого процесу пошкодження трансплантованої нирки імунними механізмами. У патогенезі хронічного відторгнення можуть відігравати роль як клітинні, так і гуморальні механізми. Роль клітинних механізмів підтверджується виявленням активованих CD8+ та CD4+ лімфоцитів, макрофагiв, які інфільтрують паренхіму та судинну стінку.
Гіперпродукція цитокінів активованими лімфоцитами призводить до хронічного запалення з наступним розвитком фіброзу. Фіброз, проліферація та гіперплазія гладком’язових клітин розвиваються і в судинах, що призводить до порушення внутрішньониркового кровотоку, своєю чергою посилюючи фіброз. Цитокіни також зумовлюють апоптоз епітеліальних клітин, їх мезенхімальну трансформацію у фібробласти та прискорене старіння.
При хронічному антитіло-опосередкованому відторгненні невиявлені передіснуючі донор-специфічні антитіла, які утворилися після трансплантації, відкладаються на ендотелії капілярів. Пошкодження ендотелію викликає гіпертрофію клітин гломерулярних і перитубулярних капілярів, субендотеліальні відкладення фібрилярного матеріалу, розширення та подвоєння гломерулярних базальних мембран або інтерпозицію мезангіальних клітин (ефект двоконтурності базальних мембран, який ми бачимо при морфологічному дослідженні біоптату).
Підтвердження участі гуморальних механізмів алоімунної відповіді в патогенезі хронічного відторгнення полягає в наступному:
- виявлення лінійних депозитів активованого компонента комплементу С4d та молекул імуноглобулінів, фіксованих до базальної мембрани перитубулярних і гломерулярних капілярів;
- виявлення антитіл проти HLA-антигенів (антигенів до головного комплексу гістосумісності) донора в крові реципієнта;
- виявлення тканинних антитіл (до компонентів базальних мембран) в крові реципієнта.
Стратегічні напрямки терапії хронічної реакції відторгнення НАТ
Важливу роль у патогенезі хронічного відторгнення НАТ відіграють В-клітини, які продукують антитіла до антигенів трансплантата. Попередниками плазматичних клітин, які власне і продукують антитіла, є В-лімфоцити. Один з основних лікувальних напрямків – ліквідація активації В-лімфоцитів за допомогою введення ритуксимабу, препарату анти-CD20 антитіл, які виводять з кровотоку В-клітини. Безпосередньо вплинути на плазматичні клітини можна за допомогою бортезомібу, який є похідним борної кислоти, а за допомогою плазмаферезу можна видалити вже циркулюючі у кровотоці антитіла. Ще один препарат для лікування хронічного відторгнення НАТ – екулізумаб, який є антитілом проти С5 компонента комплементу, що перешкоджає утворенню комплексу мембранної атаки.
Професор Р.О. Зограб’ян та співавт. провели випробування, метою якого було виділення груп пацієнтів з різними типами хронічного відторгнення ниркових трансплантатів на основі морфологічного дослідження біоптатів останніх, оцінка ефективності застосування терапевтичних схем лікування у пацієнтів різними типами хронічного відторгнення, а також вибір оптимальної схеми лікування для кожного окремого типу хронічної реакції відторгнення.
Для досягнення мети були поставлені такі завдання:
- виявлення факторів ризику розвитку хронічної реакції відторгнення НАТ;
- вивчення морфологiчних проявів хронічної реакції відторгнення НАТ;
- розробка підходів до лікування хронічної реакції відторгнення НАТ;
- оцінка ефективності розроблених методів профілактики, діагностики та лікування хронічного відторгнення трансплантата.
При аналізі факторів ризику хронічного відторгнення НАТ виявлено, що особливо значущими з них є повторні ранні кризи відторгнення та пізні кризи відторгнення. Важливим є вибір режиму імуносупресивної терапії. Так, пацієнти, які отримують циклоспорин, мають в ранньому післятрансплантаційному періоді більше кризів гострого відторгнення, ніж ті, які лікуються такролімусом. Недостатній рівень імуносупресанту в крові (нижче терапевтичного діапазону), який є результатом недотримання хворими призначеного лікарем режиму терапії, також підвищує ризик хронічного відторгнення. Важливий чинник, що впливає на результат трансплантації нирки, – вік донорів, а саме старших за 65 років, і це є суттєвим фактором ризику хронічного відторгнення НАТ. Активна цитомегаловірусна інфекція у післяопераційному періоді також може бути причиною розвитку хронічного відторгнення.
Морфологічна характеристика біоптатів НАТ у пацієнтів з хронічною дисфункцією останнього показує, що на першому місці серед причин цього явища стоїть хронічна реакція відторгнення (59%); далі – неспецифічні зміни, такі як інтерстиціальний фіброз і канальцева атрофія, нефротоксичність інгібіторів кальциневрину, повернений та de novo гломерулонефрит, інфекційно-запальні захворювання трансплантата, ВК-вірусна нефропатія НАТ.
Морфологічні прояви хронічного відторгнення НАТ
Під час дослідження за морфологічними проявами було виділено три форми хронічного відторгнення НАТ (n=49).
1. Антитіло-опосередковане відторгнення (ХАОВ) – 59,5% (n=29), яке мало наступні ознаки:
- потовщення базальних мембран клубочків із формуванням подвійних контурів гломерулярних мембран;
- гломеруліт;
- фіброз інтерстицію;
- фокальна атрофія канальців;
- фіброз інтими артерій з розривами внутрішньої еластичної мембрани.
2. Т-клітинно-опосередковане відторгнення (ХТкОВ) – 28,6 % (n=14), проявами якого були:
- фокальна атрофія канальців;
- фіброз строми;
- хронічна ішемічна гломерулопатія (потовщення стінки клубочків, гломерулосклероз);
- фіброз інтими артерій з розривом внутрішньої еластичної мембрани;
- мононуклеарна інфільтрація стінок артерій.
3. Змішана форма хронічного відторгнення (ЗФХВ) – 11,9% (n=6).
У рамках даного дослідження була вивчена ефективність різних схем лікування хронічного відторгнення НАТ у 49 реципієнтів віком 18-56 років (28 чоловіків, 21 жінка). Діагностика хронічного відторгнення ґрунтувалась на клініко-лабораторних даних (поступово прогресуюча дисфункція НАТ) та даних біопсії трансплантата, за результатами якої виділяли ХАОВ, ХТкОВ та ЗФХВ.
На основі морфологічних типів хронічного відторгнення було сформовано три досліджувані групи: І – 29 реципієнтів з ХАОВ, ІІ – 14 реципієнтів з ХТкОВ, ІІІ – 6 реципієнтів із 3ФХВ.
Лікування хронічного відторгнення НАТ
Група пацієнтів з ХАОВ (n = 29)
- Середній термін після трансплантації на момент хронічної реакції відторгнення (ХРВ) – 3,2 роки.
- Рівень креатиніну на момент ХРВ – 160-290 мкмоль/л.
- Рівень артеріального тиску (АТ) – 140-170/90-100 мм рт. ст.
- Протеїнурія – 0,6-9,4 г/добу.
Із 29 пацієнтів:
- циклоспорин А (CsA) отримували 18;
- такролімус (Тас) – 11;
- у 60% хворих рівень CsA був на 30% нижче референтних значень;
- у 30% осіб рівень Тас був на 20% нижче референтних значень.
Призначено такі лікарські засоби:
- плазмаферез – 3-5 сеансів;
- анти-CD20 моноклональні антитіла – ритуксимаб 375 мг/м2;
- внутрішньовенне введення імуноглобуліну – 0,5 г/кг;
- підвищення базової дози стероїдів;
- корвітин 0,5 г внутрішньовенно крапельно № 10, дипіридамол 200 мг/доб, нікотинову кислоту.
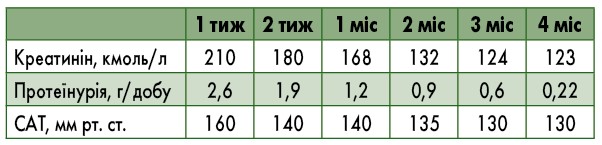
У 20 (69%) пацієнтів із 29 спостерігалось зниження рівня креатиніну протягом 4 міс:
- у 3 хворих рівень креатиніну знизився на 25% від вихідного значення (10 %);
- в 11 – рівень креатиніну знизився на 35% від вихідного значення (38%);
- у 6 – рівень креатиніну нормалізувався повністю (21%).
У 9 (31%) осіб із 29 був відсутній терапевтичний ефект.
Група пацієнтів з ХТкОВ (n=14)
- Термін після операції на момент ХРВ – 3,2 року.
- Рівень креатиніну на момент ХРВ – 160-320 мкмоль/л.
- Рівень АТ – 140-160/90-100 мм рт. ст.
- Протеїнурія – 0,4-3,5 г/добу.
Із 14 пацієнтів:
- CsA отримували семеро;
- Tac – семеро;
- рівень CsA y 53% реципієнтів був на 25% нижче референтних значень;
- рівень Тас був в межах референтних значень.
Призначено:
- пульс-терапію стероїдами (солу-медрол) 1-2 г або підвищення рівня базової дози до 32 мг;
- у стероїдорезистентних випадках антитимоцитарний імуноглобулін (АТГ, тимоглобулін) дозою 5-6 мг/кг;
- корвітин 0,5 г внутрішньовенно крапельно № 10, дипіридамол 200 мг/добу, нікотинову кислоту.
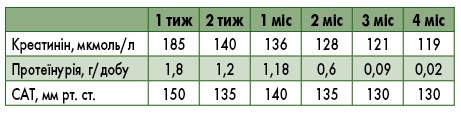
У 10 (71%) осіб із 14 відбулося зниження рівня креатиніну протягом 4 міс:
- у двох хворих рівень креатиніну знизився на 25% від вихідного значення (14%);
- у п’яти – рівень креатиніну знизився на 35% від вихідного значення (36%);
- У трьох – рівень креатиніну нормалізувався повністю (21%).
У 4 (29%) пацієнтів був відсутній терапевтичний ефект.
Група пацієнтів із ЗФХВ (n=6)
- Термін після операції на момент ХРВ – 1,5 року.
- Рівень креатиніну на момент ХРВ – 180-240 мкмоль/л.
- Рівень АТ – 140-180/90-100 мм рт. ст.
- Протеїнурія – 1,3-5,4 г/добу.
Із шести пацієнтів:
- CsA отримували чотири;
- Тас – два;
- рівень CsA y 50% хворих був на 25% нижче референтних значень;
- рівень Тас у 50% реципієнтів був на 15% нижче референтних значень.
Призначено:
- плазмаферез 3-6 сеансів;
- ритуксимаб 375 мг/м2;
- внутрішньовенне введення імуноглобуліну 0,5 г/кг;
- тимоглобулін, АТГ;
- пульс-терапію солу-медролом;
- корвітин 0,5 г внутрішньовенно крапельно № 10, дипіридамол 200 мг/добу, нікотинову кислоту.
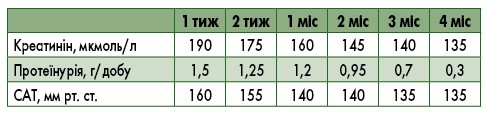
У трьох (50%) випадках із шести спостерігалася зупинка прогресування хронічної дисфункції НАТ, у трьох (50%) випадках – відсутність ефекту від терапії.
Висновки
Факторами ризику розвитку ХРВ НАТ є:
- вік донора старшого за 65 років;
- вік реципієнта молодшого за 30 років;
- режим імуносупресивної терапії:
- вибір інгібітора кальциневрину;
- субтерапевтичний рівень інгібітора в крові;
- повторні ранні та пізні кризи гострого відторгнення;
- активна цитомегаловірусна інфекція протягом перших 6 міс після операції.
За результатами біопсії хронічне відторгнення в 59% випадків є причиною дисфункції трансплантата.
Визначено три морфологічні форми хронічного відторгнення НАТ:
- хронічне антитіло-опосередковане відторгнення – 59,5%;
- хронічне клітинно-опосередковане відторгнення – 28,6%;
- змішана форма – 11,9%.
Отже, вибір методики лікування хронічного відторгнення ниркового трансплантата залежить від морфологічної форми відторгнення та рівня креатиніну в крові на момент початку лікування і включає проведення плазмаферезу, введення ритуксимабу, внутрішньовенне введення імуноглобуліну та підвищення дози стероїдів або пульс-терапію. У стероїдорезистентних випадках можливе введення тимоглобуліну.
Запропоновані методики лікування хронічного відторгнення дають можливість досягнути позитивного результату в 50-70 % випадків залежно від морфологічної форми відторгнення та рівня креатиніну в крові на момент початку лікування.
Підготувала Анастасія Романова
Тематичний номер «Урологія. Нефрологія. Андрологія» № 4 (21), 2020 р.
СТАТТІ ЗА ТЕМОЮ Нефрологія
Інфекції сечовивідних шляхів (ІСШ) у всьому світі посідають провідне місце серед інфекційних захворювань дорослого населення. Поряд із тим серед фахівців зростає занепокоєння щодо триваючого зростання стійкості бактерій до більшості антибіотиків. Експерти провідних міжнародних товариств наголошують на необхідності розсудливого і виваженого призначення антимікробних препаратів. Про основні принципи раціональної антибіотикотерапії в урології, зокрема при проведенні діагностичних і хірургічних втручань, ми попросили розповісти завідувача відділу відновної урології та новітніх технологій ДУ «Інститут урології ім. акад. О.Ф. Возіанова НАМН України», доктора медичних наук, професора В’ячеслава Миколайовича Григоренка. ...
Процедура трансректальної біопсії простати супроводжується високим ризиком інфекційних ускладнень, тому проведення антимікробної профілактики при цьому втручанні є обов’язковим. Однак зростання антибіотикорезистентності, а також нещодавні рекомендації щодо обмеження призначень фторхінолонів значно звужують спектр можливих варіантів такої профілактики. Міжнародною мультидисциплінарною групою експертів на основі літературних джерел та клінічного досвіду було розроблено ряд настанов стосовно запобігання інфекційним ускладненням при біопсії простати та обґрунтовано доцільність і переваги призначення з цією метою фосфоміцину ...
Кількість людей, які страждають і помирають від вірусного гепатиту В (ВГВ), можна порівняти з кількістю хворих на коронавірусну хворобу 2019 року (COVID‑19), яка наразі викликає велике занепокоєння в усьому світі. Тому вкрай важливим залишається питання передачі вірусу, у тому числі через статеві клітини. Попередніми дослідженнями встановлено, що гени ВГВ, інтегровані в людські сперматозоїди, здатні до реплікації та експресії після передачі ембріонам. Однак досі це явище не було підтверджено клінічними дослідженнями у пацієнтів. Автори вивчали особливості інтеграції ВГВ у геном сперматозоїдів пацієнтів та аналізували можливі клінічні наслідки для потомства ...
За визначенням робочої групи Міжнародного товариства з проблем утримання сечі (ICS), у чоловіків термін «урологічний синдром хронічного тазового болю (СХТБ)» включає хронічний простатит (ХП) або СХТБ (ХП/СХТБ). Серед пацієнтів, які перебувають під амбулаторним спостереженням із приводу простатиту, понад 90% осіб мають діагноз ХП/СХТБ, що свідчить про високу поширеність цього урологічного захворювання в загальній структурі (Yang C.C. et al., 2018). Саме з наявністю ХП пов’язують підвищений ризик розвитку нетримання сечі, доброякісної гіперплазії передміхурової залози (ДГПЗ), запальних процесів сечостатевої системи, утворення каменів, кіст у ПЗ та виникнення раку ПЗ (РПЗ). Адже відомо, що в генезі останнього відіграють роль різні фактори, зокрема ампліфікація та мутація генів, що кодують гени-супресори пухлини, онкогени, а також фактори росту та цитокіни [1, 2]. Учені довели, що інгібування запалення, у тому числі за допомогою нестероїдних протизапальних препаратів (НПЗП), може зменшувати прогресування ХП та опосередковано впливати на зменшення ризику виникнення РПЗ. Водночас потужні анальгетичні властивості НПЗП дозволяють ефективно усувати хронічний тазовий біль та асоційовані з ним симптоми...




