Неінвазивні біомаркери у діагностиці запальних захворювань кишечнику у дітей
 Запальні захворювання кишечнику (ЗЗК) – група хронічних рецидивуючих захворювань, які виникають унаслідок невідповідності імунної відповіді на кишкові коменсальні мікроорганізми у генетично схильних осіб, що призводить до запальної реакції з формуванням виразок у шлунково-кишковому тракті (ШКТ). В останні роки як патогенетичні механізми розглядають роль мікробіому, підвищеної проникності слизової оболонки кишечнику, оксидативного стресу й епігенетики [1]. До ЗЗК належать такі захворювання, як виразковий коліт (ВК) та хвороба Крона (ХК). При ВК запальний процес характеризується безперервним запаленням у слизовому та підслизовому шарі товстої кишки, при ХК трансмуральне сегментарне запалення може уражати весь ШКТ (від ротової порожнини до ануса).
Запальні захворювання кишечнику (ЗЗК) – група хронічних рецидивуючих захворювань, які виникають унаслідок невідповідності імунної відповіді на кишкові коменсальні мікроорганізми у генетично схильних осіб, що призводить до запальної реакції з формуванням виразок у шлунково-кишковому тракті (ШКТ). В останні роки як патогенетичні механізми розглядають роль мікробіому, підвищеної проникності слизової оболонки кишечнику, оксидативного стресу й епігенетики [1]. До ЗЗК належать такі захворювання, як виразковий коліт (ВК) та хвороба Крона (ХК). При ВК запальний процес характеризується безперервним запаленням у слизовому та підслизовому шарі товстої кишки, при ХК трансмуральне сегментарне запалення може уражати весь ШКТ (від ротової порожнини до ануса).
ЗЗК можуть мати загрозливі ускладнення, у тому числі такі, що потребують оперативного втручання, при цих захворюваннях наявний ризик розвитку колоректального раку. Захворюваність на ВК становить 10-20 на 100 000 осіб на рік (у дітей 2,0-6,8 на 100 000 на рік), а на ХК – 5-10 на 100 000 осіб на рік (у дітей 1-8 на 100 000 на рік). При ВК гендерне співвідношення серед дітей становить 1:1, хоча у ранньому віці частіше хворіють хлопчики, а у підлітковому – дівчатка. ВК може дебютувати у будь-якому віці, однак пік захворюваності припадає на підлітковий вік. ХК у дітей діагностують у різному віці, проте переважно в 12-14 років, частіше хворіють хлопчики [1-3].
Клінічні прояви ЗЗК залежать від ділянки ураження ШКТ і дуже часто мають неспецифічний характер, що затримує діагностику цих захворювань. Симптоматика може нагадувати синдром подразненого кишечнику (СПК), целіакію, харчову непереносимість або гастроінтестинальні форми харчової алергії, лактазну недостатність, інфекційну діарею, антибіотикасоційовану діарею (зумовлену Clostridium difficile), паразитози (лямбліоз), мікроскопічний коліт, ВІЛ-ентеропатію, колоректальний рак. Відсутність специфічних клінічних проявів також утруднює диференційну діагностику ХК та ВК, особливо при ураженні товстої кишки. Скарги у пацієнтів із ЗЗК дуже різноманітні і, зокрема, включають [3, 4]:
- абдомінальний біль (при ВК частіше навколо пупка та у лівому нижньому квадранті живота, при ХК – частіше у правому нижньому квадранті живота);
- діарею (без слизу, крові та гною);
- нудоту та блювання (частіше при ХК);
- втрату маси тіла (частіше при ХК з ураженням тонкої кишки внаслідок мальабсорбції та зниження апетиту);
- лихоманку;
- підвищену пітливість;
- втомлюваність (внаслідок запалення, болю та анемії);
- артралгії;
- затримку росту та статевого дозрівання у дітей;
- позакишкові прояви (артрит, увеїт, гепатит);
- діарею криваву, з тенезмами (частіше при ВК);
- ураження періанальної ділянки (нориці, абсцеси) – майже у 50% осіб із ХК;
- запор (при ВК з ураженням прямої кишки).
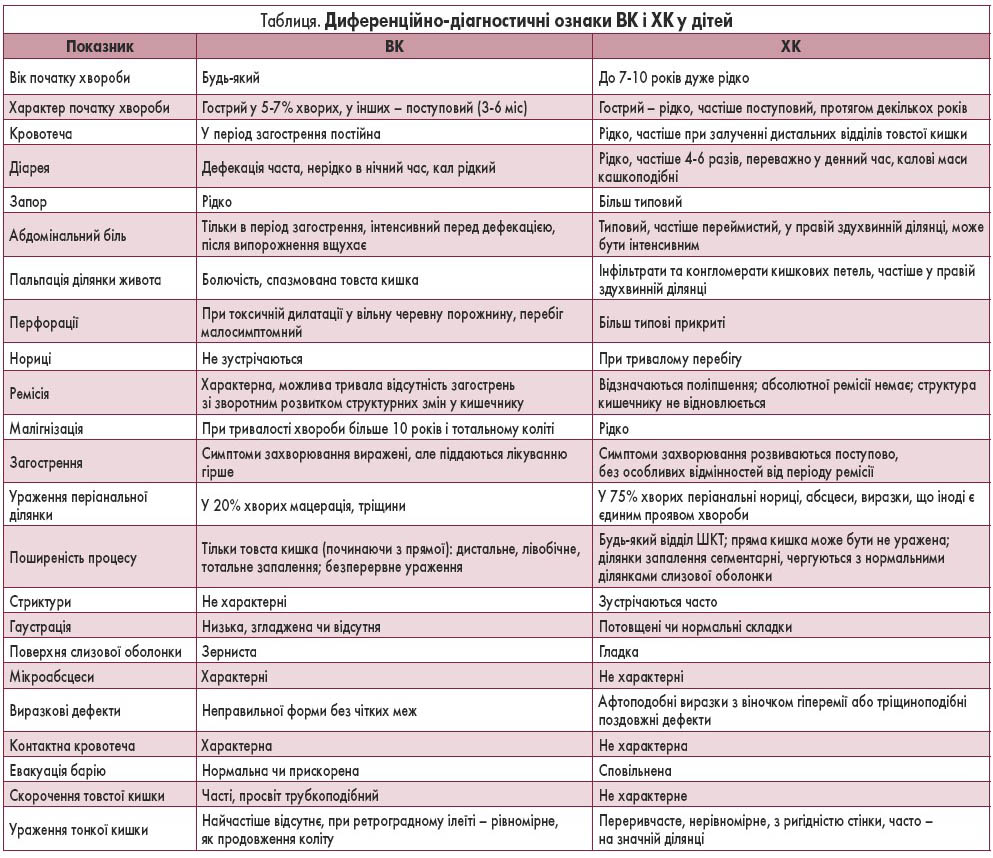
Основні диференційно-діагностичні ознаки ВК і ХК у дітей представлені у таблиці 1.
Незважаючи на те що ендоскопія з біопсією залишається золотим стандартом діагностики ЗЗК, важливим є використання клініцистами біомаркерів запалення у крові, калі, сечі та тканинах кишечнику. Це можуть бути білки, які синтезуються у гострій фазі запалення і пов’язані зі згортанням крові та фібринолізом (протромбін, фібриноген, плазміноген, фактор згортання VIII, компоненти системи комплементу), транспортні білки (гаптоглобін і церулоплазмін), інгібітори протеїназ (α1-антитрипсин та α1-антихімотрипсин), а також цитокіни (фактор некрозу пухлини, інтерферон-β, трансформуючий фактор росту-β, інтерлейкіни-1β, -6, -8, -12, -17 і -23). Крім того, запалення у кишечнику супроводжується посиленим синтезом С-реактивного протеїну, феритину, фібронектину. Реагують і компоненти крові, що призводить до збільшення кількості лейкоцитів, тромбоцитів і ШОЕ, це також є ознакою запалення [5, 6].
Серологічні маркери діагностики ЗЗК включають перинуклеарні антинейтрофільні цитоплазматичні антитіла (pANCA), антитіла проти Saccharomyces cerevisiae (ASCA), антипорин (анти-OmpC), білок зовнішньої мембрани Escherichia coli, флагелін (анти-Cbir1) та анти-Pseudomonas fluorescens (анти-I2). Отримано докази, що наявність pANCA дозволяє диференціювати ВК від ХК, а наявність ASCA має високу специфічність для ідентифікації ХК. Не було виявлено зв’язку позитивного тесту на pANCA з активністю ВК або з ризиком рецидиву. Однак серологічні маркери мають невисоку чутливість, тому лише їх спільне використання може підвищити діагностичний потенціал [7-12].
Як неінвазивний біомаркер ЗЗК широко використовується фекальний кальпротектин (ФК). Кальпротектин – білок активної фази, який є основним білком цитозолю з молекулярної масою 36 кДа, що зв’язує кальцій і цинк та продукується поліморфно-ядерними нейтрофілами, моноцитами і плоским епітелієм (крім епітелію шкіри). Після зв’язування з кальцієм він стає стійким до розщеплення під дією лейкоцитарних і мікробних ферментів. Кальпротектин проявляє протимікробну активність завдяки здатності пригнічувати цинкзалежні ферментні системи та залишається стабільним при кімнатній температурі протягом 4-7 днів, що є його важливою перевогою як лабораторного маркера [13, 14].
Виявлення ФК є надійним, але неспецифічним маркером запалення у ШКТ. Підвищений вміст ФК може бути визначений при харчовій алергії на білок коров’ячого молока, муковісцидозі, дивертикуліті, аденовірусній, ротавірусній, норовірусній діареї, а також сальмонельозі, кампілобактерній інфекції, целіакії, неоплазіях, у пацієнтів з ожирінням, при прийомі протизапальних лікарських засобів та інгібіторів протонної помпи [15-17]. Клінічне значення визначення ФК полягає насамперед у скринінгу ЗЗК у пацієнтів із симптомами ураження ШКТ, а також у контролі активності запального процесу у пацієнтів із ЗЗК [18-23].
Рівень ФК від 30 до 50 мкг/г свідчить про незапальний стан (наприклад СПК), а референтне значення ФК >50 мкг/г найчастіше використовується у літературі та у комерційних тестових наборах ELISA для дорослих та дітей старших 4 років для диференціювання ЗЗК від функціональних захворювань кишечнику [17, 20, 22].
Питання референтного значення ФК у дітей залишається дискусійним, хоча доказово визнано, що рівень ФК у дітей перших років життя значно перевищує такий у дорослих [24-26]. У дітей підвищений рівень ФК спостерігається у ранньому віці, з часом він знижується. Високий рівень ФК у дітей перших місяців життя пов’язують із незрілою бар’єрною функцією кишечнику, що зумовлює підвищену проникність слизової оболонки кишечнику та трансепітеліальну міграцію гранулоцитів. Також виявлена залежність рівня ФК від типу вигодовування. Так, у дітей на грудному вигодовуванні рівень ФК вищий, ніж у дітей на штучному вигодовуванні, що характеризує імуномодулюючий вплив грудного молока на слизову оболонку кишечнику. Крім того, підвищення рівня ФК у дітей можливе при заборі проби калу з підгузка, що пояснюється поглинанням у нього води [27, 28].
Згідно з дослідженнями Oord та співавт., порогові значення ФК у дітей віком до 4 років є значно вищими, ніж у дорослих, і становлять [27]:
- в 1-6 місяців – 538 мкг/г;
- у 6 місяців – 3 роки – 214 мкг/г;
- у 3-4 роки – 75 мкг/г;
- у 4 роки та дорослих – 50 мкг/г.
У дослідженнях F. Li та співавт. наведено визначення рівня ФК у здорових дітей від 0 до 18 місяців [28]:
- в 1-3 місяці – 375,2 мкг/г;
- у 3-6 місяців – 217,9 мкг/г;
- у 6-9 місяців – 127,7 мкг/г;
- в 9-12 місяців – 96,1 мкг/г;
- у 12-18 місяців – 104,0 мкг/г.
Цинлін Чжу та співавт. отримали такі результати дослідження рівня ФК у здорових дітей від 1 до 4 років [29]:
- в 12-24 місяців – 96,14 мкг/г;
- у 24-36 місяців – 81,48 мкг/г;
- у 36-48 місяців – 65,36 мкг/г.
Гендерної різниці не виявлено, та спостерігалася тенденція до зниження рівня ФК з віком.
Опубліковані результати дослідження рівня ФК у здорових дітей 4-16 років та запропонована номограма для оцінки 50-го та 95-го перцентилів, що підтверджує наявність вищого референтного рівня у дітей, ніж у дорослих, і цей рівень знижується з віком (рис. 1) [30].
На жаль, на сьогодні не встановлено єдиного порогового рівня ФК, при якому можна діагностувати активну стадію ЗЗК у дітей, оскільки їх значення істотно відрізняються у різних дослідженнях [31-33]. Однак рівень ФК <100 мкг/г зазвичай відповідає стадії ремісії, а рівень >250 мкг/г – активному запаленню кишечнику та є показанням до ендоскопічного дослідження [34].
За даними досліджень, порогові значення ФК при ендоскопічно активній стадії ЗЗК у дорослих коливаються від 50 до 280 мкг/г. При підвищенні порогового значення ФК спостерігалось збільшення специфічності, але зменшення чутливості методу [35].
У дітей порогове значення ФК для диференціювання активної стадії ЗЗК становить від 250 до 800 мкг/г. Таким чином, необхідно продовжувати дослідження для встановлення порогових значень ФК при ЗЗК для ширшого використання цього неінвазивного методу [36-38].
У лютому 2021 р. група експертів з Великобританії, Німеччини, Швейцарії, Канади опублікувала керівництво для лікарів, метою якого було скорочення призначення необґрунтованих інвазивних обстежень (ендоскопія, біопсія) та направлень до вузьких спеціалістів (дитячий хірург, дитячий гастроентеролог) дітям з гастроінтестинальними симптомами і рівнем ФК >50 мкг/г. У цьому керівництві наголошується, що при наявності у дитини гастроінтестинальних скарг, характерних для ЗЗК та симптомів тривоги («червоних прапорців»), а саме шлунково-кишкової кровотечі, втрати маси тіла та змін одного чи більше лабораторних показників (анемія, тромбоцитоз, підвищення рівня С-реактивного протеїну/швидкості осідання еритроцитів/трансаміназ, гіпоальбумінемія), необхідно направити такого пацієнта до дитячого гастроентеролога, який призначить дослідження ФК та вирішить питання щодо подальшого обстеження.
Якщо у дитини відсутні «червоні прапорці», але є зміни в аналізі крові, педіатр або сімейний лікар повинен призначити тест на ФК двічі з інтервалом 4 тижні. При рівні ФК <250 мкг/г у двох пробах діагноз ЗЗК малоймовірний і додаткове обстеження не потрібне. При рівні ФК >250 мкг/г у першій пробі необхідна консультація дитячого гастроентеролога для виключення ЗЗК [39].
Таким чином, показаннями до визначення рівня ФК є:
- диференційна діагностика запальних (ВК, ХК) і функціональних (СПК) захворювань кишечнику;
- моніторинг ендоскопічної та гістологічної активності запалення та прогноз рецидивування при ЗЗК;
- додаткове діагностичне дослідження при новоутвореннях (посідає друге місце за значимістю після кількісного визначення фекального гемоглобіну і фекального трансферину);
- виявлення маркера раннього рецидиву при хронічних ЗЗК;
- оцінка запального процесу, ступеня відновлення слизової оболонки кишечнику після перенесених інфекційних захворювань;
- підозра на наявність некротизуючого ентероколіту у новонароджених і моніторинг його перебігу;
- оцінка ефективності лікування пацієнтів з гельмінтозами, особливо пов’язаними з грибковими захворюваннями, ешерихіозом (О157), дизентерією та вірусними кишковими інфекціями.
Оскільки перебіг ЗЗК може супроводжуватись такими ускладненнями, як шлунково-кишкові кровотечі, анемія, а також (при тривалості захворювання 10 років і більше) формуванням колоректального раку, важливим є постійний ендоскопічний скринінг і контроль активності запалення.
Значущим неінвазивним маркером шлунково-кишкової кровотечі є дослідження калу на приховану кров (наявність гемоглобіну і трансферину). Дослідження на приховану кров у калі (гемоглобін і трансферин) використовується для діагностики прихованих кровотеч із верхніх та нижніх відділів ШКТ [40]. Наявність гемоглобіну у калі людини є специфічним маркером кровотечі з нижніх відділів ШКТ, оскільки гемоглобін – нестабільна сполука, яка перетворюється при проходженні по кишечнику. Трансферин – більш стабільна сполука та використовується як маркер кровотечі і з верхніх, і з нижніх відділів ШКТ.
Позитивний результат дослідження на вміст гемоглобіну та трансферину у калі свідчить про наявність кровотечі з верхніх та нижніх відділів ШКТ і значну імовірність кровотечі саме з нижніх відділів. При негативному результаті на наявність гемоглобіну та позитивному – на наявність трансферину діагностується кровотеча з верхніх відділів ШКТ, при позитивному результаті тесту на гемоглобін та негативному на трансферин – кровотеча з нижніх відділів ШКТ. Відсутність гемоглобіну та трансферину у калі означає, що кровотеча відсутня (рис. 2).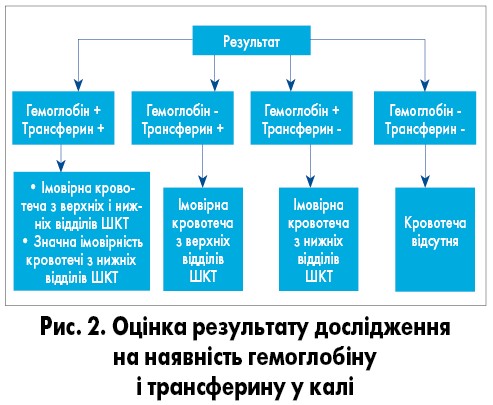
Перевагами дослідження є:
- відсутність перехресних реакцій з гемоглобіном і трансферином тваринного походження, тому пацієнту не потрібно перед дослідженням дотримуватися дієти з виключенням м’ясних продуктів;
- висока чутливість (>99%) та специфічність (>99%) імунохроматографічного методу, яким проводиться дослідження, що значно переважає хімічні методи (гваякову та бензидинову проби);
- можливість швидкого отримання результату (5 годин);
- можливість доставки біологічного матеріалу;
- можливість збереження стабільності за умови використання різних температурних режимів (при температурі від 20 до 25 °С – до 4 годин, від 2 до 8 °С – до 2 днів, при температурі -20 °С – до 14 днів).
Використання обох тестів (визначення вмісту гемоглобіну та трансферину у калі) одночасно забезпечує підвищення ефективності діагностики та зменшення виконання необґрунтованих ендоскопічних досліджень, враховуючи їх вартість та можливість потенційних ускладнень, особливо у дітей.
Таким чином, використання у пацієнтів із ЗЗК неінвазивних біомаркерів запалення – ФК та гемоглобіну й трансферину (при наявності шлунково-кишкової кровотечі) – має високу прогностичну значимість для прогнозування рецидивів захворювання, контролю лікування, можливого хірургічного втручання або госпіталізації, особливо в умовах пандемії COVID-19, яка вимагає дотримання соціальної дистанції.
Література
- Abraham C., Cho J.H. Inflammatory bowel disease. N Engl J Med. 2009; 361(21): 2066-2078. doi:10.1056/NEJMra0804647.
- Faecal calprotectin diagnostic tests for inflammatory diseases of the bowel Diagnostics guidance [DG11]. Published date: 02 October 2013 https://www.nice.org.uk/guidance/dg11/chapter/3-Clinical-need-and-practice.
- Денисова М.Ф. Современные подходы к диагностике язвенного колита у детей // Современная педиатрия. – 2014. – № 3. – С. 113-115.
…
40. Gies A. et al. Fecal immunochemical test for hemoglobin in combination with fecal transferrin in colorectal cancer screening. United European gastroenterology journal. – 2018; 6 (8): 1223-1231. doi: 10.1177/2050640618784053 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6169043.
Повний список літератури знаходиться в редакції.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1 (59) 2021 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...