Вивчення довгострокової серцево-судинної безпеки фебуксостату порівняно з алопуринолом у пацієнтів із подагрою: дослідження FAST
Подагра – це порушення обміну речовин, за якого тривале підвищення рівня уратів у сироватці крові може призвести до відкладання кристалів урату натрію, утворення тофусів, розвитку хронічного запального артриту, сечокам’яної хвороби та нефропатії. Також імовірні повторні спалахи гострого артриту й бурситу. Подагра часто асоційована з супутніми захворюваннями, такими як хронічна хвороба нирок, ожиріння, цукровий діабет, артеріальна гіпертензія, серцево-судинні (СС) патології, а також зі збільшенням смертності серед пацієнтів. Фебуксостат та алопуринол – уратознижувальні препарати, що застосовують для лікування хворих на подагру. Торік I.S. Mackenzie et al. провели дослідження з метою аналізу СС-безпеки фебуксостату порівняно з алопуринолом при лікуванні осіб із подагрою. Результати дослідження свідчать про те, що фебуксостат є не гіршим за алопуринол щодо первинної кінцевої СС-точки, та його тривале застосування не пов’язане з підвищеним ризиком серйозних побічних явищ або смерті порівняно з алопуринолом. Отримані результати доступні за посиланням https://doi.org/10.1016/S0140‑6736(20)32234‑0.
На додаток до зменшення кількості та інтенсивності загострень за допомогою протизапальних засобів, лікування пацієнтів із подагрою потребує тривалого часу. Уратознижувальна терапія (УЗТ) передбачає стійке зменшення вмісту сироваткових уратів нижче за поріг кристалізації з метою розчинення та запобігання подальшому відкладанню кристалів, повторним спалахам подагри і прогресивному ураженню суглобів.
Найбільш широко використовуваними препаратами для УЗТ є інгібітори ксантиноксидази фебуксостат та алопуринол. Профілактику загострень подагри рекомендовано проводити при ініціюванні УЗТ або після збільшення дози інгібітора ксантиноксидази, зазвичай на період до шести місяців (Hui et al., 2017).
Фебуксостат був ліцензований після отримання результатів 6-місячного рандомізованого контрольованого дослідження CONFIRMS, в якому його порівнювали з алопуринолом у 2269 учасників (Becker et al., 2010). При застосуванні обох препаратів спостерігалися зіставна частота (0,4%) СС-подій та відсутність пов’язаних із ними летальних випадків у пацієнтів групи фебуксостату. Однак через стурбованість із приводу можливого підвищеного СС-ризику при лікуванні фебуксостатом Європейське агентство з лікарських засобів (ЕМА) вказало на доцільність проведення післяреєстраційного дослідження для оцінки СС-ефектів фебуксостату порівняно зі стандартною УЗТ алопуринолом у пацієнтів із подагрою.
Матеріали й методи дослідження
Дизайн дослідження та когорта учасників
I.S. Mackenzie et al. (2020) провели проспективне рандомізоване відкрите багатоцентрове дослідження FAST зі сліпими кінцевими точками при залученні пацієнтів із подагрою, що проходили спостереження у 18 регіональних центрах Великої Британії (Шотландія та Англія), Данії та Швеції (MacDonald et al., 2014). Із грудня 2011 по жовтень 2017 рр. 6603 хворих дали письмову інформовану згоду на участь та були оцінені на відповідність критеріям включення. Як наслідок, 6128 пацієнтів випадковим чином розподілили (1:1) для отримання фебуксостату (n=3063) або алопуринолу (n=3065). Хворі припинили призначене лікування наприкінці грудня 2019 р.; дослідження завершилося у серпні 2020 р. після остаточного аналізу кінцевих точок.
У дослідження увійшли пацієнти ≥60 років, що страждали на подагру (85,3% чоловіків та 14,7% жінок), на думку лікаря-практика потребували застосування УЗТ, а також ті, що мали принаймні один додатковий фактор СС-ризику та вже отримували терапію алопуринолом (Taylor et al., 2015). СС-патології в анамнезі, як-от інфаркт міокарда (ІМ), інсульт, транзиторна ішемічна атака (ТІА), гострий коронарний синдром (ГКС), коронарна реваскуляризація, стенокардія або серцева недостатність (СН), мали 33,4% осіб, цукровий діабет – 22,5%. Не були включені хворі на безсимптомну гіперурикемію, особи з ІМ або інсультом в анамнезі за попередні шість місяців та із застійною серцевою недостатністю функціонального класу III або IV за критеріями Нью-Йоркської асоціації серця (NYHA) чи тяжкою нирковою недостатністю.
На момент скринінгу 58,6% пацієнтів приймали статини, 35,4% – антиагреганти (зокрема 29,8% – ацетилсаліцилову кислоту), 40,3% – інгібітор ангіотензинперетворювального ферменту.
Терапевтичні заходи
Хворі групи фебуксостату приймали препарат у пероральній формі по 80 мг/добу протягом перших двох тижнів після рандомізації. Через два тижні було виміряно сироватковий рівень уратів; якщо не вдавалося досягти цільових показників, встановлених Європейською антиревматичною лігою (EULAR), дозу збільшували до 120 мг/добу. Пацієнти групи алопуринолу отримували препарат у таблетованій формі по 100 або 300 мг у дозі, визначеній до рандомізації. Учасники обох груп пройшли період вимивання тривалістю 7‑21 день перед початком досліджуваної терапії.
Під час скринінгового візиту у хворих вимірювали концентрацію уратів у сироватці крові. Якщо перед включенням у дослідження в пацієнтів при прийманні алопуринолу показник не відповідав цільовому згідно зі встановленим EULAR <0,0357 ммоль/л (<6 мг/дл), дозу збільшували на 100 мг/добу кожні два тижні до досягнення цільового рівня уратів або максимальної дозволеної (900 мг/добу) чи переносимої дози (Richette et al., 2012).
Пацієнти могли продовжувати спостереження, навіть якщо цільової концентрації уратів не було досягнуто після максимального збільшення дозування. Лікар мав право зменшити або збільшити добову дозу фебуксостату чи алопуринолу в межах граничних добових дозувань залежно від клінічних умов (проблеми з переносимістю, неадекватний контроль рівня уратів тощо). Крім того, після рандомізованого розподілу на групи всім пацієнтам запропонували пройти 6-місячну профілактику нападів подагри за допомогою колхіцину (0,5 мг 1‑2 рази на день), альтернативний варіант – нестероїдні протизапальні засоби (напроксен, диклофенак або мелоксикам) із захистом шлунка (омепразол або ранітидин).
Клінічні результати
Первинним клінічним наслідком лікування у дослідженні була комбінована кінцева точка, що поєднувала госпіталізацію із приводу нефатального ІМ або ГКС із позитивним результатом на біомаркери, нефатальний інсульт та смерть внаслідок СС-подій. Вторинні клінічні наслідки включали госпіталізацію із приводу нефатального ІМ або ГКС із позитивним результатом на біомаркери, СН, нестабільної стенокардії, ТІА, нефатальної зупинки серця, тромбозу вен та периферичних артерій, аритмії без ознак ішемії, для проведення реваскуляризації коронарних артерій чи головного мозку, а також нефатальний інсульт, летальні випадки через СС-ускладнення або з будь-яких причин.
Як кінцеві точки досліджуваної ефективності науковці також оцінювали частку пацієнтів із концентрацією уратів у сироватці крові <0,0357 або <0,0297 ммоль/л (<6 чи <5 мг/дл відповідно) через кожний рік лікування. Щодо побічних явищ, які також були потенційними кінцевими точками, детальнішу інформацію було зібрано з медичних карт хворих та свідоцтв про смерть.
Статистичний аналіз
Вихідні характеристики фіксувалися відповідно до груп лікування як середнє квадратичне відхилення або міжквартильний діапазон для безперервних змінних та як число й відсоток – для категоріальних. Клінічні результати аналізували на основі часу до першої події з використанням регресії Кокса, за винятком частоти нападів подагри. Для аналізу повторюваних епізодів слугувала негативна біноміальна регресія.
При оцінюванні ефекту лікування фебуксостатом порівняно з алопуринолом враховували відносний ризик (ВР) для регресії Кокса та коефіцієнт захворюваності для негативної біноміальної регресії (для обох 95% довірчий інтервал [ДІ]). Значення р обчислювали за тестом Вальда. Міжгрупові відмінності сироваткового рівня уратів щорічно оцінювали методом ANCOVA. Аналіз безпеки проводили для всіх пацієнтів, які отримали принаймні одну дозу досліджуваних препаратів.
Результати дослідження
Первинний аналіз залежно від призначеного (intention-to-treat; ІТТ) та отриманого (on-treatment; OT) лікування показав, що фебуксостат був не гіршим за алопуринол при оцінці частоти первинної комбінованої кінцевої точки. За даними двостороннього аналізу, також не спостерігалося значної різниці між групами стосовно ризику первинної кінцевої точки. Оцінка вторинних наслідків призначеного та отриманого лікування продемонструвала зіставні дані із впливу фебуксостату й алопуринолу щодо смерті від будь-яких причин, кожного окремого компонента первинного результату, включно із летальними випадками через СС-ускладнення.
Дані щодо кумулятивної частоти первинної комбінованої та окремих вторинних кінцевих точок наведені на рисунках 1 і 2.
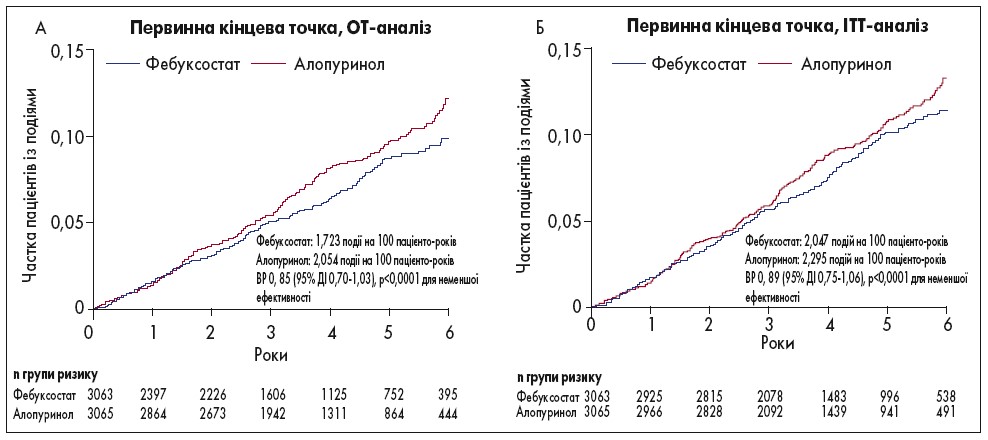 Рис. 1. Кумулятивна частота первинної комбінованої кінцевої точки (n=6128)
Рис. 1. Кумулятивна частота первинної комбінованої кінцевої точки (n=6128)
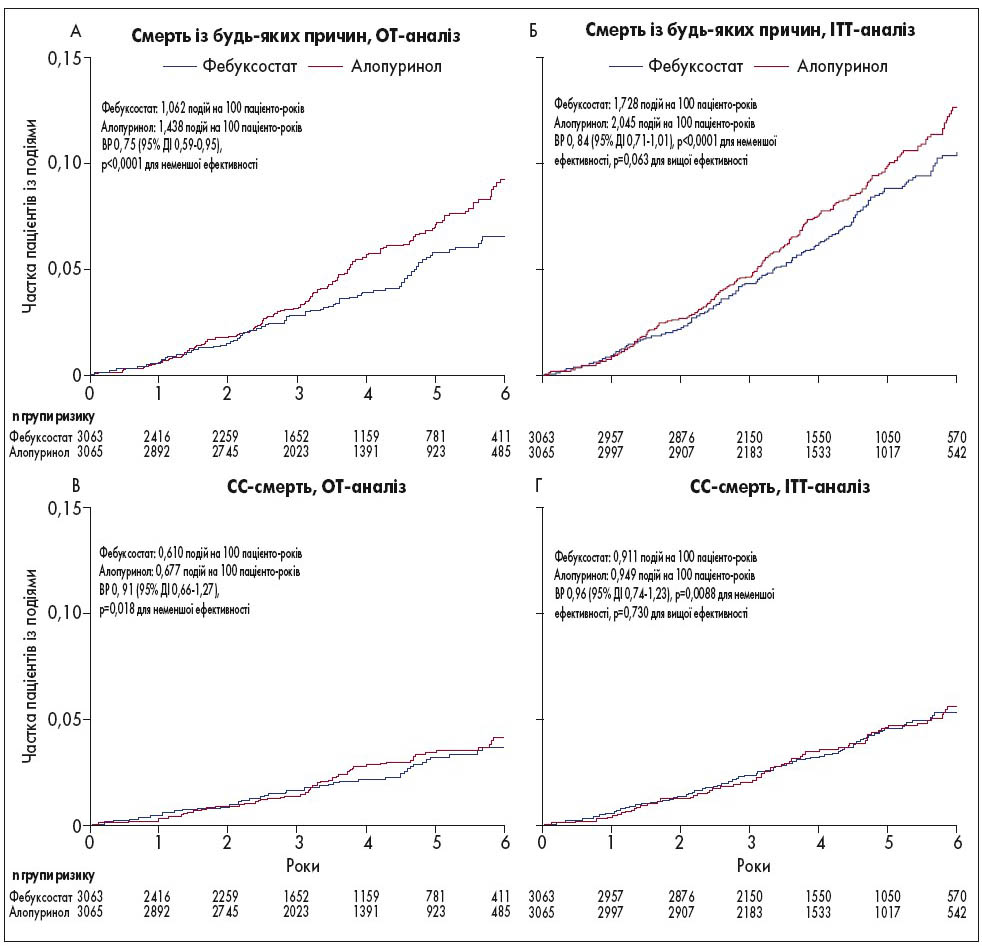 Рис. 2. Кумулятивна частота окремих вторинних кінцевих точок (n=6128)
Рис. 2. Кумулятивна частота окремих вторинних кінцевих точок (n=6128)
Під час лікування фебуксостатом й алопуринолом 98 та 99,5% пацієнтів відповідно застосовували принаймні одну дозу досліджуваного препарату та були включені до групи аналізу безпеки (n=6051). Частота ендокринних розладів була вищою, а новоутворень – нижчою у групі фебуксостату порівняно з алопуринолом. Щонайменше одне значення вище верхньої межі норми концентрації креатиніну (>106 та >80 мкмоль/л у чоловіків і жінок відповідно) мали 33,6% осіб у групі фебуксостату та 30,9% – алопуринолу.
У групі алопуринолу побічними ефектами, пов’язаними з лікуванням, були стенокардія, тромбоцитопенія, диспепсія та артралгія. У групі фебуксостату мали місце серйозний панкреатит, поодинокі випадки діареї, фібриляції передсердь, холециститу, гематурії, гастроезофагеального рефлюксу, некардіального болю за грудиною тощо. Оскільки всі пацієнти вже приймали алопуринол на початок дослідження, вони мали меншу ймовірність розвитку несприятливих явищ, пов’язаних із терапією, порівняно з групою фебуксостату (нове лікування).
Загальний аналіз чутливості (ОТ- та ІТТ-аналіз) комбінованої первинної кінцевої точки, із заміною СС-смерті на таку з будь-яких причин, виявив не меншу ефективність фебуксостату порівняно з алопуринолом. При оцінці цієї комбінованої кінцевої точки (включно зі смертю від будь-яких причин) з корегуванням результатів з огляду на вік, стать, рівень холестерину ліпопротеїнів низької та високої щільності, високочутливий тропонін І, систолічний артеріальний тиск, статус куріння (поточний, у минулому чи ніколи) та цукровий діабет, гіпертонію, СС-патології в анамнезі фебуксостат також був не гіршим, ніж алопуринол.
Зміну концентрації уратів порівняно з вихідними показниками оцінювали між двома групами лікування щороку протягом 1‑7 років. Зниження рівня уратів було більш значущим при використанні фебуксостату, ніж алопуринолу, із суттєвими відмінностями між групами щороку та середньою різницею >0,08 ммоль/л упродовж 1‑6 років.
Висновки
У дослідженні I.S. Mackenzie et al. (2020) за участю понад 6 тис. пацієнтів із подагрою, які отримували УЗТ інгібітором ксантиноксидази у дозах, призначених для зниження концентрації уратів до цільового рівня відповідно до EULAR (<0,0357 ммоль/л) протягом семи років, фебуксостат виявився не гіршим за алопуринол із точки зору виникнення основних СС-наслідків.
Важливо те, що повідомлення про збільшення смертності були відсутні, при цьому частота летальних випадків через будь-які причини та СС-події виявилася нижчою у групі фебуксостату, ніж алопуринолу. Таким чином, довгострокове використання фебуксостату не пов’язане з підвищеним ризиком смерті або серйозними побічними явищами порівняно з алопуринолом. З огляду на отримані сприятливі висновки, попередні рекомендації уникати застосування фебуксостату в осіб із СС-патологіями мають бути переглянуті та змінені.
Підготувала Олена Коробка
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 1 (74) 2021 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9). Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи. ...
Застосування статинів середньої інтенсивності в комбінації з езетимібом порівняно зі статинами високої інтенсивності окремо може забезпечити більше зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у пацієнтів із нещодавнім ішемічним інсультом. Пропонуємо до вашої уваги огляд статті Keun-Sik Hong et al. «Moderate-Intensity Rosuvastatin Plus Ezetimibe Versus High-Intensity Rosuvastatin for Target Low-Density Lipoprotein Cholesterol Goal Achievement in Patients With Recent Ischemic Stroke: A Randomized Controlled Trial», опублікованої у виданні Journal of Stroke (2023; 25(2): 242‑250). ...
Артеріальна гіпертензія (АГ) сьогодні є одним із найпоширеніших серцево-судинних захворювань (ССЗ), що асоціюється з високим кардіоваскулярним ризиком, особливо в коморбідних пацієнтів. Навіть помірне підвищення артеріального тиску (АТ) пов’язане зі зменшенням очікуваної тривалості життя. До 40% хворих на АГ не підозрюють у себе недугу, бо це захворювання на початку може мати безсимптомний перебіг. Оптимальний контроль АТ є вагомим чинником профілактики фатальних серцево-судинних подій (ССП) для забезпечення якісного та повноцінного життя таких хворих. ...




