COVID‑19 і хронічне обструктивне захворювання легень
Станом на 11 липня 2020 року тяжким гострим респіраторним синдромом коронавірусу 2 (SARS-CoV‑2) – вірус, відповідальний за пандемію коронавірусу 2019 (COVID‑19), – було інфіковано понад 12,7 млн людей в усьому світі. Понад 560 тис смертей стали наслідком цієї хвороби [1]. З огляду на руйнівний вплив, який COVID‑19 може мати на легені, природно його побоюватися пацієнтам з основним хронічним обструктивним захворюванням легень (ХОЗЛ). Оцінка надмірного ризику зараження цієї когорти пацієнтів COVID‑19 і, зокрема, його більш серйозних респіраторних проявів була складною справою в цій пандемії з різних причин. По-перше, звітність про випадки зараження була передусім зосереджена на госпіталізованих та реанімаційних хворих, а не на легких амбулаторних випадках. Частково це пов’язано з варіативністю стратегій тестування в усьому світі: деякі країни з жорсткішими вимогами до тестування та обмеженими ресурсами зосереджувалися на тестуванні лише тих, хто потребував госпіталізації. Ще не визначено, скільки пацієнтів із ХОЗЛ впродовж цього часу могли прийняти рішення не звертатися до лікарні в період пандемії, щоб згодом опинитися в статистиці надлишкової смертності [2, 3]. По-друге, недооцінка поширеності ХОЗЛ у загальній популяції є проблемою, яка існувала до появи COVID‑19 [4-6] і яка, можливо, загостриться в переповнених хворими лікарнях, адже в таких умовах доволі складно точно встановити супутні захворювання, а спірометрію зробити неможливо.
Ключові слова: COVID‑19, коронавірус, ХОЗЛ, дихальні шляхи, інгаляційні кортикостероїди, системні кортикостероїди, β2-агоністи
Чи є ХОЗЛ фактором ризику при COVID‑19?
З початку пандемії найповніший збір даних проводився в Китаї, де фонова частота ХОЗЛ у дорослих віком >40 років становить 13,6% [7]. Переважна більшість досліджень була зосереджена на госпіталізованих хворих; лише одне на сьогодні вивчало як госпіталізованих, так і амбулаторних пацієнтів (з яких тільки 1,1% мали діагноз ХОЗЛ [8]), а одне дослідження – безсимптомних пацієнтів (з них тільки 1,6% хворіли на ХОЗЛ [9]). За даними досліджень у Китаї, що вивчали госпіталізованих пацієнтів, частота ХОЗЛ коливалася від 0 до 10% [10-41]. За даними, які надходили з інших країн, частота ХОЗЛ серед госпіталізованих пацієнтів із COVID‑19 виявилася подібною і за оцінками становила у Нью-Йорку від 2,4 до 14% [42-45], а в Італії – від 5,6 до 9,2% [46-48]. Однак дані досліджень за участю лише пацієнтів із реанімаційного відділення виявилися більш варіабельними. В одному з італійських досліджень із загальною кількістю 1591 пацієнт відділення інтенсивної терапії (ВІТ) [49] та в одному в Сіетлі (США) за участю 24 пацієнтів ВІТ ХОЗЛ реєстрували в 4% хворих [50]. Набагато вища частота ХОЗЛ була зареєстрована в пацієнтів ВІТ в Іспаніїї – із 48 пацієнтів 38% мали ХОЗЛ [51].
Проте з’являється все більше доказів того, що ХОЗЛ може бути фактором ризику тяжчого перебігу COVID‑19 [57]. Аналіз супутніх захворювань в 1590 хворих на COVID‑19 в усьому Китаю продемонстрував, що показник відношення шансів (ВШ) госпіталізації у ВІТ, штучної вентиляції легень або смерті при ХОЗЛ становить 2,681 (95% ДІ 1,424-5,048; p=0,002) навіть після корекції за такими показниками, як вік і куріння [13]; 62,5% пацієнтів із тяжкими формами захворювання мали ХОЗЛ в анамнезі (проти лише 15,3% у разі нетяжких випадків), 25% померлих хворіли на ХОЗЛ (проти лише 2,8% із тих, хто вижив). У багатоцентровому китайському дослідженні пацієнти з ХОЗЛ становили 15,7% тяжкохворих, але лише 2,3% – хворих середнього ступеня тяжкості (р<0,001) [16]. Інші дослідження виявили подібні, хоча й статистично слабші, відмінності в показниках ХОЗЛ між пацієнтами ВІТ та неВІТ (8,3 проти 1,0% відповідно; р=0,054) [10], з тяжкими та нетяжкими випадками (4,8 проти 1,4%; p=0,026) [17], а також між померлими й тими, хто вижив (7 проти 1%; p=0,047) [11].
Що відбувається в дихальних шляхах пацієнтів із ХОЗЛ при COVID‑19
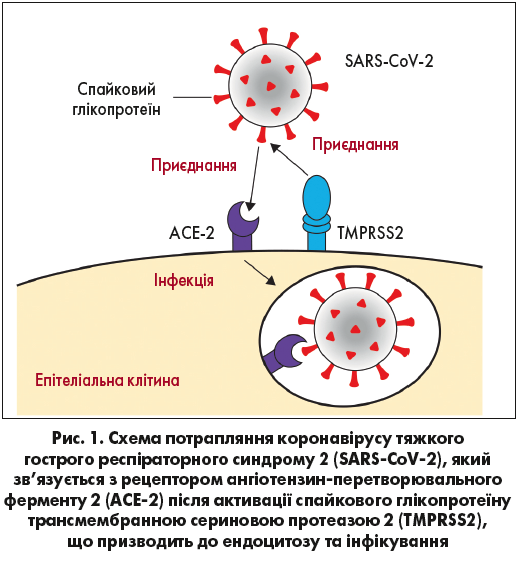
Питання, чому в пацієнтів із ХОЗЛ нібито розвиваються гірші наслідки в разі COVID‑19 (навіть якщо ризик зараження на початку може бути невисоким), варто визнати дискутабельним. По-перше, нещодавно з’явилися докази того, що пацієнти з ХОЗЛ та курці можуть мати різні механізми проникнення SARS-CoV‑2 у клітину. Подібно до SARS-CoV (який був відповідальним за пандемію SARS 2002-2003 рр.) [58], SARS-CoV‑2 має спайковий білок для полегшення злиття вірусу з рецептором ангіотензин-перетворювального ферменту 2 (АПФ-2, АСЕ‑2) та надходження в клітину (рис. 1, 2) [59-62]. Нещодавно було продемонстровано, що в трьох окремих когортах пацієнтів з наявними профілями експресії генів епітеліальних клітин бронхів експресія АПФ‑2 була значно підвищена у хворих на ХОЗЛ проти контрольної групи [63]. Куріння також було пов’язане з вищою експресією АСЕ‑2, якщо порівняти з особами, які ніколи не палили або кинули палити. Це було виявлено в окремих вибірках зразків легеневої тканини та епітелію дихальних шляхів (ДШ) [64-66], а також підтверджено додатковими доказами, які асоціюють експресію АСЕ‑2 із впливом нікотину [67, 68]. Однак важливо зазначити, що досі не було продемонстровано, що експресія АСЕ‑2 підвищує сприйнятливість до захворювання або обтяжує його перебіг. Ба більше, відносно низька експресія АСЕ‑2 в епітелії бронхів, якщо порівняти з епітелієм носа [69], має незрозумілі наслідки для сприйнятливості до захворювання в пацієнтів із переважно патологією малих ДШ.
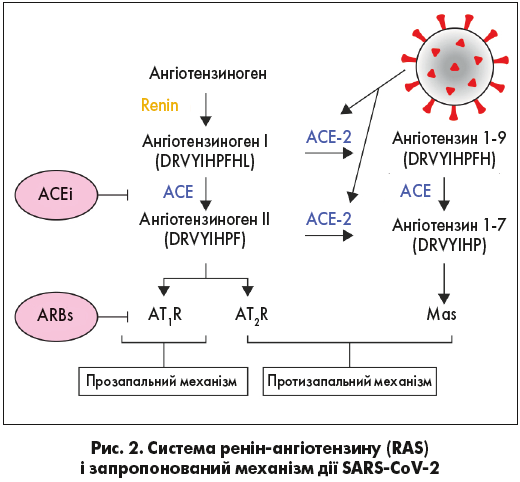
Утворення ангіотензину II з ангіотензину I за участю ангіотензин-перетворювального ферменту (АСЕ) індукує вазоконстрикцію судин і прозапальний ефект завдяки зв’язуванню рецептора ангіотензину II типу 1 (AT1R), тоді як рецептор типу 2 (AT2R) може чинити протилежну дію. Інгібітори АСЕ (ACEі) та блокатори рецепторів ангіотензину II (ARBs) є дуже дієвими антигіпертензивними засобами, які сприяють розширенню судин. АСЕ‑2 пригнічує активність ангіотензину II, перетворюючи ангіотензин I на ангіотензин 1-9 та ангіотензин II на ангіотензин 1-7, який зв’язується з протоонкогенним рецептором MAS1 (Mas), що зумувлює протизапальну дію. Після зв’язування SARS-CoV‑2 з АСЕ‑2 відбувається зсув співвідношення АСЕ/АСЕ‑2 у бік переважання АСЕ, що призводить до активації прозапальних ефектів і пошкодження тканин
Лікування хворих на ХОЗЛ під час пандемії COVID‑19
У період пандемії виникли дві клінічні проблеми допомоги пацієнтам із ХОЗЛ:
- чи можна застосовувати звичайні алгоритми медикаментозного лікування ХОЗЛ;
- як впоратися з проблемою різкого скорочення немедикаментозних заходів, спричиненою цією пандемією.
Хоча наше розуміння COVID‑19 значуще зросло в основному за короткий проміжок часу, указані проблеми були сферою експертної думки і не узгоджувалися з вагомими науковими доказами. Залишаються відкритими питання щодо ефектів загальних респіраторних препаратів, які застосовують у лікуванні ХОЗЛ, зокрема інгаляційних і системних кортикостероїдів (ІКС та СКС), β2-агоністів короткої та тривалої дії, а також мускаринових антагоністів короткої та тривалої дії, у разі полегшення або загострення перебігу COVID‑19. Епідеміологічні дані, отримані з Китаю та інших ранніх епіцентрів, поки не є достатньо деталізованими для визначення шкоди або користі цих засобів у пацієнтів із COVID‑19 та ХОЗЛ. Однак Peters і співавт. [70] нещодавно показали, що експресія АСЕ‑2 в епітеліальних клітинах ДШ, отриманих у хворих на астму, була меншою в пацієнтів, що приймали ІКС, проти тих, кому вони не були призначені; це підвищує ймовірність того, що ІКС можуть зменшувати проникнення вірусу. Чи справедливе таке твердження для ДШ при ХОЗЛ, чия схильність до пневмонії внаслідок застосування ІКС добре задокументована, ще не встановлено. Сьогодні, за відсутності даних щодо дійсної шкоди чи користі ІКС, їх та інші інгалятори тривалої дії не варто скасовувати в повсякденній практиці, також не рекомендується пропонувати їх як профілактичний засіб пацієнтам із ХОЗЛ під час пандемії коронавірусу [71].
Більше занепокоєння спричиняє використання СКС, які є основою лікування загострення ХОЗЛ. До відома, історичні дані про застосування СКС під час вірусних пандемій не є цілком позитивними. Уроки пандемії SARS та близькосхідного респіраторного синдрому свідчать про потенційну шкоду СКС. Чотири дослідження показали шкоду при SARS, у тому числі уповільнене очищення від вірусу та підвищений рівень психозу [72]. Наразі найбільш перспективним щодо застосування кортикостероїдів при COVID‑19 є проведене у Великій Британії рандомізоване контрольоване дослідження (РКД) дексаметазону (RECOVERY), в якому було продемонстроване зниження смертності на третину [75]. Між тим опубліковані результати невеликих ретроспективних досліджень, що видаються суперечливими, причому в двох дослідженнях показано відсутність користі [76, 77], а в інших двох – покращення показників смертності та збільшення обсягу медичної допомоги [78, 79]. Однак, з огляду на результати дослідження RECOVERY, цілком імовірно, що дексаметазон стане стандартним лікуванням у пацієнтів із COVID‑19, у тому числі хворих на ХОЗЛ.
Вплив пандемії гостро відчувається пацієнтами з ХОЗЛ у багатьох аспектах свого життя. Візити до лікаря в клініку скорочені, як і сеанси легеневої реабілітації та програми домашнього відвідування хворих на ХОЗЛ. Пацієнти, яких зазвичай госпіталізували під час загострення, можуть вирішити залишитися вдома через страх інфекції, а це призведе до невчасної медичної допомоги, як це траплялося за інших станів, таких як інфаркт міокарда [80, 81].
Довгострокові наслідки цієї паузи в рутинному догляді ще очікують своєї належної оцінки. Сьогодні системам охорони здоров’я довелося адаптуватися до цих умов, інтенсифікуючи телемедицину та онлайн-прийоми. На щастя, у декількох РКД з оцінки застосування телемедицини у хворих на ХОЗЛ продемонстровано її доцільність, такий онлайновий спосіб надання вчасної допомоги принаймні не поступається звичайному, коли йдеться про загострення хвороби, госпіталізацію тим паче якість життя [82-86]. Онлайнові програми легеневої реабілітації виявилися так само ефективними, як і особисті сеанси [87-89]. Якщо ж заходи соціального дистанціювання діятимуть упродовж багатьох місяців, ми виступаємо за створення таких віртуальних програм, щоб забезпечити нашим пацієнтам можливість отримувати оптимальний догляд.
Список літератури – у редакції.
Leung J.M. et al. COVID‑19 and COPD Eur Respir J 2020; 56: 2002108. https://doi.org/10.1183/13993003.02108-2020
Переклав з англ. Назар Лукавецький
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 1 (54), 2021 р.
СТАТТІ ЗА ТЕМОЮ Пульмонологія та оториноларингологія
Реімбурсація – це повне або часткове відшкодування аптечним закладам вартості лікарських засобів або медичних виробів, що були відпущені пацієнту на підставі рецепта, за рахунок коштів програми державних гарантій медичного обслуговування населення. Серед громадськості програма реімбурсації відома як програма «Доступні ліки». Вона робить для українців лікування хронічних захворювань доступнішим....
Хронічна кропив’янка (ХК) – це патологія, яка характеризується рецидивними нестійкими висипаннями з/без ангіоневротичного набряку, які виникають мало не щодня впродовж більш як 6 тиж [1]. Розрізняють два варіанти ХК – хронічна індукована кропив’янка (ХІК), або фізична кропив’янка, зумовлена певними фізичними подразниками, такими як тиск, тепло або холод, і більш поширена хронічна спонтанна кропив’янка (ХСК), яка розвивається у 80-90% випадків і характеризується відсутністю відомих екзогенних чинників і причин [2]. На це захворювання страждає від 0,5 до 1% населення світу, переважно особи жіночої статі [3]. Повторні симптоми часто призводять до порушень сну та чинять виражений негативний вплив на якість життя (QoL) [4]. ...
Риносинусит (РС) незмінно потрапляє до десятки найпоширеніших діагнозів в амбулаторній лікарській практиці та посідає 5-те місце серед захворювань, щодо яких призначається антибактеріальна терапія [1]. Симптоми гострих РС маніфестують тоді, коли уражаються слизові оболонки приносових пазух і порожнини носа. Оскільки слизова оболонка носа та приносових пазух – єдине ціле, гострий запальний процес уражатиме ці слизові оболонки, а ізольоване запалення слизової оболонки порожнини носа чи будь-якої з приносових пазух може визначатися при хронічних захворюваннях [2]. Це обґрунтовує доцільність використання терміна «РС». ...
Застуда та інші інфекції дихальних шляхів – актуальна проблема охорони здоров’я через високий рівень захворюваності, що перевищує такий інших інфекційних патологій. З метою підвищення кваліфікації лікарів загальної практики та обміну досвідом з актуальних питань лікування інфекційних захворювань у лютому була проведена науково-практична конференція «Академія сімейного лікаря. Для кого небезпечні сезонні інфекції? Загроза сезонних інфекцій. Погляд пульмонолога, інфекціоніста, алерголога, ендокринолога, кардіолога, педіатра» за участю провідних вітчизняних спеціалістів-практиків....