Спінальна м’язова атрофія: реальна терапевтична можливість порятунку
.jpg) Знання новітніх даних щодо клінічних особливостей та шляхів порятунку пацієнтів зі спінальною м’язовою атрофією (СМА) в контексті сьогодення є одним із базових для лікаря будь-якої спеціальності. Адже клініцист має можливість призначити ефективне лікування, доступне для пацієнта та його родини, яке кардинально змінює перебіг захворювання, що раніше вважалося летальним.
Знання новітніх даних щодо клінічних особливостей та шляхів порятунку пацієнтів зі спінальною м’язовою атрофією (СМА) в контексті сьогодення є одним із базових для лікаря будь-якої спеціальності. Адже клініцист має можливість призначити ефективне лікування, доступне для пацієнта та його родини, яке кардинально змінює перебіг захворювання, що раніше вважалося летальним.
СМА – рідкісне прогресуюче нервово-м’язове захворювання, яке виникає внаслідок мутації в гені виживання мотонейронів (SMN1), що призводить до недостатнього рівня продукції білка SMN (Mercuri et al., 2012). У нормі ген SMN1 відповідає за синтез білка SMN, проте в пацієнтів зі СМА він не здатний виконувати цю функцію. Частково синтез білка SMN може бути забезпечений завдяки існуванню гена SMN2, який синтезує трохи інший варіант білка, що є дуже нестабільним (у нормі його максимальна частка становить ~10%), який не здатний задовольнити потреби організму (Bowerman et al., 2017; Артеменко та співавт., 2018; Nery et al., 2019; Mercuri et al., 2018).
Загалом SMN експресується у всіх евкаріотичних клітинах і наявний як у ядрі, так і цитоплазмі. SMN бере участь у низці базових клітинних процесів (Simone et al., 2016; Singh et al., 2017; Flávia, 2019):
- підтримання гомеостазу клітинного середовища;
- процесинг РНК, включно зі збіркою рибонуклепротеїну, сплайсингом, транскрипцією і транспортом матричної РНК (мРНК);
- виживання клітин.
Знижений рівень білка SMN у центральній нервовій системі та периферичних тканинах відіграє ключову роль у патогенезі СМА. Клінічна картина СМА включає ураження низки систем організму, таких як:
- Нервова – порушення керування соматичною мускулатурою.
- М’язова – «первинна» слабкість тканини м’язів, вроджені аномалії, сколіоз.
- Респіраторна – слабкість дихальних м’язів, дихальна недостатність.
- Ниркова – порушення функції нирок, нефрокальциноз та фіброз, полікістоз нирок.
- Репродуктивна – гіпофункція яєчок, безпліддя.
- Судинна – дистальні некрози пальців (Belter et al., 2018; Bowerman et al., 2017; Nery et al., 2019).
- Серцева – аритмія, брадиаритмія, кардіоміопатія, затримка та дефекти розвитку серцевого м’яза (Butchbach et al., 2016; Markowitz et al., 2012; Zaworski et al., 2016).
- Кісткова – дегенерація міжхребцевих дисків, зниження мінеральної щільності кісток та переломи, оскільки білок SMN взаємодіє з фактором стимуляції остеобластів (Jain et al., 2019).
- Імунна – рівень білка SMN знижений у периферичних мононуклеарах і фібробластах (Zaworski et al., 2016).
- Травна – порушення функції ковтання; гастроезофагеальна рефлюксна хвороба; стеатоз печінки; підвищена схильність до дисліпідемії; панкреатит, аномалії острівцевих клітин: порушення толерантності до глюкози та цукровий діабет; порушення вегетативної іннервації гладкої мускулатури кишечника; порушення моторики шлунково-кишкового тракту, затримка евакуації шлункового вмісту; хронічна судинна недостатність кишечника, закреп (Lipnick et al., 2019; Abati et al., 2020; Farrar et al., 2017).
СМА класифікують на п’ять підтипів (від 0 до 4: менше число вказує на більшу тяжкість), які визначаються відповідно до досягнутої максимальної моторної функції та віку появи симптомів (Mercuri et al., 2012; Yeo et al., 2020). СМА 1-го типу характеризується симптомокомплексом млявої дитини, порушенням ковтання, недостатністю кашльового поштовху, внаслідок чого виникають респіраторні інфекції. Наявність прогресуючої дихальної недостатності призводить до необхідності застосування апаратів штучної вентиляції легень до 12-місячного віку (Finkel et al., 2014). Без респіраторної підтримки очікувана тривалість життя складає два роки (De Sanctis et al., 2016; Finkel et al., 2014; Kolb et al., 2017).
На сьогодні в Україні зареєстровано два лікарські засоби для фармакотерапії СМА: нусінерсен і рисдиплам. Також у світі для лікування СМА існує онасемноген абепарвовек, який не зареєстровано в Україні.
Нусінерсен – синтетичний одноланцюговий олігодезоксинуклеотид, SMN2-орієнтований антисмисловий (антисенс) препарат для інтратекального введення, застосовуваний у дорослих і дітей (FDA, 2016). Онасемноген абепарвовек – препарат генно-трансферної терапії на базі вірусного вектора для внутрішньовенного введення пацієнтам віком до двох років із біалельною мутацією в гені SMN1, за наявності до 3 копій гена SMN2 включно (FDA, 2019).
Рисдиплам був схвалений для лікування пацієнтів віком від 2 місяців зі СМА (FDA, 2020). Препарат застосовують у формі рідини для перорального введення; діюча речовина вибірково зв’язується з транскриптами ділянок 7 екзону та інтрону пре-мРНК гена SMN2 (Sivaramakrishnan et al., 2017). Рисдиплам сприяє включенню включенню кодуючої послідовності екзону 7 у транскрипт мРНК, результатом чого є збільшення експресії повноцінної за довжиною мРНК і, відповідно, підвищення вмісту функціонального білка SMN (Ratni et al., 2018).
Загалом наявні чотири дослідження ефективності та безпеки рисдипламу:
- FIREFISH (Study to Investigate Safety, Tolerability, Pharmacokinetics, Pharmacodynamics and Efficacy of Risdiplam in Infants With Type1 SMA): СМА 1-го типу, немовлята віком 1‑7 місяців (І частина, n=21 – завершена, ІІ частина, n=41 – триває);
- SUNFISH (Study to Investigate the Safety, Tolerability, Pharmacokinetics, Pharmacodynamics and Efficacy of Risdiplam in Type 2 and 3 SMA Participants): СМА 2-го і 3-го типів, діти і молоді люди віком 2-25 років із використанням плацебо-контролю (І частина, n=51 – вже завершена, ІІ частина, n=180 – ще триває);
- JEWELFISH (Study of Risdiplam in Adult and Pediatric Participants With SMA): СМА 1, 2 і 3-го типів, діти і дорослі віком 6 місяців – 60 років, пацієнти після попередньої терапії (n=180 – триває);
- RAINBOWFISH (Study of Risdiplam in Infants With Genetically Diagnosed and Presymptomatic SMA): пресимптоматична СМА, від народження до 6 тижнів (n=25 – триває).
Дослідження FIREFISH
Матеріали та критерії включення/виключення
За дизайном І частина FIREFISH – відкрите двоетапне багатоцентрове дослідження рисдипламу в 21 немовляти віком від 1 до 7 місяців із симптоматичною, генетично підтвердженою 5q-автосомно-рецесивною СМА 1-го типу та двома копіями SMN2. Критерії виключення: застосування в анамнезі препаратів етіопатогенетичної терапії СМА.
Режим дозування: пероральний прийом (або череззондове введення) рисдипламу зі збільшенням дози (пошук дозування): початкова доза – 0,00106 мг/кг один раз на добу, надалі – 0,0106; 0,04; 0,08; 0,2 і 0,25 мг/кг один раз на добу; ескалація дози базувалася на регулярному перегляді фармакокінетичних показників та даних щодо безпеки з подальшим корегуванням дози для досягнення визначеного протоколом цільового рівня (середня площа під кривою залежності концентрації рисдипламу в плазмі крові від часу протягом 24 год у стабільному стані) 700 нг × год/мл у когорті низької дози та 2000 нг × год/мл – високої.
ІІ частина дослідження (підтверджувальна) – визначення ефективності та безпеки дози, обраної в І частині.
Результати
Дозування. Остаточні дози, визначені методом ескалації, становили 0,08 мг/кг один раз на добу в когорті низької дози і 0,2 мг/кг один раз на добу – високої. Когорта низької дози включала четверо немовлят: троє отримували препарат у низькій дозі принаймні за 12 місяців до її збільшення до високої та ще одне – низьку дозу, але було виключене з дослідження на 19-й день у зв’язку з початком паліативної допомоги через прогресування захворювання. П’яте немовля померло від ускладнень, пов’язаних із хворобою, приблизно через три тижні після зарахування у дослідження і до запланованого збільшення дози. Тому дозу для четвертого немовляти було підвищено приблизно через 2,5 місяці лікування. Четверте немовля і всі згодом зараховані складали когорту високої дози (17 немовлят).
Демографічні та клінічні характеристики пацієнтів на базовому рівні. Віковий діапазон немовлят у дебюті захворювання становив від 28 днів (0,9 місяця) до трьох місяців. Середній вік немовлят при зарахуванні – 6,7 місяця (діапазон – 3,3‑6,9 місяця).
Медіанна базова оцінка за тестом дитячої лікарні Філадельфії для оцінки рухових функцій при нейром’язових захворюваннях у новонароджених (CHOP-INTEND) була 24 бали (від 0 до 64, де вищі показники вказують на кращу моторну функцію) та за шкалою оцінки неврологічного статусу дітей молодшого віку, розробленою в лікарні Хаммерсміт, модуль 2 (HINE‑2) – 1 бал, що відповідає тяжкому захворюванню (Kolb et al., 2017; Finkel et al., 2017). При цьому ніхто з немовлят не міг сидіти без підтримки, 5 із 21 (24%) отримували респіраторну підтримку, четверо з яких – профілактично. На 12-му місяці дослідження середній вік немовлят становив 17,7 місяця.
Концентрація білка SMN у цільній крові. В когорті низької дози концентрація білка SMN у крові зросла до найвищого медіанного значення 4,49 нг/мл (діапазон – 2,61‑5,55 нг/мл) серед трьох немовлят на 4-му тижні, що вище на 243% від базового показника 1,31 нг/мл (діапазон – 0,58‑4,82 нг/мл) (табл. 1). У когорті високих доз концентрація білка SMN у крові зросла до найвищого медіанного значення 5,87 нг/мл (діапазон – 2,84‑8,76 нг/мл) серед 17 немовлят на 4-му тижні, що вище на 131% від вихідного показника 2,54 нг/мл (діапазон – 1,10‑6,40 нг/мл).
Клінічні результати приймання рисдипламу протягом І частини – 12 місяців (Baranello et al., 2019):
- 90,5% пацієнтів (19 із 21): троє немовлят у когорті низької дози і 16 – високої живі, без потреби у постійній вентиляції (тобто без трахеостомії або двофазної вентиляції з позитивним тиском у дихальних шляхах [BiPAP] ≥16 год/добу безперервно протягом >3 тижнів або без безперервної інтубації >3 тижнів, за відсутності гострої оборотної події або після одужання від неї) (рис. 1);
- 94,7% пацієнтів (18 із 19) були спроможні ковтати самостійно;
- 78,9% пацієнтів (10 із 17) харчувалися перорально;
- у 84,2% пацієнтів (16 із 19) не було кашлю або задухи під час та після їди або пиття;
- 41% пацієнтів (7 із 17) сиділи без підтримки принаймні 5 с за шкалою Бейлі для оцінки розвитку немовлят та малюків, третє видання (BSID-III);
- 88% пацієнтів мали підвищення на ≥4 бали від вихідного рівня показника за шкалою CHOP-INTEND, що свідчить про поліпшення моторної функції;
- 59% пацієнтів (10 з 17) досягли показника ≥40 балів за шкалою CHOP-INTEND.
- 65% пацієнтів сиділи, 59% переверталися на бік, 6% стояли (за HINE‑2) (рис. 2);
- не було пацієнтів, які потребували б постійної вентиляції, трахеотомії або втратили здатність ковтати;
- жодні дані щодо безпеки не призвели до відмови від лікування.
 Рис. 1. І частина FIREFISH: результати застосування препарату Еврісді (рисдиплам) протягом 12 місяців
Рис. 1. І частина FIREFISH: результати застосування препарату Еврісді (рисдиплам) протягом 12 місяців
Примітки: * Дитина жива без постійної вентиляції (тобто відсутність трахеостомії або BiPAP ≥16 год на день безперервно протягом >3 тижнів або безперервної інтубації >3 тижнів, за відсутності або після одужання від гострої оборотної події).
Адаптовано за G. Baranello et al., 2019
 Рис. 2. І частина FIREFISH: постійне зростання моторних навичок між 12-м і 24-м міс. (HINE-2) на тлі лікування рисдипламом
Рис. 2. І частина FIREFISH: постійне зростання моторних навичок між 12-м і 24-м міс. (HINE-2) на тлі лікування рисдипламом
Адаптовано за L. Servais et al., 2020
Клінічні результати прийому рисдипламу протягом ІІ частини – через 12 місяців (Servais et al., 2020):
- 93% пацієнтів (38 із 41) були живі (рис. 3);
- 85% пацієнтів (35 із 41) не потребували постійної вентиляції (тобто без трахеостомії або BiPAP ≥16 год/добу безперервно протягом >3 тижнів або без безперервної інтубації >3 тижнів, за відсутності гострої оборотної події або після одужання від неї);
- 29% пацієнтів (12 із 41) сиділи без підтримки принаймні 5 с за оцінкою відповідно до BSID-III, первинної кінцевої точки було досягнуто (p<0,0001);
- 95% пацієнтів (36 із 38) були живими та зберігали здатність ковтати після 12 місяців лікування;
- 49% пацієнтів (20 із 41) не потребували госпіталізації ≥1 ночі протягом 12 місяців терапії;
- пацієнти досягли значущого поліпшення рухової функції за шкалою CHOP-INTEND (p<0,0001);
- 56% пацієнтів (23 Із 41) досягли оцінки за CHOP-INTEND ≥40 балів на 12-му місяці (рис. 4);
- 62% пацієнтів сиділи, 22% стояли, 2% підстрибували при перевірці за HINE‑2, що неможливо за природного перебігу СМА;
- жодні дані щодо безпеки не призвели до відмови від лікування.
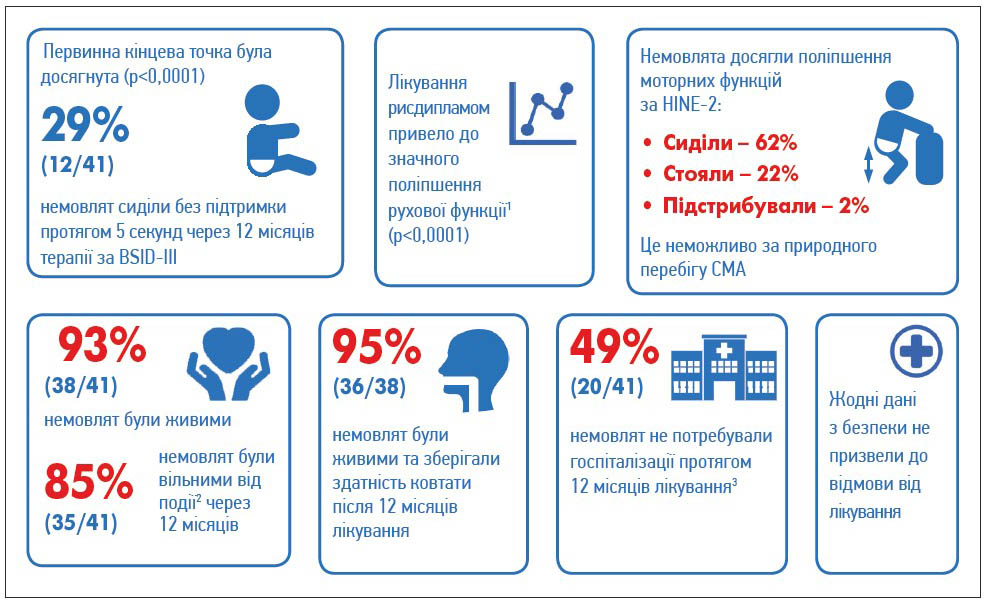 Рис. 3. ІІ частина FIREFISH: результати через 12 місяців
Рис. 3. ІІ частина FIREFISH: результати через 12 місяців
Примітки: 1 За вимірюванням CHOP-INTEND; 2 дитина жива без постійної вентиляції (тобто відсутність трахеостомії або BiPAP ≥16 год на день безперервно протягом >3 тижнів або безперервна інтубація >3 тижнів, за відсутності або після одужання від гострої зворотної події); 3 госпіталізація у лікарню ≥1 ночі.
Адаптовано за L. Servais et al., 2020
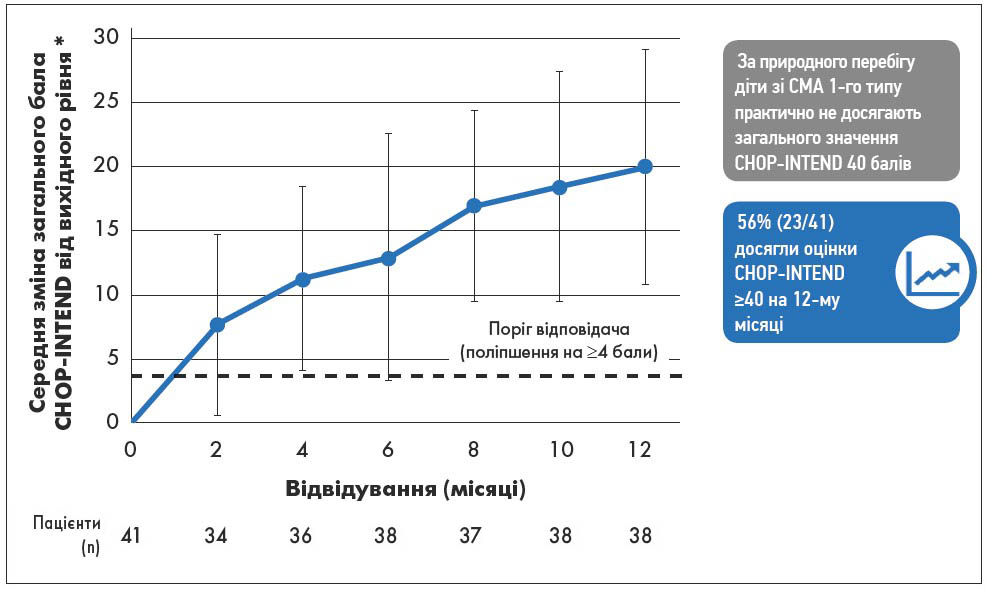 Рис. 4. ІІ частина FIREFISH: продовження поліпшення загального бала CHOP-INTEND протягом 12 місяців
Рис. 4. ІІ частина FIREFISH: продовження поліпшення загального бала CHOP-INTEND протягом 12 місяців
Примітки: * ± стандартне відхилення; р<0,0001, критерій ефективності – 17%, точний біноміальний тест. Припинення збору даних: 14.11.2019.
Адаптовано за L. Servais et al., 2020
Медіана зміни від базової лінії у процентилях для віку серед усіх немовлят на 12-му місяці становить 3 (діапазон – 66‑89), а середній процентиль для вікових груп – 27-й (діапазон – 7‑90). Медіана зміни від базової лінії у процентилі довжини або висоти серед усіх немовлят на 12-му місяці становить 11 (діапазон – 57‑69), а медіана довжини або в исоти для вікового процентилю – 69 (діапазон – 9‑100).
Поліпшення часу виживання без подій через 24 місяці лікування у немовлят, які отримували рисдиплам, порівняно із природним перебігом СМА відображене на рисунку 5.
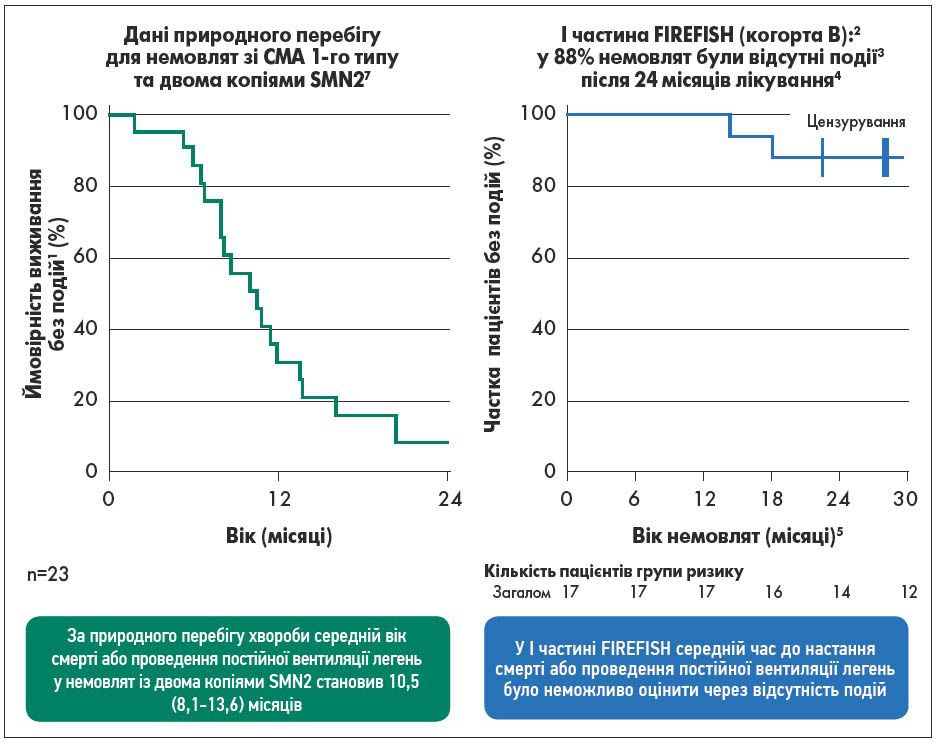 Рис. 5. Поліпшення часу виживання без подій через 24 місяці лікування у немовлят, які отримували рисдиплам, порівняно із природним перебігом СМА
Рис. 5. Поліпшення часу виживання без подій через 24 місяці лікування у немовлят, які отримували рисдиплам, порівняно із природним перебігом СМА
Примітки:1 Виживання без кінцевих точок означало виживання, що не потребувало проведення неінвазивної вентиляції легень щонайменше 16 год/день протягом принаймні 2 тижнів. 2 Когорта високих доз, дозу скореговано відповідно до протоколу. Популяція, яка підлягає лікуванню. 3 Відсутність подій у FIREFISH означала виживання без постійної вентиляції легень (тобто без трахеостомії або BiPAP ≥16 год/добу безперервно протягом >3 тижнів або без безперервної інтубації >3 тижнів, за відсутності гострої оборотної події або після одужання від неї). 4 Летальні наслідки були зареєстровані у двох немовлят когорти В: летальна зупинка серця та дихальна недостатність на 236-й день дослідження у дівчинки віком 7 місяців на тлі початку нічної вентиляції легень (BiPAP <16 год/день) внаслідок підозри на аспірацію; інфекція дихальних шляхів з початком на 386-й день дослідження у дівчинки віком 5 місяців та 3 тижні на момент включення у дослідження. За відсутності лихоманки та наявності помірної симптоматики (закладеність носа та утруднене дихання), яка, здавалося, покращувалася, немовля не було госпіталізоване і померло через 1 день після початку інфекції дихальних шляхів. Ще одне немовля померло приблизно через 3,5 місяці після припинення лікування. Зупинка серця та гіпоксія в контексті пневмонії у хлопчика віком 3 місяців та 3 тижні на момент включення у дослідження, у якого припинили застосовувати рисдиплам на 585-й день за проханням батьків, та стався летальний результат орієнтовно через 3,5 місяці. 5 Немовлята у FIREFISH мали бути віком від 1 до 7 місяців на момент включення у дослідження; середній вік при зарахуванні до І частини (когорта B) становив 6,3 місяця (3,3‑6,9). Припинення збору даних: 03.03.2020.
Безпека. Рисдиплам добре переносився; несприятливих подій, пов’язаних із лікуванням рисдипламом, не було. Всі несприятливі події відображали основне захворювання. Було зареєстровано 24 серйозні несприятливі події: ≥1 серйозної несприятливої події – 10 (48%), ≥1 несприятливої події 3‑5-го рівня – 9 (43%). Найпоширенішими були пневмонія (у 3 немовлят), інфекція дихальних шляхів, вірусна інфекція дихальних шляхів, гостра дихальна недостатність та респіраторний дистрес (у 2 немовлят). Загалом зафіксовано 202 несприятливі події. Троє немовлят померли на момент здійснення зрізу даних. Після зрізу даних для одного немовляти було припинене лікування рисдипламом (на 585-й день) на прохання батьків; немовля померло приблизно через 3,5 місяці через респіраторне ускладнення, пов’язане зі СМА. Небажаних явищ, що призвели б до припинення терапії, не зареєстровано.
Дослідження SUNFISH
Матеріали та критерії включення/виключення
За дизайном SUNFISH – подвійне сліпе плацебо-контрольоване багатоцентрове дослідження ефективності рисдипламу в дітей та молодих людей віком 2‑25 років зі СМА 2-го і 3-го типів. Критерії виключення: застосування в анамнезі таргетної або генної терапії з приводу СМА, планове (протягом 18 місяців) або попереднє (до одного року) оперативне втручання із приводу сколіозу або фіксації стегна. Протягом І частини був зарахований 51 пацієнт, упродовж ІІ – 180 пацієнтів.
Режим дозування:
- І частина дослідження (дослідна частина пошуку дози): визначення дози рисдипламу для ІІ частини при співвідношенні рисдиплам : плацебо 2:1 протягом щонайменше 12 тижнів із подальшим відкритим продовженням у ключовій дозі з дозою, обраною для ІІ частини.
- ІІ частина дослідження: визначення ефективності за шкалою моторних функцій із 32 пунктами оцінки (MFM32) та безпеки (реєстрацію завершено) рисдипламу; застосування рисдипламу : плацебо (2:1) протягом 12 місяців, далі додатково 12 місяців активного лікування, надалі – відкрите продовження.
Результати
Клінічні результати приймання рисдипламу порівняно із плацебо через 12 місяців (Mercuri et al., 2020):
- рисдиплам значно поліпшив моторну функцію через 12 місяців використання порівняно із плацебо згідно зі шкалою MFM32 і переглянутим модулем для оцінювання функцій верхніх кінцівок за СМА (RULM);
- рисдиплам сприяв поліпшенню самостійності пацієнтів за шкалою оцінки незалежності пацієнтів зі СМА (SMAIS), яка включає 22 елементи для визначення рівня самостійності при виконанні повсякденних дій: вживання їжі за допомогою рук, виделки або ложки, чищення зубів, писання / використання ручки;
- жодні дані щодо безпеки не призвели до скасування терапії.
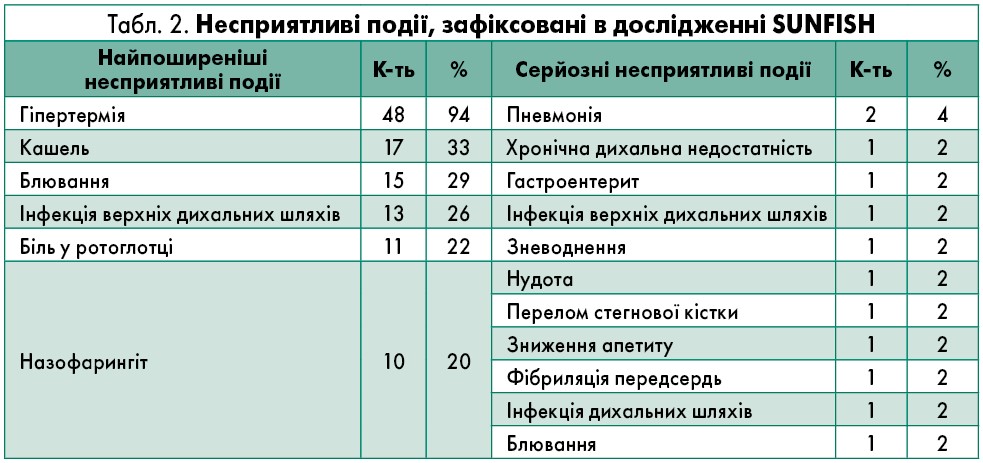
Безпека. Рисдиплам добре переносився; несприятливих подій, пов’язаних із лікуванням рисдипламом, не було. Всі несприятливі події відображали основне захворювання. У 48 пацієнтів (94%) було зафіксовано наявність несприятливих подій; у 9 (18%) виявлено наявність ≥1 серйозної несприятливої події (табл. 2) (Mercuri et al., 2019). Небажаних явищ, що призвели б до припинення терапії, не зареєстровано.
Висновки
Таким чином, отримані достовірні дані на користь ефективності та безпеки застосування рисдипламу в пацієнтів зі СМА 1, 2 і 3-го типу віком 1 місяць – 25 років. Як було зазначено вище, наразі тривають активні дослідження, присвячені пошуку доказів на користь застосування рисдипламу в осіб зі СМА різних вікових груп (від народження до 60 років). Рисдиплам значно розширює можливості терапії СМА та має вагомі клінічні переваги з точки зору виживання, виживання без постійної вентиляції легень, ковтання та здатності до перорального харчування, частоти госпіталізацій, досягнення вікових етапів моторного розвитку.
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 2 (57) 2021 р.
СТАТТІ ЗА ТЕМОЮ Неврологія
Проблема когнітивних розладів є однією з найважливіших у сучасній клінічній медицині. Це зумовлено не тільки збільшенням частки людей старшого віку серед населення, а й посиленням ролі стресу та інших патогенетичних чинників. У березні відбувся семінар «Академія сімейного лікаря. Біль в грудній клітині. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста», у якому прийняли участь провідні вітчизняні науковці і фахівці різних галузей. У рамках заходу професор кафедри військової терапії Української військово-медичної академії Міністерства оборони України, кандидат медичних наук Мар’яна Миколаївна Селюк представила доповідь «Війна та когнітивні порушення. Причина чи наслідок? Як вирішити проблему?». Подаємо огляд цієї доповіді у форматі «запитання – відповідь»....
Хоча нестероїдні протизапальні препарати (НПЗП) мають численні серйозні побічні ефекти, вони належать до найчастіше застосовуваних препаратів у всьому світі (McGettigan P., Henry D., 2013). Через часте застосування побічні дії НПЗП становлять значну загрозу для громадського здоров’я. Так, уже декілька декад тому було описано підвищення артеріального тиску та ризик загострень серцевої недостатності на тлі прийому цих препаратів (Staessen J. et al., 1983; Cannon P.J., 1986)....
У лютому відбувся медичний форум Ukraine Neuro Global 2024, організований ГО «Українська асоціація медичної освіти» (м. Київ). Під час заходу обговорювалися найактуальніші проблеми сучасної неврології. У рамках форуму відбувся сателітний симпозіум «Актуальні питання фармакотерапії в неврології». Слово мала в.о. завідувача кафедри неврології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор Марина Анатоліївна Тріщинська з доповіддю «Краніоцервікалгії: особливості діагностики та лікування»....
Запаморочення є поширеним та іноді стійким симптомом після струсу мозку чи легкої черепно-мозкової травми (лЧМТ). Терміном «запаморочення» часто описують декілька симптомів, як-от головокружіння (вертиго; ілюзія руху), порушення рівноваги (нестійкість, нестабільність) і, власне, запаморочення (пресинкопальний стан). Запаморочення після струсу мозку є клінічним викликом, оскільки існує багато причин цього розладу, а його ведення залежить від етіології [1-3]. Однією з таких причин є пошкодження периферичної вестибулярної системи (внутрішнього вуха). У разі травм, отриманих під час війни, лЧМТ часто пов’язана з вибуховою дією, яка може пошкоджувати внутрішнє вухо. Лікарям важливо розуміти вестибулярні наслідки вибухової лЧМТ, оскільки ЧМТ є дуже характерною для сучасних війн [4]....