Леналідомід і помалідомід у лікуванні множинної мієломи
 За ініціативи Громадської організації «Асоціація гематологів України» 19-21 травня у м. Київ відбулася науково‑практична конференція з міжнародною участю «Нові можливості та невирішені питання гематології». Спікерами були як провідні українські фахівці, так і запрошені іноземні гості. Окремого висвітлення заслуговує доповідь Eleftheria Hatzimichael (Греція) «Леналідомід, помалідомід – сьогодення та майбутнє лікування множинної мієломи».
За ініціативи Громадської організації «Асоціація гематологів України» 19-21 травня у м. Київ відбулася науково‑практична конференція з міжнародною участю «Нові можливості та невирішені питання гематології». Спікерами були як провідні українські фахівці, так і запрошені іноземні гості. Окремого висвітлення заслуговує доповідь Eleftheria Hatzimichael (Греція) «Леналідомід, помалідомід – сьогодення та майбутнє лікування множинної мієломи».
Множинна мієлома (ММ) – злоякісне неопластичне захворювання, яке характеризується надмірною проліферацією моноклональних плазматичних клітин у кістковому мозку із появою моноклонального парапротеїну у сироватці крові або сечі, зниженням рівня нормальних імуноглобулінів і деструктивними змінами у кістках. Відмічаються індивідуальні відмінності у відповіді на терапію та виживаності пацієнтів, які отримують однакове лікування.
Можна виділити два варіанти сучасного лікування мієломи залежно від доступності трансплантації кісткового мозку. Якщо ця опція доступна, спочатку проводять індукційну терапію, потім – консолідацію з подальшою підтримуючою терапією. Якщо можливість провести трансплантацію кісткового мозку відсутня, тоді після індукційної терапії призначають тривалу підтримуючу терапію. Застосування інгібіторів протеасом та імуномодулюючих препаратів у комбінації з аутологічною трансплантацією стовбурових клітин дозволяє покращити загальну виживаність хворих.
Новітні стратегії передбачають використання потрійної комбінації та пролонговане лікування. Потрійна комбінація включає один імуномодулюючий препарат та один препарат групи інгібіторів протеасом для індукційної терапії. Пролонговане лікування полягає у призначенні підтримуючої терапії після аутологічної трансплантації стовбурових клітин у молодших пацієнтів або продовження терапії старших хворих. Це дозволяє отримати кращу відповідь на лікування, підвищити частоту повної відповіді та покращити виживаність без прогресування (ВБП), а у деяких випадках – досягти відсутності залишкової хвороби.
Леналідомід у першій лінії терапії. Результати дослідження FIRST (T. Facon et al., 2018) продемонстрували ефективність леналідоміду у пацієнтів, яким неможливо провести трансплантацію кісткового мозку. Порівнювали комбінації леналідомід + дексаметазон і мелфалан + преднізолон + талідомід (схема MPT). Відмічено істотно більшу медіану ВБП у пацієнтів, які тривалий час отримували леналідомід + дексаметазон (Rd) порівняно з терапією за аналогічною схемою з обмеженою тривалістю – 18 міс (Rd18) чи МРТ. Цей показник становив відповідно 26,0; 21,0 та 21,9 міс, а 4-річна ВБП – 32,6; 14,3 та 13,6% (відношення ризиків – ВР – 0,69; 95% довірчий інтервал – ДІ – 0,59-0,79; p<0,00001). Відповідно до результатів дослідження FIRST, 4-річна загальна виживаність (ЗВ) становила 59% у групі Rd, 58% – Rd18, 51,7% – МРТ (ВР 0,78; 95% ДІ 0,67-0,92; p=0,0023).
A. Larocca (2018) окремо було проведено дослідження у групи пацієнтів старших 65 років із симптомною супутньою патологією щодо порівняння схеми Rd із застосуванням 9 індукційних циклів за цією схемою і продовженням терапії леналідомідом без дексаметазону. Запропонований полегшений варіант призначення леналідоміду з відміною дексаметазону після 9 циклів забезпечував аналогічні показники ВБП і ЗВ при більш прийнятному профілі токсичності.
За даними O’Donnell (2018), ефективним є призначення так званої полегшеної схеми, що включає бортезоміб, леналідомід і дексаметазон, у пацієнтів похилого віку з вираженою супутньою патологією. Досягнуто прийнятні рівні ВБП і ЗВ при задовільному профілі токсичності.
Згідно з протоколами NССN (2021), у пацієнтів зі вперше виявленою ММ VRd є схемою вибору для первинної терапії та єдиною схемою, застосування якої подовжує ЗВ.
У рандомізованому дослідженні III фази SWOG S0777 (B.G. Durie et al., 2017) порівнювали комбінації леналідомід + дексаметазон (Rd) та бортезоміб + леналідомід + дексаметазон (VRd) як первинне лікування пацієнтів із ММ (рис. 1). У дослідженні взяли участь 525 пацієнтів, які були рандомізовані на дві групи.
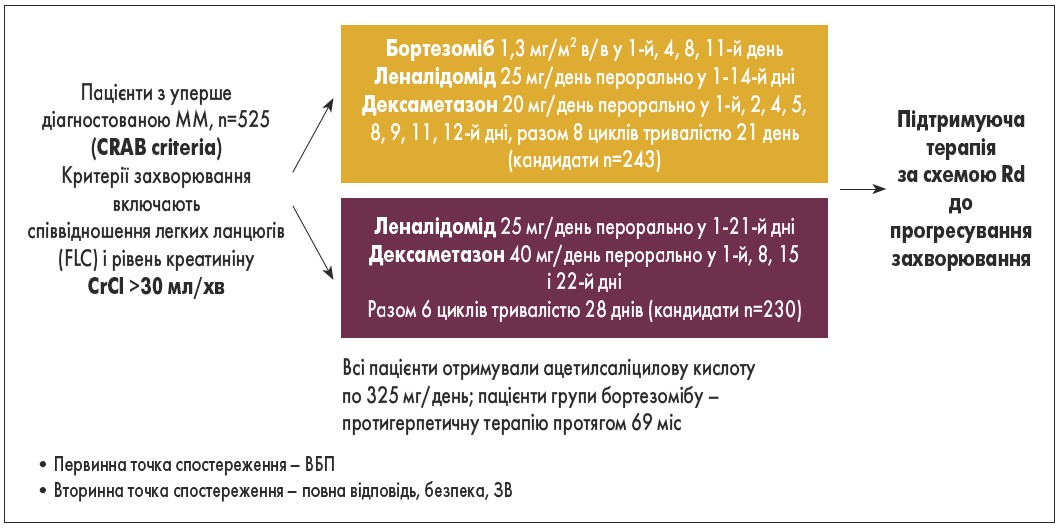 Рис. 1. Дизайн дослідження SWOG S0777
Рис. 1. Дизайн дослідження SWOG S0777
Пацієнти 1-ї групи (n=242) отримували лікування за схемою VRd, пацієнти 2-ї групи (n=229) – за схемою Rd. Додатково всі пацієнти приймали ацетилсаліцилову кислоту по 325 мг/добу; пацієнти групи бортезомібу також отримували протигерпетичну терапію. Первинною кінцевою точкою була ВБП, вторинною кінцевою точкою – ЗВ (рис. 2). Спостереження за пацієнтами тривало 10 років. Результати показали, що при лікуванні комбінацією VRd була відмічена більша частота відповіді на терапію (при Rd – 72%, VRd – 82%), а також більша медіана ВБП (30 та 43 міс відповідно; ВР 0,71; 95% ДІ 0,560-0,906; p=0,0018) та ЗВ (64 та 75 міс відповідно; ВР 0,79; 95% ДІ 0,524-0,959; p=0,0250). Загалом у групі VRd ЗВ перевищила 7 років, ВБП становила понад 3 роки.
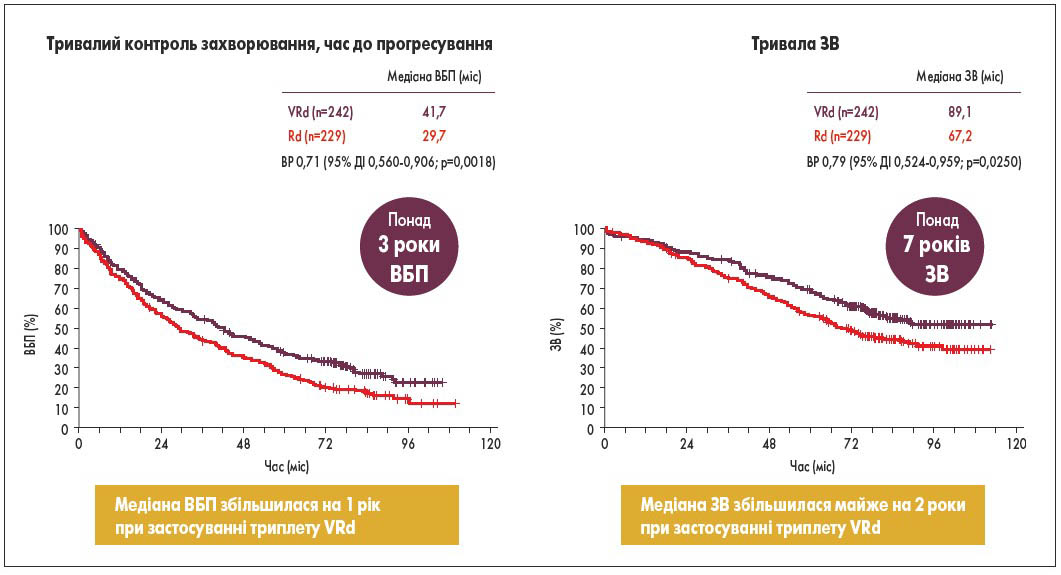
Рис. 2. Схема VRd у порівнянні з Rd для терапії вперше виявленої ММ
Якщо аналізувати результати досліджень з вивчення застосування леналідоміду, найкращі показники досягнуті у дослідженні MAIA (N. Bahlis et al., 2019). У цьому дослідженні до леналідоміду та дексаметазону додали даратумумаб (DaraRd). При медіані спостереження 36,4 міс медіана ВБП у групі пацієнтів, які отримували лікування за схемою Rd, становила 33,8 міс, в той час як у групі DaraRd вона не була досягнута і відмічалося зменшення на 44% ризику прогресування захворювання чи смерті.
На сьогодні комбінація VRd входить до рекомендацій Європейського товариства медичної онкології (ESMO) щодо лікування множинної мієломи у першій лінії незалежно від можливості проведення аутологічної трансплантації кісткового мозку. Окрім цього, DaraRd є опцією вибору у терапії першої лінії для пацієнтів, які не є кандидатами на аутологічну трансплантацію кісткового мозку.
Підтримуюча терапія з використанням леналідоміду. Наразі наявні результати трьох досліджень III фази та проведеного за їх даними метааналізу (McCarthy, 2017). Відмічено, що при застосуванні леналідоміду для підтримуючої терапії після аутологічної трансплантації стовбурових клітин спостерігалося зниження на 26% ризику смерті та подовження на 2,5 року медіани ЗВ. Семирічна ЗВ зросла із 50% у групі спостереження до 62% у групі хворих, які отримували підтримуючу терапію леналідомідом (ВР 0,74; 95% ДІ 0,62-0,89; p=0,001).
За результатами дослідження Myeloma XI (G.H. Jackson, 2017) було також продемонстровано істотне покращення медіани ВБП (з 30,1 до 56,9 міс; ВР 0,48; 95% ДІ 0,40-0,58; p<0,0001) та збільшення 3-річної ЗВ (з 80,2 до 87,5%; ВР 0,69; 95% ДІ 0,52-0,93; p<0,013). Такий ефект спостерігався незалежно від групи цитогенетичного ризику.
Згідно з чинними рекомендаціями ESMO, леналідомід показаний пацієнтам як підтримуюча терапія після аутологічної трансплантації кісткового мозку.
Рецидив мієломи. Незважаючи на вищенаведені результати успішного лікування мієломи, більшість пацієнтів матиме рецидив захворювання з коротшими періодами ремісії та резистентністю до лікарських засобів. Вибір подальшого лікування залежатиме від багатьох факторів, як пов’язаних із біологічними особливостями захворювання чи використаних терапевтичних опцій, так і з самим пацієнтом (вік, загальний стан, супутня патологія, соціально-економічний статус тощо).
За даними 8 рандомізованих досліджень було продемонстровано перевагу трикомпонентної терапії порівняно з двокомпонентною. Більш ефективним було додавання до леналідоміду з дексаметазоном карфілзомібу або елотузумабу, або іксазомібу, або даратумумабу. Це дозволило істотно покращити результати лікування.
За даними дослідження POLLUX (M.A. Dimopoulos et al., 2017), медіана 30-місячної ВБП була більшою у пацієнтів, яких лікували за схемою DaraRd, і становила 58%, порівняно з тими, хто отримував схему Rd – 35% (ВР 0,44; 95% ДІ 0,34-0,55; p<0,001). Якщо пацієнти попередньо отримували одну лінію протипухлинного лікування, то зазначені показники були вищими і становили 39% у групі Rd та 65% у групі DaraRd (ВР 0,41; 95% ДІ 0,29-0,59; p<0,001 ).
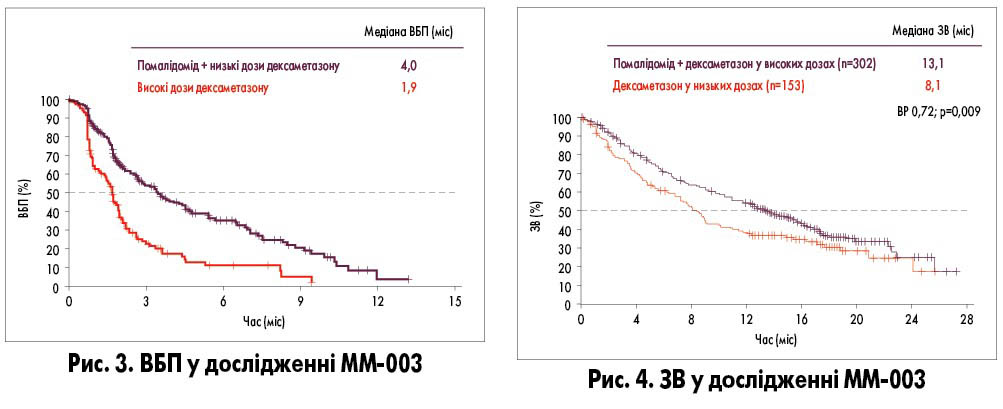
Нові комбінації. Зважаючи на широке використання леналідоміду, у частини пацієнтів розвивається рефрактерність до цього лікарського засобу. За даними дослідження ММ‑003 (M.A. Dimopoulos et al., 2015) продемонстровано збільшення частоти відповіді на терапію з 11% при використанні дексаметазону у високих дозах до 32% при застосуванні комбінації дексаметазону у низьких дозах помалідомідом. При цьому спостерігалося збільшення медіани ВБП з 1,9 до 4,0 міс (p<0,001) та медіани ЗВ з 8,1 до 13,1 міс (р=0,009; рис. 3, 4).
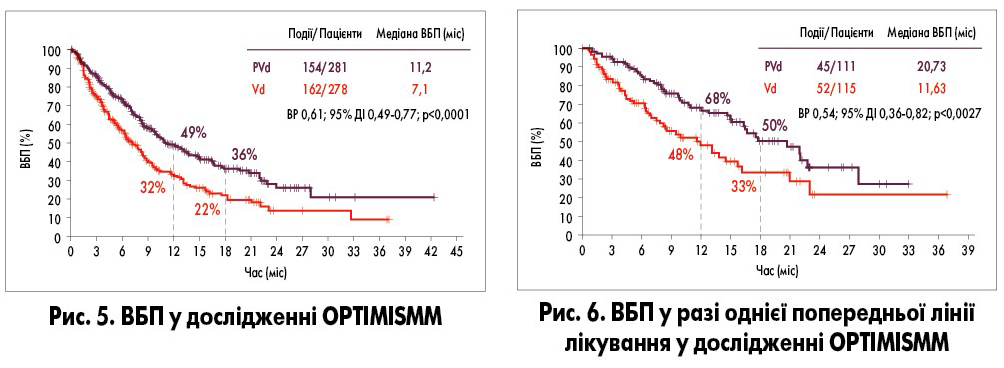
Окремої уваги заслуговує рандомізоване відкрите дослідження OPTIMISMM (P. Richardson et al., 2018) – єдине дослідження III фази, результати якого засвідчили покращення ВБП у пацієнтів з ранньою стадією РРММ, котрі мали рефрактерність до леналідоміду, на 70%. У дослідження були включені 559 пацієнтів зі 133 лікарень і дослідницьких центрів 21 країни. Дослідники порівнювали схеми бортезоміб + дексаметазон (Vd) з помалідомідом або без нього. Відмічено істотне збільшення частки пацієнтів з відповіддю на терапію у групі бортезоміб + дексаметазон + помалідомід (PVd). Крім цього, спостерігали довшу медіану ВБП у групі PVd, ніж Vd: 11,2 та 7,1 міс відповідно (ВР 0,61; 95% ДІ 0,49-0,77; p<0,0001; рис. 5). Більш виражений позитивний ефект від додаткового призначення помалідоміду відмічали при його ранньому застосуванні (одна попередня лінія лікування). У такому випадку медіана ВБП становила 11,63 міс у групі Vd та 20,73 міс у групі PVd (ВР 0,54; 95% ДІ 0,36-0,82; p=0,0027; рис. 6).
Численні опції щодо другої лінії терапії множинної мієломи наведені у рекомендаціях ESMO (2021).
Комбінація бортезомібу з леналідомідом та дексаметазоном – стандарт надання допомоги незалежно від можливості проведення трансплантації кісткового мозку. Підтримуюча терапія леналідомідом показана усім пацієнтам після аутологічної трансплантації кісткового мозку. Оскільки все більше пацієнтів отримують леналідомід у першій лінії лікування або у підтримуючій терапії, відмічається зростання кількості осіб із рефрактерною формою захворювання. Помалідомід може замінити леналідомід при рецидиві множинної мієломи. Комбінація помалідоміду з бортезомібом і дексаметазоном є оптимальною для терапії першого рецидиву у рефрактерних до леналідоміду хворих. Очікуються результати клінічних досліджень щодо інших терапевтичних комбінацій.
Підготувала Олена Поступаленко
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 3 (70) 2021 р
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...