Трофологічний статус і саплементація вітаміном D дітей із ревматичними хворобами
 Ревматичні хвороби займають вагоме місце в структурі тяжкої соматичної патології та інвалідності в дитячому віці. За останні роки досягнуто суттєвих успіхів у вивченні особливостей їх патогенезу та клінічного перебігу, розширилися діагностичні та лікувальні можливості в сфері дитячої ревматології. Однак хронічний перебіг захворювань, базисні лікарські протиревматичні препарати через побічні ефекти, у т.ч. з боку шлунково-кишкового тракту, гепатобіліарної та інших систем і органів нерідко призводять до серйозних порушень в організмі, затримки росту, статевого розвитку, а нерідко й до тяжких незворотних нутритивних розладів, які можуть обтяжувати прогноз та наслідки захворювання і негативно впливати на самопочуття та якість життя хворих. Аналізуючи сучасну медичну літературу, присвячену цій проблемі, можна відзначити, що в дитячій ревматології питанням оцінки трофологічного статусу хворих дітей та використанню трофологічного підходу в комплексі лікувальних і реабілітаційних сучасних заходів приділяється недостатньо уваги.
Ревматичні хвороби займають вагоме місце в структурі тяжкої соматичної патології та інвалідності в дитячому віці. За останні роки досягнуто суттєвих успіхів у вивченні особливостей їх патогенезу та клінічного перебігу, розширилися діагностичні та лікувальні можливості в сфері дитячої ревматології. Однак хронічний перебіг захворювань, базисні лікарські протиревматичні препарати через побічні ефекти, у т.ч. з боку шлунково-кишкового тракту, гепатобіліарної та інших систем і органів нерідко призводять до серйозних порушень в організмі, затримки росту, статевого розвитку, а нерідко й до тяжких незворотних нутритивних розладів, які можуть обтяжувати прогноз та наслідки захворювання і негативно впливати на самопочуття та якість життя хворих. Аналізуючи сучасну медичну літературу, присвячену цій проблемі, можна відзначити, що в дитячій ревматології питанням оцінки трофологічного статусу хворих дітей та використанню трофологічного підходу в комплексі лікувальних і реабілітаційних сучасних заходів приділяється недостатньо уваги.
Клінічна трофологія – міждисциплінарна наука, що вивчає особливості асиміляції їжі у хворої дитини на всіх етапах трофічного ланцюга з метою диференційованої, а в міру необхідності й фармакологічної корекції, наявних структурно-функціональних та метаболічних порушень в інтересах оптимізації гомеостазу та адаптаційних можливостей організму при хронічній соматичній патології. Сучасні протоколи лікування дітей із ревматичними захворюваннями (РЗ) в основному зводяться до медикаментозної терапії та не акцентують увагу лікаря на необхідності профілактики і корекції розладів харчування і білково-енергетичної та вітамінної недостатності у пацієнтів, що сприятиме розвитку різного ступеня нутритивної недостатності або трофологічних порушень [1].
У 1992 р. введено термін «трофологічний статус» (ТС), який комплексно характеризує стан харчування людини та є показником її здоров’я і фізичного розвитку. Раніше в педіатрії оперували терміном «фізичний розвиток», який оцінював масо-ростові антропометричні показники. ТС – більш широке поняття, включає не тільки антропометричні параметри, а й цілий ряд лабораторних та інструментальних критеріїв, які об’єктивно висвітлюють нутритивний стан організму дитини [2].
ТС – це зумовлена конституцією, статтю і віком, супутньою соматичною патологією дитини сукупність адекватних структурно-функціональних і метаболічних взаємовідносин в організмі, які забезпечують його належний гомеостаз і адаптаційні можливості. Звісно, ТС – це найбільш широке поняття, що характеризує стан здоров’я та фізичного розвитку маленького пацієнта, пов’язаний не тільки з харчуванням, а й з особливостями функціонування всіх внутрішніх органів, трофічним ланцюгом та умовами життя [3].
Сучасний стан проблеми оцінки ТС полягає в неможливості повноцінного визначення стану живлення жодним з існуючих тестів; належні висновки робляться на підставі антропометричних і лабораторних даних з урахуванням анамнезу та результатів фізикального обстеження. Базисну оцінку стану харчування слід проводити не пізніше 48 годин з моменту надходження хворого в стаціонар і надалі повторювати кожні 10 днів. Однак багато клініцистів, на жаль, цього не роблять.
В останні роки все більше уваги приділяють синдрому трофологічної (білково-енергетичної) недостатності (ТН). ТН – синдром, який характеризується дисбалансом між потребами організму і надходженням поживних речовин, що спостерігається при недостатньому споживанні їх з їжею та/або при порушенні утилізації в організмі, чи зумовленим патологічними незворотними (аутоімунними) процесами в організмі [4].
Традиційно ТН поділяють на два основних типи: первинну (дефіцит надходження харчових речовин) і вторинну (розвивається на тлі захворювання), патогенез якої включає 3 механізми – гіперметаболізм, мальабсорбцію і порушення харчування [1, 5].
За даними літератури, при РЗ у дорослих ТН різного ступеня залежить від форми і тяжкості перебігу основного захворювання, зустрічається більш ніж у половині випадків, проте в більшості має субклінічний перебіг. Але в дитячому віці на тлі патогенетичної імунодепресивної терапії ТН може мати незворотний характер [6].
Однією з важливих тканин, яка безпосередньо впливає на ТС дитини, є жирова. Доведено, що жирова тканина як імунний та ендокринний орган бере участь у розвитку запального процесу в організмі, оскільки має дві базові функції, такі як ліпогенез і ліполіз. Обмінні процеси у ній регулюються за допомогою безлічі нервових імпульсів і гуморальних реакцій, а також біологічними речовинами – адіпокінами, які включають у себе адіпонектин, інтерлейкін 6 (IL-6), фактор некрозу пухлини альфа (TNF-α), резистин, васпін, вісфатін і багато інших, які складають жирову тканину як ендокринний орган [8, 9]. Серед цієї групи біологічно активних речовин особливу увагу приділяють лептину.
Лептин – це пептидний гормон, здатний регулювати кількість і обсяг жиру в депо жирової тканини. Лептин належить до першого класу цитокінів (сигнальних білків), що циркулює в крові у вільній і пов’язаній формах. Вміст лептину в загальній циркуляції крові підпорядковується добовому ритму з нічним підйомом, а його секреція носить імпульсний характер. Синтез цього гормону контролюється ob-геном, геном ожиріння [10].
Основними ефектами дії лептину є підвищення печінкового глюкогенолізу і захоплення глюкози скелетними м’язами; підвищення швидкості ліполізу і зменшення вмісту тригліцеридів в білій жировій тканині; посилення термогенезу; стимуляція центральної нервової системи (ЦНС); зниження вмісту тригліцеридів в печінці, скелетних м’язах і підшлунковій залозі без підвищення неетерифікованих жирних кислот у плазмі [11]. Увесь спектр його впливів пов’язаний з активацією лептинових рецепторів і вивчений недостатньо [12].
Рівень лептину в сироватці підвищується при збільшенні маси жирової тканини, його продукція в підшкірній жировій клітковині вища, ніж у вісцеральних жирових депо, при цьому рівень лептину відображає не тільки кількість накопиченого жиру, але і порушення енергетичного обміну: при голодуванні він значно знижується, при переїданні підвищується. Склад спожитої їжі (особливо вміст у ній макро- і мікроелементів, наприклад цинку) і різні інші чинники також впливають на рівень лептину. У ряді досліджень було показано, що деякі прозапальні цитокіни (TNF-α, IL-1, IL-6) знижують рівень лептину [13]. Цікаво й те, що вміст лептину в крові залежить від статі. У жінок він виявився вищим, ніж у чоловіків, що може бути пов’язано з різним характером розподілу жирової тканини, а також стимулюючою дією естрогенів і прогестерону [14].
У роботі R. Wolk та співавт. (2001) показана роль лептину як предиктору майбутніх несприятливих серцево-судинних подій, таких як інфаркт міокарду, інсульт незалежно від інших факторів ризику, у тому числі ліпідного статусу і рівня С-реактивного білка у пацієнтів із коронарним атеросклерозом, підтвердженим ангіографічним методом.
Лептин має тісний зв’язок із ЦНС, впливає на енергетичні витрати організму, на потребу в харчуванні та опосередковано, через гіпоталамічні рецептори, регулює апетит [17]. Впливаючи на симпатичну нервову систему, лептин підвищує артеріальний тиск, частоту серцевих скорочень, включається в регуляцію процесів, пов’язаних із термогенезом. У фізіологічних умовах лептин пригнічує синтез інсуліну, який стимулює продукцію лептину [20].
Значення лептину підвищується у зв’язку з його впливом на стан серцево-судинної системи та еластичність артерій. Зв’язок лептину та серцево-судинних захворювань існує постійно поза зв’язком з іншими факторами ризику, що призводять до розвитку цих хвороб. Підвищена ймовірність розвитку тромбозу в зв’язку із взаємодією лептину та його рецепторів на тромбоцитах, які беруть участь у згортанні крові [21]. Не слід забувати і про роль лептину в розвитку інсулінонезалежного цукрового діабету, який виникає завдяки розвитку інсулінорезистентності при великій кількості лептину. У дослідженні H.A. Khafaji та співавт. (2018) показано, що рівень лептину може підвищуватися після інфаркту міокарда, а також виступати прогностичним показником фракції викиду лівого шлуночка [22]. Також показано, що гіперлептинемія, гіперінсулінемія і гіперглікемія призводять до більш активного вивільнення в організмі запальних цитокінів: TNF-α, IL-6, IL-1β, що може запускати процеси запалення. У роботі P.C. Tsiotra та співавт. (2017) людські мононуклеарні клітини від десяти здорових осіб віком від 31 до 41 року протягом 24 годин in vitro були схильні до впливу високих концентрацій інсуліну, лептину і глюкози (окремо або в комбінації). Доведено, що лептин та інсулін окремо або в комбінації значно підвищували продукцію IL-6 (p<0,05), IL-1β (p<0,05) і TNF-α (p<0,02). Крім того, локально синтезований лептин у каротидних атеросклеротичних бляшках може бути асоційований із нестабільністю гемостазу і виникненням надалі церебральної емболії [23]. В одному з останніх досліджень відзначено, що лептин індукує хемотаксис нейтрофілів і модулює фагоцитоз [25].
При ТН та розладах живлення поряд із білково-енергетичною недостатністю в організмі виникає дефіцит вітамінів, мінералів та інших біологічно активних речовин. Серед них привертає увагу дефіцит вітаміну D, який, згідно із сучасними даними, є одним із регуляторів обміну ліпідів та білків в організмі [10].
Вивчення метаболізму вітаміну D триває вже понад 100 років, із часу відкриття McCollum та співавт. (1913) «жиророзчинного фактора росту», який вони виявили у риб’ячому жирі. Зараз спостерігається значна еволюція знань про вітамін D, його уточнені метаболічні шляхи і відкриті нові рецепторно-опосередковані механізми дії (імуномодулювальна, протизапальна, антиканцерогенна дія та ін.). Отже, вітамін D – це стероїдний гормон з ендокринним, паракринним і аутокринним ефектами [5, 19].
Встановлено, що низький рівень забезпеченості вітаміном D асоційований із ризиком розвитку серцево-судинних, хронічних запальних, алергічних, аутоімунних, інфекційних і неопластичних захворювань. Визнано, що вітамін D перетнув кордони метаболізму кальцію і фосфатів і став фактором забезпечення найважливіших фізіологічних функцій, серед яких і підтримка ТС дитини [2].
Синтезований у шкірі під впливом сонячного світла вітамін D та той, що надійшов в організм з їжею, зберігається у печінці та жировій тканині, що забезпечує його достатній рівень у крові, тобто жирова тканина бере участь у становленні нутритивного статусу дитини через різні механізми, серед яких виділяються ефекти дії лептину та вітаміну D [10].
Більшість наукових робіт стосуються вивчення впливу вітаміну D та лептину на ТС при соматичній патології, участь у них брали дорослі хворі; аналогічні дослідження при РЗ поодинокі, а також повністю відсутні у дітей, хворих на РЗ.
У відділенні дитячої ревматології та аутозапальних захворювань ДУ «Інститут ПАГ ім. акад. О.М. Лук’янової НАМН України» проведено дослідження ТС, вмісту лептину та вітаміну D при РЗ у дітей. Обстежено 48 дітей, із них 16 – з ювенільним ідіопатичним артритом (ЮІА), суглобовим, 7 – із системним ЮІА, 9 пацієнтів із системним червоним вовчаком (СЧВ), змішаним захворюванням сполучної тканини (синдром Шарпа), 10 – з ювенільною системною склеродермією (ЮССД), 6 – з ювенільним дерматоміозитом (ЮДМ).
Середній вік обстежених склав 11,15±2,37 років. Переважали дівчата – 29 (60,4%) і пацієнти препубертатного і пубертатного віку – 36 (75,0%). Середня тривалість захворювання 4,1±3,2 років. Усі хворі знаходилися в активному періоді хвороби (більшість І-ІІ ступінь активності) і одержували медикаментозну терапію, що включала базисні препарати (плаквеніл або метотрексат), нестероїдні протизапальні препарати (НПЗП – німесулід, вольтарен, ібупрофен), симптоматичні ліки; 17 дітей отримували глюкокортикостероїди (ГКС), 13 з них – у підтримувальних дозах. Середня тривалість застосування ГК склала 2,5±1,5 років.
Для верифікації діагнозу ССД та СЧВ застосовувалися критерії Американської ревматологічної асоціації (АРА, 1997), діагностичні критерії ЮІА згідно з ILAR (Міжнародна антиревматична ліга, 1997), для діагностики ювенільного дерматоміозиту застосовувалися діагностичні критерії R. Spencer (1999).
Усім хворим проводили комплексне клінічне (збір скарг, вивчення анамнезу, результатів огляду дитини з оцінкою параметрів, що відображають нутритивний статус) та лабораторне обстеження, яке включало клінічний аналіз крові і сечі, біохімічні й імунологічні аналізи крові, а також антропометричне, рентгенологічне, ультразвукове, електрокардіографічне обстеження.
Особливу увагу приділяли клінічним ознакам недостатності харчування: змінам шкіри, волосся, очей, нігтів, слизової оболонки ротової порожнини, оцінці порушень психоневрологічного статусу та проявам трофічних ушкоджень з боку інших органів і систем.
Оцінка стану харчування проводилася способом анкетування за допомогою мінішкали (Mini Nutrition Assessment – MNA), адаптованої для дитини та її батьків, яка оцінює ризик розвитку, наявність або відсутність очевидної гіпотрофії.
Визначення індексу маси тіла (ІМТ) – індексу Кетле – розраховували за формулою:
ІМТ (кг/м2) = МТ факт (кг)/Р2 (м2),
де МТ факт – фактична маса тіла (кг), Р – зріст (м).
У нормі ІМТ визначається в діапазоні 20-24 кг/м2. При ТН відмічається зниження показника ІМТ нижче 20 кг/м2, при підвищенні значення ІМТ більше 24 кг/м2 діагностують надмірну масу тіла, при ІМТ більше 29 кг/м2 визначають ожиріння.
Оскільки важливим показником ТС є лептин сироватки крові, в обстежуваної групи дітей із РЗ вимірювали його рівень, після чого визначали коефіцієнт ТС (КТС) за формулою:
КТС = М/Л,
де М – маса тіла (кг), Л – показник концентрації лептину сироватки крові (нг/мл).
При значенні коефіцієнта від 4 до 5 діагностують відсутність ТН; при значенні коефіцієнта від 6 до 7 – помірний ступінь ТН, при значенні коефіцієнта від 14 до 18 і вище – виражений ступінь ТН.
Рівень лептину у плазмі крові визначався шляхом використання імуноферментного набору для визначення лептину людини (DSL-10-23100 diagnostic system laboratories, USA).
Рівень 25ОНD визначали з використанням імуноферментного набору для кількісного визначення 25-гідроксивітаміну D та інших гідроксильованих метаболітів у сироватці або плазмі виробництва Immunodiagnostic Systems Ltd (Велика Британія).
Ступінь забезпеченості організму вітаміном D оцінювали за прийнятими критеріями (M.F. Holick et al., 2011), згідно з якими його дефіцит встановлюється при рівні 25ОНD нижче 50 нмоль/л, недостатність – при показниках 25ОНD у межах 50-75 нмоль/л. Рівень 25ОНD від 75 до 125 нмоль/л вважається фізіологічною нормою [19].
Результати порівнювали з аналогічними показниками 15 дітей контрольної групи, які знаходилися у клініко-діагностичному відділенні на обстеженні, не мали відхилень у фізичному та статевому розвитку.
Усі отримані цифрові дані опрацьовані статистично за допомогою комп’ютерного пакету програм Microsoft Excel. Достовірність різниць оцінювали за допомогою t-критерію Стьюдента. Різницю між порівнюваними величинами вважали достовірною при р<0,05.
Результати проведених досліджень свідчили, що у 78,5% обстежених хворих на РЗ мало місце порушення ТС. Клінічне обстеження дітей із РЗ показало наявність у них неспецифічних проявів трофологічних змін в організмі, зокрема різного ступеня фолікулярного гіперкератозу (36,4%), сухості з підвищеним лущенням шкіри (21,3%), екхімозів та екстравазатів (9,3%), ксерозу кон’юнктиви (8,7%), койлоніхій (32,7%), пухких і кровоточивих ясен (25,6%), явищ ангулярного стоматиту (17,8%), гіперемії та гіпертрофії сосочків язика (9,8%), рідше – їх атрофію (7,5%), «відбитків» зубів по краю язика (27,3%), відчуття печіння язика (11,7%), різного ступеню проявів карієсу (46,9%), ламкого, тьмяного та рідкого волосся (35,4%), зниження гостроти зору в темну пору доби (13,7%), психомоторних порушень (38,5%), поганого сну (29,3%). У 54,7% дітей діагностували вторинну кардіоміопатію, яка характеризувалася приглушеними серцевими тонами, систолічним шумом у I та V точках, а також метаболічними розладами за даними ехокардіографії. Усі ці ознаки опосередковано свідчать про порушення ТС організму з наявністю дефіциту макро- та мікронутрієнтів при РЗ у дітей.
Для уточнення порушень травлення та ступеню ТН було проведено анкетування за допомогою мінішкали MNA, адаптованої для дітей та батьків. Аналіз анкетування свідчив, що тільки у 23,7% дітей із РЗ харчування було в нормі, ризик гіпотрофії був відсутній і не було необхідності в проведенні другого етапу оцінки, оскільки сумарний бал на першому етапі склав 12 балів і більше (максимально 14 балів). 76,3% дітей із РЗ потребували другого етапу анкетування, який продемонстрував наявність у 41,9% ризику розвитку гіпотрофії, а в 34,4% – очевидну гіпотрофію. Середні значення ризику розвитку гіпотрофії становили від 17 до 23,5 балів, а очевидна гіпотрофія – менше 17 балів. Загальна оцінка за двома етапами анкетування максимально складала 30 балів.
Порівняння ступеню ТН за клінічними та анкетними даними серед пацієнтів із РЗ показало, що найтяжчі порушення харчування реєструються у дітей із системним ЮІА, а також у дітей із ЮДМ та ЮССД. У групі дітей із СЧВ ТН спостерігалася у 64,2% випадків і була оцінена як легка або середнього ступеня. Клінічно цю групу складали дівчата, переважно пубертатного періоду, з ознаками екзогенного гіперкортицизму, надмірним відкладенням жирової тканини на тулубі внаслідок тривалої терапії ГКС. Однак, незважаючи на зовнішні ознаки достатнього або підвищеного харчування, у цих пацієнтів за клінічними проявами та анкетними даними мали місце ознаки дефіциту білків, окремих макро- і мікроелементів та вітамінів.
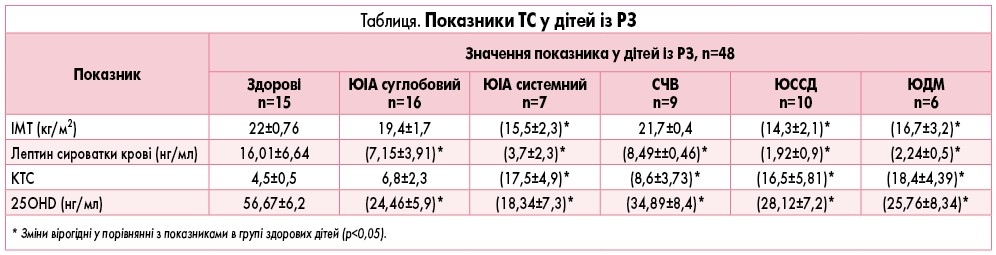
Згідно з отриманими даними (табл.), значно знижений ІМТ констатований в дебюті у дітей із системним ЮІА з високою активністю процесу (15,5±2,3), а також при ЮДМ (16,7±3,2) та ЮССД (14,3±2,1; р<0,05). У той же час цей показник практично не відрізнявся від норми у пацієнтів із суглобним ЮІА (19,4±1,7) та СЧВ (21,7±0,4) порівняно із показником у здорових дітей (22±0,76).
Аналізуючи вміст лептину в сироватці крові у дітей із РЗ, встановлено, що найнижчий рівень лептину визначається у хворих на ЮССД (1,92±0,9 нг/мл) та ЮДМ (2,24±0,5 нг/мл). У дітей із системним ЮІА (3,7±2,3 нг/мл), суглобовою формою (7,15±3,91 нг/мл) та СЧВ (8,49±0,46 нг/мл) цей показник теж знижений, порівняно зі здоровими дітьми (р<0,05), що свідчить про наявність у них ТН (табл.).
За результатами КТС для більш об’єктивної оцінки ТС пацієнтів із РЗ, помірний ступінь ТН виявлений тільки у дітей із суглобовим ЮІА (6,8±2,3), СЧВ (8,6±3,73). Виражений ступінь ТН діагностовано у пацієнтів із системним ЮІА (17,5±4,9), ЮССД (16,5±5,81) та ЮДМ (18,4±4,39; р<0,05).
В усіх обстежених пацієнтів також мало місце зниження забезпеченості організму вітаміном D, що теж можна розглядати як один із показників нутритивної недостатності. Більш виражений дефіцит вітаміну D діагностований у дітей, які хворіють більше двох років, незважаючи на менший ступінь ТН. Це пов’язано із недостатнім перебуванням дітей в умовах природної інсоляції, негативною дією застосованої терапії ГКС, НПЗП, базисних та біологічних препаратів на забезпеченість організму хворої дитини вітаміном D та відсутність своєчасного призначення препаратів цього вітаміну.
Виявлено досить високий прямий кореляційний зв’язок тяжкості ТН між ступенем та активністю РЗ, низьким вмістом лептину та концентрації вітаміну D в крові (r=0,60).
Відмічено, що діти, які тривалий час хворіють на РЗ (більше двох років), мають менш виражену ТН, на відміну від дітей, які захворіли нещодавно, але більш глибокий дефіцит вітаміну D.
З урахуванням отриманих результатів дослідження дітям із РЗ та проявами ТН рекомендується після визначення вмісту кальцитріолу 25ОНD у сироватці крові при недостатності вітаміну D призначати препарати цього вітаміну у добовій дозі 2 тис. МО та при дефіциті – 4-5 тис. МО з моніторуванням забезпеченості цим вітаміном організму дитини 1 раз у 36 міс.
Цільовим є вміст кальцидіолу в сироватці крові 30-50 нг/мл, що відповідає достатньому рівню забезпеченості цим вітаміном, після чого рекомендується приймати підтримувальну дозу протягом 1-2 міс. Можна також скористатися курсовим методом призначення вітаміну D, коли рекомендується доза 2-4 тис. МО на добу протягом місяця з перервою 2-3 міс. – 3 курси на рік.
Заключення
Аналіз даних літератури свідчить, що РЗ супроводжуються розвитком трофологічних порушень і нутритивної недостатності, але ці дані здебільшого стосуються дорослих пацієнтів. У педіатричній літературі зустрічаються лише окремі публікації щодо наявності тих чи інших проявів порушень ТС у дітей із ЮІА та іншими нозологічними формами РЗ. Результати клінічних та лабораторних досліджень, виконаних в інституті, свідчать, що 78,5% дітей із РЗ мають клінічні ознаки ТН, зниження вмісту лептину в сироватці крові, що асоціюється зі зниженням забезпеченості вітаміном D або його дефіцитом в організмі. Перспективним є подальше дослідження з оцінки ТС хворих залежно від тривалості їх лікування протиревматичними базисними, синтетичними і біологічними препаратами, а також дослідження корекції харчування хворих дітей із нутритивною недостатністю та визначення потенційної користі призначення спеціальних енергетичних лікувальних сумішей для ентерального вживання в комплексі з препаратами вітаміну D. Ці дослідження можуть сприяти вирішенню проблем нормалізації ТС у дітей із РЗ, підвищенню ефективності їх лікування та покращенню якості життя і прогнозу перебігу РЗ.
Література
- World Health Organization (2014) Global database on child growth and malnutrition.http://www.who.int/nutgrowthdb/about/introduction/en/index5.html [Accessed: August 18, 2015].
- Луфт В.М., Луфт В.В. Трофологический статус: критерии оценки и диагностики трофической недостаточности // Руководство по клиническому питанию/под ред. В.М. Луфта, С.Ф. Багненко. Изд. 2-е, доп. СПб.: Арт-Экспресс, 2013. С. 57-84.
- Hari A., Rostom S., Hassani A., El Badri D., Bouaadi I., Barakat A., Chkirat B., Elkari K., Bouchra A., Hajjaj-Hassouni N. Body composition in children with juvenile idiopathic arthritis: effect of dietary intake of macronutrient: results from a cross sectional study // The Pan African Medical Journal, 2015; 20: 244. doi:10.11604/pamj.2015.20.244.4488.
- Gajewski M., Rzodkiewicz P., Wojtecka-Lukasik E. The role of physiological elements in the future therapies of rheumatoid arthritis. II. The relevance of energy redistribution in the process of chronic inflammation. Reumatologia. 2015; 53: 1-6. PubMed.
- Racil G., Coquart J.B., Elmontassar W., Haddad M., Goebel R., Chaouachi A., Amri M., Chamari K. Greater effects of high- compared with moderate-intensity interval training on cardio-metabolic variables, blood leptin concentration and ratings of perceived exertion in obese adolescent females \\ Biol Sport. 2016 Jun; 33 (2): 145-52. doi: 10.5604/20831862.1198633. Epub 2016, Apr 1.
- Matusik P., Prokopowicz Z., Norek B., Olszanecka-Glinianowicz M., Chudek J., Malecka-Tendera E. Oxidative/Antioxidative status in obese and sport trained children: a comparative study. Biomed Res Int. 2015; 315747. doi: 10.1155/2015/315747. Epub 2015, Mar 31.
- Madeira I., Bordallo M.A., Rodrigues N.C., Carvalho C., Gazolla F., Collett-Solberg P., Medeiros C., Bordallo A.P., Borges M., Monteiro C., Ribeiro R. Leptin as a predictor of metabolic syndrome in prepubertal children \\ Arch Endocrinol Metab. 2016, Sep 5. doi: 10.1590/2359-3997000000199.
- Gajewski M., Gajewska J., Rzodkiewicz P., Wojtecka-Lukasik E. Influence of exogenous leptin on redox homeostasis in neutrophils and lymphocytes cultured in synovial fluid isolated from patients with rheumatoid arthritis // Reumatologia, 2016; 54, 3: 103-107.
- Gajewski M., Rzodkiewicz P., Gajewska J., Wojtecka-Lukasik E. The effect of leptin on the respiratory burst of human neutrophils cultured in synovial fluid // Reumatologia, 2015; 53: 21-25. PubMed.
- Cui H., Lopez M., Rahmouni K. The cellular and molecular bases of leptin and ghrelin resistance in obesity. Nat Rev Endocrinol, 2017, Vol. 13, no. 6, pp. 338-351.
…
26. https://doi.org/10.1016/j.mbs.2015.06.008/
Повний список літератури знаходиться в редакції.
Тематичний номер «Педіатрія» № 3 (59) 2021 р.
СТАТТІ ЗА ТЕМОЮ Педіатрія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....
Зв’язок між рівнем сироваткової сечової кислоти (ССК) і ризиком серцево-судинних захворювань (ССЗ) упродовж багатьох років є предметом вивчення дослідників. Установлено, що рівень ССК – незалежний предиктор смерті від усіх причин і серцево-судинної смерті, зокрема від гострого коронарного синдрому, інсульту та серцевої недостатності (СН). Також опубліковано багато робіт про зв’язок між ССК і функцією нирок. Попри значну кількість публікацій, деякі моменти, а саме: яким є оптимальний поріг ССК для визначення ризику ССЗ, чи необхідна корекція значень ССК для функції нирок, чи є ССК ключовим патологічним елементом метаболічної дисрегуляції, потребують прояснення....