Хронічне обструктивне захворювання легень і рак легень
Хронічне обструктивне захворювання легень (ХОЗЛ) – це стан, якому можна запобігти і який можна вилікувати. Він характеризується стійкими респіраторними симптомами і посиленою запальною реакцією на дію шкідливих частинок і газів. Незважаючи на те що ХОЗЛ часто асоціюють з іншими хронічними захворюваннями, зокрема емфіземою і бронхітом, у значної частини пацієнтів розвиваються загострення, які часто потребують госпіталізації. Збільшення частоти тяжких загострень ХОЗЛ пов’язане із суттєвим погіршенням результатів виживаності. На ХОЗЛ страждає 8-10% дорослого населення країн із високим рівнем доходу і 15-20% курців. Всесвітня організація охорони здоров’я прогнозує, що якщо не вжити життєво важливих заходів для зменшення основних факторів ризику, здебільшого куріння тютюну і впливу забруднювачів довкілля, то до 2030 року ХОЗЛ стане третьою провідною причиною смерті у світі.
Ключові слова: хронічне обструктивне захворювання легень, ХОЗЛ, рак легень, мікробіом легень, тютюновий дим, генетика, епігенетика, соматичні мутації, діагностичні біомаркери, позаклітинні везикули
Рак легень (РЛ) є основною причиною смертності від онкологічних захворювань, саме на РЛ припадає майже п’ята частина всіх випадків смерті від раку в усьому світі. За оцінками, до 2030 року кількість смертей від РЛ зросте до 10 млн на рік. Незважаючи на покращення результатів виживаності пацієнтів з іншими типами раку, загальний 5-річний рівень виживаності пацієнтів із РЛ – 16% упродовж останніх трьох десятиліть залишався порівняно незмінним.
Виділяють два основні підтипи РЛ –дрібно- і недрібноклітинний (ДКРЛ і НДКРЛ); які диференціюють за їхнім клітинним походженням і фенотипом. НДКРЛ становить більшість (85%) випадків і розвивається з епітеліальних клітин легені. Далі НДКРЛ поділяється на аденокарциному, плоскоклітинний і крупноклітинний рак. ДКРЛ має чіткі гістологічні особливості нейроендокринної диференціації і дрібних клітин із мізерною цитоплазмою і становить приблизно 15% випадків.
Епідеміологічні дані, що пов’язують ХОЗЛ і РЛ
Куріння
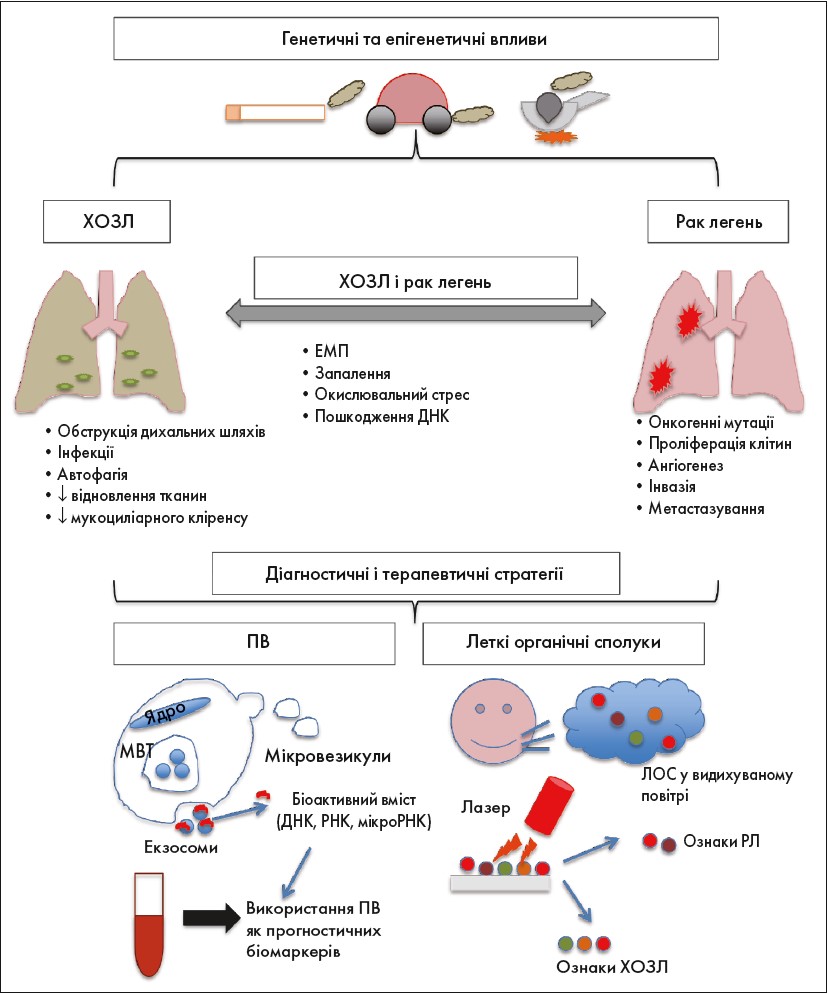
Тютюновий дим – найпоширеніший (майже 90% випадків) фактор ризику розвитку ХОЗЛ і РЛ. Під найбільший ризик захворіти на РЛ підпадають саме пацієнти з ХОЗЛ, що свідчить про спільні патологічні механізми, як-от хронічне запалення, епігенетичні зміни й порушення процесів відновлення ДНК у результаті оксидативного стресу. Останній, унаслідок екзогенних і ендогенних факторів, експресії аутоантитіл, активності протеази і вивільнення запальних цитокінів, як відомо, спричиняє руйнування дихальних шляхів (ДШ), гіперінфляцію легень і захоплення повітря, пошкоджуючи легені у хворих на ХОЗЛ (рис.). Таке регулярне пошкодження легень зрештою призводить до обмеження потоку повітря, а згодом – до подальшого порушення кліренсу вдихуваних токсичних частинок і збільшення експозиції на рівні епітелію. Як наслідок, хронічне запалення, інфільтрація імунних клітин і оксидативний стрес зберігаються ще довго після припинення впливу сигаретного диму.
Рис. Генетичні та епігенетичні впливи, які можуть призвести до розвитку ХОЗЛ і РЛ
ХОЗЛ і РЛ, хоча і є різними захворюваннями, мають подібні механізми патогенезу, у тому числі епітеліально-мезенхімальний перехід (ЕМП), запалення, окислювальний стрес і пошкодження ДНК. Нові діагностичні і терапевтичні стратегії, що сьогодні досліджують, стосуються позаклітинних везикул (ПВ) – вони утворюються в мультивезикулярних тільцях (МВТ), які потім зливаються з плазматичною мембраною, щоб вивільнити біоактивний «вантаж» у позаклітинний простір; леткі органічні сполуки (ЛОС), які можна виявити у видихуваному повітрі пацієнтів, також мають діагностичний потенціал при захворюваннях легень завдяки виявленню унікальних ознак.
У пацієнтів із ХОЗЛ, які при цьому ще й курять, приблизно в 70-80% випадків саме їхня хвороба передує розвитку РЛ. Дослідження Mannino та співавт. виявило чіткий лінійний зв’язок доза-реакція між тяжкістю ХОЗЛ і ризиком виникнення РЛ. Велике ретроспективне дослідження хворих на РЛ показало, що супутнє ХОЗЛ асоціюється зі значно гіршими результатами виживаності. Встановлено, що наявність емфіземи створює значний ризик розвитку РЛ, особливо плоскоклітинного раку і ДКРЛ. Загалом пацієнти з ХОЗЛ мають підвищений ризик (від 4 до 6 разів) розвитку РЛ незалежно від історії куріння, віку і статі.
Забруднення повітря
Вплив деяких металів, пилу і промислових парів є недооціненими факторами ризику розвитку ХОЗЛ. Водночас вважається встановленим причинно-наслідковий зв’язок між шкідливим впливом азбестових волокон і радону на здоров’я людини і розвитком РЛ. Доведено, що збільшення концентрації в міському повітрі дрібних твердих частинок на кожні 10 г/м3 призводить до збільшення ризику розвитку РЛ на 14%. Нещодавній аналіз, здійснений Liu та співавт., виявив потужний зв’язок між поширеністю ХОЗЛ і вмістом твердих частинок у міському повітрі.
У країнах із низьким рівнем доходу забруднене повітря в приміщеннях є провідним фактором ризику розвитку ХОЗЛ і РЛ. Забруднення атмосферного повітря внаслідок спалювання деревини й вугілля підвищують ризик захворювання через збільшення вмісту токсичних твердих частинок, поліциклічних ароматичних вуглеводнів і гетероциклічних ароматичних сполук.
Жительки Південно-Східної Азії мають непропорційно високий рівень захворюваності на РЛ проти жінок інших етнічних груп, незважаючи на те що куріння сигарет є рідкістю в цій демографічній групі. Декілька епідеміологічних досліджень повідомляють про випари олії і недостатню вентиляцію кухні як фактор ризику РЛ і ХОЗЛ. Наступні дослідження за участю жінок у Китаї і Тайвані показують дозозалежний ризик виникнення РЛ унаслідок використання летких органічних сполук у зв’язку з мутагенною або окислювальною дією різних компонентів, що містяться в олійних випарах.
Генетичні та епігенетичні механізми, які пов’язують ХОЗЛ і РЛ
Фенотипово ХОЗЛ і РЛ дуже різнорідні захворювання. Особливістю ХОЗЛ є хронічне ураження легень, яке характеризується незворотним обмеженням потоку повітря, запаленням малих ДШ і прогресувальним руйнуванням дистальної дихальної паренхіми легень, що призводить до емфіземи. Для порівняння, у разі РЛ відбувається пошкодження ДНК, яке спричинює перевиробництво стимулювальних білків, надмірної нерегульованої проліферації і дефектної регуляції контрольної точки клітинного циклу, що надає селективну біологічну перевагу над нормальними клітинами. Попри те що куріння вважають основним фактором ризику розвитку РЛ і ХОЗЛ, лише в 10-20% курців розвивається ХОЗЛ, а в 10-15% осіб, які ніколи не курили, – РЛ. Хоча не в усіх курців розвинеться РЛ, вплив довкілля, тютюнового диму й летких агентів виявляє основні генетичні відмінності і різну сприйнятливість до цих легеневих захворювань серед курців.
ХОЗЛ
Ранні генетичні дослідження сімейних зв’язків при ХОЗЛ виявили, що мутації гена SERPINA1 призводили до серйозного дефіциту альфа1-антитрипсину (AAT), їх частота становила приблизно 1% випадків. Зовсім недавно були проведені дослідження геномних асоціацій (genome-wide association studies, GWAS) для виявлення зв’язку між ділянками хромосом і фенотипами хвороби для прогнозування ризику або сприйнятливості до захворювання. GWAS і метааналіз Cho та співавт. підтвердили, що 3 відомі локуси в CHRNA3, CHRNA5, FAM13A і HHIP асоційовані з підвищеним ризиком розвитку ХОЗЛ, а також MMP12, TGFB2 і новий локус RIN3.
Рак легень
Широкомасштабні дослідження геномного профілювання виявили молекулярну складність РЛ. Незважаючи на встановлений причинно-наслідковий зв’язок між тютюновим димом і розвитком РЛ, є накопичувані докази про спадковий компонент захворювання. Успадковуваність РЛ, за оцінками, становить від 15 до 25%, при цьому в пацієнтів, які мають родичів першого ступеня, ризик зростає приблизно на 50%, особливо коли РЛ у родичів діагностували в молодому віці і були випадки, коли хворіло декілька членів сім’ї. Ранній аналіз зв’язків 52 сімей із хворими на РЛ виявив локус сприйнятливості з високою пенетрантністю в регіоні 6q23-25. Подальші аналізи 93 сімей високого ризику підтвердили, що цей рідкісний генетичний варіант значуще підвищує ризик захворіти на РЛ.
Частка пацієнтів, які ніколи не курили, становить 25% випадків серед хворих на РЛ, до того ж ці особи мають певні молекулярні і патологічні особливості. Понад 50% жінок, хворих на РЛ, ніколи не курили; однак ці цифри різняться залежно від географічного регіону (Азія >Північна Америка >Європа). Дослідження показали, що на цю унікальну підгрупу пацієнтів можуть впливати гормональні чинники, спадковий ризик і шкідливий вплив довкілля. Поліморфізм CYP1A1 і GTSM1, ферментів метаболізму ксенобіотиків, пов’язаний із ризиком РЛ у некурців європеоїдної раси, а поліморфізм MLH1, ферменту відновлення невідповідності, відіграє роль у розвитку раку за відсутності впливу тютюнового диму. У тих, хто ніколи не палив, поліморфізм генів, пов’язаних із запальним механізмом, у тому числі інтерлейкіну (IL)-10, фактора некрозу пухлини (TNF), IL1-RN та IL‑6, асоційований із підвищеним ризиком виникнення РЛ.
Генетичне перехрещення РЛ і ХОЗЛ
Через спільну генетичну сприйнятливість ХОЗЛ і РЛ можуть існувати поза їх патогенними процесами, спричиненими курінням. Дослідження GWAS виявило асоціації, які підтверджують думку, що деякі локуси, які визначають сприйнятливість до ХОЗЛ, також важливі для виникнення РЛ у курців. Патогенетичною особливістю ХОЗЛ і РЛ є ЕМП, а також запалення, а генотип rs7326277TT у VEGFR1 сприяє цим процесам, а також росту пухлини і є локусом, що провокує обидва захворювання (рис.). Крім того, підвищений ризик розвитку ХОЗЛ і РЛ також був продемонстрований при поліморфізмі гена протизапального IL‑10.
Зовсім недавно дослідження GWAS за участю понад 250 тис осіб виявило 35 нових генетичних локусів ризику ХОЗЛ, із них 13 були пов’язані з функцією легень, підтримуючи компонент генетичної сприйнятливості розвитку ХОЗЛ. Біоінформатичний аналіз цих даних додатково з’ясував біологічні шляхи, були залучені гени й клітини і потенційні терапевтичні мішені.
Соматичні мутації
Соматично набуті «мутації втрати функцій» (loss-of-function mutations) PTEN і TP53, а також «мутації посилення функції» (gain-of-function mutations) EGFR і Ras часто наявні в епітелії курців і хворих на РЛ. Мутації онкогенів EGFR і KRAS найчастіше виявляють при аденокарциномі легень, причому надмірну експресію EGFR спостерігають у 40-80% випадків НДКРЛ, що пов’язано з вищим рівнем метастатичної і пухлинної проліферації, вищою стадією хвороби і гіршим прогнозом. Подальші мутантні форми EGFR (делеція в екзоні 19 і L858R в екзоні 21) з активністю тирозинкінази відіграють певну роль у канцерогенезі легень і вважаються терапевтичними мішенями. Це привело до розробки специфічних інгібіторів тирозинкінази EGFR, таких як гефітиніб і ерлотиніб, які були затверджені FDA (Управлінням із санітарного нагляду за якістю харчових продуктів і медикаментів США) як терапевтичні засоби для прогресувального й метастатичного НДКРЛ. Дія цих препаратів полягає в пригніченні фосфорилювання рецепторів у внутрішньоклітинному домені, конкуруючи з аденозинтрифосфорною кислотою (АТФ) та АТФ-зв’язувальну ділянку. Вважається, що частота мутацій EGFR зумовлена генетичною нестабільністю, що спричинює ампліфікацію генів.
Через доведений мутаційний вплив сигаретного диму вважають, що молекулярному патогенезу ХОЗЛ можуть сприяти набуті соматичні мутації, а не поліморфізми зародкової лінії. Отже, посилення сигналізації NF-κB і AP‑1 опосередковує експресію запальних цитокінів і протеїназ у відповідь на окислювальний стрес. Крім того, наявність цих соматичних мутацій і їхніх проміжних молекул конвергує з факторами транскрипції, що спричинює зміну фенотипу бронхіального епітелію у вигляді плоскоклітинної метаплазії. Цей порушений фенотип спричинює розвиток ХОЗЛ внаслідок порушення імунного захисту, що сприяє стійкому запаленню, повторним інфекціям і резистентності до інгаляційних кортикостероїдів у деяких пацієнтів.
Епігенетика
На відміну від соматичних мутацій і основної генетичної схильності епігенетичні зміни – це модифікації, які впливають на експресію генів без змін послідовності нуклеотидів. Показано, що в пацієнтів із РЛ і ХОЗЛ модифікації ДШ і легень унаслідок куріння спричинюють епігенетичні зміни, зокрема метилювання ДНК, експресію мікроРНК та ацетилювання гістону.
Метилювання ДНК
Метилювання ДНК – це зворотна модифікація структури ДНК шляхом додавання метильної групи до положення 5‘ залишку цитозину. Цей процес може зачіпати відрізок CpG або кластеру генів супресорів пухлини, які посилюють проліферацію. Щодо ХОЗЛ, метилювання ДНК, імовірніше, пов’язане з гіпометилюванням імуномодулювальних генів, як-от SERPINA1, який кодує AAT, що призводить до надмірної експресії генів.
У разі РЛ спостерігається гіперметилювання як промоторних, так і супресорних генів. Зворотність метилювання робить його привабливою мішенню для терапії раку. Профілі метилювання ДНК можуть різнитися в курців і пацієнтів із ХОЗЛ, а також різними підтипами НДКРЛ, і тому характеристика панелі метилювання в периферичній крові може зіграти потенційно важливу роль як біомаркер діагностики і моніторингу захворювань.
У широкому епігеномному дослідженні виявлено, що метилювання ДНК і репресія генів CCDC37 і MAP1B значуще переважають у пацієнтів, що мають одначасно ХОЗЛ і РЛ, якщо порівняти з випадками без ХОЗЛ. У хворих на РЛ виявлено вищий проти пацієнтів із ХОЗЛ ступінь метилювання.
МікроРНК регуляція
МікроРНК (мiРНК) – це невеликі некодуючі молекули РНК і первинні епігенетичні медіатори, які беруть участь у критичній посттранскрипційній регуляції шляхом поступальної репресії або деградації мішеневої міРНК. Понад 60% генів, які кодують білок, регулюються за допомогою мiРНК. Завдяки широкому спектру генів-мішеней мiРНК беруть участь у регуляції багатьох ключових фізіологічних процесів, таких як клітинний метаболізм, апоптоз, диференціація тканин і відновлення ДНК, а також ініціювання й прогресування патогенних процесів, що призводять до хронічної інфекції, запалення і виникнення пухлини.
У процесі нещодавнього дослідження встановлено значне зниження регуляції miR‑218-5p у легеневій тканині хворих на ХОЗЛ, проти не-курців, а також суттєву кореляцію цього явища з тяжкістю обструкції ДШ. Клінічна й доклінічна перевірка також показала, що найвища експресія miR‑218-5p була локалізована в епітелії бронхів. Подальші експерименти свідчать про те, що miR‑218-5p може відігравати роль у захисті від запалення, спричиненого сигаретним димом, і патогенезі ХОЗЛ.
Характерні для захворювання моделі експресії мікроРНК є перспективними діагностичними і прогностичними біомаркерами в разі НДКРЛ і ХОЗЛ. Keller та співавт. профілювали міРНК у крові хворих на ХОЗЛ і виявили значне зниження регуляції дев’яти міРНК у пацієнтів, в яких розвинувся РЛ. Певні мiРНК були залучені до регулювання шляхів, пов’язаних із раком, у тому числі MAP-кінази, передачі сигналів інтегрину і фокальна адгезія. Крім того, за допомогою класифікатора трьох міРНК (miR‑450a‑5p, miR‑4677-3p та miR‑9-3p) площа під кривою (AUC) 0,87 вказувала на вірогідність розвитку РЛ у хворих на ХОЗЛ.
Нещодавно Mateu-Jimenez та співавт. показали, що вираженість профілю експресії чотирьох мiРНК (miR‑21, miR‑200b, miR‑210, miR-let7c) і загального метилювання ДНК у хворих на РЛ і ХОЗЛ збільшена проти пацієнтів без ХОЗЛ. Крім того, пухлини легень пацієнтів (хворих одночасно на ХОЗЛ) демонстрували знижену експресію мішеневих генів мiРНК, зокрема PTEN, MARCK і KRAS, якщо порівняти з пацієнтами без ХОЗЛ. Це дослідження підтвердило значну роль епігенетики в регулюванні клітинних шляхів, що збільшують ризик пухлинного розвитку на тлі ХОЗЛ, і те, як епігенетичні профілі можуть впливати на ефективність лікування раку в пацієнтів із супутніми респіраторними захворюваннями.
Експресія генів у разі ХОЗЛ і РЛ
Були проведені масштабні дослідження профілювання експресії генів для кращого розуміння патогенезу ХОЗЛ і РЛ шляхом кількісної оцінки транскриптому. Досягнення оміксних технологій (omics) сприяли переходу до аналізу і публікації наборів даних multi-omics, завдяки чому використання даних транскриптому, транслатому і протеому використовують для підвищення точності і валідності молекулярних досліджень. Строма легень – це композиція фібробластів і мезенхімальних стромальних клітин, які утворюють структурну і функціональну підтримувальну мережу для тканини. Нещодавно Сандрі та співавт. застосували підхід multi-omics для характеристики двох різних моделей експресії стромальних генів при РЛ, які відрізнялися за функцією легень (FEV1 – об’єм форсованого видиху за 1-шу секунду). У пацієнтів із нормальними показниками і порушеннями легкого ступеня продемонстровано переважну активацію mTOR для сприяння розвитку раку. І навпаки, строма пацієнтів із тяжкими обструктивними порушеннями координувала передачу сигналів, пов’язаних із раком, через фіброзний позаклітинний матрикс (англ. extracellular matrix, ECM).
Неоплазія і пухлинне мікрооточення
Куріння негативно впливає на епітелій ДШ, провокуючи прозапальний та імунодепресивний ефект. Було проведено дослідження впливу куріння на імунне мікросередовище нормального епітелію ДШ людини шляхом вимірювання рівнів активації та інфільтрації Т-клітин за допомогою експресії генів. Повідомлено, що рівень імуносупресії мав ступеневу кореляцію зі збільшенням експозиції куріння. У разі ХОЗЛ гіперплазія і метаплазія епітелію є наслідком впливу сигаретного диму і/або інфекцій, що спричинюють повторне пошкодження слизової оболонки епітеліального тракту.
Доведено, що РЛ розвивається в межах метапластичного мікросередовища. Запалення може спричинити появу гіперпластичних вогнищ у непухлинних умовах, однак якщо ці ураження зазнають неконтрольованої проліферації, вони можуть трансформуватися і демонструвати неопластичні й атипові аденоматозні прояви, набуваючи інвазивних, ангіогенних і метастатичних властивостей.
Повідомляється, що на ріст і прогресування пухлини впливають двонаправлені перехресні зв’язки між пухлинними клітинами та оточуючою їх стромою, а позаклітинні сигнали в мікросередовищі пухлини також можуть регулювати прогресування і метастазування раку. Тому важливо розуміти, як і коли мікросередовище легень долучається до процесу і клітини починають сприяти ангіогенезу, пов’язаному з пухлинним запаленням. Попередні дослідження змогли виявити потенційні біомаркери РЛ, проаналізувавши і порівнявши генетичні та епігенетичні мутації гістологічно нормальної тканини FFPE з тканиною пухлини. У процесі дослідження Р. Keohavong та співавт. мутації KRAS у гістологічно нормальній тканині, що оточує пухлину легень, виявили в 16% пацієнтів з аденокарциномою легень.
Поле канцеризації
Теорія поля канцеризації описує широкі невибіркові молекулярні і клітинні зміни поверхневого епітелію, що відбуваються в певній анатомічній ділянці під впливом канцерогенів. Ранні дослідження Slaughter та співавт. описують початковий ефект канцерогенів і «поле канцеризації» епітеліальних тканин, що призводить до розвитку пухлини. Концепція передбачає, що гістологічні зміни розвиваються як у пухлині, так і в прилеглій нормальній тканині, і полягають у гіперплазії епітелію і гіперкератинізації. Результати цих досліджень дали науковцям підстави висунути гіпотезу, згідно з якою соматичні зміни можуть відбуватися природним шляхом або в результаті мутагенного впливу і сприяти формуванню презлоякісного простору, що після клональної експансії може призвести до неопластичного росту. Презлоякісний простір часто виникає без жодних гістопатологічних змін і може або призвести до пухлини, або ні.
Біологічні механізми, спільні для ХОЗЛ і РЛ
Запалення
У хворих на ХОЗЛ розвивається виражене запалення, яке корелює з тяжкістю захворювання, і оскільки це руйнівне запалення спостерігається при емфіземі, воно може спричинити розвиток РЛ. Подальші дослідження виявили властивості імунних клітин, специфічні для ХОЗЛ, які відрізняються від таких при РЛ, а саме – у хворих на ХОЗЛ спостерігають зсув фенотипу альвеолярних макрофагів у бік M1, як показано на клітинах рідини бронхоальвеолярного лаважу, що поляризують до фенотипу Th1 через інтерферон-γ (IFN-γ). Виділені цитокіни представлені CXCL10, який може індукувати еластазу макрофагів. Вивільнення IL‑8 альвеолярними макрофагами і клітинами епітелію легень спричинює утворення нейтрофільних інфільтратів у хворих на ХОЗЛ. Імовірно, цей цитотоксичний профіль Th1 є сприятливим для пухлинного мікрооточення, однак не спостерігається при великих пухлинах, що представляють фенотип Th2, активований макрофагами М2.
Через природу запальних клітин, що оточують РЛ, в емфізематозних легенях можуть виникати мікросередовища, які конкурують із захворюваннями. Встановлено, що в разі ХОЗЛ цитотоксичне середовище сприяє утворенню пухлини внаслідок ROS-генотоксичного впливу через макрофаги і нейтрофіли, що сприяє утворенню аддуктів ДНК, які призводять до генетичної мутації. Це дає можливість новоутворенням на ранніх стадіях у навколишньому мікрооточенні вивільняти хемокіни й цитокіни (такі як TNFα, IL‑1β, IL‑6 і [транскрипційний ядерний фактор] NF-κB), які змінюють склад імунних клітин і виявляють прямий вплив на пухлинні клітини. Крім того, запалення пов’язане з багатьма аспектами прогресування пухлини легень, зокрема з проліферацією клітин, метастазуванням і відповіддю на хіміотерапевтичне лікування. Наприклад, IL‑17C, який сприяє рекрутуванню нейтрофілів, може спричинити запалення в мікрооточенні пухлини і посилювати її ріст.
Незалежно від мутагенної дії тютюнового диму хронічне запалення, яке спостерігається при ХОЗЛ, є потенційним фактором розвитку РЛ. Низка структурних і запальних клітин бере участь у патогенезі ХОЗЛ і РЛ, у тому числі нейтрофіли, а також CD4+- і CD8+-лімфоцити.
Оксидативний стрес
Майже завжди в пухлинній тканині розвивається запалення, і цілком можливо, що хронічне запалення, яке супроводжує ХОЗЛ, може бути потужним фактором розвитку РЛ. Запалення також є основним джерелом активних форм азоту й кисню (RNOS), рівень яких у хворих на ХОЗЛ постійно підвищений. Мітохондрії є основним клітинним джерелом RNOS, і при ХОЗЛ їхня функція порушена. Кілька досліджень пов’язують метилювання фактора транскрипції А при ХОЗЛ і плоскоклітинному РЛ.
Механізми пошкодження і відновлення ДНК при ХОЗЛ і РЛ
Пошкодження ДНК, спричинене реактивними кисневими частинками (ROS), одноланцюговими розривами і ділянками, з видаленими азотистими основами, збільшується при ХОЗЛ і РЛ. Дослідження показали, що збільшення пошкодження ДНК відбувається не лише через сигаретний дим. У хворих на ХОЗЛ у легенях частіше виявляють дволанцюгові розриви , якщо порівняти з курцями і некурцями без ХОЗЛ. Це можливо зумовлено тим, що у хворих на ХОЗЛ, спостерігають вищі рівні мікросателітної нестабільності й частоти соматичних мутацій, а також втрати гетерозиготності. Подальший підвищений рівень окисного пошкодження ДНК виявляється в кластерах функціонально значущих послідовностей, що свідчить про те, що роль окисного пошкодження ДНК є не випадковою.
Імунні механізми, що лежать в основі ХОЗЛ і РЛ
Роль імунної системи при захворюваннях легень становить найбільший клінічний інтерес. У хворих на ХОЗЛ імунологічні зміни відбуваються внаслідок як порушення регуляції Т-клітин (збільшення вмісту CD8+, зниження CD4+), так і виснаження Т-клітин, де в результаті хронічного зв’язування контрольних точок імунної системи ефекторна функція втрачається. Крім того, було показано, що експресія PD‑1 у виснажених Т-клітинах веде до змінення імунної функції у хворих на ХОЗЛ.
У пацієнтів із НДКРЛ терапевтичне інгібування білка контрольної точки імунної системи PD‑1 пригнічує Т-клітинну активність, ухилення від імунітету і згодом індукує імуно-опосередковану загибель пухлинних клітин. ХОЗЛ зазвичай вважають негативним прогностичним чинником у хворих на РЛ, однак останні дослідження продемонстрували збільшення виживаності без прогресування в пацієнтів із поширеною стадією НДКРЛ із супутнім ХОЗЛ, які отримували анти-PD‑1 терапію. Крім того, коекспресія PD‑1 і Т-клітинного імуноглобуліну, а також молекули, що містить домен муцину‑3 (TIM‑3) на CD8+-Т-клітинах, зростає з вираженістю ХОЗЛ. Висока ефективність анти-PD‑1 терапії в цих пацієнтів може пояснюватись імунологічною дисрегуляцією, яку спостерігають у разі ХОЗЛ, що призводить до збільшення експресії імунних контрольних точок серед Т-клітин.
Зміни складу імунних клітин можуть бути корисним біомаркером або терапевтичною мішенню комбінації ХОЗЛ + РЛ. Нещодавнє дослідження продемонструвало, що збільшення Т1-поляризованих CD4+ Т-клітин у легеневій тканині асоційоване з тяжкістю ХОЗЛ і може слугувати корисним біомаркером прогресування захворювання. Нещодавно роль Th17 у ХОЗЛ і прогресуванні РЛ була досліджена в низці клінічних і доклінічних досліджень. На моделі мишей Chang та співавт. забезпечили вагомі докази патогенної ролі Th17-клітин в опосередкуванні запалення і канцерогенезу в легенях. Додаткові дослідження підтвердили, що експресія Th17 посилюється під впливом тютюнового диму і є потенційною терапевтичною мішенню при ХОЗЛ.
Є суперечливі дані щодо кореляції ступеня тяжкості ХОЗЛ і захворюваності на РЛ. De Torres і співавт. виявили, що остання зменшується зі збільшенням ступеня тяжкості ХОЗЛ. Наприклад, IV стадія ХОЗЛ (згідно з GOLD – Глобальної ініціативи щодо ХОЗЛ) демонструє менше половини випадків захворюваності на РЛ, якщо порівняти зі стадією I. Такі дані можна пояснити тим, що в курців, хворих на ХОЗЛ легкого ступеня, імунна система може бути більш пригніченою і менш активною проти туморогенезу, ніж активна, нетолерантна імунна система в пацієнтів із ХОЗЛ тяжкого ступеня. І навпаки, довготривале дослідження (n=5402) першого Національного обстеження здоров’я і харчування показало, що частота випадків РЛ зростає зі збільшенням тяжкості ХОЗЛ (легкий: відношення ризиків (ВР) 1,4; 95% ДІ 0,8-2,6; помірний тяжкий: ВР 2,8; 95% ДІ 1,8-4,4) проти нормальної функції легень.
Мікробіом легень
Легеневий мікробіом – це поняття, яке охоплює спільноту бактерій, вірусів і грибків, що мешкають в ДШ і паренхіматозній тканині. Зміни мікробіому легень можуть впливати на сприйнятливість організму-хазяїна до різних респіраторних захворювань через порушення механізмів імунного захисту. Нижні ДШ легені заселені безліччю видів мікроорганізмів. Отже, якщо різноманітність бактерій зменшується, це, імовірно, призводить до домінування одного виду бактерій, що спричинює порушення імунітету слизової оболонки і дисбіозу ДШ.
Мікробіом змінюється залежно від впливу різних чинників довкілля, а вдихання тютюнового диму спричинює порушення цілісності епітеліального бар’єра ДШ і контакту клітина-клітина внаслідок деградації білків із щільним з’єднанням, індукуючи аутофагію війок клітин, гіперплазію келихоподібних клітин і збільшення проникності епітелію.
ХОЗЛ
Наявність бактерій у пацієнтів із ХОЗЛ пов’язана з гіперсекрецією слизу, набряком бронхіальної стінки, третинними лімфоїдними фолікулами і запаленням ДШ і паренхіми внаслідок неповноцінності мукоциліарного кліренсу. Структура і цілісність ДШ порушуються, а клітинні реакції змінюються, що є життєво важливим для контролю росту бактерій.
Хворі на ХОЗЛ схильні до мікробної колонізації та інфікування ДШ, де патогенні бактерії, які певною мірою не є шкідливими, персистують у ДШ, призводячи до пошкодження епітелію ДШ і хронічного запалення і можуть зумовлювати загострення.
Ідентифікація переважальних видів бактерій під час стабільного стану і загострень ХОЗЛ залишається предметом дискусій. Erb-Downward та співавт. встановили, що протеобактерії є панівними у легеневій тканині хворих на дуже тяжкий ступінь ХОЗЛ. Ці висновки збігалися з результатами, які отримали Hilty та співавт., однак більшість інших досліджень дійшли висновку, що тип Firmicutes найпоширеніший при середній і тяжкій формах ХОЗЛ. На сьогодні встановлено, що атипові Haemophilus influenzae, Streptococcus pneumoniae, Moraxella catarrhalis і Pseudomonas aeruginosa є патогенами, чия причетність до ХОЗЛ чітко доведена.
Ідентифікація мікробіоти варіює залежно від популяції, тяжкості захворювання і методів, які використовують для виділення і характеристики мікробіому. Наявність різних мікроніш у різних відділах легень також може пояснити ці різні результати. Ранні дослідження повідомляли, що бактеріальне різноманіття зменшується зі збільшенням ступеня тяжкості ХОЗЛ, але це не було підтверджено подальшими випробуваннями. Застосування метагеноміки може надати функціональні дані стосовно мікробних взаємодій і допомогти в інтервенційних дослідженнях при ХОЗЛ.
Рак легень
Встановлено, що в пацієнтів із хронічними захворюваннями легень, наприклад із ХОЗЛ, мікробіом легень, порівнюючи з групою контролю (здорові волонтери), змінюється. Однак мало відомо про те, чи є ключові види мікроорганізмів або загальні профілі мікроорганізмів легень, які підвищують сприйнятливість до РЛ або посилюють його прогресування. Наявність запалення у відповідь на Mycobacterium tuberculosis асоціюється з підвищеним ризиком розвитку РЛ. Результати низки досліджень продемонстрували канцерогенний вплив бактерій, у тому числі Bacteroides fragilis і Fusobacterium nucleatum, на розвиток раку товстої кишки. Механістичний вплив мікробіому легень на розвиток пухлини – це напрям досліджень, що швидко розвивається. Нещодавно Jin та співавт. висловили припущення, згідно з яким симбіонтна мікробіота легень сприяє запаленню і проліферації пухлини шляхом активації γδ Т-клітин і вироблення IL‑17 у легенях. Ще одне недавнє дослідження продемонструвало унікальну бактерійну палітру в пацієнтів із пухлинами легень, які мають мутації TP53. Це свідчить про те, що мікробний склад легень у разі РЛ може бути мутаційним, проте необхідне подальше з’ясування молекулярних і мікробних взаємодій.
Недавня демонстрація взаємозв’язку між мікробіомом кишечнику і реакцією на імунотерапію показала, що склад мікробіому передбачає ефективність анти-PD‑1 терапії меланоми та епітеліальних пухлин, у тому числі НДКРЛ. Згадані випробування показують помітний вплив мікробіому кишечнику на терапевтичну відповідь, що, як очікується, матиме глибокий вплив на діагностику й терапевтичну стратегію, оскільки ця область досліджень продовжує розвиватися.
Діагностичні і терапевтичні біомаркери
Позаклітинні везикули (ЕV)
ЕV – це нанорозмірні мембранозні везикули, секретовані як нормальними, так і хворими клітинами в їх позаклітинне середовище. EV відіграють ключову роль у місцевій і системній міжклітинній комунікації завдяки обміну біоактивними молекулами, такими як ДНК, мРНК, міРНК, білки й ліпіди. EV можуть бути класифіковані за трьома основними підтипами везикул: 1) апоптотичні тіла, 2) мікровезикули та 3) екзосоми, які диференціюють залежно від їхнього розміру, внутрішньоклітинного походження і біогенезу. Зростає кількість досліджень, де вивчають вплив EV на різні патологічні процеси шляхом селективного перенесення нуклеїнових кислот, білків і ліпідів. Молекулярний вантаж, який міститься в EV, відображає їх клітинне походження, він захищений і циркулює в крові, що робить його привабливим біомаркером захворювань, зокрема ХОЗЛ і РЛ.
Роль EV у захворюванні полягає в модуляції імунної системи, ангіогенезі, ремоделюванні паренхіми і формуванні попередніх метастатичних ніш. Поглинання EV клітинами-мішенями є специфічною взаємодією, яка відбувається шляхом прямого злиття, ендоцитозу або зв’язування з рецепторами. Автори багатьох досліджень стверджували, що горизонтальне поширення і поглинання нуклеїнової кислоти з EV може бути ключовим фактором, що впливає на неоднорідність раку.
Щодо ХОЗЛ, то нещодавні випробування виявили нові молекулярні механізми розвитку захворювання, які регулюються EV та їхнім умістом, висвітлюючи нову парадигму паракринної сигналізації. Повідомляється, що різні стресові тригери сприяють секреції циркулюючих EV із клітин ендотелію легень і можуть бути корисним прогностичним біомаркером для оцінки ступеня ураження ендотелію легень при ХОЗЛ та прогресуванні захворювання.
Було висловлено припущення, що міРНК і білки EV можуть також бути корисними діагностичними біомаркерами РЛ; показано, що міРНК відіграють важливу роль у пухлинному розвитку, метастазуванні і відповіді на лікарські засоби. Це зумовлено тим, що міРНК EV, отримані з ураженої раком тканини легень, можуть слугувати показниками прогресування раку, адже їхній уміст відображає молекулярну динаміку поведінки пухлини як in situ, так і в разі метастазування.
На додаток до значення EV як циркулюючих біомаркерів, потенціал екзосом як мішеней для генної терапії є новою та інтересною темою. Міжклітинна взаємодія через обмін трансляційною РНК забезпечує ймовірність створення екзосом, що містять ДНК або РНК для терапевтичного втручання. На сьогодні такий генетичний обмін продемонстровано в пухлинному мікрооточенні за допомогою механізму, подібного до ендокринного сигналізування в системному кровообігу. Відсутність імуногенності у створених in vitro екзосом має велику перевагу перед вірусними векторами, багато з яких ініціюють імунне відторгнення.
Нещодавнє дослідження Costales та співавт. уперше продемонструвало потенціал використання міРНК як лікарських препаратів, призначених для лікування раку молочної залози. Невелика небілкова молекула була розроблена з метою використання РНКази для селективного розщеплення miR‑96, спричинюючи апоптоз у пухлині молочної залози, але не в нормальних клітинах. Клінічну корисність міРНК було також виявлено у випробуванні, яке повідомляє, що селективне розщеплення miR‑96 індукує апоптоз у клітинах пухлини молочної залози і є потенційною терапевтичною мішенню. Використання унікальної біологічної природи екзосом із лікувальною метою потребує подальшого з’ясування екзосомного вантажу та їхніх біологічних функцій, щоб допомогти в створенні екзосом із чітко визначеним складом і активністю.
ЛОС для діагностики ХОЗЛ і РЛ
ЛОС – це побічний продукт клітинних процесів, які можуть безпосередньо виводитися з клітин у кровоносне русло й проникати у видихуване повітря через альвеолярну мембрану. Модифікації клітинного метаболізму, мікросередовища і різні патологічні зміни можуть створити унікальний профіль ЛOC. Аналіз профілів ЛOC у видихуваному повітрі проводиться за допомогою одного з двох часто використовуваних методів: газової хроматографії-мас-спектрометрії (GC-MS) або приладів штучного інтелекту, як-от електронний ніс. Аналіз ЛOC є перспективним неінвазивним методом діагностики РЛ і ХОЗЛ і нині інтенсивно досліджується.
І ХОЗЛ, і РЛ характеризуються запаленням і наявністю оксидативного стресу в легеневій тканині, унаслідок чого утворюються різні ЛОС, які можуть виділятися під час видиху. У декількох дослідженнях був виявлений клінічний потенціал визначення видихуваних ЛOC як біомаркера легеневих захворюваннь, а в одному з нещодавніх випробувань використовувалися ЛOC для класифікації 17 захворювань (і РЛ включно) у 1404 пацієнтів із точністю 86%.
Незважаючи на те що це економічно ефективний неінвазивний метод, який широко досліджується при різних захворюваннях, сьогодні застосування цих технологій сумнівне через різноманіття патологічних станів і змінних, як-от історія куріння, дієта, уживання медикаментозних препаратів, вік пацієнта. Крім того, донині немає стандартизованого методу або засобів для порівняння надійності і відтворюваності результатів, отриманих у дослідженнях.
Висновки
ХОЗЛ і РЛ є провідними причинами смертності в усьому світі, вони мають ключові фактори ризику, які можна модифікувати і яким можна запобігати, у тому числі куріння і вплив забрудненого повітря. Лише незначна частка (10-15%) курців у кінцевому підсумку захворіє на ХОЗЛ або РЛ, а це свідчить про те, що ключовою для розуміння цих захворювань є складна взаємодія між генетикою, епігенетикою і факторами довкілля. Точні механізми збільшення захворюваності на РЛ у пацієнтів із ХОЗЛ ще не визначені, однак останні дослідження дають вагомі докази ролі імунної дисфункції, мікробіому легень, епігенетичної регуляції та EV у розвитку ХОЗЛ і РЛ. Подальші випробування з вивчення зв’язків між ключовими молекулярними шляхами продовжуватимуть з’ясовувати механізми, які лежать в основі розвитку ХОЗЛ і РЛ, і надаватимуть дані для розробки нових діагностичних і прогностичних інструментів раннього виявлення і персоналізованого лікування цих захворювань.
Реферативний огляд статті Brielle A. Parris et al. Chronic obstructive pulmonary disease (COPD) and lung cancer: common pathways for pathogenesis», J Thorac Dis 2019;11(Suppl 17)
Підготував Назар Лукавецький
Повну версію дивіться: https://jtd.amegroups.com
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 2 (55), 2021 р.
СТАТТІ ЗА ТЕМОЮ Пульмонологія та оториноларингологія
Реімбурсація – це повне або часткове відшкодування аптечним закладам вартості лікарських засобів або медичних виробів, що були відпущені пацієнту на підставі рецепта, за рахунок коштів програми державних гарантій медичного обслуговування населення. Серед громадськості програма реімбурсації відома як програма «Доступні ліки». Вона робить для українців лікування хронічних захворювань доступнішим....
Хронічна кропив’янка (ХК) – це патологія, яка характеризується рецидивними нестійкими висипаннями з/без ангіоневротичного набряку, які виникають мало не щодня впродовж більш як 6 тиж [1]. Розрізняють два варіанти ХК – хронічна індукована кропив’янка (ХІК), або фізична кропив’янка, зумовлена певними фізичними подразниками, такими як тиск, тепло або холод, і більш поширена хронічна спонтанна кропив’янка (ХСК), яка розвивається у 80-90% випадків і характеризується відсутністю відомих екзогенних чинників і причин [2]. На це захворювання страждає від 0,5 до 1% населення світу, переважно особи жіночої статі [3]. Повторні симптоми часто призводять до порушень сну та чинять виражений негативний вплив на якість життя (QoL) [4]. ...
Риносинусит (РС) незмінно потрапляє до десятки найпоширеніших діагнозів в амбулаторній лікарській практиці та посідає 5-те місце серед захворювань, щодо яких призначається антибактеріальна терапія [1]. Симптоми гострих РС маніфестують тоді, коли уражаються слизові оболонки приносових пазух і порожнини носа. Оскільки слизова оболонка носа та приносових пазух – єдине ціле, гострий запальний процес уражатиме ці слизові оболонки, а ізольоване запалення слизової оболонки порожнини носа чи будь-якої з приносових пазух може визначатися при хронічних захворюваннях [2]. Це обґрунтовує доцільність використання терміна «РС». ...
Застуда та інші інфекції дихальних шляхів – актуальна проблема охорони здоров’я через високий рівень захворюваності, що перевищує такий інших інфекційних патологій. З метою підвищення кваліфікації лікарів загальної практики та обміну досвідом з актуальних питань лікування інфекційних захворювань у лютому була проведена науково-практична конференція «Академія сімейного лікаря. Для кого небезпечні сезонні інфекції? Загроза сезонних інфекцій. Погляд пульмонолога, інфекціоніста, алерголога, ендокринолога, кардіолога, педіатра» за участю провідних вітчизняних спеціалістів-практиків....